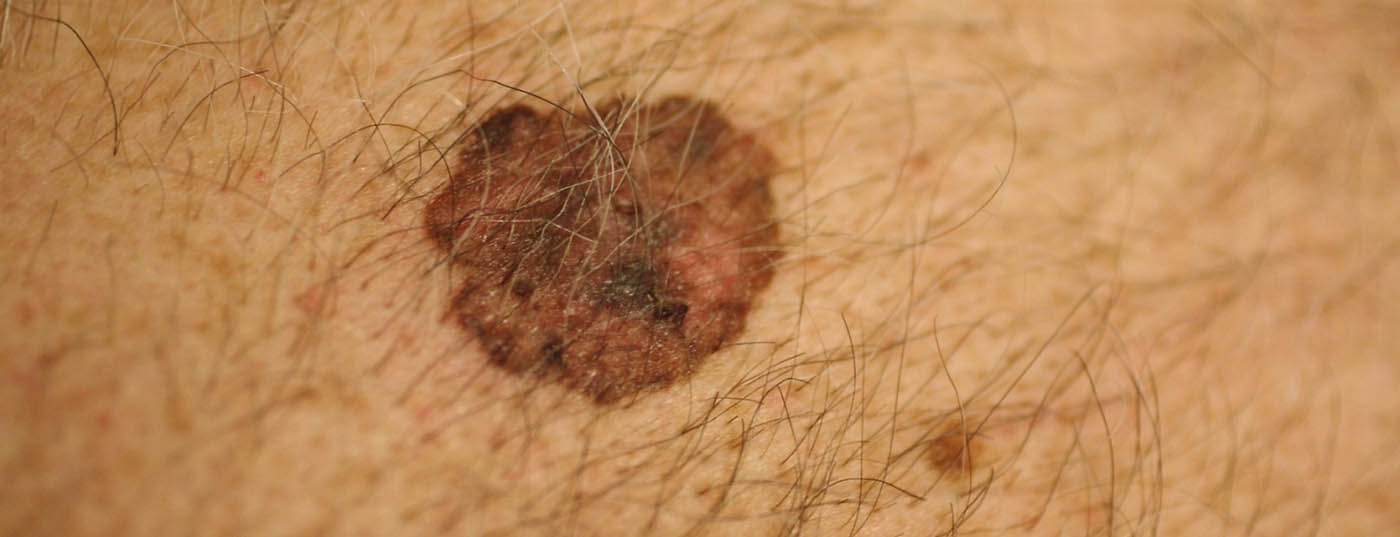
Les données de deux études de phase III (toutes deux menées par le groupe de recherche du Dr Caroline Robert, Institut Gustave Roussy à Villejuif, Paris), publiées au début de cette année, illustrent l’évolution rapide dans le domaine du mélanome malin. Le nivolumab et le traitement combiné dabrafenib-trametinib pourraient bientôt être proposés aux patients atteints de mélanome métastatique. Le nivolumab donne également de bons résultats dans les cas de BRAF sauvage, tandis que la combinaison représente une amélioration pour les cas mutés.
Un mélanome métastatique réfractaire à l’ipilimumab répond mieux à l’administration de nivolumab qu’à la chimiothérapie – c’est une certitude. La question de savoir si le nivolumab apporte également un avantage chez les patients atteints de mélanome avancé qui n’avaient pas été traités auparavant a maintenant été étudiée en phase III. L’étude CheckMate 066 a été publiée au début de l’année dans le New England Journal of Medicine (en ligne depuis novembre) et a attiré l’attention parce qu’il s’agit de la première étude randomisée de phase III à démontrer un avantage en termes de survie du blocage de PD1 [1]. Depuis fin décembre 2014, le produit est autorisé aux États-Unis. Dans l’UE (et en Suisse également), l’autorisation de mise sur le marché pour le mélanome avancé ne devrait plus tarder.
Le blocage de PD1 prolonge la vie
Le nivolumab est un anticorps anti-PD1 (“programmed cell death protein 1”). Le blocage provoque une augmentation de la défense des cellules T contre les tumeurs. L’étude a porté sur 418 patients naïfs de traitement atteints de mélanome métastatique de stade III ou IV (sans mutation de BRAF). Ils ont reçu soit du nivolumab, soit de la dacarbazine, l’agent chimiothérapeutique standard en première ligne au moment de la planification de l’étude (2012). La dose était de 3 mg/kgKG toutes les deux semaines dans le bras nivolumab et de 1000 mg/m2 toutes les trois semaines dans le bras dacarbazine. Les différentes fréquences thérapeutiques ont été compensées au moyen d’un placebo, ce qui a permis de réaliser un test en aveugle. Le critère d’évaluation principal était la survie globale (OS). En outre, la survie sans progression (PFS) et le taux de réponse (selon les critères RECIST 1,1) ont été évalués.
Pour en venir aux faits concrets, 72,9 vs. 42,1% (nivolumab vs. dacarbazine) des patients étaient encore en vie (OS) après un an , ce qui représente une réduction considérable de 58% du risque de décès (HR 0,42, 99,79% IC 0,25-0,73 ; p<0,001). La médiane de la PFS était de 5,1 mois contre 2,2 mois. L’anticorps a donc réduit le risque de progression ou de décès de 57% (HR 0,43, IC à 95% 0,34-0,56 ; p<0,001). Le taux de réponse objective était de 40 vs. 13,9%. Les chances de réponse étaient donc quatre fois plus élevées sous nivolumab que sous dacarbazine (odds ratio 4,06 ; p<0,001). Les résultats étaient cohérents dans tous les sous-groupes pré-spécifiés.
La fatigue (20%), les nausées (16,5%) et le prurit (17%) ont été fréquemment observés sous l’inhibiteur de point de contrôle immunitaire. Les effets secondaires de grade 3 et 4 ont été moins fréquents sous nivolumab, survenant dans 11,7 vs 17,6% des cas (dacarbazine). En outre, moins de patients ont abandonné le traitement dans le groupe nivolumab que dans le groupe chimiothérapie.
Combinaison – deux plus forts qu’un ?
Si CheckMate 066 concernait les patients porteurs d’une mutation BRAF de type sauvage, qui représentent environ 60% de tous les patients atteints de mélanome, une autre étude publiée en janvier 2015 s’est concentrée sur les quelque 40% restants porteurs d’une mutation BRAF V600. Ces patients bénéficient de deux substances, le vémurafénib (Zelboraf®) et le dabrafénib (Tafinlar®), également autorisées en Suisse. Tous deux ont prouvé leur efficacité à plusieurs reprises.
L’étude de phase III s’est alors focalisée sur la combinaison du dabrafenib et du tramétinib, un inhibiteur de la MEK déjà autorisé dans plusieurs pays, mais pas en Suisse [2]. L’étude a porté sur 704 patients atteints de mélanome métastatique de stade IIIC/IV avancé non traités auparavant et porteurs de la mutation V600 de BRAF (90% avec V600E et 10% avec V600K). Ils ont reçu soit la combinaison (dabrafenib 2× 150 mg/j, trametinib 1× 2 mg/j), soit la monothérapie par vemurafenib à la dose standard (2× 960 mg/j). Le critère d’évaluation principal était la survie globale.
L’analyse intérimaire prévue de l’OS a montré que 72 vs. 65% (combinaison vs. vemurafenib) des patients étaient vivants à un an. Cela correspond à une réduction significative de 31% du risque lié à la combinaison (HR 0,69, IC à 95% 0,53-0,89 ; p=0,005). La médiane de la PFS était de 11,4 mois contre 7,3 mois, soit là aussi une réduction significative de 44% de la probabilité de progression/décès (HR 0,56, IC 95% 0,46-0,69, p<0,001). Le taux de réponse objective était de 64 vs. 51%, la différence était significative.
Le nombre d’effets secondaires graves et d’arrêts de traitement était comparable dans les deux groupes d’étude. Les tumeurs cutanées secondaires sont un effet secondaire des inhibiteurs de BRAF qui ne met pas la vie en danger, mais qui est inquiétant. L’association a obtenu de meilleurs résultats que la monothérapie en ce qui concerne cet effet secondaire : des carcinomes épidermoïdes cutanés et des kératoacanthomes ne sont apparus que chez 1% des patients sous l’association thérapeutique, contre 18% des patients dans le groupe vémurafénib.
Le principal problème des inhibiteurs de kinase, seuls ou combinés, reste toutefois le développement de résistances. Elle semble être le prix à payer pour obtenir une réponse et une rémission rapides. Il n’est donc pas surprenant que les efforts de recherche dans ce domaine soient importants. Aucune solution à plus long terme n’est en vue pour le moment. Malgré ce bémol, l’allongement de la durée de vie en combinaison est remarquable et représente un progrès décisif dans le traitement du mélanome à mutations BRAF – d’autant plus que ce bénéfice n’a pas été obtenu au prix d’une toxicité accrue.
Littérature :
- Robert C, et al : Nivolumab in Previously Untreated Melanoma without BRAF Mutation. N Engl J Med 2015 ; 372 : 320-330.
- Robert C, et al : Improved Overall Survival in Melanoma with Combined Dabrafenib and Trametinib. N Engl J Med 2015 ; 372 : 30-39.
DERMATOLOGIE PRATIQUE 2015 ; 25(2) : 19-20