L’arsenal des pharmacothérapies disponibles pour le traitement de l’épilepsie s’est considérablement élargi ces dernières années. Une sélection et une hiérarchisation plus ciblées en fonction de la forme d’épilepsie, la prise en compte des comorbidités et l’inclusion des caractéristiques individuelles des patients sont désormais possibles. L’absence ou la faible induction enzymatique des antiépileptiques de deuxième et troisième générations permet d’éviter les effets secondaires autrefois typiques des antiépileptiques tels que l’ostéoporose, les polyneuropathies et les syndromes métaboliques.
Depuis 1990, plus de 20 médicaments sont devenus disponibles pour la prophylaxie des crises d’épilepsie. Ils diffèrent non seulement par leur mode d’action mais aussi par leur dosage, leur tendance à interagir et leurs effets secondaires typiques. D’une part, leur utilisation ciblée nécessite davantage de connaissances de la part de l’utilisateur, mais d’autre part, elle permet une sélection de plus en plus individuelle et orientée vers le patient. Dans le présent article, les indications pour une sélection appropriée des médicaments anti-épileptiques sont données en référence à des groupes de patients en fonction de l’âge, du sexe et des comorbidités.
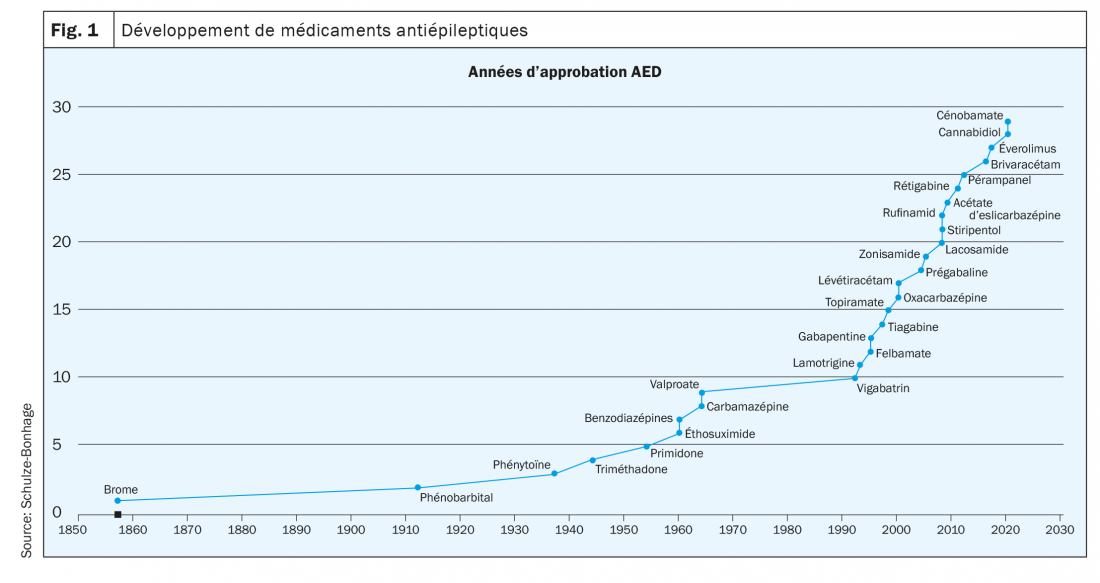
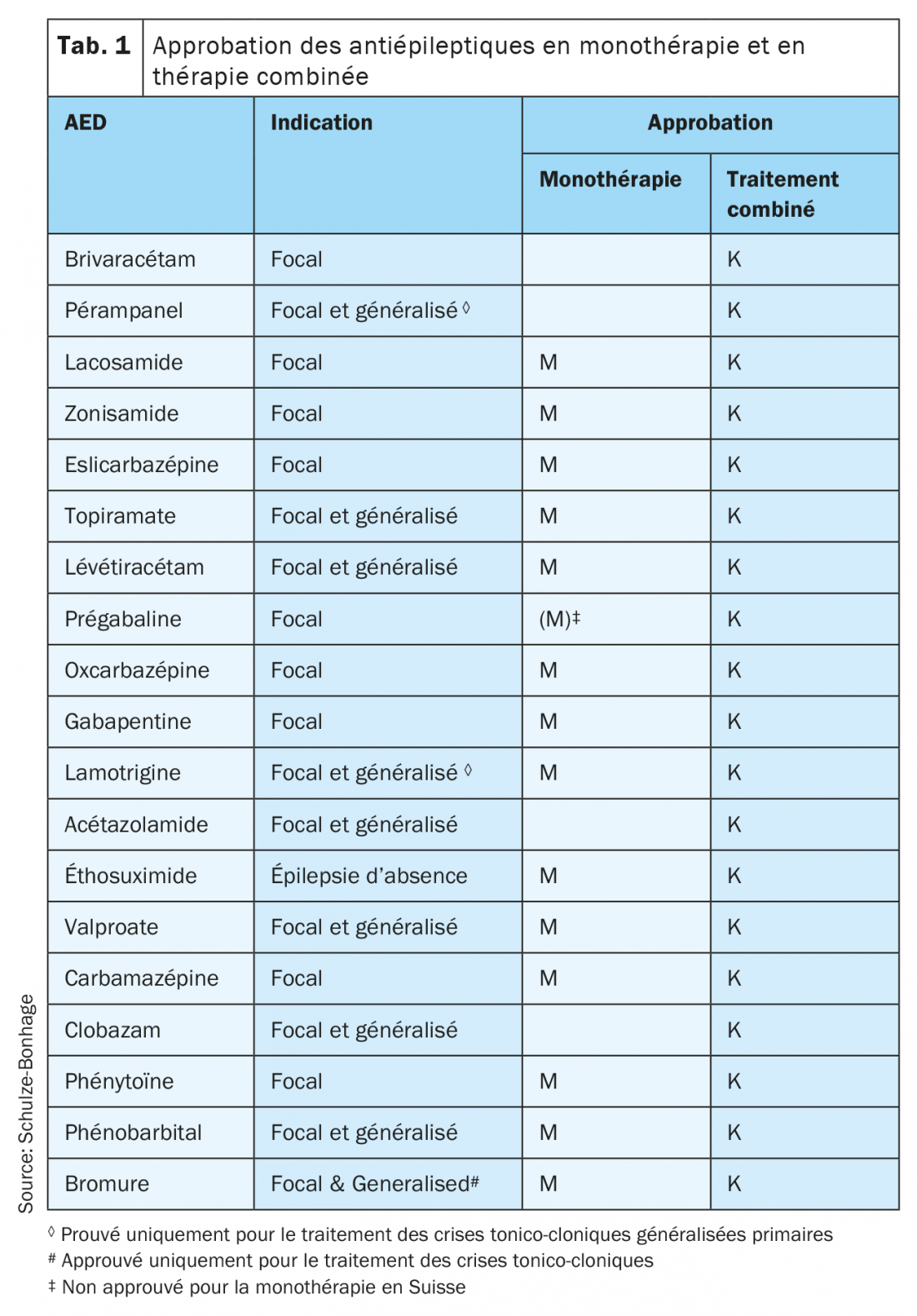
Depuis l’introduction des antiépileptiques de deuxième génération au cours des 30 dernières années, l’arsenal des phamacothérapies disponibles pour le traitement de l’épilepsie s’est énormément développé. (fig. 1). Bien que cette expansion n’ait pas encore résolu le problème de la phamacorésistance chez environ un tiers des patients épileptiques, elle permet une sélection et une priorisation plus ciblées en fonction de la forme d’épilepsie, la prise en compte des comorbidités et l’inclusion des caractéristiques individuelles des patients, telles que le sexe, l’âge et les exigences professionnelles (tab. 1).
Syndromes épileptiques et thérapie anticonvulsive
Les principaux groupes d’épilepsies traitées à l’âge adulte sont, d’une part, les épilepsies structurelles à début focal (ou multifocal) et, d’autre part, les épilepsies génétiques présumées à début généralisé, c’est-à-dire impliquant précocement les deux hémisphères. Plus de 60% des épilepsies de l’adulte sont classées comme focales, et la proportion de patients dont le contrôle des crises est incomplet est supérieure à 40% dans ce groupe. En conséquence, la majorité des nouveaux développements de médicaments antiépileptiques ont été réalisés dans le but de traiter les épilepsies focales et leurs crises.
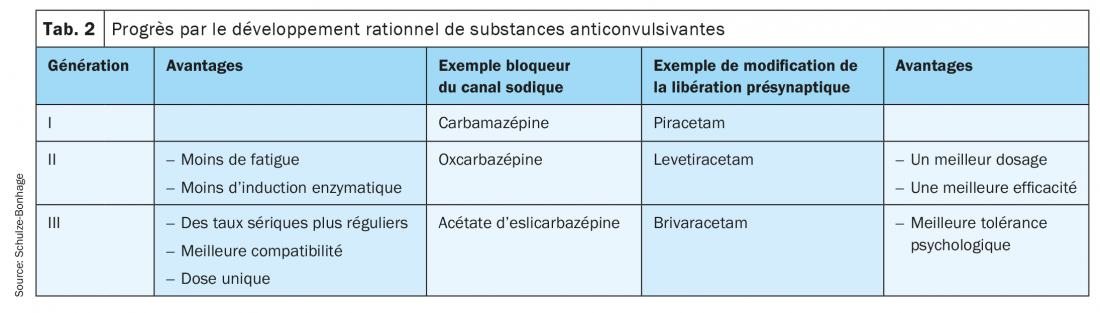
Les nouveaux développements de la dernière décennie pour le traitement des épilepsies focales comprennent le brivaracétam, l’acétate d’eslicarbazépine, le pérampanel, le lacosamide et plus récemment le cénobamate*. Le brivaracétam et l’acétate d’eslicarbazépine sont des médicaments antiépileptiques de troisième génération qui ont été développés rationnellement à partir de substances prédécesseurs. Le brivaracétam est un dérivé de troisième génération du piracétam et du lévétiracétam, avec une efficacité spécifique plus élevée au point de départ et une meilleure tolérance, notamment en ce qui concerne les effets secondaires psychiatriques. L’acétate d’eslicarbazépine, en tant que pro-drogue, est une évolution de la carbamazépine et de l’oxcarbazépine avec une utilisation plus sélective d’un énantiomère et une pharmacocinétique considérablement améliorée permettant une dose unique sans pics plasmatiques perturbateurs. Le lacosamide a également un mode d’action modifié sur les canaux sodiques et appartient donc au groupe des bloqueurs des canaux sodiques dont le potentiel d’interaction est particulièrement faible. Le pérampanel est un nouveau développement qui cible les sous-récepteurs du glutamate et élargit ainsi le spectre des approches disponibles. Le cénobamate combine deux mécanismes d’action (blocage des canaux sodiques et renforcement de l’inhibition GABAergique) en une seule substance (Tab. 2).
* actuellement non encore approuvé en Suisse
Comment utiliser avec profit cette multitude d’antiépileptiques chez le patient individuel?
Dans certains pays, en plus de la preuve d’efficacité dans des essais contrôlés par placebo pré-spécifiés, la supériorité dans des comparaisons directes est requise pour certifier un bénéfice supplémentaire. Cependant, ces études ne répondent pas aux exigences internationales en matière d’études d’enregistrement et ne sont donc généralement pas disponibles; de plus, les résultats des comparaisons directes, du moins dans les études courtes, dépendent considérablement de certains paramètres de l’étude (taux de dosage, doses cibles).
Les principales informations comparatives sur l’efficacité et la tolérance des monothérapies proviennent des essais SANAD menés au Royaume-Uni (tab. 3). Ici, après la randomisation de la substance de traitement mais un traitement ouvert avec une marge de manœuvre dans le dosage, le taux de rétention sur des périodes de plusieurs années a été enregistré comme paramètre de résultat pertinent pour la pratique – le taux de rétention enregistre les aspects de l’efficacité et de la tolérance suffisante à long terme.
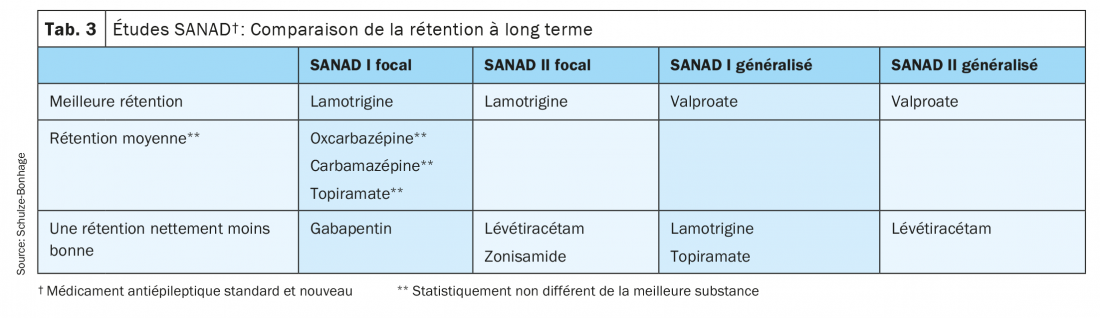
La première étude SANAD a ainsi démontré la supériorité de la lamotrigine et l’infériorité de la gabapentine pour la première fois dans un grand collectif avec une sélection correspondant à la pratique clinique; l’oxcarbazépine y a également obtenu de bons résultats, le topiramate plutôt moins bons. Dans l’étude SANAD-II récemment publiée, la lamotrigine était en concurrence avec le lévétiracétam et le zonisamide – là aussi, la lamotrigine a obtenu les meilleurs résultats, en grande partie grâce à sa tolérance souvent très bonne; en comparaison, le lévétiracétam, souvent privilégié, a présenté beaucoup plus fréquemment des effets secondaires psychiatriques tels que la dépression et l’irritabilité. Globalement, il y a donc de bonnes raisons d’envisager la lamotrigine et l’oxcarbazépine en monothérapie des épilepsies focales.
Les traitements des épilepsies généralisées diffèrent dans leur efficacité
Alors que les différences d’efficacité dans le traitement des épilepsies focales sont graduelles et que d’autres aspects jouent généralement le rôle principal dans le choix des médicaments, il existe une hiérarchie claire de l’efficacité dans les épilepsies généralisées: Le valproate s’est révélé significativement supérieur à la lamotrigine, au lévétiracétam et au topiramate dans diverses études, dont les deux études SANAD. Ce n’est qu’en cas d’absence de traitement que l’éthosuximide peut être considéré comme aussi efficace.
Cependant, l’exemple du valproate montre de manière particulièrement claire que l’efficacité n’est qu’un critère pour le choix individuel d’un médicament. En effet, les effets secondaires du valproate sont multiples et pertinents pour les patients traités. Ces effets indésirables comprennent une prise de poids persistante dépassant souvent 5 kg, le syndrome métabolique, le syndrome des ovaires polykystiques, la thrombocytopénie, l’encéphalopathie, la coagulopathie, l’ostéopathie, la perte de cheveux, les tremblements, le risque significativement accru de tératogénicité et le risque de troubles de l’intelligence en cas d’exposition pendant la grossesse. Nombre de ces risques n’apparaissent pas du tout dans les résultats des études de courte durée, comme les études habituelles de trois mois, et sont à peine perceptibles dans les paramètres des résultats, même dans les études d’un an ou plus. Malgré les données de l’étude montrant une nette préférence pour le valproate, au moins chez les femmes en âge de procréer, compte tenu des risques et des effets secondaires, le valproate n’est choisi comme médicament de dernier recours que lorsque les autres options disponibles échouent.
Sélection individualisée des médicaments antiépileptiques
Par conséquent, la prise en compte de l’individualité du patient se substitue au schéma d’une séquence thérapeutique générale. Les aspects importants pour le choix du médicament sont l’âge, le sexe, la situation des crises et l’observance (fig. 2).
Le rôle de l’étiologie
L’étiologie de l’épilepsie est un facteur majeur dans les chances d’obtenir une absence totale de crises. Ainsi, le risque de pharmacorésistance est particulièrement élevé dans les malformations du développement cortical, notamment la dysplasie corticale ou la tubérosité, et dans la sclérose hippocampique. L’imagerie joue donc un rôle essentiel dès l’éducation précoce sur les chances réalistes de traitement et les traitements non médicamenteux précoces éventuellement utiles, comme la chirurgie de l’épilepsie.
Dans les épilepsies difficiles à traiter, des traitements combinés utilisant des antiépileptiques particulièrement puissants (tels que le topiramate, le pérampanel ou le cénobamate) sont plus fréquemment nécessaires que, par exemple, dans les épilepsies vasculaires, où des monothérapies avec des antiépileptiques tels que la lamotrigine, l’acétate d’eslicarbazépine/oxcarbazépine ou la prégabaline sont souvent suffisantes.
Avec le développement des médicaments orphelins, le syndrome épileptique fait l’objet d’une attention particulière. Par exemple, le cannabidiol et la fenfluramine sont depuis peu disponibles pour le syndrome de Dravet et le syndrome de Lennox-Gastaut, et la vigabatrine, le cannabidiol et l’évérolimus se sont révélés efficaces pour la sclérose tubéreuse. L’évérolimus est un exemple d’influence pionnière sur l’épileptogenèse dans la sclérose tubéreuse, avec des fenêtres de temps plus longues jusqu’à l’obtention d’une efficacité complète, avec une approche d’action spécifique à la maladie pour la première fois.
Situation de saisie
Le degré d’acuité de la gravité et de la fréquence des crises chez un patient peut jouer un rôle important dans la décision de doser un médicament antiépileptique. Un traitement efficace peut être obtenu avec la première dose de prégabaline, de lévétiracétam et de brivaracétam, en l’espace d’une semaine par de nombreux inhibiteurs des canaux sodiques, à l’exception de la lamotrigine; en revanche, la lamotrigine, le zonisamide et le cénobamate* mettent de nombreuses semaines à plusieurs mois pour atteindre des concentrations efficaces tolérables.
Pour les séries à haute fréquence, la disponibilité d’une forme d’administration intraveineuse peut également être un avantage; cependant, en règle générale, un dosage complémentaire par voie orale est suffisant. En particulier, l’aspect d’une option de traitement par voie intraveineuse ne doit pas conduire au choix d’un médicament réellement non préféré (tel que la phénytoïne).
Régime posologique et observance
Le respect du régime médicamenteux prescrit et l’adhésion à long terme des patients traités sont d’une importance capitale pour le succès à long terme du traitement. Les traitements avec des substances qui ne doivent être administrées qu’une fois par jour (acétate d’eslicarbazépine, pérampanel, cénobamate*, à mon avis aussi zonisamide ou valproate) sont favorables à une prise régulière; si possible, les protocoles de prise trois fois par jour sont à éviter.
* actuellement non encore approuvé en Suisse
Un autre facteur clé est que le traitement soit bien toléré. Dans les épilepsies qui répondent bien aux faibles doses, il s’agit souvent d’un problème mineur, mais lorsque des doses plus élevées et une polythérapie sont nécessaires, le choix des médicaments bien tolérés individuellement et de leur association appropriée devient important. Les effets secondaires sont vécus subjectivement de manière très différente; prendre au sérieux les informations individuelles du patient est crucial pour la coopération entre le médecin et le patient.
Les schémas posologiques complexes (comme ceux de la lamotrigine) peuvent surcharger les patients de faible intelligence ou souffrant de troubles de la mémoire et les empêcher d’atteindre les doses cibles prévues. Une stratégie mutuellement acceptée est également d’une grande importance pour un retrait progressif coordonné des traitements.
Pour les patients ayant des problèmes connus pour suivre les instructions de médication, les médicaments ayant une longue demi-vie (pérampanel, dans certains cas zonisamide, acétate d’eslicarbazépine et valproate) peuvent présenter des avantages car une seule dose oubliée entraîne une moindre fluctuation de la concentration sérique).
Le rôle de l’âge
Selon toutes les données disponibles, les médicaments antiépileptiques fonctionnent en principe à tout âge; c’est pourquoi, à l’exception de la dernière fois, tous les médicaments ont également été testés chez des adultes, puis administrés avec succès à des patients plus âgés et à des enfants. En conséquence, la FDA s’éloigne également des études d’approbation spécia-les pour la tranche d’âge 4–18 ans.
Néanmoins, les particularités liées à l’âge doivent être prises en compte:
- La composition des récepteurs de neurotransmetteurs peut varier considérablement, en particulier pendant la période prénatale et au cours de la première année de vie. Pour les récepteurs GABA en particulier, on sait que cela peut inverser les effets des substances GABA-ergiques avec des effets proconvulsifs possibles.
- Dans les premiers mois de la vie, l’élimination hépatique de nombreuses substances est retardée, ce qui augmente le risque de symptômes d’intoxication avec des médicaments dont l’élimination hépatique est prédominante.
- Chez les enfants d’âge préscolaire et scolaire, en revanche, l’élimination rénale est plus rapide que chez les adultes; cela nécessite l’utilisation de doses plus élevées et, si nécessaire, l’administration plus fréquente de doses uniques pour atteindre le niveau d’effet souhaité.
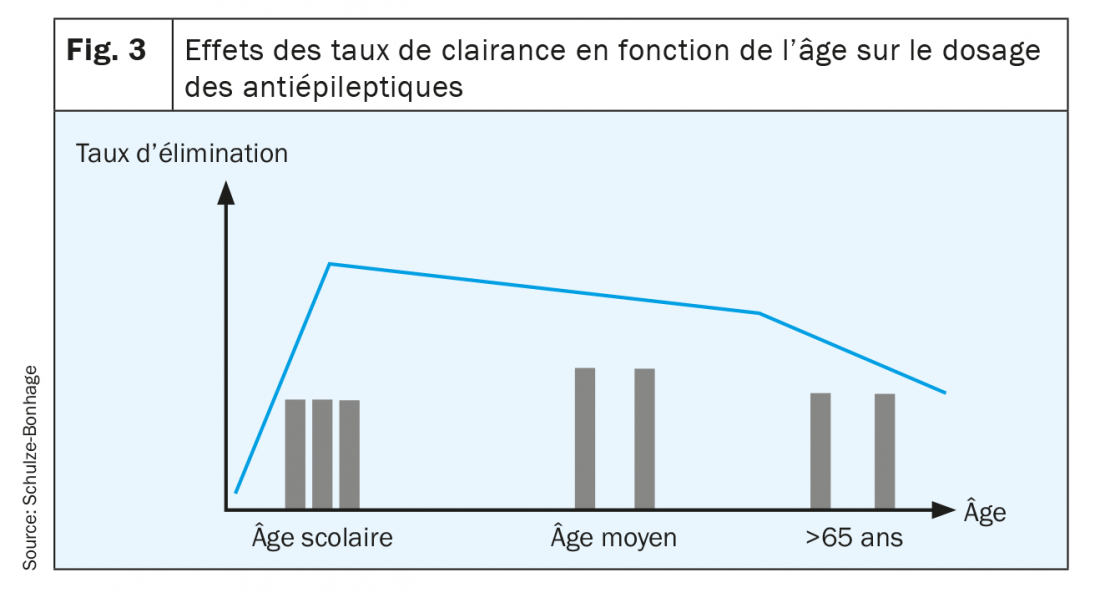
- A un âge avancé, l’élimination rénale diminue en particulier; ceci permet l’utilisation de doses plus faibles ou d’intervalles plus longs entre les doses individuelles (fig. 3).
- À un âge avancé, le risque d’effets secondaires augmente, notamment ceux qui affectent le métabolisme osseux. En cas de tendance générale à l’ostéoporose, les inducteurs enzymatiques puissants et le valproate sont associés à un risque significativement accru de fracture et doivent être évités.
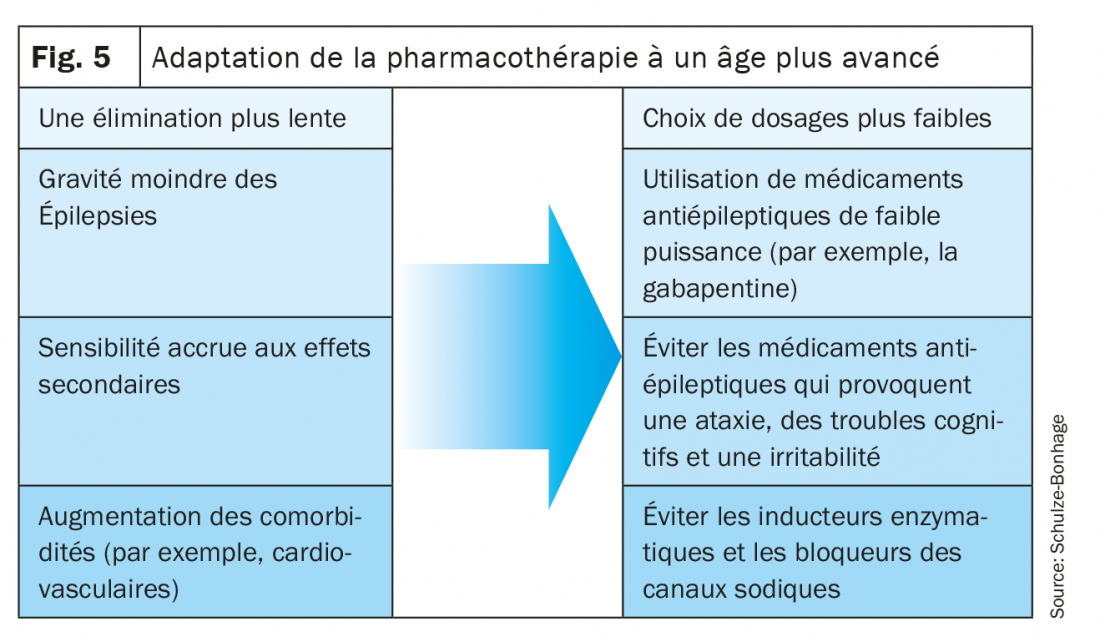
- Avec l’âge, la tolérance aux effets secondaires diminue, en particulier pour les bloqueurs des canaux sodiques et les médicaments altérant les fonctions cognitives. Les différences entre les traitements qui ont peu d’effet à l’âge moyen deviennent ici significatives, comme la moins bonne tolérance de la carbamazépine par rapport à la lamotrigine ou à la gabapentine (fig. 5) [1].
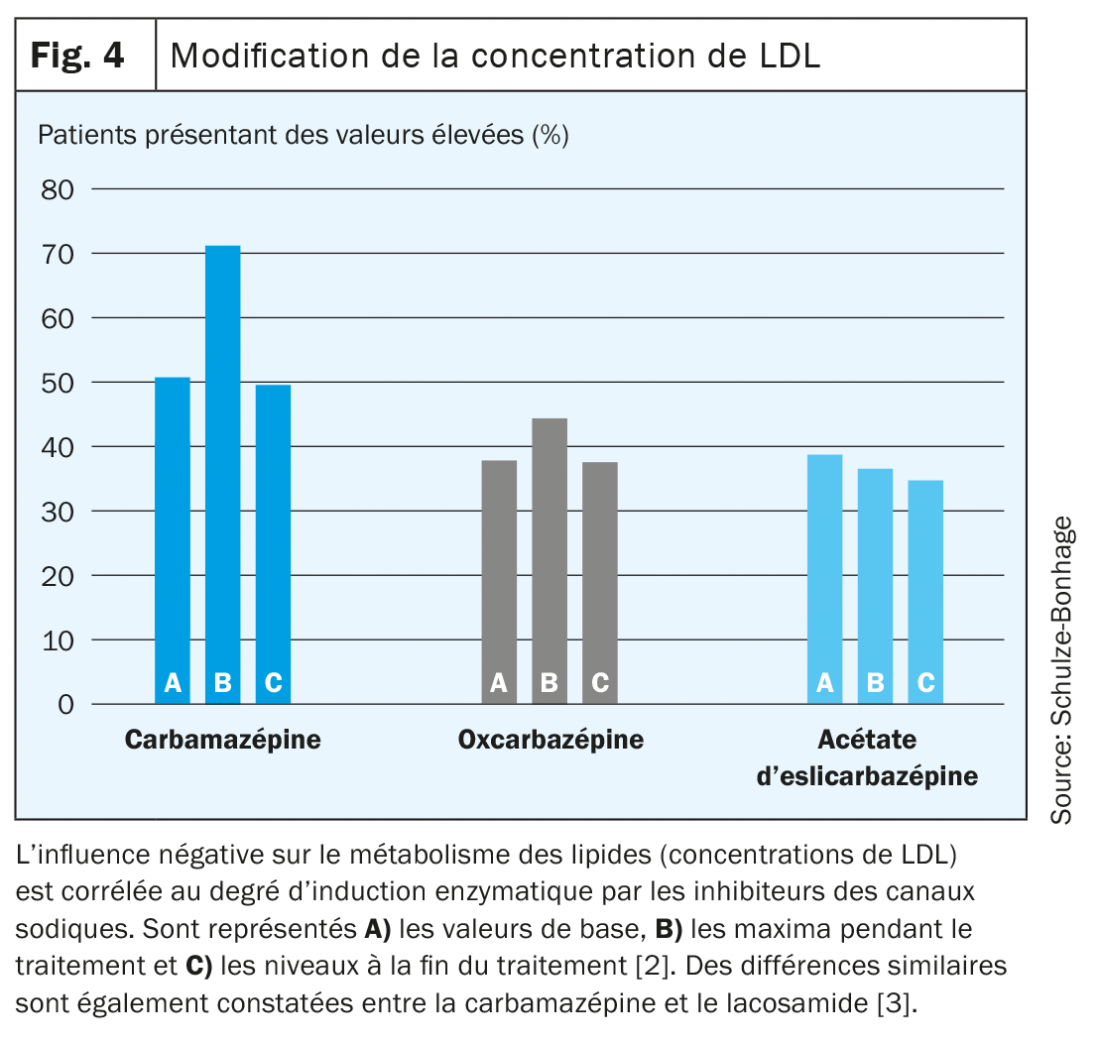
- Enfin, le spectre étiologique des épilepsies évolue au cours de la vie. Pour les épilepsies de novo chez les personnes âgées, qui représentent désormais la majorité des épilepsies, cela signifie une bonne réponse à des médicaments même moins puissants comme la gabapentine (fig. 4).
Aspects spécifiques du traitement des femmes
Tous les anticonvulsivants établis présentent une efficacité comparable chez les hommes et les femmes. Cependant, il existe des différences dans la volonté de tolérer certains effets secondaires. En particulier, les médicaments qui entraînent souvent une prise de poids (comme la carbamazépine, la vigabatrine, la prégabaline, le valproate) sont plus susceptibles d’être rejetés par les femmes que par les hommes, tout comme la perte de cheveux sous traitement par le valproate ou les taches cutanées sous lamotrigine. D’autre part, les inducteurs enzymatiques puissants provoquent souvent une impuissance aiguë et inquiétante chez les hommes.
Les femmes en âge de procréer: Avec la ménarche, les fluctuations des concentrations d’oestrogènes ont des effets pertinents sur la pharmacocinétique des antiépileptiques éliminés par voie hépatique; des taux élevés d’oestrogènes entraînent une dégradation accélérée de la lamotrigine et de l’oxcarbazépine en particulier. Ces fluctuations peuvent amplifier les effets proconvulsifs intrinsèques des œstrogènes et entraîner des augmentations cycliques de la fréquence des crises. Le choix d’antiépileptiques dont les fluctuations des concentrations sériques sont plus faibles peut être bénéfique dans ce cas.
Des effets similaires se produisent dans le cas de la protection de la conception par la prise d’inhibiteurs de l’ovulation contenant des oestrogènes: aux doses choisies ici, outre les diminutions cliniquement pertinentes des concentrations sériques de lamotrigine, d’oxcarbazépine et de lévétiracétam, on observe également un effet proconvulsif propre. Cette situation entraîne régulièrement des crises récurrentes chez les jeunes femmes à qui l’on prescrit une protection contraceptive à base d’œstrogènes sans ajustement du traitement anticonvulsivant, même après un contrôle prolongé des crises. Les préparations progestatives pures («mini-pill») ou les dispositifs intra-utérins («DIU») sont préférables pour la protection de la conception.
Dans la préparation et le traitement pendant la grossesse, l’aspect de la minimisation du risque de tératogénicité est au premier plan. La prophylaxie par l’acide folique, le traitement en monothérapie et l’utilisation préférentielle des doses minimales requises de lamotrigine, de levetiracetam et d’oxcarbazepine tout en évitant le valproate sont d’une grande importance, notamment pour la phase d’embroyage. En péripartum, une légère augmentation de la dose du médicament de base ou une administration supplémentaire temporaire et à faible dose de clobazam (5–10 mg) peut contribuer à réduire le risque de crises.
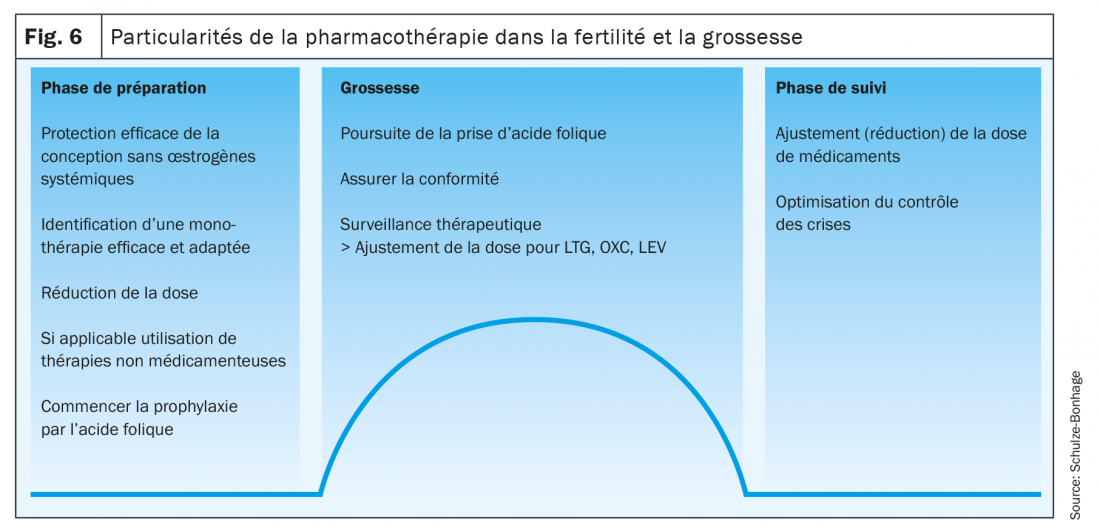
Après l’accouchement, les concentrations d’anticonvulsivants augmentent à nouveau au cours des premières semaines; malgré un sommeil nocturne souvent perturbé, une augmentation de la posologie effectuée pendant la grossesse peut être progressivement annulée. Les concentrations d’anticonvulsivants qui passent dans le lait maternel sont inoffensives avec les antiépileptiques modernes et ne constituent pas une raison pour s’abstenir d’allaiter l’enfant (fig. 6).
Femmes âgées de 45 ans et plus: Pendant la ménopause, le contrôle des crises se détériore chez environ un quart des patients épileptiques. Parfois, le risque de crises augmente, en particulier chez les femmes présentant une sensibilité élevée aux fluctuations des hormones sexuelles et une dépendance de la fréquence des crises par rapport au cycle (épilepsies dites cataméniales). En conséquence, une intensification du traitement peut s’avérer nécessaire; il est avantageux que le spectre des médicaments antiépileptiques applicables puisse être entièrement épuisé ici.
La ménopause s’accompagne d’un risque accru d’ostéoporose, qui peut être aggravé par les anticonvulsivants et constitue un risque particulier en cas de crises accompagnées de chutes. L’hormonothérapie substitutive, qui est efficace en prophylaxie, augmente le risque de convulsions en raison des œstrogènes qu’elle contient; en conséquence, une dose plus élevée de traitement anticonvulsivant peut être nécessaire.
Cependant, l’incidence des fractures augmente considérablement, surtout avec l’utilisation d’inducteurs enzymatiques puissants et du valproate; un passage à des substances moins inducteurs enzymatiques est donc indiqué (par exemple, de la carbamazépine à des bloqueurs des canaux sodiques moins inducteurs enzymatiques tels que la lamotrigine, le lacosamide, l’oxcarbazépine ou l’acétate d’eslicarbazépine).
Aspects professionnels
Une performance professionnelle aussi peu altérée que possible est un objectif essentiel du traitement socio-médical. Si le fait d’obtenir un bon contrôle des crises et surtout d’éviter les crises graves et stigmatisantes ainsi que les troubles post-traumatiques prolongés y contribue évidemment, la tolérance cognitive, psychologique et motrice a également une importance considérable pour le maintien dans l’emploi. En particulier dans les activités intellectuelles, il faut donc éviter les substances sédatives (comme la carbamazépine, le phénobarbital) et les substances posant des problèmes cognitifs (le topiramate, dans certains cas également des doses plus élevées de zonisamide, les benzodiazépines et les barbituriques) et préférer les substances bien tolérées sur le plan cognitif (par exemple le brivaracétam/levetiracetam, le lacosamide, la lamotrigine, l’acétate d’eslicarbazépine, la prégabaline ou également le valproate).
Chez les patients ayant des exigences motrices élevées, les médicaments qui provoquent des tremblements (valproate, lacosamide, lamotrigine) ou qui entraînent une ataxie (en particulier les bloqueurs des canaux sodiques avec des pics plasmatiques tels que l’oxcarbazépine ou le lacosamide non retardé à dose élevée, à mon avis également le pérampanel dans certaines combinaisons) ne sont pas des médicaments de premier choix.
Les effets secondaires psychiatriques des médicaments antiépileptiques peuvent également être essentiels à l’intégration professionnelle. Les problèmes les plus fréquents sont les humeurs dépressives ainsi que l’irritabilité accrue, qui est fréquente avec le traitement par levetiracetam. Ces symptômes doivent faire l’objet d’une enquête active, et il est conseillé de changer de médicament avant que des conflits professionnels ne se développent.
La polythérapie et le rôle de la comédication
Avec le spectre croissant des médicaments antiépileptiques disponibles, la possibilité de les combiner se multiplie. Les règles de base importantes pour une thérapie combinée rationnelle sont les suivantes:
- Eviter les inducteurs enzymatiques en association avec les antiépileptiques à métabolisme hépatique (exemple: association défavorable de carbamazépine et de lamotrigine)
- Sélection de médicaments ayant des modes d’action différents afin d’obtenir au moins un effet additif et des effets secondaires sous-additifs
- Éviter les associations avec plus de deux antiépileptiques
- Observation de la dose totale et ajustement des doses individuelles afin de laisser la place au développement d’un médicament donné en plus.
Les interactions jouent également un rôle important dans l’utilisation de médicaments pour le traitement d’autres maladies. Les médicaments psychotropes revêtent une importance particulière chez les patients épileptiques; il faut tenir compte des interactions pharmacodynamiques indésirables avec l’amoxapine, le bupropion, la clomipramine et la maprotiline, et des interactions pharmacocinétiques avec la sertraline et la fluoxétine.
Comorbidités
Les comorbidités sont un aspect pertinent des épilepsies en fonction de l’âge et sont essentielles pour éviter les effets indésirables. Les maladies psychiatriques et internes jouent ici le plus grand rôle (fig. 7).
- En présence d’une dépression, les substances potentiellement dépressogènes doivent être évitées (barbituriques, phénytoïne, levetiracetam et avec restriction zonisamide).
- Les substances stabilisatrices de l’humeur telles que les bloqueurs des canaux sodiques, la gabapentine/prégabaline et le valproate sont particulièrement adaptées.
- L’utilisation du lévétiracétam et du pérampanel doit être évitée en cas de troubles psychotiques.
- Pour les troubles du sommeil, les substances qui améliorent la structure du sommeil (comme la prégabaline, avec restriction pérampanel) sont bénéfiques
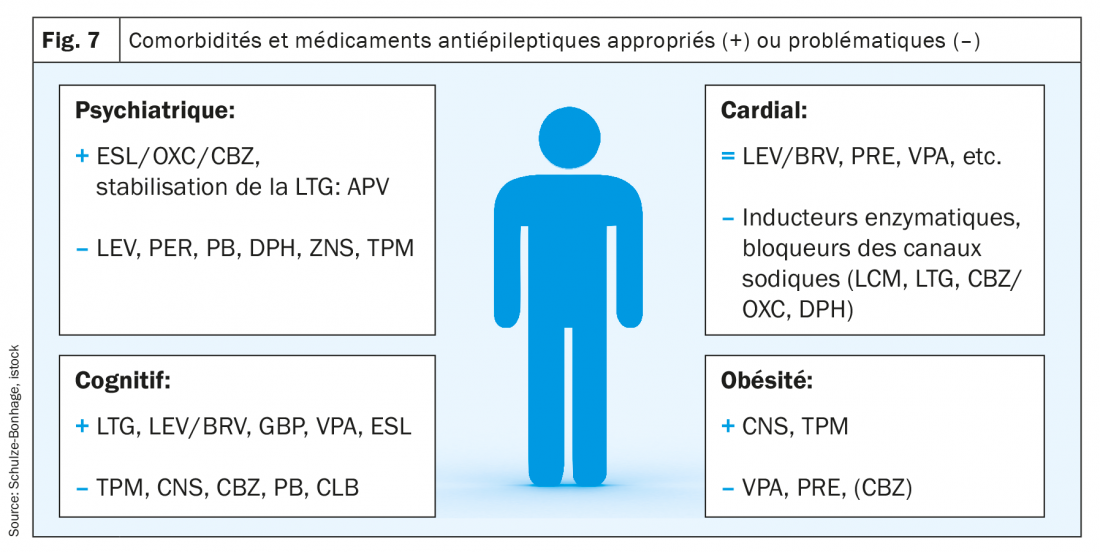
Le spectre des comorbidités internes possibles est large. Les plus fréquentes sont les suivantes:
- Conditions cardiaques préexistantes: Les inhibiteurs des canaux sodiques doivent être évités en cas d’arythmies cardiaques ou de troubles de la conduction ou doivent être surveillés par des enregistrements ECG s’ils sont utilisés
- En surpoids: Les médicaments antiépileptiques présentant un risque de développer un syndrome métabolique doivent être évités (en particulier le valproate, la prégabaline et la carbamazépine avec restriction)
- En cas d’insuffisance hépatique ou rénale, les substances à élimination alternative sont à privilégier.
Résumé
Le grand nombre d’antiépileptiques disponibles permet un choix de médicaments adapté à chaque patient. Divers aspects jouent un rôle à cet égard, comme le montre l’article. De nombreux médicaments récents offrent une bonne tolérance, même en cas d’utilisation prolongée, et des schémas posologiques favorables à l’observance. Un autre avantage de nombreux antiépileptiques modernes est un risque considérablement réduit d’interactions médicamenteuses, en particulier chez les patients âgés. Il est donc intéressant de ne pas travailler avec un régime médicamenteux fixe, mais d’utiliser un spectre d’antiépileptiques adapté au patient.
En règle générale, les inducteurs enzymatiques et les médicaments présentant un risque important d’effets secondaires tels que le valproate et les benzodiazépines doivent être évités. Des substances nouvellement développées telles que le brivaracétam, l’acétate d’eslicarbazépine et le lacosamide peuvent également être utilisées à un stade précoce du point de vue de leur meilleure tolérance, tandis que d’autres nouveaux développements très puissants tels que le pérampanel et le cenobamate* ouvrent de nouvelles perspectives pour les épilepsies difficiles à traiter.
* actuellement non encore approuvé en Suisse
Messages Take-Home
- L’absence ou la faible induction enzymatique des antiépileptiques de deuxième et troisième générations permet d’éviter les effets secondaires autrefois typiques des antiépileptiques tels que l’ostéoporose, les polyneuropathies et les syndromes métaboliques. Il s’agit du lacosamide, du lévétiracétam, de la prégabaline et d’autres antiépileptiques récemment mis au point comme le brivaracetam, l’acétate d’eslicarbazépine et le cenobamate.
- Pour les patients plus âgés, les bloqueurs des canaux sodiques avec peu ou pas d’induction enzymatique (lacosamide, lamotrigine, acétate d’eslicarbazépine) offrent une option importante.
- Les données de tératogénicité issues des registres de grossesse montrent que les risques les plus faibles sont liés aux traitements à faible dose de lamotrigine, de levetiracetam et d’oxcarbazépine.
- L’option de la dose unique pour l’acétate d’eslicarbazépine et le pérampanel est propice à l’observance.
- En particulier à partir de 50 ans, les antiépileptiques ayant un faible potentiel d’interaction, un effet neutre sur le métabolisme osseux et le métabolisme lipidique et de faibles effets cardiaques présentent des avantages.
Littérature:
- Rowan AJ, Ramsay RE, Collins JF, et al.: VA Cooperative Study 428 Group. New onset geriatric epilepsy: a randomized study of gabapentin, lamotrigine, and carbamazepine. Neurology 2005; 64: 1868–1873.
- Ley M, Principe A, Rocamora R: Efectos a largo plazo de las dibenzacepinas sobre los parámetros metabólicos: comparación retrospectiva de carbamacepina, oxcarbacepina y acetato de eslicarbacepina en el mundo real. Rev Neurol. 2020; 71: 54–60.
- Mintzer S, Dimova S, Zhang Y, et al.: Effects of lacosamide and carbamazepine on lipids in a randomized trial. Epilepsia. 2020; 61(12): 2696–2704.
Lectures complémentaires:
- Marson A, Burnside G, Appleton R, et al.: SANAD II collaborators. The SANAD II study of the effectiveness and cost-effectiveness of valproate versus levetiracetam for newly diagnosed generalised and unclassifiable epilepsy: an open-label, non-inferiority, multicentre, phase 4, randomised controlled trial. Lancet 2021; 397(10282): 1375–1386.
- Marson A, Burnside G, Appleton R, et al.: SANAD II collaborators. The SANAD II study of the effectiveness and cost-effectiveness of levetiracetam, zonisamide, or lamotrigine for newly diagnosed focal epilepsy: an open-label, non-inferiority, multicentre, phase 4, randomised controlled trial. Lancet 2021; 397(10282): 1363–1374.
- Marson AG, Al-Kharusi AM, Alwaidh M, et al.: SANAD Study group. The SANAD study of effectiveness of valproate, lamotrigine, or topiramate for generalised and unclassifiable epilepsy: an unblinded randomised controlled trial. Lancet 2007; 369(9566): 1016–1026.
- Marson AG, Al-Kharusi AM, Alwaidh M, et al.: SANAD Study group. The SANAD study of effectiveness of carbamazepine, gabapentin, lamotrigine, oxcarbazepine, or topiramate for treatment of partial epilepsy: an unblinded randomised controlled trial. Lancet. 2007; 369(9566): 1000–1015.
- Sake JK, Hebert D, Isojärvi J, et al.: A pooled analysis of lacosamide clinical trial data grouped by mechanism of action of concomitant antiepileptic drugs. CNS Drugs 2010; 24(12): 1055–1068.
- Schulze-Bonhage A: Epilepsien: Formen, Diagnostik und Therapie. Medizinische Monatsschrift für Pharmazeuten 2021, 44: 160–170
- Schulze-Bonhage A, Hintz M: Perampanel in the management of partial-onset seizures: a review of safety, efficacy, and patient acceptability. Patient Prefer Adherence 2015; 9: 1143–1151.
- Semah F, Picot MC, Adam C, et al.: Is the underlying cause of epilepsy a major prognostic factor for recurrence? Neurology 1998; 51: 1256–1262.