Les opioïdes forment un groupe pharmacologiquement hétérogène de substances synthétiques, semi-synthétiques et naturelles, dont la caractéristique commune est la liaison aux récepteurs opioïdes. Les récepteurs opioïdes du système nerveux central sont essentiels au déploiement des effets analgésiques. L’activation des récepteurs opioïdes présynaptiques dans la corne postérieure de la moelle épinière inhibe la transmission de l’influx douloureux.
Le terme opioïde est emprunté au grec et signifie “semblable à l’opium”. Les opioïdes forment un groupe pharmacologiquement hétérogène de substances synthétiques, semi-synthétiques et naturelles, dont la caractéristique commune est la liaison aux récepteurs opioïdes. Les récepteurs opioïdes se trouvent à la fois dans le système nerveux périphérique et central. Les récepteurs opioïdes du système nerveux central sont essentiels au déploiement des effets analgésiques. L’activation des récepteurs opioïdes présynaptiques dans la corne postérieure de la moelle épinière inhibe la transmission de l’influx douloureux. L’activation des récepteurs opioïdes dans certaines régions du tronc cérébral, provoquée par les opioïdes, entraîne une stimulation supplémentaire des voies nerveuses inhibitrices descendantes. Cela permet d’inhiber la transmission des signaux de douleur arrivant dans la corne postérieure. Dans les régions sous-corticales du système limbique, l’activation des récepteurs opioïdes entraîne une atténuation de la composante émotionnelle et affective de la perception d’une sensation douloureuse [1].
Le corps humain produit lui-même des opioïdes endogènes, qui sont libérés dans le cadre de réactions de stress et entraînent la suppression de la douleur et de la sensation de faim. Dans la pratique médicale, les opioïdes synthétiques sont en principe utilisés. Les différences pharmacodynamiques entre les différents opioïdes se manifestent par une affinité différente pour les récepteurs opioïdes ou pour les sous-types de récepteurs individuels. Dans la pratique clinique quotidienne, la connaissance précise de ces différences pharmacodynamiques aide à évaluer les effets attendus d’un opioïde donné.
Épidémiologie
L’enquête suisse sur la santé de 2017 a montré qu’en Suisse, environ 2,5 millions de personnes souffrent de douleurs chroniques. Environ 0,6 million de personnes souffrent de douleurs modérées à sévères, qui ont un effet limitant sur l’activité et la qualité de vie. Les femmes sont plus nombreuses à déclarer souffrir de douleurs chroniques [2].
Bien qu’il existe différentes approches thérapeutiques pour traiter la douleur, les opioïdes sont de plus en plus souvent prescrits, même en Suisse. L’utilisation d’opioïdes est parfaitement reconnue pour le traitement de la douleur aiguë sévère, par exemple dans le cadre périopératoire, et est généralement très utile. Les opioïdes représentent également souvent une option thérapeutique indispensable et reconnue dans le monde entier pour le traitement des douleurs liées aux tumeurs [3]. En revanche, les douleurs chroniques non cancéreuses constituent généralement une moins bonne indication pour un traitement prolongé par opioïdes. Il n’est pas certain que l’utilisation d’opioïdes à forte puissance se traduise par une amélioration du contrôle des douleurs chroniques non cancéreuses à moyen et long terme [4].
C’est précisément pour cette raison qu’il est inquiétant de constater que 85% de tous les opioïdes prescrits aujourd’hui sont utilisés pour traiter des douleurs non cancéreuses [5]. Environ 25% des patients concernés reçoivent les opioïdes prescrits pendant une durée >90 jours. Une utilisation à long terme pendant des années en est souvent la conséquence.
Taxonomie des mécanismes de la douleur
Un traitement pharmacologique adéquat et efficace de la douleur peut être atteint de la manière la plus fiable possible si les mécanismes d’apparition de la douleur sont délimités le mieux possible. Une anamnèse détaillée et un examen clinique ciblé sont fondamentaux pour identifier le mécanisme d’apparition de la douleur. En fonction de la situation, en cas de questions spécifiques, des examens radiologiques, de laboratoire et autres examens complémentaires sont utiles. Les mécanismes de douleur suivants doivent alors être identifiés ou exclus :
Douleur nociceptive : ce mécanisme est responsable du maintien de l’intégrité physique et est également compris comme une sensation de douleur “normale, habituelle”. Les signaux nociceptifs de la douleur permettent d’éviter les blessures. La douleur dépend du stimulus, elle est généralement de courte durée et les tissus stimulés restent intacts. La persistance d’un stimulus nociceptif peut entraîner des modifications neuronales au niveau de la corne postérieure de la moelle épinière. Ces changements sont généralement de courte durée et disparaissent. Des phénomènes de sensibilisation à la douleur persistants ne sont pas attendus.
Douleurs nociceptives-inflammatoires : lorsque les tissus sont déjà endommagés, des douleurs aiguës à subaiguës apparaissent. Les déclencheurs sont des médiateurs inflammatoires libérés (par exemple, les interleukines). D’une part, il y a une activation directe des terminaisons des fibres douloureuses périphériques, d’autre part, dans le cadre de ce processus, de nouvelles fibres douloureuses, jusqu’alors inactives, sont recrutées et sensibilisées en plus. Globalement, il y a un abaissement du seuil d’excitabilité électrophysiologique. Cela permet la formation de phénomènes de sensibilisation périphérique.
Douleurs neuropathiques : les douleurs neuropathiques se manifestent également de manière aiguë ou subaiguë. Cependant, la cause du signal de douleur n’est pas ici le tissu environnant, mais le système somatosensoriel lui-même [6]. Les lésions des cellules nerveuses elles-mêmes sont à la base des douleurs neuropathiques. Pratiquement toujours, il en résulte des phénomènes de sensibilisation périphériques et centraux. En règle générale, des phénomènes de sensibilisation “positifs” et/ou “négatifs” peuvent être documentés. Il existe souvent un écart important entre l’intensité de la douleur dont se plaint le patient, l’étendue de la zone touchée par la douleur et les résultats objectifs que l’examinateur peut constater.
L’hyperalgésie est un phénomène de sensibilisation important. Elle se produit à la fois dans les états douloureux d’origine neuropathique et inflammatoire. L’hyperalgésie peut être définie comme un état pendant lequel un stimulus normalement légèrement douloureux est perçu comme excessivement douloureux (p. ex. piquer avec un cure-dent). L’allodynie est un autre phénomène de sensibilisation “positif” et constitue une forme d’aggravation de l’hyperalgésie. Dans une zone cutanée touchée par l’allodynie, un stimulus en principe indolore est perçu comme douloureux (par exemple, le contact avec un pinceau).
Douleurs nociplastiques : les douleurs nociceptives/inflammatoires et les douleurs neuropathiques sont en fin de compte des entités définies de manière mécanique. La différence essentielle est que dans le cadre des états douloureux nociceptifs, il existe un fonctionnement normal du système somatosensoriel, alors que c’est précisément ce système qui est endommagé dans les états douloureux neuropathiques. De nombreux patients souffrant de douleurs chroniques ne peuvent être classés avec certitude dans aucune de ces entités [7]. Chez ces patients, on ne peut supposer ni l’activation de nocicepteurs ni une lésion du système somatosensoriel. Dans de tels cas, il s’agit d’une problématique de douleur nociplastique. Un large groupe de patients est concerné : Douleurs dorsales non spécifiques, douleurs non spécifiques dans les articulations périphériques, fibromyalgie, syndrome de douleur régionale complexe (CRPS) de type 1.
Superposition des mécanismes de la douleur/”Mixed Pain” : très souvent, chez les patients souffrant de douleurs chroniques, on peut constater/supposer une superposition des mécanismes de la douleur mentionnés ci-dessus. En cas de “douleur mixte”, tous les mécanismes décrits ci-dessus sont souvent impliqués dans l’apparition ou la modulation du signal de douleur. En général, l’un ou l’autre des mécanismes de la douleur est au premier plan.
Les opioïdes jouent un rôle important dans le traitement des douleurs nociceptives, mais peuvent également contribuer à un bon contrôle de la douleur dans le cas des douleurs neuropathiques. Dans le cas d’états douloureux d’origine nociplastique, la valeur thérapeutique des opioïdes est généralement inexistante.
Les 4 piliers de l’analgésie
Pour obtenir un traitement analgésique aussi satisfaisant que possible, il est essentiel d’identifier les mécanismes de douleur et de sensibilisation présentés ci-dessus. Indépendamment de la modalité thérapeutique, un traitement ciblé des états douloureux, ou l’obtention d’une “analgésie”, repose donc sur les quatre piliers suivants : “antinociception”, “anti-inflammation”, “antihyperalgésie” et “antineuropathie” [8].
Dans le cadre d’un traitement analgésique pharmacologique, il est donc crucial d’utiliser des médicaments d’une ou de plusieurs classes de substances qui peuvent couvrir autant que possible l’ensemble du spectre des mécanismes de la douleur diagnostiqués.
Mesures recommandées avant de commencer un traitement de la douleur par un opioïde
La question de savoir si une tentative de traitement par un analgésique opioïde est utile ou non doit être soigneusement évaluée conjointement par le médecin et le patient. Le fait de savoir si des opioïdes à faible ou à forte puissance doivent être utilisés ne joue qu’un rôle secondaire. Les points suivants doivent être spécifiquement pris en compte [9] :
- Les mécanismes d’apparition sous-jacents à la problématique de la douleur doivent être recherchés et identifiés de manière ciblée.
- Il est recommandé de procéder à une anamnèse psychosociale plus précise et à un dépistage de la présence d’influences d’origine psychologique sur la problématique de la douleur.
- Dans la mesure du possible, les douleurs chroniques non cancéreuses ne devraient jamais être traitées exclusivement par des opioïdes. Les données scientifiques indiquent que les opioïdes ne sont pas plus efficaces que les autres analgésiques pour le traitement de la douleur chronique non cancéreuse.
- Avant d’envisager un traitement de la douleur par opioïdes, il convient donc d’avoir déjà pris ou au moins essayé diverses autres mesures thérapeutiques (physiques, physiothérapeutiques, médicamenteuses, interventionnelles, psychologiques).
- Des objectifs thérapeutiques raisonnables et réalisables doivent être élaborés avec le patient. L’accent doit être mis sur des objectifs tels qu’une réduction de la douleur d’au moins 30%, la reprise du travail ou l’exécution de tâches quotidiennes, par exemple les tâches ménagères.
- Les patients doivent être informés en détail des risques potentiels qui peuvent survenir dans le cadre d’un traitement à long terme par opioïdes. Outre les effets secondaires connus tels que la constipation, la sécheresse de la bouche, les nausées, les malaises, les états confusionnels, les chutes, il convient également d’attirer l’attention sur la dépression respiratoire potentiellement mortelle qui peut résulter d’une erreur ou d’un surdosage.
- Les patients doivent être informés qu’un traitement par opioïde entraîne généralement une dépendance physique.
- Il faut s’abstenir de conduire ou d’utiliser des machines pendant les 1 à 2 premières semaines de traitement, pendant la phase d’ajustement, lors d’une augmentation de la dose ou lors du passage à un autre opioïde. Pendant cette période, les effets secondaires sont fréquents et limitent la capacité de réaction.
Quand peut-on envisager un traitement à long terme >120 jours avec des opioïdes ?
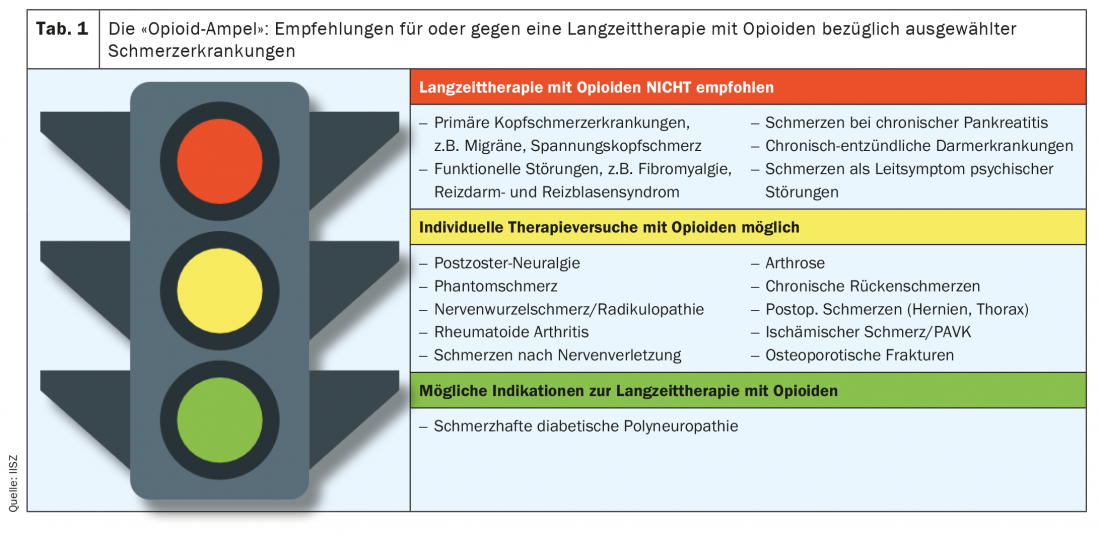
Le principe est que les opioïdes ne doivent être utilisés pour le traitement à long terme (>120 jours) d’un état douloureux chronique que si le patient concerné a pu enregistrer une réduction significative de la douleur et/ou une amélioration de son état général au cours d’un traitement probatoire de 4 à 12 semaines. En outre, les directives nationales et internationales devraient être prises en compte dans la réflexion sur l’indication. Une ressource recommandée est par exemple la directive sur “l’utilisation à long terme des opioïdes dans les douleurs chroniques non tumorales (LONTS)” [9] de la Société allemande de la douleur. Actuellement, un traitement à long terme avec un opioïde n’est recommandé qu’en présence d’une polyneuropathie diabétique douloureuse. En revanche, dans le cas de plusieurs autres affections douloureuses chroniques, il est même concrètement déconseillé de suivre un traitement à long terme par opioïdes (voir également le tableau 1).
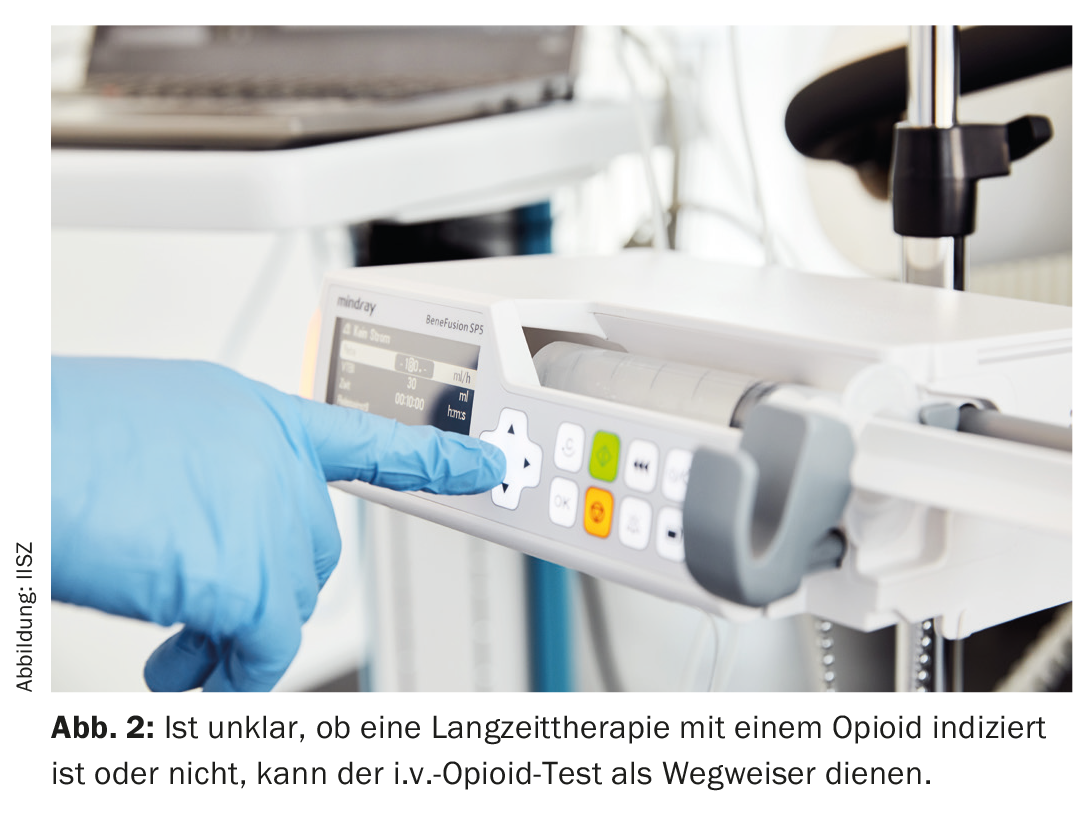
En cas de doute : le test i.v. aux opioïdes pour vous guider
En cas d’incertitude sur l’opportunité de poursuivre un traitement de la douleur par opioïdes pendant plus de 12 semaines, un test aux opioïdes par voie intraveineuse (i.v.) réalisé en ambulatoire peut s’avérer utile [10] (fig. 2). De tels tests sont proposés en Suisse par différents centres de médecine de la douleur. L’administration i.v. protocolisée d’un opioïde à action ultra-courte permet généralement de déterminer si une affection douloureuse peut être traitée efficacement par un opioïde ou non.
Opioïdes à courte durée d’action vs. opioïdes à longue durée d’action
Pour le traitement des douleurs chroniques, il convient d’utiliser autant que possible des préparations à galénique retardée ou à longue durée d’action. La prise doit se faire selon un schéma fixe. L’expérience montre qu’il est ainsi possible d’obtenir un meilleur contrôle de la douleur et une meilleure adhésion au traitement. En outre, cette approche permet de réduire le risque de complications.
Les opioïdes à courte et ultra-courte durée d’action ne doivent être utilisés qu’exceptionnellement dans le cadre du traitement des douleurs chroniques non tumorales. Ils ne sont pas non plus recommandés comme médicaments à la demande. L’expérience clinique montre que les opioïdes à courte durée d’action peuvent également entraîner rapidement une dépendance psychique. Malheureusement, il en résulte souvent une utilisation abusive.
Résultats d’un traitement à long terme par opioïdes
Les preuves scientifiques actuellement disponibles pour évaluer l’efficacité d’un traitement par opioïdes >120 jours pour les douleurs chroniques non tumorales sont insuffisantes. Cela implique automatiquement des chances de succès incertaines [11].
Dans le cadre d’une utilisation chronique d’opioïdes, il n’est pas rare que la médication opioïde utilisée perde de son efficacité. Il existe plusieurs diagnostics différentiels qui peuvent expliquer cette évolution. Même dans le cas de douleurs chroniques non tumorales, il peut y avoir une progression de la maladie qui entraîne une aggravation du problème de la douleur. Cependant, il arrive souvent que les traitements chroniques aux opioïdes entraînent le développement d’une tolérance avec une diminution consécutive de l’effet analgésique de l’opioïde utilisé. On pense que la cause est une migration des récepteurs opioïdes de la surface cellulaire vers l’intérieur de la cellule, de sorte qu’ils ne sont plus disponibles pour l’effet analgésique. L’hyperalgésie induite par les opioïdes est un autre phénomène qui peut se produire dans le cadre d’une augmentation de la douleur sous un traitement en cours avec des opioïdes. Les mécanismes d’apparition d’une hyperalgésie induite par les opioïdes sont multiples et vont d’une régulation négative des récepteurs opioïdes à une potentialisation synaptique à long terme, en passant par une éventuelle sensibilisation centrale.
Effets indésirables de l’utilisation à long terme
L’utilisation à long terme d’opioïdes peut entraîner les effets indésirables suivants :
- perte du désir sexuel
- Impuissance
- Troubles du cycle menstruel chez la femme
- Augmentation de la mortalité globale
- Passivité/absence de motivation
- Troubles de la mémoire
- Risque accru de chute
Quand faut-il arrêter un traitement opioïde à long terme ?
Un traitement à long terme par un opioïde doit être réévalué périodiquement. Si l’on ne sait pas si le traitement par un opioïde permet de soulager la douleur, il faut s’efforcer d’arrêter ce traitement. Il est recommandé d’arrêter progressivement un traitement par un opioïde lorsque
- pendant la phase d’ajustement (4 à 12 semaines), les objectifs thérapeutiques fixés individuellement n’ont pas été atteints et/ou des effets secondaires significatifs sont apparus.
- une perte d’efficacité de l’opioïde utilisé est constatée au cours du traitement et ne peut être évitée par une adaptation modérée de la dose ou le passage à un autre opioïde.
- des indices de mésusage apparaissent en cours de traitement (augmentation de la dose de son propre chef, prescription par plusieurs médecins).
Conclusion
Les opioïdes constituent l’une des principales classes de substances utilisées pour traiter les douleurs intenses. Ils ne sont jamais utilisés comme option de première ligne et doivent toujours être accompagnés de mesures non médicamenteuses. Un traitement à long terme n’est mis en place que pour les patients répondeurs au traitement, dont l’effet doit être régulièrement évalué par la définition et le suivi d’objectifs thérapeutiques. Un traitement non fonctionnel par opioïdes doit être arrêté à temps.
Take-Home-Messagess
- Avant de commencer un traitement pharmacologique de la douleur en général, et un traitement par opioïdes en particulier, il est nécessaire de délimiter le mécanisme sous-jacent de la douleur.
- Les opioïdes sont souvent le traitement de choix des douleurs aiguës sévères et tumorales.
- En revanche, le traitement à long terme des douleurs chroniques non tumorales doit être exceptionnel et, dans la mesure du possible, associé à des mesures non médicamenteuses.
- Un traitement à long terme par opioïdes doit être axé sur des objectifs mesurables. Si ces objectifs ne sont pas atteints, le traitement opioïde doit être suspendu.
- Dans le cadre d’un traitement à long terme avec des opioïdes, une dépendance physique se développe toujours, qui est parfois accompagnée d’une composante psychique, au sens d’une addiction.
Littérature :
- Ossipov MH, Dussor GO, Porreca F : Modulation centrale de la douleur. J Clin Invest 2010 ; 120 : 3779-3787.
- Enquête suisse sur la santé 2017, Santé et genre, Office fédéral de la statistique, numéro OFS 213-1718. 2020.
- Wertli MM, Steurer J : In Process Citation. Pratique 2015 ; 104(11) : 541-542.
- Breivik H, Stubhaug A : La charge de la maladie est souvent aggravée par le traitement opioïde des patients souffrant de douleurs chroniques : étiologie et prévention. PAIN 2014 ; 155(12) : 2441-2443.
- Wertli M, Held U, Signorell A, et al. : Analyse de l’évolution des pratiques de prescription des médicaments contre la douleur et du sommeil entre 2013 et 2018 en Suisse. Hôpital universitaire de Berne 2020.
- Jensen T, Baron R, et al : Une nouvelle définition de la douleur neuropathique. Douleur 2011 ; 152 : 2204-2205.
- Trouvin AP, Perrot S : New concepts of pain. Best Practice & Research Clinical Rheumatology 2019 ; 33(3).
- Maurer K : Thérapie par étapes pratique pour le médecin généraliste. Le médecin informé 2017.
- Utilisation à long terme des opioïdes dans les douleurs chroniques non tumorales (LONTS), 2e mise à jour 2020 ; AWMF-Leitlinien-Register Nr. 145/003.
- Gustorff B : Test de dépistage des opioïdes par voie intraveineuse chez les patients souffrant de douleurs chroniques non cancéreuses. Eur J Pain 2005 ; 9(2) : 123-125.
- Chou R, Turner JA, et al : The Effectiveness and Risks of Long-Term Opioid Therapy for Chronic Pain : A Systematic Review for a National Institutes of Health Pathways to Prevention Workshop. Ann Int Med 2015 ; doi : 10.7326/M14-2559.
InFo DOULEUR & GERIATRIE 2021 ; 3(1) : 10-14