“Nous ne sommes pas nos gènes !” Avec cette déclaration, le professeur Katharina Domschke de Fribourg a souligné l’importance des influences environnementales – et la manière dont elles façonnent notre santé mentale par le biais de processus épigénétiques. Ce mécanisme est particulièrement important dans les maladies anxieuses et pourrait ouvrir la voie à de nouvelles options thérapeutiques.
L’un des points forts du symposium anniversaire de la Société suisse pour l’anxiété et la dépression (SSAD) de cette année a été la conférence du professeur Katharina Domschke, directrice médicale de la clinique de psychiatrie et de psychothérapie de l’hôpital universitaire de Fribourg (D). Elle a attiré l’attention sur la dimension épigénétique des troubles anxieux. En effet, les maladies anxieuses sont en grande partie déterminées par nos gènes.
Fréquents, contraignants et coûteux
Les troubles anxieux représentent les maladies les plus fréquentes dans le domaine neuropsychiatrique, avec 14% de personnes touchées dans toute l’Europe. Ils sont deux fois plus fréquents que la dépression unipolaire ou l’insomnie, qui constituent les groupes suivants en termes de fréquence. En raison de leur forte chronicité, les troubles anxieux sont également des maladies très coûteuses : Après les troubles affectifs, la démence et les maladies psychotiques, les maladies anxieuses se classent au 4e rang en termes de coût . Elles sont également très coûteuses. Cette charge pour les personnes concernées, leurs proches ainsi que le système de santé est d’autant plus lourde que les maladies anxieuses entraînent souvent des maladies psychiques et/ou somatiques. Ainsi, l’anxiété prédispose de manière hautement significative au développement ultérieur d’un épisode dépressif ou d’un trouble dépressif [1].
L’épigénétique, interprète entre l’environnement et la génétique
Dans ce contexte, la compréhension de l’étiologie revêt une grande importance. Les troubles anxieux sont polygéniques, c’est-à-dire qu’ils sont formés par un grand nombre de gènes. 30 à 60% des patients présentent déjà une prédisposition génétique à l’anxiété. Cependant, cette prédisposition ne détermine pas directement l’expression de la maladie, mais plutôt un enchaînement de facteurs : l’altération des systèmes de neurotransmetteurs et des réseaux neuronaux, certaines attitudes psychophysiologiques (par exemple,la sensibilité au CO2 et les réactions physiologiques correspondantes), ainsi que des facteurs environnementaux tels que les toxines, les traumatismes et les événements de la petite enfance ou prénataux (Fig. 1).

L’épigénétique joue le rôle d’intermédiaire entre les facteurs environnementaux et la génétique. Ceci est très pertinent pour la psychiatrie, qui se base sur le modèle de vulnérabilité au stress. Ce modèle part du principe que la vulnérabilité individuelle est déterminée génétiquement et par des facteurs environnementaux déclencheurs. L’épigénétique joue en quelque sorte le rôle d'”interprète” entre le niveau des facteurs environnementaux et celui de la génétique. L’épigénétique désigne les processus biochimiques qui modifient la fonction de certains gènes en altérant l’ADN et sa structure spatiale. “Cela va à l’encontre du modèle déterministe”, explique le professeur Domschke. “Certes, nous sommes en partie déterminés par nos gènes, mais : nous ne sommes pas nos gènes”. Les gènes peuvent donc être modifiés par l’épigénétique – mais comment ?
Comment l’épigénétique façonne notre santé
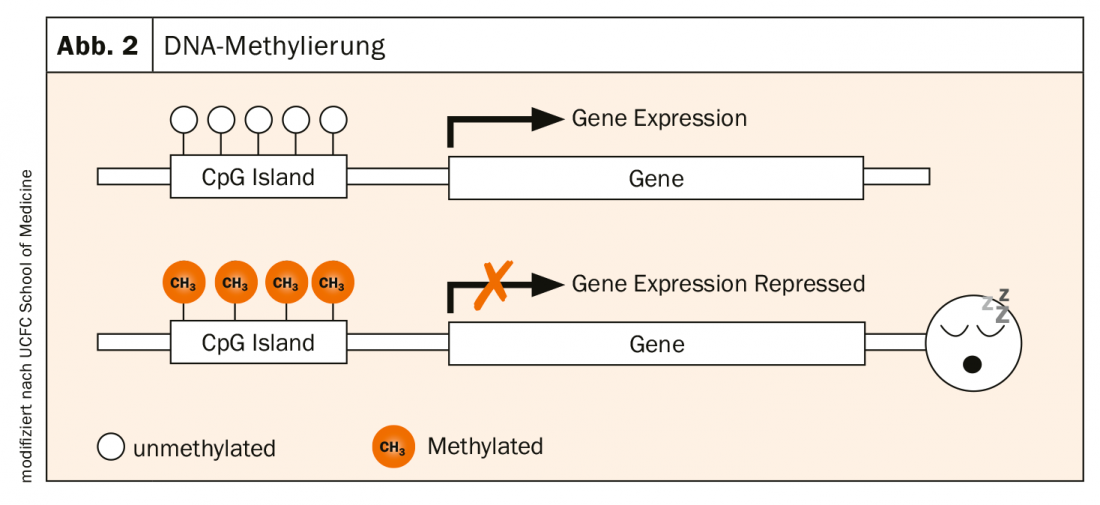
L’activité des gènes est déterminée par différents processus. L’un d’entre eux, très central, est la méthylation de l’ADN : la fixation enzymatique de groupes méthyle (-CH3) sur les bases nucléiques (îlots CpG) de l’ADN. Il s’agit d’une modification naturelle due à l’influence de l’environnement. Les îlots CpG sont souvent présents dans la région promotrice des gènes. Si cette région n’est pas méthylée, le gène est actif et peut être supprimé. S’il est méthylé, c’est-à-dire qu’un groupe CH3 s’y fixe, le gène concerné n’est plus exprimé. Il “dort” (ill. 2).
La monoamine oxydase A (MAOA) est un gène à risque pour les troubles anxieux et la dépression. Elle dégrade la sérotonine, la noradrénaline et la dopamine. Cette enzyme est bien connue dans la pratique quotidienne grâce à l’utilisation d’inhibiteurs de la MAO. Dans une étude, le professeur Domschke et ses collègues ont montré que la méthylation de la MAOA entraîne une diminution de la fonction du gène – une constatation importante pour le traitement de maladies liées à l’activité de ce gène [2]. Cette méthylation périphérique a un impact sur les processus neuronaux : Plus la méthylation périphérique de la MAOA est faible, plus l’activité de la MAOA dans le cerveau est élevée. Domschke et ses collègues ont ainsi trouvé une corrélation entre l’hypométhylation du promoteur MAOA et le trouble panique [3]. Ainsi, la méthylation de la MAOA semble être un biomarqueur de l’anxiété et de la dépression.
Le professeur Domschke et ses collègues ont mené une étude de six semaines pour déterminer si l’épigénétique pouvait également aider à prédire la réponse au traitement. Ils ont comparé la réponse à l’administration d’ISRS chez des patients présentant une méthylation élevée de la MAOA vs. des patients présentant une méthylation faible de la MAOA. Il est apparu que les patients présentant une méthylation élevée de la MAOA répondaient nettement mieux aux ISRS. Des études supplémentaires sont encore nécessaires pour mieux comprendre le mécanisme. Mais une conséquence pratique de cette découverte pourrait être que les patients qui ont déjà une faible méthylation de la MAOA devraient être traités avec un IRSN ou un inhibiteur de la MAOA plutôt qu’un ISRS.
Prévenir les maladies mentales grâce à l’épigénétique ?
“Mais ce qui est passionnant, ce n’est pas seulement ce mécanisme pathogénétique-fonctionnel, c’est qu’il y a une bidirectionnalité”, souligne le professeur Domschke. “La génétique est immuable. Mais l’épigénétique, la méthylation, est dynamique. Elle répond aux influences de l’environnement”. Les événements de la vie perçus subjectivement de manière négative contribuent à une réduction de la méthylation de la MAOA. Les traumatismes peuvent donc conduire à un statut de risque épigénétique. La bonne nouvelle à l’inverse : les événements positifs ont été corrélés positivement avec la méthylation de la MAOA. Les mesures favorisant la résilience peuvent contribuer à la prophylaxie des maladies mentales (fig. 3).
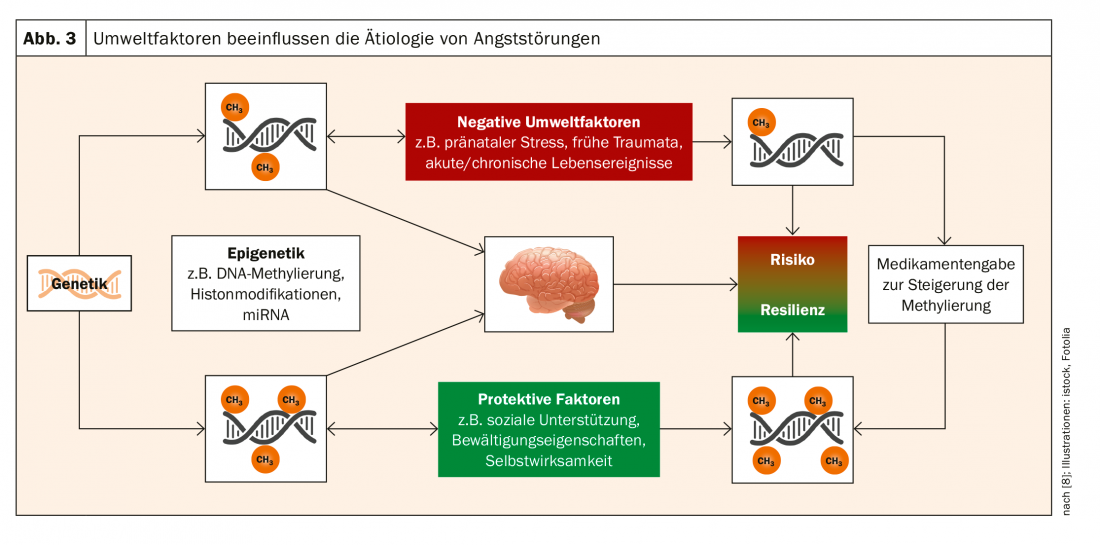
Dans ce contexte, le rôle de la psychothérapie a également été étudié. Il s’est avéré que la psychothérapie conduisait également à une normalisation de la méthylation et donc à une amélioration des symptômes. A moyen terme, une compréhension épigénétique des mécanismes d’action de la psychothérapie pourrait permettre de l’augmenter par des médicaments qui élèveraient les patients à faible méthylation MAOA au niveau des patients à méthylation élevée, selon le professeur Domschke.
Dans l’ensemble, l’épigénétique représente, en l’état actuel des connaissances, une possibilité de prédire la réponse individuelle au traitement dans le sens d’une pharmacothérapie personnalisée et d’expliquer – éventuellement – les mécanismes d’action de la psychothérapie.
Quelles sont les nouveautés en matière de pharmacothérapie ?
Les phobies spécifiques ne sont pas traitées par des médicaments, mais par une thérapie cognitivo-comportementale. Pour la phobie sociale, le trouble panique et le trouble anxieux généralisé, les ISRS et les IRSN sont le traitement de choix. Selon une étude publiée en 2017, l’agomélatine semble efficace non seulement dans la dépression, pour le traitement de laquelle elle est autorisée, mais aussi dans le traitement du trouble anxieux généralisé [4]. Off-label, l’agomélatine constitue donc un bon complément. La quétiapine, autorisée dans la schizophrénie et le trouble bipolaire, a également montré une efficacité significative en monothérapie dans le traitement du trouble anxieux généralisé [5]. L’extrait d’huile de lavande, indiqué dans l’anxiété et les troubles de l’humeur, s’est également révélé efficace dans le traitement des troubles anxieux généralisés lors d’études [6].
Un mot encore sur la prégabaline : alors que cette substance a une efficacité évidente et donc une évidence Ia, elle est soupçonnée de créer une dépendance. C’est pourquoi il n’existe actuellement qu’une recommandation B pour la prégabaline. Il en va de même pour la gabapentine. Il convient toutefois de noter que ces substances présentent le risque le plus faible par rapport à d’autres agents présentant un potentiel de dépendance. De plus, la dépendance aux gabapentinoïdes est régulièrement associée à d’autres dépendances, notamment l’opiomanie et la politoxicomanie. Il en résulte que ni la prégabaline ni la gabapentine ne devraient être abandonnées dans le traitement, sauf dans le traitement des personnes déjà dépendantes. Il convient plutôt d’éviter l’administration de benzodiazépines. Les (endo)cannabinoïdes, dont il est question de toutes parts, ne disposent actuellement pas de preuves suffisantes, de sorte qu’ils ne constituent pas non plus une option de traitement.
Source : 10e Forum suisse des troubles de l’humeur et de l’anxiété
Littérature :
- Meier SM, et al : Secondary depression in severe anxiety disorders : a population-based cohort study in Denmark. Lancet Psychiatry 2015 ; 2(6) : 515-523.
- Ziegler C, Domschke K : Signature épigénétique des gènes MAOA et MAOB dans les troubles mentaux. J Neural Transm 2018 ; 125(11) : 1581-1588.
- Domschke K, et al : Hypométhylation de l’ADN du gène de la monoamine oxydase A – un facteur de risque pour les troubles paniques ? Int J Neuropsychopharmacol 2012 ; 15(9) : 1217-1228.
- Stein DJ, et al. : Efficacité et sécurité de l’agomélatine (10 ou 25 mg/jour) chez les out-patients non déprimés souffrant de trouble anxieux généralisé : une étude de 12 semaines, en double aveugle, contrôlée par placebo. Eur Neuropsychopharmacol 2017 ; 27(5) : 526-537.
- Maneeton N, et al : Quétiapine monothérapie dans le traitement aigu du trouble anxieux généralisé : une revue systématique et méta-analyse des essais contrôlés randomisés. Drug Des Devel Ther 2016 ; 10 : 259-276.
- Kasper S, et al : La préparation d’huile de lavande Silexan est efficace dans le trouble anxieux généralisé – une comparaison randomisée, en double aveugle avec le placebo et la paroxétine. Int J Neuropsychopharmacol 2014 ; 17(6) : 859-869.
- Domschke K : Facteurs prédictifs dans les troubles anxieux. Neurologue 2014 ; 85(10) : 1263-1268.
- Ziegler C, Schiele M, Domschke K : Épigénétique pathologique et thérapeutique des maladies mentales. Neurologue 2018 ; 89 : 10.1007/s00115-018-0625-y.
InFo NEUROLOGIE & PSYCHIATRIE 2019 ; 17(3) : 24-29











