En raison de la fuite immunitaire des souches du SRAS-CoV-2, la recherche d’agents antiviraux à large spectre reste un objectif de recherche important. Une étude publiée en 2023 montre qu’un phytopharmaceutique à base de Pelargonium sidoides améliore l’évolution de la maladie chez les hamsters infectés par le SRAS-CoV-2. En outre, des effets antiviraux contre les variantes Delta AY.4 et Omicron BA.2 ont été démontrés dans les cellules épithéliales nasales et bronchiques humaines.
L’utilisation de l’extrait de Pelargonium sidoides EPs® 7630 s’est avérée être une option thérapeutique efficace et sûre pour les infections respiratoires aiguës. Les études de culture cellulaire indiquent que l’EPs® 7630 présente une activité contre le SRAS-CoV-2 comparable à celle contre d’autres virus respiratoires. Dans une étude in vitro publiée en 2021, Papies et al. de démontrer les propriétés antivirales et immunomodulatrices de l’EPs® 7630 dans des cellules pulmonaires humaines infectées par le SRAS-CoV-2 [1]. Afin d’en savoir plus sur les propriétés de l’EPs® 7630 et de ses composants fonctionnellement pertinents en relation avec les différents variants phénotypiques du SRAS-CoV-2, Emanuel et al. a mené une autre étude préclinique [2]. D’une part, ils ont utilisé un modèle animal – les études expérimentales sur le hamster syrien sont considérées comme un modèle reconnu pour l’analyse des mécanismes pathologiques du Covid-19 – et d’autre part, ils ont analysé les effets du traitement dans un modèle humain in vitro [2,3].
Effets de l’EPs® 7630 sur les hamsters infectés par le SRAS-CoV-2
Pour le premier groupe expérimental, une stratégie de prétraitement prophylactique a été utilisée, dans laquelle les hamsters ont reçu un traitement oral deux fois par jour à une dose de 50 mg/kg de poids corporel d’EPs® 7630, en commençant 24 heures avant l’infection [2]. Pour le deuxième groupe expérimental, une stratégie de traitement combinée par voie orale (p.o.) et intranasale (i.n.) a été utilisée, de sorte que les hamsters ont reçu EPs® 7630 par voie intranasale à raison d’une dose unique de 5 mg/kg de poids corporel contenant l’inoculum viral, en plus de la dose orale (50 mg/kg deux fois par jour à partir du moment de l’infection). Le groupe témoin a également été infecté par le SRAS-CoV-2 et a reçu un véhicule sans EPs® 7630.
La réplication du virus dans les voies respiratoires inférieures a été retardée : le groupe traité uniquement par voie orale et le groupe traité par voie orale et injectable ont tous deux présenté une réduction d’environ dix fois des unités formant la plaque (PFU) du SRAS-CoV-2 le deuxième jour après l’infection, par rapport aux témoins traités par le véhicule [2]. Deux jours après l’infection, les deux groupes expérimentaux EPs® 7630 ont montré une réduction statistiquement significative des titres viraux et de l’ARN viral du SRAS-CoV-2 dans les voies respiratoires inférieures, avec des effets légèrement plus prononcés dans le groupe traité par voie orale plus i.n.
Début retardé de la pneumonie : l’histopathologie pulmonaire (tissu des poumons gauches inclus dans la paraffine ; coloration à l’hématoxyline-éosine) a été réalisée pour déterminer si le traitement par EPs® 7630 entraînait également une modification de la pathologie Covid-19 [2].
- Quatre jours après l’infection, les hamsters traités avec EPs® 7630 présentaient significativement moins de surfaces pulmonaires montrant des signes de pathologie que les témoins traités avec le véhicule.
- Les hamsters traités avec Vehicle ont présenté un pic de bronchite 2 jours après l’infection, tandis que les hamsters traités avec EPs® 7630 n’ont présenté un pic que 4 jours après l’infection.
- Les hamsters traités p.o. et i.n. avec EPs® 7630 avaient un score de pneumonie significativement plus bas 4 jours après l’infection, mais des scores comparables à ceux des témoins 7 jours après l’infection, ce qui suggère un retard de début de pneumonie médié par EPs® 7630.
- Les hamsters traités avec EPs® 7630 ont présenté un œdème pulmonaire nettement moins important que les témoins traités avec le véhicule 4 jours après l’infection. Cela a été le plus marqué dans le groupe de traitement combiné par voie orale et injectable.
Propriétés antivirales de l’EPs® 7630 dans les cellules épithéliales humaines
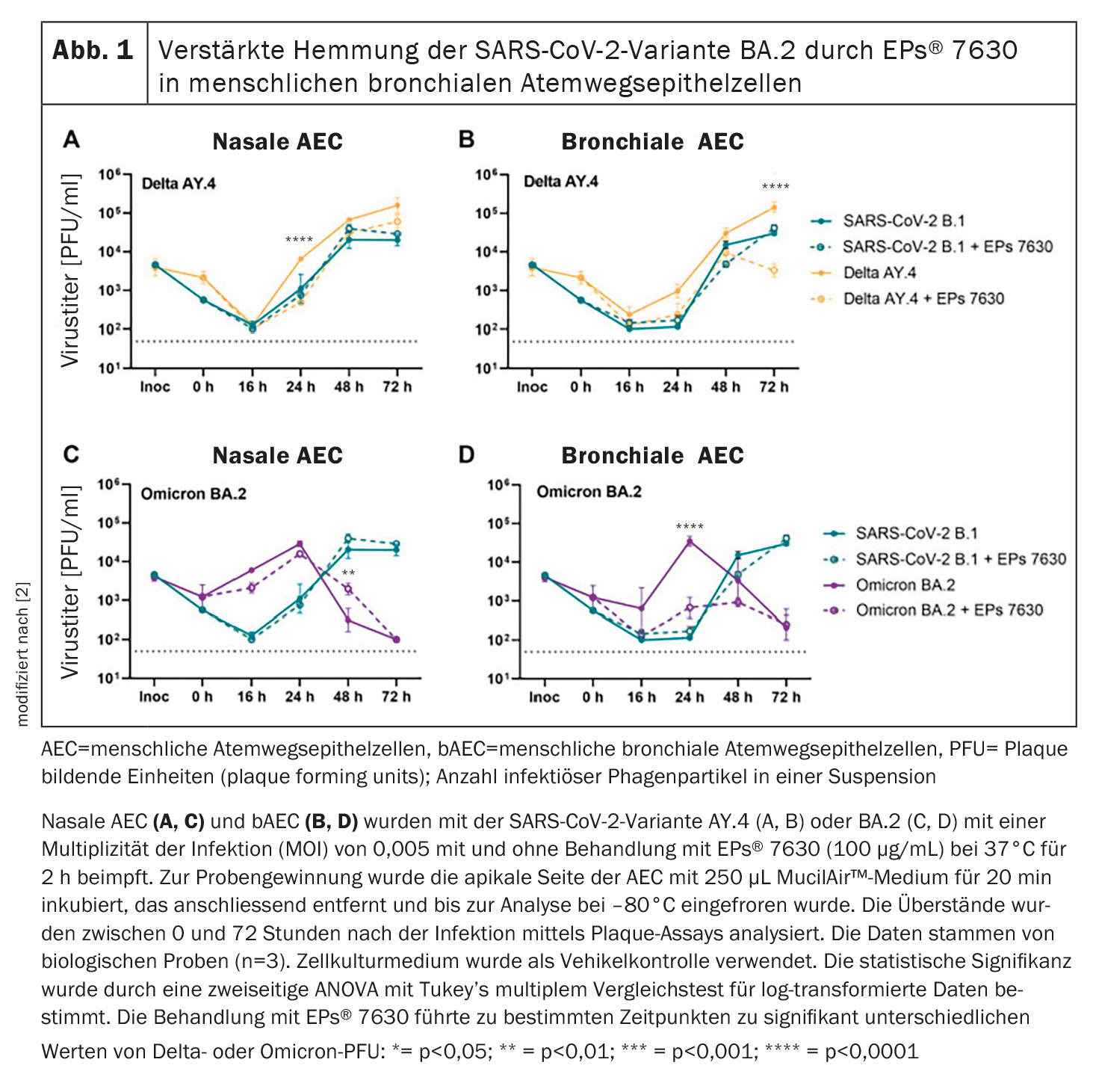
Dans les cellules épithéliales nasales et bronchiques humaines, EPs® 7630 inhibe différemment les variants du SRAS-CoV-2 [2]. Des effets antiviraux significatifs ont été observés contre Delta AY.4 et Omicron BA.2 à la fois dans les cellules épithéliales nasales et bronchiques humaines (AEC), ce qui indique un effet antiviral spécifique à la variété. (Fig. 1). Selon les auteurs de l’étude, il semble plausible que l’efficacité thérapeutique de l’EPs® 7630 repose sur une combinaison d’inhibition de l’entrée virale et d’effets anti-inflammatoires directs. Ceci est également en accord avec les effets positifs de l’EPs® 7630 observés dans d’autres infections respiratoires dans des cadres cliniques [4–7].
De plus, il a été démontré qu’au moins deux composants moléculaires de l’EPs® 7630, à savoir la (-)-épigallocatéchine et la (+)-taxifoline, exercent des effets antiviraux sur la réplication du SRAS-CoV-2 et l’entrée dans les cellules. En outre, il s’est avéré que le mécanisme par lequel l’épigallocatéchine bloque le SARS-CoV-2 dépend du variant du SARS-CoV. L’épigallocatéchine et son composant, l’épigallocatéchine gallate, ont montré une plus forte inhibition à l’entrée contre Omicron BA.2 par rapport à B.1 et Delta AY.117. Cela correspond à l’activité antivirale accrue de l’EPs® 7630 ou des deux ingrédients susmentionnés contre Omicron BA.2 (Fig. 1).
Littérature :
- Papies J, et al. : Effets antiviraux et immunomodulateurs du Pelargonium sidoides DC. Root Extract EPs® 7630 dans des cellules pulmonaires humaines infectées par le SRAS-CoV-2. Front Pharmacol 2021 ; 12 : 757666. doi : 10.3389/fphar.2023.1214351
- Emanuel J, et al. : Effets in vitro et in vivo de l’extrait de racine de Pelargonium sidoides DC. EPs® 7630 et de ses constituants sélectionnés contre le SARS-CoV-2 B.1, Delta AY.4/AY.117 et Omicron BA.2. Front Pharmacol 2023 Jul 26 ; 14 : 1214351.
- Osterrieder N, et al. : Progression de l’infection par le SRAS-CoV-2 chez les hamsters syriens en fonction de l’âge. Viruses 2020 ; 12 : 779. 10.3390/v12070779
- Kamin W, et al. : Efficacité et tolérance de EPs 7630 chez les enfants et adolescents atteints de bronchite aiguë – essai multicentrique randomisé, en double aveugle, contrôlé par placebo, avec une préparation médicamenteuse à base de racines de Pelargonium sidoides. Int J Clin Pharmacol Ther 2010a ; 48, 184-191.
- Kamin W, et al. : Efficacité et tolérance de l’EPs 7630 chez les patients (âgés de 6 à 18 ans) atteints de bronchite aiguë : une étude clinique randomisée, en double aveugle, contrôlée par placebo, à la recherche de la dose. Acta Paediatr 99 : 537-543.
- Matthys H, et al. : Efficacité et tolérance des comprimés EPs 7630 chez les patients atteints de bronchite aiguë : une étude randomisée, en double aveugle, contrôlée par placebo de détermination de la dose avec une préparation médicamenteuse à base de Pelargonium sidoides. Curr Med Res Opin 2010 ; 26 : 1413-1422.
- Riley DS, et al : Le traitement avec EPs 7630, un extrait de racine de Pelargonium sidoides, est efficace et sûr chez les patients souffrant du froid commun : résultats d’un essai clinique randomisé, en double aveugle, contrôlé par placebo. Integr Med (Encinitas) 2019 ; 18 (1) : 42-51.
PRATIQUE DU MÉDECIN DE FAMILLE 2024 ; 19(1) : 48-50