Souvent, les patients atteints de psoriasis ne souffrent pas seulement de lésions cutanées, mais sont également touchés par diverses comorbidités et par la stigmatisation. Afin de limiter l’impact négatif sur les aspects physiques et psychosociaux, il est important, en cas de psoriasis modéré à sévère, d’obtenir le meilleur contrôle possible des symptômes dès le début de l’évolution de la maladie. L’utilisation de produits biologiques modernes joue un rôle important à cet égard.
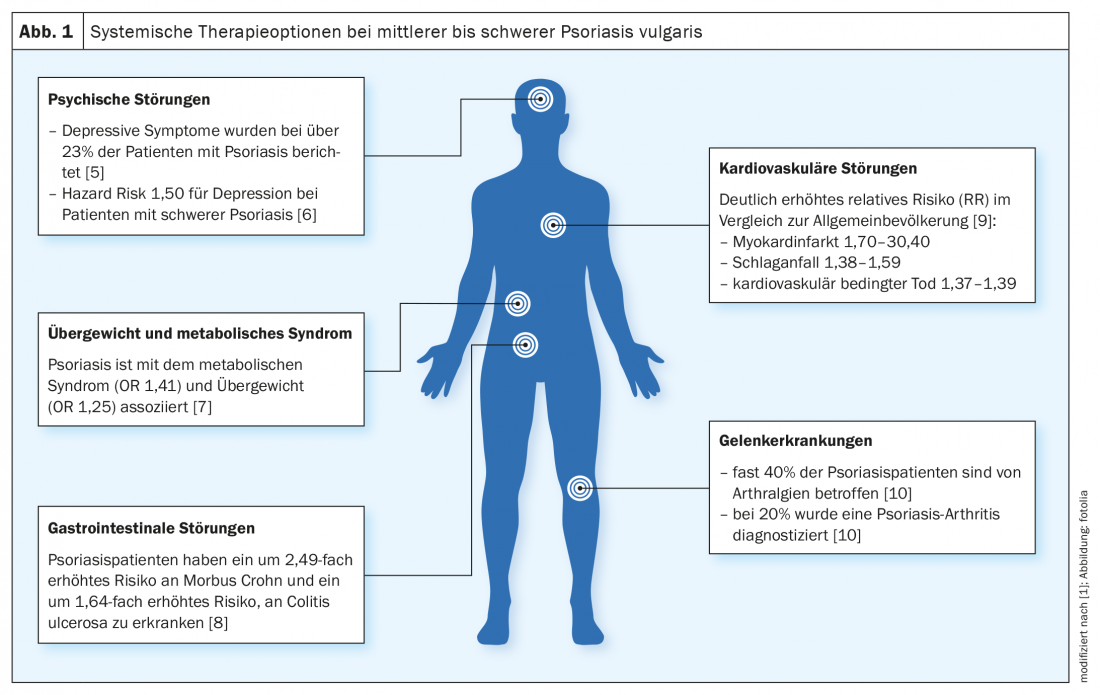
“Le psoriasis n’est pas seulement une maladie de la peau, c’est aussi une maladie systémique”, explique PD Dr. med. Julia-Tatjana Maul, médecin-chef et responsable de la consultation psoriasis, Hôpital universitaire de Zurich, à l’occasion de l’événement de formation continue virtuelle “Nouveaux horizons” [1]. Des comorbidités se manifestent souvent, mais la stigmatisation et l’observance influencent également l’état et la qualité de vie. Parmi les comorbidités les plus fréquentes figurent la dépression, l’obésité, le syndrome métabolique, les maladies inflammatoires chroniques de l’intestin et l’arthrite psoriasique (Fig. 1). “Et nous savons aussi que les facteurs de risque cardiovasculaires jouent un rôle important chez les patients atteints de psoriasis”, ajoute-t-elle avant d’expliquer : “Avec les nouvelles options thérapeutiques, nous ne voulons pas seulement traiter les lésions cutanées, mais aussi les comorbidités”.
Réduire le “fardeau de la maladie” et améliorer la qualité de vie
Mais quelle est la meilleure stratégie pour minimiser l’impact cumulatif du psoriasis ? Un facteur important pour limiter la charge de la maladie est un traitement personnalisé administré à temps, pour lequel il existe aujourd’hui un large éventail de médicaments très efficaces. De nombreuses publications ont montré qu’une peau exempte d’imperfections est un facteur très important de la qualité de vie mesurée par le “Dermatology Life Quality Index” (DLQI). “Les patients dont le psoriasis était peu sévère avaient la meilleure qualité de vie” [2,3], résume le PD Dr Maul. En général, un bon traitement avec un début d’effet rapide est souhaitable, a déclaré l’intervenante. Cela permet également de réduire les handicaps cumulés liés à la maladie et donc les comorbidités.
Au cours des dernières décennies, le paysage thérapeutique du traitement systémique du psoriasis en plaques a considérablement évolué et de nombreux nouveaux médicaments ont été autorisés, en particulier dans le domaine des produits biologiques. Si un patient atteint de psoriasis n’atteint pas les objectifs de traitement avec les thérapies systémiques conventionnelles, le passage aux médicaments biologiques doit être envisagé. Il s’agit de coordonner au mieux les différentes options de traitement du psoriasis.
Définir des objectifs thérapeutiques communs
“S’il y a un déséquilibre entre le traitement et les comorbidités physiques et psychologiques et la stigmatisation, le patient souffrira davantage de son traitement au cours de sa vie et le handicap cumulatif augmentera”, explique le PD Dr Maul. Les agents systémiques modernes ont un grand potentiel thérapeutique. “Les produits biologiques peuvent donner de meilleurs résultats thérapeutiques que les traitements systémiques conventionnels”, a-t-elle déclaré. Outre la sévérité du psoriasis et les éventuelles comorbidités, les traitements antérieurs du patient jouent également un rôle, de même que le fait de savoir si les conditions pour un traitement biologique sont remplies*. On choisit alors la substance active appropriée, on initie le traitement et on met en place le monitoring qui l’accompagne. Si la réponse au traitement n’est pas suffisante après une période de 4 à 6 mois, il convient d’adapter la dose ou de changer de traitement. Il est très important d’en discuter avec le patient et de se mettre d’accord sur des objectifs de traitement communs [1].
* Limitation de l’utilisation des produits biologiques en Suisse : réponse insuffisante à la thérapie systémique conventionnelle ou à la PUVA (psoralène et UV-A) ou contre-indications ou intolérance à ces thérapies. [11]
Taux de réponse PASI élevé du risankizumab dans le cadre d’un traitement à long terme
Dans l’étude en ouvert LIMMitless**, le risankizumab, un inhibiteur de l’IL23p19, a montré une efficacité élevée et durable, aussi bien après un changement d’ustékinumab ou d’adalimumab qu’après une administration continue de risankizum [4]. Les participants à l’étude ont reçu un traitement à long terme par risankizumab 150 mg toutes les 12 semaines. Parmi les patients randomisés dans le bras ustékinumab dans le cadre d’UltIMMa-1 ou UltIMMa-2 (n=199), 172 ont été inclus dans l’étude LIMMitless et ont été transférés au risankizumab. Le taux de réponse PASI90# était de 83% à la semaine 84 contre 47% à la ligne de base (sous ustékinumab). Les taux de réponse PASI75 correspondants étaient de 98% contre 78% et une proportion considérable de 57% a atteint le PASI 100, contre seulement 27% dans le bras ustékinumab. L’évaluation des scores DLQI (Dermatology Life Quality Index) montre que la qualité de vie des patients s’est considérablement améliorée sous traitement par l’inhibiteur d’IL23. A la semaine 72, 81% des participants à l’étude sous risankizumab avaient un score DLQI de 0 ou 1 (LOCF$), une augmentation significative par rapport à la ligne de base où ce score était de 50%.
** L’étude LIMMitless a inclus des patients ayant participé à l’une des sept études de phase II/III (y compris UltIMMa-1, UltIMMa-2 et IMMvent) [4].
# cas observés (“observed cases”), pas d’imputation des valeurs manquantes (“missing values”) ; les analyses des taux de réponse PASI par les méthodes “last observation carried forward (LOCF)” et “modified non-responder imputation” ont donné des résultats similaires [4].
$ LOCF= “dernière observation effectuée”.
Dans l’ensemble, les inhibiteurs de l’IL23 et de l’IL17 présentent généralement une très bonne efficacité à long terme, selon le PD Dr Maul, même s’il existe certaines différences au sein de ces groupes. Les inhibiteurs de l’IL23, en particulier, sont également considérés comme des médicaments très sûrs, à côté des inhibiteurs de l’IL17, comme le montrent d’une part les données réelles de notre registre suisse du psoriasis SDNTT, mais aussi les données de sécurité à 3-5 ans, selon la responsable de la consultation du psoriasis à l’hôpital universitaire de Zurich [1].
Congrès : USZ Nouveaux Horizons 2021
Littérature :
- Maul JT : Optimisation de la prise en charge du psoriasis. PD Dr. med. Julia-Tatjana Maul, USZ Nouveaux Horizons, 15.04.2021.
- Takeshita J, et al. : Patient-reported outcomes for psoriasis patients with clear versus almost clear skin in the clinical setting. JAAD 2014 ; 71(4) : 633-641.
- J-T Maul, et al : Le genre et l’âge déterminent de manière significative les besoins des patients et les objectifs de traitement dans le psoriasis – une leçon pour la pratique. JEADV 2019 ; 33(4) : 700-708.
- Blair HA : Risankizumab : A Review in Moderate to Severe Plaque Psoriasis. Drogues 2020 ; 80 : 1235-1245.
- Dowlatshahi EA, et al. : The prevalence and odds of depressive symptoms and clinical depression in psoriasis patients : a systematic review and meta-analysis.
- J Invest Dermatol 2014 ; 134(6) : 1542-1551.
- Egeberg JP, Thyssen JJ, Wu L, Skov A : Risk of first-time and recurrent depression Risk of first-time and recurrent depression in patients with psoriasis : a population-based cohort study. British Journal of Dermatology 2019 ; 180(1) : 116-121.
- Langan SM, et al : Prevalence of metabolic syndrome in patients with psoriasis : a population-based study in the United Kingdom. J Invest Dermatol 2012 ; 132(3 Pt 1) : 556-562.
- Vlachos C, et al : Psoriasis et maladie inflammatoire de l’intestin : liens et risques. Psoriasis (Auckl) 2016 ; 6 : 73-92.
- Egeberg A, et al : Le rôle de la voie interleukine-23/Th17 dans la comorbidité cardiométabolique associée au psoriasis. JEADV 2020 ; 34(8) : 1695-1706.
- Stern RS : The epidemiology of joint complaints in patients with psoriasis. J Rheumatol 1985 ; 12(2) : 315-320.
- BAG : www.bag.admin.ch (dernière consultation 07.06.2021)
DERMATOLOGIE PRAXIS 2021 ; 31(4) : 28-29 (publié le 18.8.21, ahead of print)