Le psoriasis pustuleux généralisé (PPG) est une maladie inflammatoire neutrophilique de la peau dont l’évolution peut être potentiellement fatale. Des données récentes sur l’immunopathogénie indiquent que le groupe des cytokines interleukine (IL)-36 est le moteur central des réactions auto-inflammatoires dans la GPP. L’anticorps monoclonal spesolimab inhibe l’activation du récepteur IL-36 (IL-36R) et est également autorisé en Suisse depuis l’année dernière pour le traitement des patients adultes atteints de GPP.
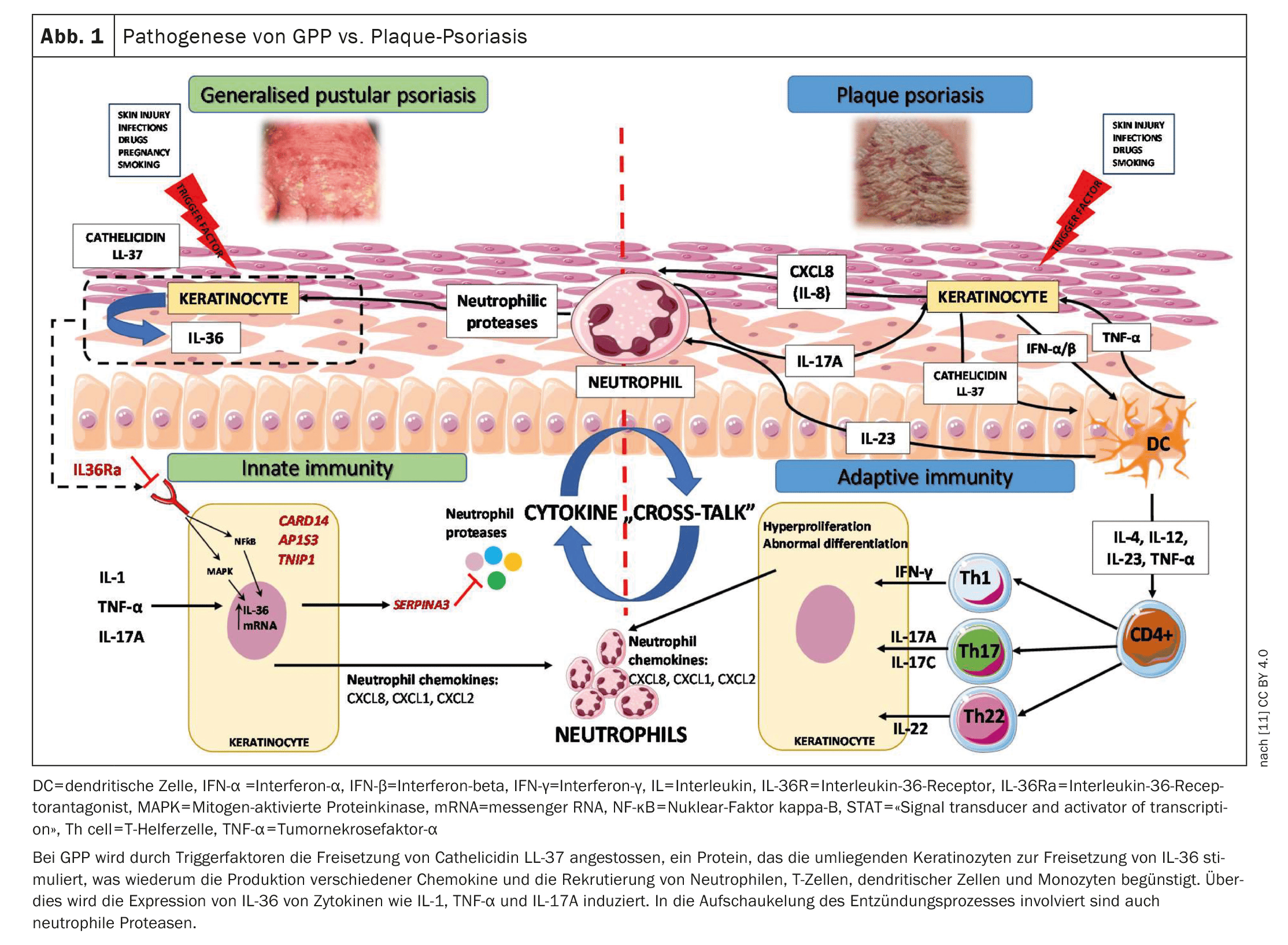
Le réseau européen d’experts ERASPEN (European Rare and Severe Psoriasis Expert Network) définit le psoriasis pustuleux généralisé (PGP) comme une maladie caractérisée par des pustules primaires, stériles et macroscopiquement visibles sur une peau non acrale. Le GPP se caractérise par des poussées avec formation de pustules étendues, qui peuvent être associées à des réactions inflammatoires systémiques** et à des complications extracutanées graves. Les critères d’inflammation systémique sont une fièvre >38 °C et une leucocytose£ [1]. Les poussées de GPP sont généralement suivies de phases sans activité ou avec une activité réduite de la maladie, mais il existe également des évolutions avec des symptômes persistants (>3 mois). Au cours d’une poussée aiguë, les symptômes tels que la douleur, les démangeaisons et la fatigue sont très éprouvants pour les personnes atteintes, ce qui réduit considérablement leur qualité de vie [2–4]. Dans l’immunopathogénèse des GPP (figure 1), la surexpression des cytokines IL-36 joue un rôle central [5,6]. Le spesolimab, un anticorps antirécepteur IL-36, bloque la voie de signalisation du récepteur (R) IL-36. La liaison du spesolimab à l’IL-36R empêche l’activation ultérieure de l’IL-36R par ses ligands (IL36 α, β et γ) et l’activation en aval des voies de signalisation pro-inflammatoires [7]. Cela permet d’atténuer les réactions inflammatoires et de réduire les symptômes de la GPP [8]. Le spesolimab (Spevigo®) est indiqué dans le traitement des poussées de la maladie GPP chez les patients adultes [9]. La dose recommandée est de 900 mg en une seule fois (2 flacons de 450 mg chacun), administrée en perfusion intraveineuse [8].
** Définition selon l’American Society of Chest Physicians
£ Leucocytose = nombre de globules blancs >12× 109/l
Patient de 63 ans : poussée aiguë de GPP et état général diminué
Le patient s’est présenté à [10] avec une poussée aiguë depuis trois jours d’une GPP pré-connue. A l’admission, l’état général était altéré et la peau présentait des plaques érythémateuses étendues avec des pustules multiples, parfois confluentes, sur l’ensemble du tégument. Les analyses de laboratoire ont révélé une augmentation significative des paramètres inflammatoires.
Traitements antérieurs : Depuis le diagnostic initial en 2011, les traitements ont été le méthotrexate, le fumarate de diméthyle et l’ustékinumab. Ce dernier a été arrêté il y a 6 mois après plusieurs années suite à une opération.
Traitement en cours : Initialement, un traitement stéroïdien systémique a été administré à raison de 80 mg/j de prednisolone. Des produits externes contenant des stéroïdes ont été utilisés en topique. Après avoir effectué les examens préliminaires nécessaires, un traitement par spesolimab 900 mg i.v. en une seule prise a été mis en place. Sous traitement, une réduction significative de l’activité de la maladie a été observée dès le lendemain, avec une disparition complète des pustules trois jours seulement après la perfusion et une amélioration rapide du TA. Au cours de la semaine suivante, les plaques se sont nettement estompées et les taux d’inflammation ont diminué, si bien que le patient a pu quitter l’hôpital dix jours après la perfusion. La prednisolone a pu être réduite à 60 mg/j au moment de la sortie. Au cours de l’évolution, une réintroduction ambulatoire de l’ustékinumab, en tant que traitement d’entretien, est prévue. En résumé, dans ce cas, le traitement par spesolimab a montré une amélioration rapide des symptômes de la poussée aiguë de GPP, ce qui est conforme aux résultats des études cliniques.
Congrès : la dermatologie en bref et en pratique
Littérature :
- Bone RC, et al. : Définitions du sepsis et de la défaillance d’organe et lignes directrices pour l’utilisation de thérapies innovantes dans le sepsis. Le Comité de Consensus ACCP/SCCM. American College of Chest Physicians/Society of Critical Care Medicine. Chest 1992 ; 101 : 1644-1655.
- Burden AD, et al : Symptom Experience and Content Validity of the Psoriasis Symptom Scale (PSS) in Patients with Generalized Pustular Psoriasis (GPP). Dermatol Ther (Heidelb) 2022 ; 12(6) : 1367-1381.
- Lebwohl M, et al : La charge de morbidité du psoriasis pustuleux généralisé : preuves mondiales réelles du registre du psoriasis de CorEvitas. Journal of Psoriasis and Psoriatic Arthritis 2022 ; 7(2) : 71-78.
- Reisner DV, et al : Impact du psoriasis pustuleux généralisé du point de vue des personnes vivant avec la condition : résultats d’une enquête en ligne. Am J Clin Dermatol 2022 ; 23(Suppl 1) : 65-71.
- Marrakchi S, et al : Déficience de l’antagoniste du récepteur de l’interleukine-36 et psoriasis pustuleux généralisé. N Engl J Med 2011 ; 365 : 620-628.
- Gooderham MJ, Van Voorhees AS, Lebwohl MG: An update on generalized pustular psoriasis. Expert Rev Clin Immunol 2019 ; 15 : 907-919.
- Agence européenne des médicaments, https://ec.europa.eu/health/documents/community-register/2022/
20221209157574/anx_157574_fr.pdf, (dernière consultation 16.05.2024) - Swissmedic : Spevigo® (principe actif : spesolimab), Public Summary SwissPAR du 29.02.2024, première autorisation en Suisse : 09.08.2023
- Swissmedic : Information sur les médicaments, www.swissmedicinfo.ch,(dernière consultation 16.05.2024)
- Kluck R, et al. : Traitement d’une poussée aiguë de psoriasis pustuleux généralisé avec le spesolimab, P046. JDDG 2024 ; 22, Issue S1 : 1-40.
- Samotij D, Szczęch J, Reich A : Psoriasis pustuleux généralisé : divergence de l’immunité innée et adaptative. International Journal of Molecular Sciences. 2021 ; 22(16) : 9048. www.mdpi.com/1422-0067/22/16/9048,(dernière consultation 16.05.2024).
DERMATOLOGIE PRAXIS 2024 ; 34(3) : 26-27 (publié le 14.6.24, ahead of print)