L’objectif thérapeutique d’une disparition totale des symptômes est réaliste dans de nombreux cas grâce aux options de traitement disponibles aujourd’hui. Les antihistaminiques H1 sont toujours considérés comme le traitement de première ligne, et l’utilisation de l’omalizumab est recommandée en cas d’absence de réponse. Un autre anticorps IgE est actuellement dans le pipeline et les données des études menées jusqu’à présent sont extrêmement prometteuses. Pour mesurer l’évolution, des instruments standardisés tels que le score d’activité de l’urticaire (UAS7) et le test de contrôle de l’urticaire (UCT) sont utiles.
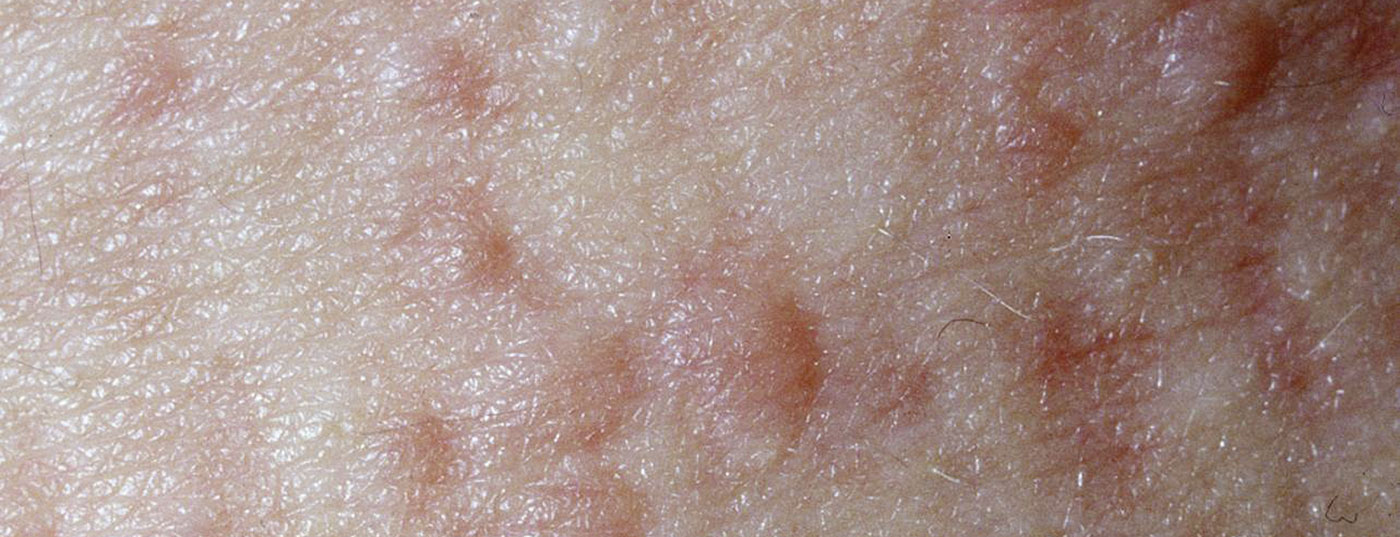
L’urticaire chronique est définie par l’apparition de démangeaisons et/ou d’angio-œdèmes pendant plus de six semaines. Il s’agit d’une maladie fréquente et très invalidante pour de nombreux patients. Les performances dans la vie quotidienne peuvent être considérablement réduites et l’urticaire chronique s’accompagne souvent de dépression, de troubles anxieux et de troubles du sommeil. Le professeur Marcus Maurer, allergologue dermatologue au centre d’allergie de la médecine universitaire de la Charité à Berlin, a donné un aperçu actuel de la prise en charge de l’urticaire à l’occasion de la réunion annuelle de la DDG de cette année [1]. La nouvelle ligne directrice S3 a été récemment approuvée et sa publication est prévue pour 2021. La ligne directrice actuelle EAACI/GA²LEN/EDF/WAO fait actuellement autorité en matière de recommandations de traitement (figure 1).

Alors que dans l’urticaire chronique inductible, les symptômes peuvent être expliqués par des déclencheurs spécifiques reproductibles, comme le froid ou la pression, dans l’urticaire chronique spontanée (csU), la cascade physiopathologique est déclenchée par un facteur intrinsèque. L’auto-immunité est désormais considérée comme une cause fréquente d’urticaire chronique spontanée. Alors que dans le cas d’une csU due à une auto-immunité de type I, les auto-anticorps IgE se lient au récepteur de haute affinité des mastocytes cutanés, dans le cas d’une CSU auto-immune de type IIb, les auto-anticorps IgG dirigés contre le récepteur de haute affinité des IgE entraînent une dégranulation des mastocytes [2].
Diagnostic différentiel basé sur une anamnèse structurée
Les objectifs de l’évaluation diagnostique chez les patients suspects de csU comprennent, outre le diagnostic différentiel, la recherche de facteurs déclencheurs pertinents pour la csU (par exemple, la prise d’analgésiques), la clarification des comorbidités, la détermination de l’activité de la maladie et de son contrôle, ainsi que l’évaluation de la qualité de vie [3]. Lors du diagnostic de l’urticaire chronique spontanée, il faut penser large, souligne le conférencier. “Il ne s’agit pas seulement d’identifier les causes, il s’agit également d’identifier et de traiter les comorbidités et les conséquences chez les patients”. Après l’anamnèse, il convient de procéder à un examen physique et à un diagnostic de base en laboratoire (vitesse de sédimentation et/ou CRP et formule sanguine différentielle) [3,4]. Un diagnostic avancé n’est indiqué que dans quelques cas et doit en principe être réalisé parallèlement à un traitement.
Pour l’anamnèse et le diagnostic de base, des questions d’anamnèse ciblées sont formulées dans les lignes directrices EAACI/GA²LEN/EDF/WAO [3,4]:
- Antécédents familiaux : des antécédents familiaux positifs de quintes et d’angio-œdème peuvent indiquer des maladies congénitales telles que les syndromes auto-inflammatoires et l’angio-œdème héréditaire (AOH).
- Moment du début de la maladie : un début dans la petite enfance peut indiquer des maladies congénitales telles que le syndrome périodique associé à la cryopyrine (CAPS) ou l’AOH.
- Apparition d’un angio-œdème sans présence de papules : En cas de survenue isolée d’un angio-œdème, il convient d’envisager un angio-œdème médié par la bradykinine (par ex. angio-œdème induit par l’AOH ou les IEC/sartans).
- Durée et localisation de l’angio-œdème : Si l’angio-œdème persiste pendant plusieurs jours, s’il est localisé dans la région du larynx ou de l’abdomen ou s’il ne répond pas à un traitement par glucocorticoïdes, un AOH ou un autre angio-œdème médié par la bradykinine est possible.
- Durée et séquelles des urticaires : La présence de papules pendant une longue période (généralement >24 h) ou l’apparition d’un hématome ou d’une hyperpigmentation consécutive peuvent être le signe d’une vascularite urticarienne.
- Médicaments : En cas de prise d’IEC ou de sartans, il convient de rechercher un angio-œdème médié par l’IEC ou le sartan.
- Symptômes associés : douleurs osseuses/articulaires, signes d’inflammation ou fièvre peuvent être des indices de syndromes auto-inflammatoires.
- Dépendance de l’apparition de quintes et/ou d’angioedèmes à des déclencheurs spécifiques : La survenue exclusive de quintes et/ou d’angio-œdèmes suite à des déclencheurs spécifiques (par ex. contact de la peau avec le froid) rend probable une urticaire chronique inductible.
- Antécédents de traitement et réponse thérapeutique antérieure (y compris la dose et la durée) : La résistance au traitement peut être le signe d’un syndrome auto-inflammatoire ou d’une maladie angio-œdémateuse médiée par la bradykinine.
- Procédures/résultats de diagnostic antérieurs : Est-il possible d’établir des corrélations ?
- Apparition intermittente de l’urticaire et/ou des symptômes associés, tels que des troubles gastro-intestinaux : Cela peut indiquer une allergie alimentaire à médiation IgE.
Doser les antihistaminiques – anticorps anti-IgE en traitement de deuxième intention
L’objectif principal du traitement de la csU est de parvenir à une disparition totale des symptômes et d’atténuer ainsi les symptômes associés (par ex. dépression, anxiété, troubles du sommeil) [2]. Le traitement consiste à éviter les facteurs déclencheurs et à administrer un traitement médicamenteux adéquat (figure 1). Les antihistaminiques H1 de deuxième génération sont considérés comme le traitement de première ligne du csU (par exemple, la loratadine ou la cétirizine) [3]. En cas de manque d’efficacité, il est recommandé d’augmenter la dose standard, mais cela ne pose pas de problème si l’on tient compte d’éventuels facteurs de risque ou d’une co-médication. Si une amélioration suffisante n’est pas obtenue après deux à quatre semaines de traitement par un antihistaminique H1 de deuxième génération à dose standard ou après augmentation de la dose, un traitement supplémentaire par omalizumab (Xolair®) doit être administré. Cet anticorps monoclonal présente un bon profil de sécurité et le taux d’anaphylaxie est faible. L’utilisation de l’omalizumab est également sans danger en cas de rhume léger, de toux ou d’enrouement. Pendant le traitement à l’omalizumab, il est possible de recourir à des vaccins morts ou vivants. En l’absence d’antécédents d’anaphylaxie, les patients peuvent s’injecter eux-mêmes l’omalizumab ou le faire injecter par un soignant à partir de la quatrième utilisation (à l’exception des femmes enceintes). Si aucun résultat n’est obtenu après six mois de traitement par omalizumab, un usage hors indication de la ciclosporine A est recommandé en plus du traitement existant par antihistaminiques H1. En cas d’exacerbation aiguë, un traitement de courte durée (10 jours maximum) avec des doses moyennes peut être envisagé. Les patients peuvent être traités avec des glucocorticoïdes oraux systémiques afin de réduire la durée et l’activité de la maladie. L’utilisation des antihistaminiques loratadine et cétirizine ainsi que de l’omalizumab est également possible pendant la grossesse.
La mesure de l’historique est extrêmement importante
“Mesurez l’urticaire de vos patients”, appelle le professeur Maurer. Cela permet, d’une part, de prendre des décisions thérapeutiques basées sur des faits et, d’autre part, d’adapter le traitement en cours de route si nécessaire. Lescore hebdomadaired’activité de l’urticaire (UAS7) [5] et le score d’activité de l’angio-œdème (AAS) [6] sont utilisés pour le suivi de l’activité de la maladie. En complément, le test de contrôle de l’urticaire (UCT) doit être réalisé chez tous les patients atteints de CSU. Dans le cas de l’UAS7, les patients documentent quotidiennement les quintes et les démangeaisons par le patient dans un journal pendant sept jours consécutifs [5]. De la même manière, l’apparition d’un angio-œdème est détectée par le SAA [6]. L’UCT permet d’évaluer le contrôle de la maladie et du traitement à l’aide de quatre questions (0 à 4 points par réponse) portant sur les quatre dernières semaines. Un score total ≤11 points indique une maladie non contrôlée [7]. En complément, il est utile d’évaluer régulièrement la qualité de vie (par ex. DLQI* ou CU-Q2oL** ou AE-QoL#).
* DLQI = Indice de qualité de vie en dermatologie
** CU-Q2oL= Chronic Urticaria Quality of Life Questionnaire
# AE-QoL=Angioedema Quality of Life Questionnaire
Congrès : Réunion DDG 2021
Littérature :
- Maurer M : Urticaria chronique – Praktisches und Neues zum Management, Prof. Dr Marcus Maurer, S17 : Track Allergologie : Soforttypallergie, Urtikaria und Spezifische Immunherapie, DDG Tagung 2021, 16.04.2021.
- Maurer M, et al. : Urticaire chronique – Qu’apporte la nouvelle ligne directrice ? JDDG 2018 ; 16(5) : 585-595.
- Bauer A, et al. : Consensus d’experts sur les aspects pratiques du traitement de l’urticaire chronique. Allergo J Int 2021 ; 30 : 64-75.
- Zuberbier T, et al. : Lignes directrices EAACI/GA²LEN/EDF/OMS pour la définition, la classification, le diagnostic et la prise en charge de l’urticaire – traduction française consensuelle. Allergo Journal 2018 ; 27 : 41-69.
- Hawro T, et al : The urticaria activity score-validity, reliability, and responsiveness. J Allergy Clin Immunol Pract 2018 ; 6 : 1185-90.e1
- Weller K, et al : Development, validation, and initial results of the Angioedema Activity Score. Allergy 2013 ; 68 : 1185-1192.
- Weller K, et al : Development and validation of the Urticaria Control Test : a patient-reported outcome instrument for assessing urticaria control. J Allergy Clin Immunol 2014 ; 133 : 1365-1372, 72.e1-6
- Teach SJ, et al : Traitement présaisonnier avec soit omalizumab soit un boost de corticostéroïdes inhalés pour prévenir les exacerbations d’asthme de cas. J Allergy Clin Immunol 2015 ; 136 : 1476-1485.
- Esquivel A, et al : Efects of omalizumab on rhinovirus infections, illnesses, and exacerbations of asthma. Am J Respir Crit Care Med 2017 ; 196 : 985-992.
- Lommatzsch M, Stoll P, Virchow JC : COVID-19 chez un patient souffrant d’asthme sévère traité à l’omalizumab. Allergy 2020 ; 75 : 2705-2708.
- Klimek L, et al. : Utilisation des agents biologiques dans les maladies allergiques et les maladies inflammatoires de type 2 au cours de la pandémie actuelle de COVID-19. Allergo J 2020 ; 29 : 14-27.
- Maurer M, et al : Ligelizumab for chronic spontaneous urticaria. New England Journal of Medicine Oct 2019. doi : 10.1056/NEJMoa1900408
- Sussman G, et al : Insights and advances in chronic urticaria : a Canadian perspective. All Asth Clin Immun 2015 ; 11(7), https://doi.org/10.1186/s13223-015-0072-2
DERMATOLOGIE PRAXIS 2021 ; 31(3) : 30-31 (publié le 1.6.21, ahead of print)