La balanite est un problème fréquent qui représente une contrainte évidente pour le patient concerné. Souvent, les lésions ne se limitent pas au gland, mais s’étendent au prépuce ou à son feuillet interne, ce qui fait parler de balanoposthite. Outre les étiologies infectieuses, les dermatoses inflammatoires doivent être envisagées. Les modifications prémalignes peuvent poser des problèmes de diagnostic différentiel avec les lésions d’origine purement inflammatoire. L’article suivant donne un aperçu des principales infections, dermatoses inflammatoires et altérations prémalignes au niveau du gland.
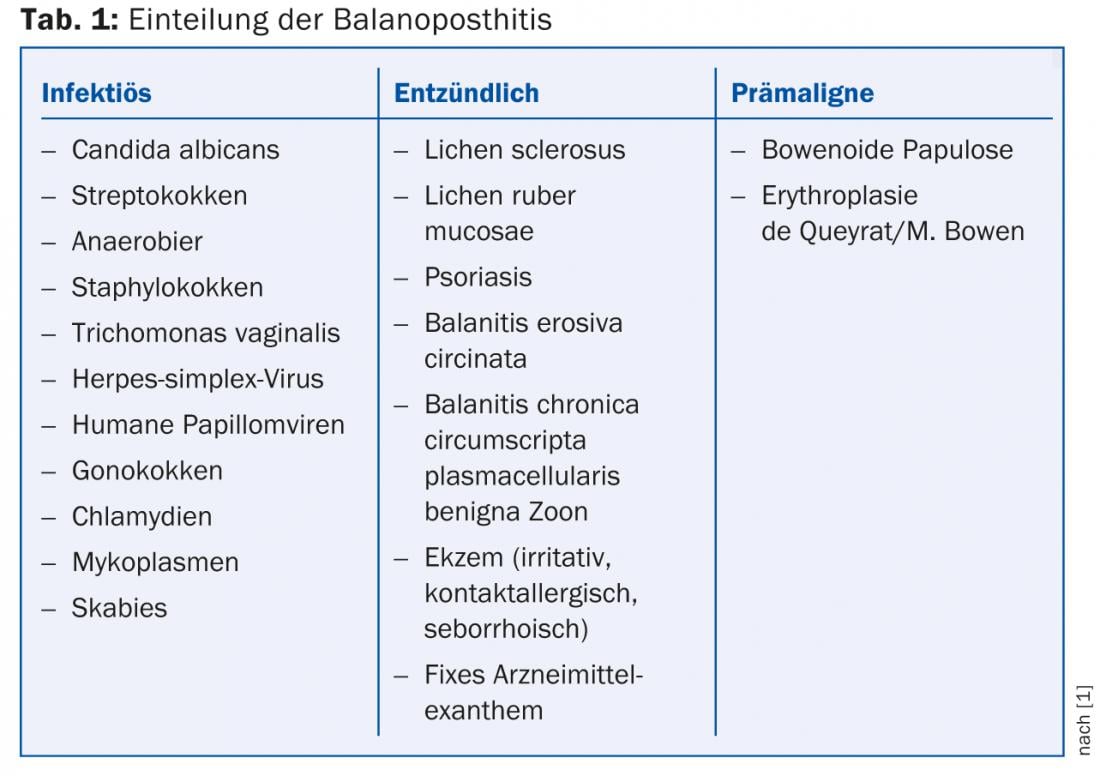
Le tableau 1 présente une classification des balanoposthites . Il convient de distinguer les patients qui ne présentent pas de balanite au sens propre du terme, mais par exemple des variantes anatomiques normales et inoffensives comme les papilles coronae glandis (fig. 1) ou des inflammations d’autres structures que la peau, comme dans le cas de la lymphangite/phlébite des sillons coronaires (fig. 2) .
Balanite infectieuse
L’espace préputial, souvent humide, peut favoriser le développement d’agents mycosiques et bactériens. Toutefois, d’autres facteurs peuvent également jouer un rôle. Ainsi, en cas de candidabalanite (figure 3), il faut également penser au diabète. Inversement, l’infestation du gland par le candida en cas de diabète sucré connu peut être interprétée comme une indication d’une glycémie insuffisamment contrôlée ou déréglée.
Outre les levures, les bactéries, notamment les streptocoques, les anaérobies et les staphylocoques, peuvent être à l’origine d’une balanite.
Les agents pathogènes des infections sexuellement transmissibles peuvent également déclencher une balanoposthite. Ainsi, les gonocoques, les chlamydias et les mycoplasmes, qui sont des agents urétraux, peuvent provoquer une balanite concomitante. Une cause moins souvent envisagée de balanite est le Trichomonas vaginalis. Les infections par le virus de l’herpès simplex et les papillomavirus humains ont un spectre clinique qui, outre la clinique typique de vésicules/érosions groupées ou de lésions de la peau, comprend également des lésions de la peau et des lésions de la peau. Les protrusions papillomateuses peuvent également inclure une balanite. La lèpre, caméléon en dermatologie, peut également se manifester par une balanite (figure 4). Enfin, la scabiose, en tant que parasitose, peut également entraîner des modifications inflammatoires typiques au niveau du gland (fig. 5) ou de la région génitale. Le symptôme révélateur est généralement un prurit prononcé, surtout nocturne, mais les lésions du gland sont presque pathognomoniques et fournissent généralement des préparations directes positives.
Dermatoses inflammatoires du gland
Le lichen scléreux (“white spot disease”) est une dermatose inflammatoire de pathogenèse incertaine, peut-être auto-immune. Outre les symptômes subjectifs tels que les démangeaisons et la dyspareunie, on observe une coloration blanchâtre et une sclérose, souvent accompagnées d’un phimosis secondaire ou même d’une sténose du méat. Un signe clinique typique est la présence d’hémorragies dans les zones sclérosées (figure 6). Sur le plan thérapeutique, on utilise des stéroïdes locaux à haute puissance (classe IV). Le lichen scléreux étant une maladie précancéreuse facultative, il convient de procéder à un suivi régulier.
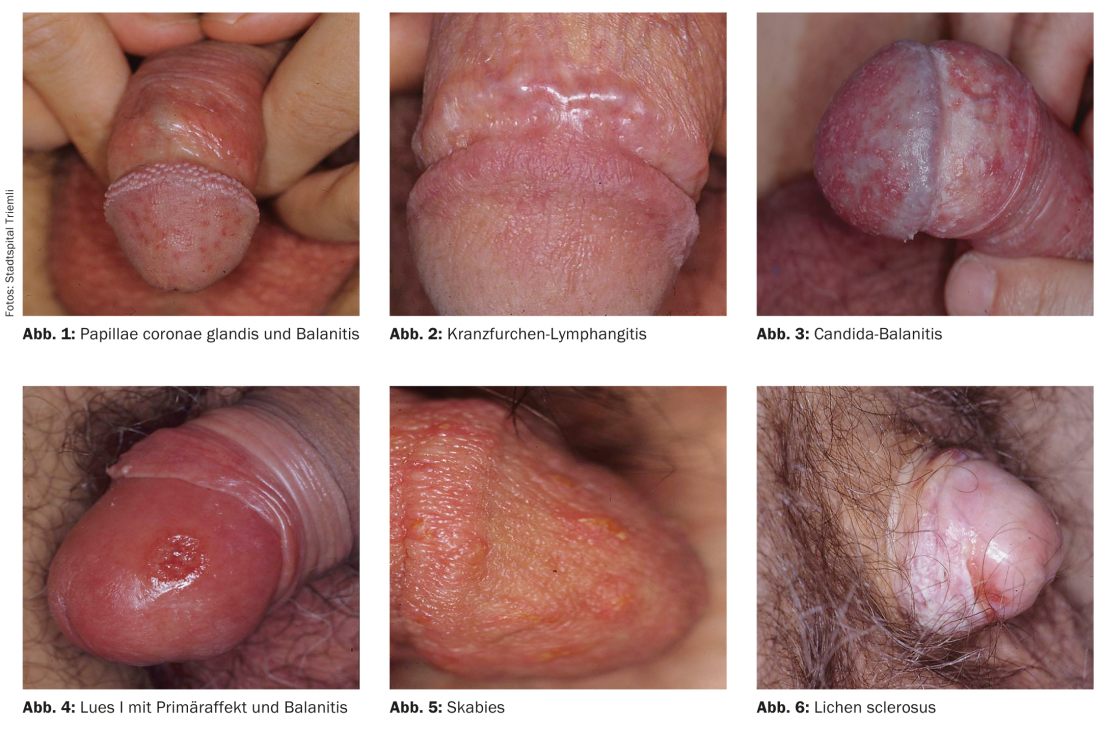
Le lichen ruber peut typiquement se manifester au niveau des muqueuses et des organes génitaux. Comme pour le reste du tégument, dont l’inspection complète peut fournir de précieux indices pour ce diagnostic, il existe une gamme clinique allant d’un dessin réticulé blanchâtre à des papules polygonales et des plaques anulaires (Fig. 7). L’aspect livide des lésions peut orienter le diagnostic. Le traitement dépend de l’ensemble du tableau, les stéroïdes topiques étant également utilisés en premier lieu dans la région génitale.
Des plaques psoriasiques peuvent être observées sur le gland comme sur le reste de la peau. Des douleurs articulaires, des symptômes oculaires et des foyers érosifs en forme de guirlande sur le gland doivent conduire au diagnostic de suspicion de balanite érosive circinée. STI incl. Le VIH doit être recherché et une entérite doit être exclue comme cause.
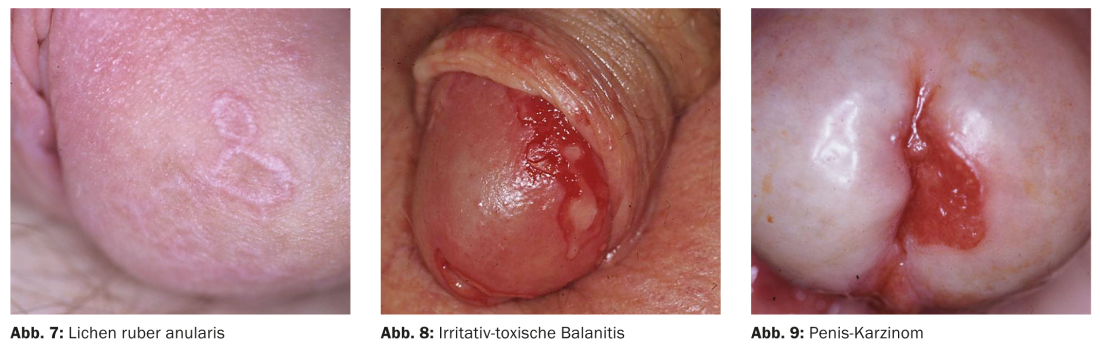
L’eczéma, qu’il soit d’origine irritative, allergique de contact ou séborrhéique, peut également se manifester parfois ou, selon le contact, exclusivement sur le gland et le prépuce. En plus d’une anamnèse précise concernant les topiques utilisés, il convient de s’interroger sur la tolérance de son propre traitement au niveau des muqueuses génitales. Par exemple, les topiques contenant de l’hexamidine peuvent entraîner des réactions toxiques prononcées au niveau du gland (figure 8) et sont donc contre-indiqués. Mais les médicaments systémiques peuvent également entraîner typiquement dans la région génitale un tableau d’exanthème médicamenteux fixe avec des macules livide, des bulles ou des érosions. Les AINS, les tétracyclines et les barbituriques sont des exemples de déclencheurs, mais ce sont souvent des épisodes répétés se manifestant au même endroit (fixe) qui conduisent au diagnostic.
La balanitis chronica circumscripta plasmacellularis benigna – souvent appelée balanitis zoon en raison de la longueur de son nom, du nom de son premier auteur – est une dermatose inflammatoire bénigne, probablement d’origine irritative, dont le traitement repose essentiellement sur la désinfection et l’assèchement. Si cela ne suffit pas, la circoncision peut être envisagée.
Modifications prémalignes du gland
Enfin, il convient d’établir un diagnostic différentiel avec les lésions précancéreuses, qui ne sont plus, à proprement parler, des balanites, c’est-à-dire des modifications purement inflammatoires. Outre la papulose bowenoïde, qui est généralement facile à reconnaître en raison de ses papules brunes et de ses plaques plates, l’érythroplasie de Queyrat/la maladie de Bowen du gland ne sont souvent reconnues comme précancéreuses qu’en raison de l’absence de détection de l’agent pathogène et, surtout, de leur résistance au traitement. Il est essentiel d’obtenir une confirmation histologique et un traitement précoces afin d’éviter la progression vers un carcinome du pénis (figure 9).
Diagnostic
Outre le diagnostic infectieux, qui doit inclure des prélèvements pour le diagnostic bactériologique et mycologique ainsi qu’un dépistage des IST, une biopsie doit être envisagée, en particulier en cas de récidives fréquentes ou de résistance au traitement.
Thérapie
Si un agent pathogène est détecté, il est traité en conséquence. En l’absence d’amélioration, il est possible de faire un essai empirique avec du métronidazole. Il faut toujours veiller à un équilibre dans l’hygiène, ce qui signifie que celle-ci doit être améliorée chez certains patients, tandis que d’autres doivent être dissuadés de se laver trop souvent avec du savon. En l’absence d’identification de l’agent pathogène, d’une bonne hygiène et d’une absence d’amélioration malgré les soins avec des émollients, l’utilisation topique d’un stéroïde de classe I comme l’hydrocortisone peut être envisagée pendant deux semaines. Si, là encore, il n’y a pas d’amélioration, il convient d’orienter le patient vers un dermatologue et/ou de pratiquer une biopsie.
Littérature :
- IUSTI 2012 Lignes directrices européennes pour la prise en charge de la balanoposthite.
- English JC, et al : Dermatoses du gland du pénis et du prépuce. J Am Acad Dermatol 1997 ; 37 : 1-24.
- Singh S, Bunker C : Dermatoses génitales masculines chez les personnes âgées. Age and Aging 2008 ; 37 : 500-504.
- Teichman JMH, et al : Lésions péniennes non infectieuses. American Family Physician 2010 ; 81 : 167-174.
- Fistarol SK, Itin PH : Diagnostic et traitement du lichen scléreux. Une mise à jour. Am J Clin Dermatol 2013 ; 14 : 27-47.
DERMATOLOGIE PRATIQUE 2013 ; 23(6) : 4-6











