La storia degli stent è segnata da numerosi successi, ma anche da battute d’arresto. Nel frattempo, sono stati superati molti “problemi di dentizione”. È disponibile un’ampia gamma di stent per situazioni diverse.
La malattia coronarica (CHD) è la triste vincitrice a livello mondiale quando si tratta di cause di morte, secondo il PD Stefan Blöchlinger, MD, PhD, del Dipartimento di Cardiologia dell’Ospedale Cantonale di Winterthur. La prima angioplastica coronarica transluminale percutanea, o PTCA o PCI, è stata eseguita a Zurigo il 16 settembre 1977 in un paziente di 38 anni con una stenosi RIVA prossimale isolata. Meno di due anni dopo, le esperienze con la nuova procedura furono pubblicate sul New England Journal of Medicine [1]. Tuttavia, l’angioplastica con palloncino presenta alcuni problemi intrinseci. Sono possibili un cosiddetto contraccolpo elastico dell’arteria, la restenosi e la formazione di trombi. Per ridurre la restenosi, evitare il collasso della parete del vaso o del vaso stesso. Per evitare il più possibile la dissezione con formazione di trombi e quindi mantenere il vaso aperto, alcuni anni dopo sono stati sviluppati gli stent coronarici. Tramite il catetere, gli “scaffold” entrano nel vaso occluso, che dovrebbe trattenere i depositi alla parete dell’arteria, dilatare in modo permanente l’arteria e migliorare il flusso sanguigno [2]. Tuttavia, con i cosiddetti stent di metallo nudo (BMS), la restenosi non è affatto scomparsa, il che è legato, tra l’altro, all’iperplasia intimale, in cui si verificano la proliferazione e la migrazione delle cellule muscolari lisce nell’area degli stent. Anche la trombosi era ancora una minaccia, a causa della trombogenicità del metallo e del danno all’endotelio.
Cosa è successo dopo?
I cosiddetti stent a rilascio di farmaco (DES) dovrebbero fornire un rimedio. Grazie alla somministrazione locale controllata di agenti antiproliferativi, questi potrebbero effettivamente migliorare l’esito dell’impianto di stent e ridurre significativamente il tasso di reintervento. Tuttavia, un problema è rimasto o, più precisamente, si è aggravato con le prime generazioni di stent a rilascio di farmaco: il verificarsi di una trombosi dello stent molto tardiva, cioè oltre un anno dopo l’impianto [3,4]. Con un’incidenza di circa lo 0,5% all’anno, i modelli più vecchi erano addirittura inferiori al BMS in questo senso. Solo con l’introduzione della nuova generazione di DES, questo problema è stato finalmente risolto e il tasso di incidenza è stato ridotto allo 0,1% all’anno. Inoltre, la nuova generazione di DES è rivestita solo con agenti che terminano in -limus (everolimus, zotarolimus e sirolimus). Una meta-analisi aveva mostrato: un rivestimento con sirolimus è di nuovo chiaramente superiore a quello con paclitaxel per quanto riguarda il tasso di restenosi [5].
Stent bioriassorbibili: il prossimo passo?
Lo sviluppo più recente è rappresentato dai DES bioriassorbibili o DES con un alto grado di “impalcature”. Il rappresentante più noto si chiama ABSORB. Tuttavia, i moderni stent metallici sono così tecnicamente avanzati da essere difficili da battere in termini di efficacia e sicurezza. La loro ritenzione nell’organismo non rappresenta attualmente un problema clinico rilevante. Gli stent bioriassorbibili sono stati quindi sviluppati non tanto per superare i gravi svantaggi dei precedenti stent di nuova generazione, quanto piuttosto per l’idea che lo stato nativo del vaso sia superiore o preferibile a una “gabbia metallica” che dura tutta la vita. Gli studi ABSORB, tuttavia, sono stati deludenti e hanno persino mostrato un peggioramento della sicurezza: tra l’altro, il rischio (molto tardivo) di trombosi era significativamente aumentato rispetto ai DES non riassorbibili [6], probabilmente dovuto principalmente a discontinuità nello scaffold, seguite da malapposizione e neoaterosclerosi [7].
Pertanto, gli stent bioriassorbibili non dovrebbero essere preferiti ai DES metallici di nuova generazione nella pratica clinica attuale. I pazienti che hanno già ricevuto stent bioriassorbibili dovrebbero, se ben tollerati, continuare la terapia antiaggregante doppia (DAPT) per la durata presunta del riassorbimento (cioè almeno 36 mesi per ABSORB) o – se precedentemente interrotta – riprenderla, a seconda del singolo caso e del rischio di trombosi-emorragia [8].
Linee guida
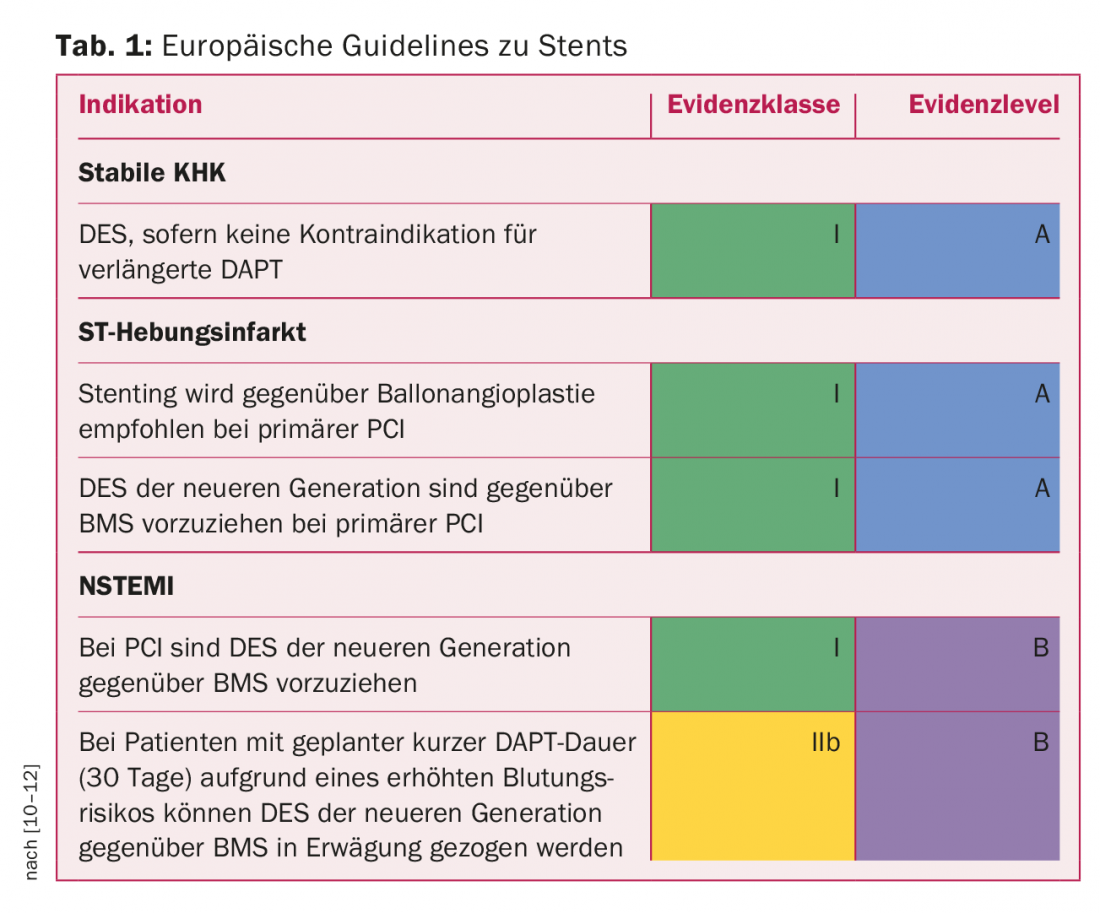
Cosa dicono le linee guida sui diversi tipi di stent? Per quanto riguarda la BMS, le attuali linee guida europee sulla rivascolarizzazione miocardica del 2014 sono relativamente chiare: la BMS in realtà non avrebbe più posto in questo campo, cioè non ci sarebbe alcuna indicazione per essa, indipendentemente dal tipo di lesione o dal paziente – questo è dovuto principalmente al suo “tallone d’Achille”, le restenosi. Non ci sono prove evidenti di differenze tra BMS e DES nel rischio di trombosi dello stent nell’interruzione non pianificata della DAPT [9]. Ulteriori raccomandazioni specifiche sono riportate nella tabella 1. In generale, si consigliano i DES di ultima generazione.
Il Dr. Blöchlinger vede anche solo alcuni casi speciali in cui la BMS può ancora essere un’opzione (ad esempio, diametri di vasi molto grandi, poiché attualmente non sono disponibili DES di queste dimensioni). Anche i cosiddetti stent coperti appartengono ai BMS. Questi stent sono rivestiti con materiale di innesto, e vengono utilizzati principalmente per problemi come la rottura del vaso durante gli interventi coronarici. Al momento, esistono cinque diversi stent di questo tipo in Europa.
Fonte: 16° Corso di revisione in Cardiologia clinica a Zurigo, 12-14 aprile 2018, Zurigo Oerlikon
Letteratura:
- Grüntzig AR, Senning A, Siegenthaler WE: Dilatazione non chirurgica della stenosi coronarica: angioplastica coronarica percutanea transluminale. N Engl J Med 1979 Jul 12; 301(2): 61-68.
- Carrié D, et al: Follow-up clinico e angiografico a dieci anni di wallstent coronarico. Am J Cardiol 2000 Jan 1; 85(1): 95-98, A8.
- Stefanini GG, et al: Esiti clinici a lungo termine degli stent a rilascio di biolimus, polimero biodegradabile, rispetto agli stent a rilascio di sirolimus, polimero durevole, nei pazienti con malattia coronarica (LEADERS): follow-up di 4 anni di uno studio randomizzato di non inferiorità. Lancet 2011 Dec 3; 378(9807): 1940-1948.
- Wenaweser P, et al: Incidenza e correlazioni della trombosi dello stent a rilascio di farmaco nella pratica clinica di routine. Risultati a 4 anni di un ampio studio di coorte a 2 istituzioni. J Am Coll Cardiol 2008 Sep 30; 52(14): 1134-1140.
- Stettler C, et al: Esiti associati agli stent a rilascio di farmaco e a metallo nudo: una meta-analisi di rete collaborativa. Lancet 2007 Sep 15; 370(9591): 937-948.
- Ali ZA, et al: Esiti a tre anni con lo Scaffold Bioassorbibile Absorb: Meta-Analisi dei dati individuali del paziente dagli studi randomizzati ABSORB. Circulation 2018 Jan 30; 137(5): 464-479.
- Yamaji K, et al: Meccanismi di trombosi molto tardiva dello Scaffold Bioresorbibile: il Registro INVEST. J Am Coll Cardiol 2017 Nov 7; 70(19): 2330-2344.
- Byrne RA, et al: Rapporto di una Task Force ESC-EAPCI sulla valutazione e l’uso degli scaffold bioassorbibili per l’intervento coronarico percutaneo: sintesi. Eur Heart J 2017 Aug 28. DOI: 10.1093/eurheartj/ehx488. [Epub ahead of print].
- Windecker S, et al.: Linee guida ESC/EACTS 2014 sulla rivascolarizzazione miocardica: la Task Force sulla rivascolarizzazione miocardica della Società Europea di Cardiologia (ESC) e dell’Associazione Europea per la Chirurgia Cardio-Toracica (EACTS) sviluppate con il contributo speciale dell’Associazione Europea degli Interventi Percutanei Cardiovascolari (EAPCI). Eur Heart J 2014 Oct 1; 35(37): 2541-2619.
- Montalescot G, et al: Linee guida ESC 2013 sulla gestione della coronaropatia stabile: la Task Force sulla gestione della coronaropatia stabile della Società Europea di Cardiologia. Eur Heart J 2013 Oct; 34(38): 2949-3003.
- Ibanez B, et al.: Linee guida ESC 2017 per la gestione dell’infarto miocardico acuto nei pazienti che presentano un sopraslivellamento del tratto ST: La Task Force per la gestione dell’infarto miocardico acuto nei pazienti che presentano un sopraslivellamento del tratto ST della Società Europea di Cardiologia (ESC). Eur Heart J 2018 Jan 7; 39(2): 119-177.
- Roffi M, et al.: Linee guida ESC 2015 per la gestione delle sindromi coronariche acute nei pazienti che si presentano senza elevazione persistente del segmento ST: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation della Società Europea di Cardiologia (ESC). Eur Heart J 2016 Jan 14; 37(3): 267-315.
CARDIOVASC 2018; 17(3): 33-34











