Nel corso degli ultimi decenni, la gamma di parametri per il chiarimento delle malattie neurologiche è aumentata in modo sproporzionato rispetto ad altre aree dell’immunologia. Molte malattie di cui non si conosceva la patogenesi o che erano state etichettate come psichiatriche sono in realtà autoimmuni.
Nel corso degli ultimi decenni, la gamma di parametri per il chiarimento delle malattie neurologiche è aumentata in modo sproporzionato rispetto ad altre aree dell’immunologia. Molte malattie di cui non si conosceva la patogenesi o che erano state etichettate come psichiatriche sono in realtà autoimmuni. Questi autoanticorpi sono divisi in due gruppi che differiscono in termini di patogenesi, clinica, associazione con il tumore, terapia, prognosi e diagnosi [1]. Gli anticorpi one riconoscono gli antigeni intracellulari, sono associati a sindromi paraneoplastiche e pertanto sono chiamati anche anticorpi onconeuronali. Gli altri sono diretti contro i domini extracellulari dei recettori o dei canali. Causano encefaliti autoimmuni, rispondono meglio all’immunoterapia e mostrano una prognosi migliore con una terapia precoce, motivo per cui è importante una diagnosi corretta. Gli anticorpi contro la GAD (glutammato decarbossilasi) occupano una posizione intermedia. L’antigene si trova a livello intracellulare presinaptico nelle vescicole sinaptiche, ma viene rilasciato nella fessura sinaptica durante la trasmissione del segnale [2].
Anticorpi contro antigeni intracellulari
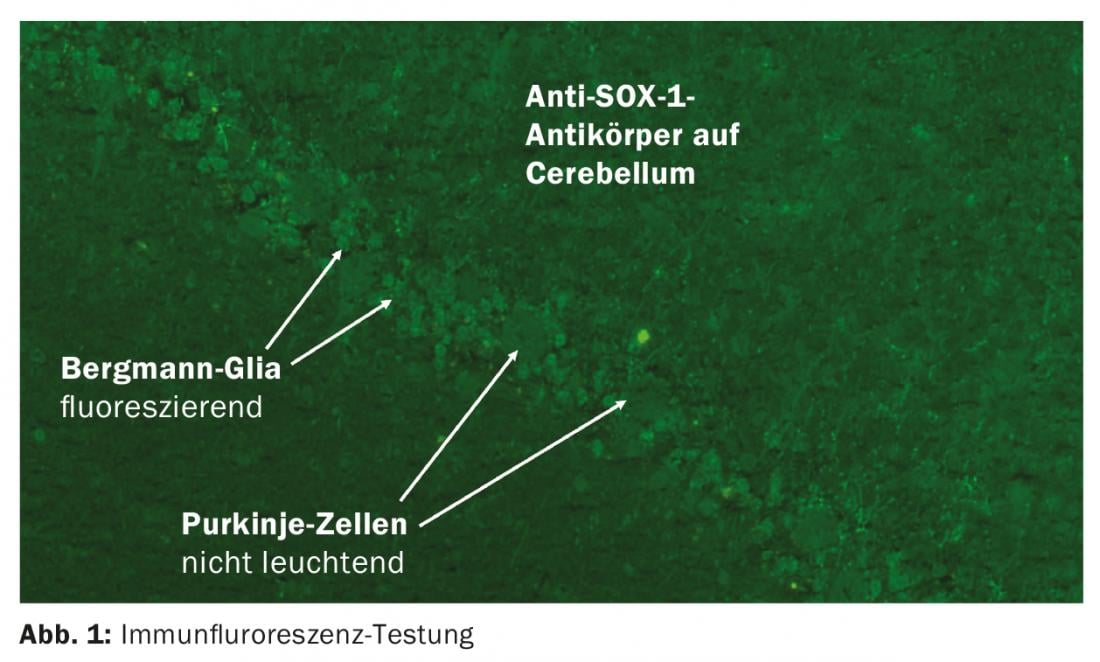
Nel contesto dei tumori, possono verificarsi sintomi neurologici che non sono innescati dal tumore stesso o dalla terapia. Se un tumore, ad esempio un carcinoma del bronco a piccole cellule, che ha origine dal neuroectoderma, esprime proteine neuronali ectopiche [3], il sistema immunitario attiva le cellule T citotossiche come difesa, che possono danneggiare secondariamente le strutture neurologiche. In due terzi dei pazienti, il tumore non è ancora noto quando compaiono i sintomi neurologici. Nel sangue si possono rilevare anticorpi paraneoplastici, che non sono di per sé patogeni, ma sono importanti per la diagnosi [4]. Di norma, questi anticorpi vengono determinati mediante immunoblot. Il siero è sufficiente, il test del liquor non fornisce informazioni aggiuntive. È essenziale che il laboratorio ricontrolli ogni risultato positivo utilizzando l’immunofluorescenza indiretta sul tessuto cerebrale (Fig. 1) [5].
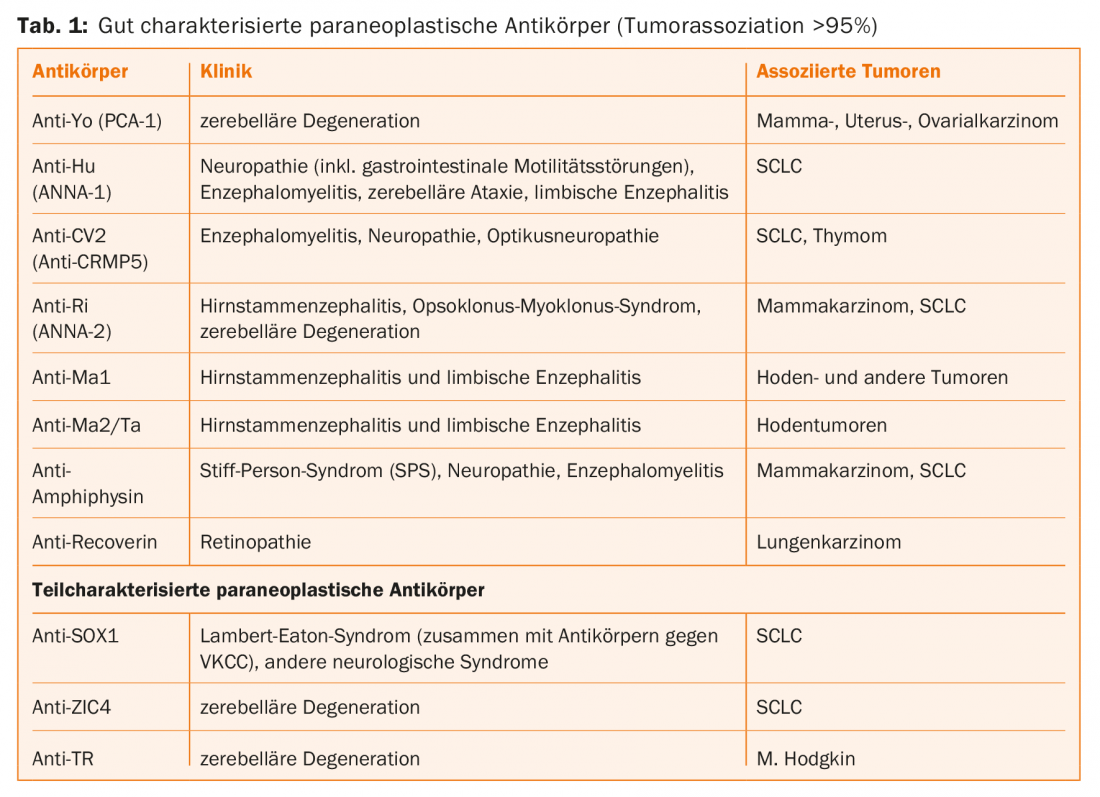
Tra gli anticorpi paraneoplastici, ci sono quelli ben caratterizzati che sono noti per avere una malignità alle spalle in >95% dei casi. Soprattutto nei bambini, ci sono anche casi senza tumore, per cui in questo gruppo di età, questi anticorpi devono essere ricercati se ci sono sintomi corrispondenti [6]. Nel caso degli anticorpi paraneoplastici parzialmente caratterizzati, il valore predittivo rispetto ai tumori non è chiaro a causa del database ancora insufficiente [5]. Gli anti-Tr e gli anti-Sox-1 sembrano essere particolarmente rilevanti come indicazione di malignità. Tuttavia, gli anticorpi paraneoplastici non possono essere rilevati in tutti i pazienti, per cui la rilevazione degli anticorpi non è obbligatoria per la diagnosi. La ricerca del tumore può essere più mirata prendendo in considerazione la sindrome clinica, l’anticorpo e le informazioni su età, sesso e storia di nicotina.
La Tabella 1 elenca gli anticorpi che vengono determinati di routine. Vengono elencate le manifestazioni neurologiche più comuni e i tumori maligni associati.
Anticorpi contro gli antigeni di superficie
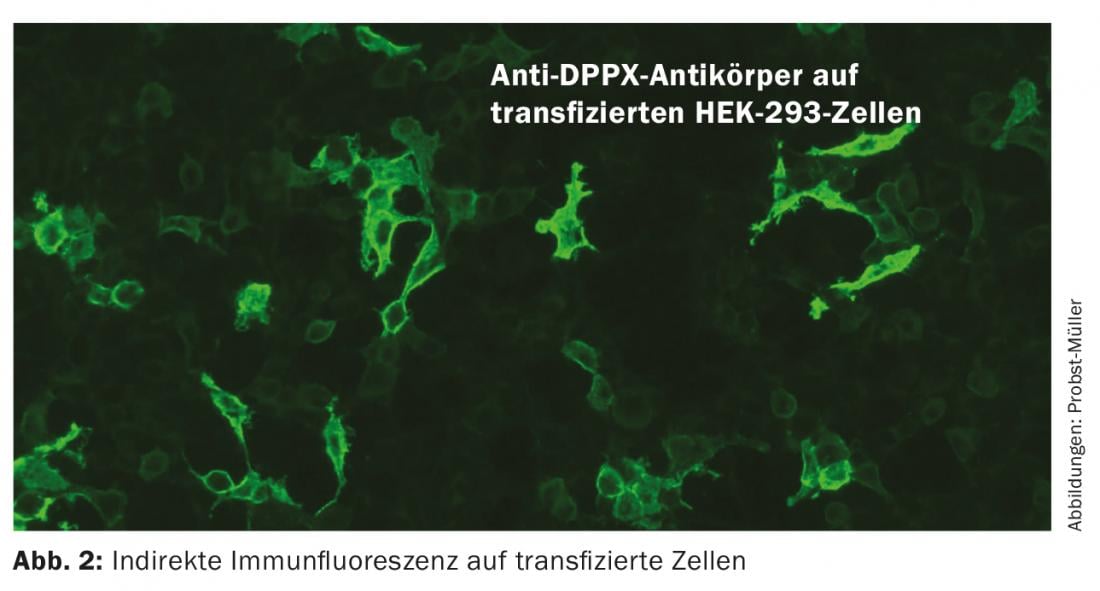
Gli anticorpi contro i canali e i recettori riconoscono epitopi complessi, a differenza degli epitopi lineari degli anticorpi intracellulari. Gli anticorpi scatenano direttamente i sintomi della malattia, in quanto portano a cambiamenti elettrofisiologici, disturbi nella trasmissione sinaptica e nella plasticità neuronale. I possibili meccanismi d’azione sono il reticolo e l’internalizzazione delle proteine. I pazienti spesso rispondono bene all’immunoterapia perché quando l’anticorpo viene rimosso, le proteine possono riprendere la loro posizione sulla membrana e svolgere la loro funzione. Il decorso è spesso monofasico, ma sono possibili recidive. Questi anticorpi hanno molte meno probabilità di essere paraneoplastici. Il rilevamento di questi anticorpi avviene mediante immunofluorescenza indiretta su cellule trasfettate (Fig. 2), per il rilevamento degli anticorpi contro i VGCC (canali del calcio voltaggio-gettati) anche mediante RIA (radioimmunoassay). Gli immunoblots non sono adatti perché denaturano le proteine, il che significa che non vengono più riconosciute dagli anticorpi. Le alterazioni infiammatorie nel liquor e nella risonanza magnetica possono essere assenti, quindi la diagnosi di queste condizioni può essere difficile. Una panoramica degli anticorpi più importanti si trova nella tabella 2.
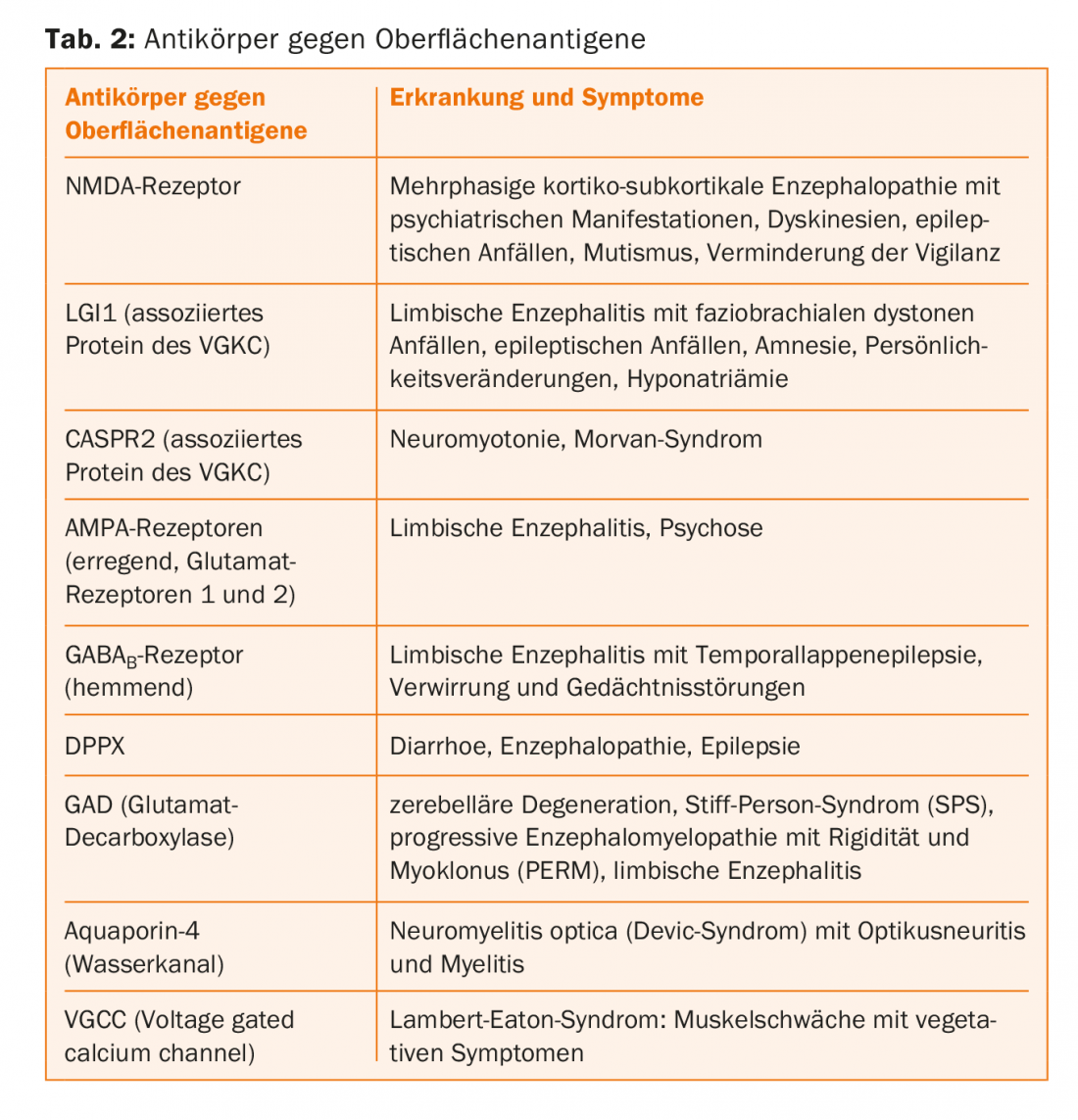
Encefalite limbica (LE): i sintomi tipici della LE sono perdita di memoria, anomalie psichiatriche e crisi epilettiche. In assenza di quest’ultima, in passato la condizione era spesso considerata psichiatrica. Il liquor spesso, ma purtroppo non sempre, mostra alterazioni infiammatorie: pleocitosi linfocitaria, elevazione delle proteine, lieve disturbo della barriera ed eventualmente bande oligoclonali. Le anomalie mediotemporali possono essere presenti nell’EEG e l’infiammazione dell’ippocampo può essere riscontrata nella risonanza magnetica. Inoltre, i pazienti devono essere sottoposti a screening per gli anticorpi associati alla LE. Idealmente, si dovrebbe analizzare il siero e, se possibile, il liquido cerebrospinale. Nella LE è stata descritta un’ampia varietà di anticorpi (Tab. 2). Anche altri mammiferi possono ammalarsi. La crisi epilettica che ha portato all’annegamento dell’orso polare Knut è stata scatenata dagli anticorpi del recettore NMDA.
Recettore NMDA AK encefalite: i recettori NMDA sono canali ionici che vengono attivati dal glutammato. Ci sono molti recettori del glutammato diversi nel sistema nervoso. Sono importanti per gli impulsi nervosi eccitatori. Il nome di recettore NMDA deriva dal fatto che questo canale è attivato dalla molecola sintetica NMDA. L’encefalite scatenata dagli anticorpi contro il recettore NMDA [7,8] è stata originariamente descritta in giovani donne o ragazze con teratoma dell’ovaio, ma sono colpiti anche altri gruppi di età e uomini. In questi pazienti non è presente alcun teratoma. All’inizio della malattia, i disturbi psichiatrici sono in primo piano, seguiti da perdite cognitive e crisi epilettiche. I disturbi della coscienza e la disregolazione autonomica possono portare al ricovero nel reparto di terapia intensiva. Nella maggior parte dei casi, la rilevazione degli anticorpi dal siero è sufficiente. Raramente, solo il liquor è positivo, per cui nei casi di forte sospetto è necessario esaminare anche il liquor.
Encefalite causata da anticorpi contro LGI1 e CASPR2: i canali del potassio voltaggio-gati (VGKC) esistono in tutto il cervello. Servono a ripristinare il potenziale di membrana durante l’iperpolarizzazione. La RIA può essere utilizzata per trovare gli anticorpi contro le VGKC nei pazienti con neuromiotonia ed encefalite limbica. Oggi sappiamo che gli anticorpi non sono diretti direttamente contro la VGKC, ma contro due proteine associate, contro LGI1 e CASPR2 [9]. I pazienti con questi anticorpi sono prevalentemente di sesso maschile. Si tratta di persone che soffrono principalmente di encefalite limbica con sintomi extralimbici come neuromiotonia con spasmi muscolari dolorosi, disturbi del movimento, disturbi del sonno e iponatriemia sierica. A seconda dell’anticorpo, questi sintomi si manifestano con frequenza variabile. Le crisi distoniche faciobrachiali si verificano solo nei pazienti LGI1-positivi. Si tratta di crisi unilaterali con smorfie e distonia del braccio omolaterale che durano meno di tre secondi, ma possono verificarsi fino a centinaia di volte al giorno. Queste crisi sono scatenate da movimenti, emozioni e rumori forti. Poiché queste crisi si verificano prima che si sviluppi l’encefalite limbica con deficit cognitivi, consentono una diagnosi e una terapia precoci. La disautonomia è pericolosa e comporta, tra l’altro, bradicardia e morte cardiaca improvvisa. Questo colpisce soprattutto i pazienti CASPR2-positivi.
I pazienti doppiamente negativi sono quelli che hanno anticorpi contro la VGKC ma sono negativi per gli anticorpi contro LGI1 e CASPR2. Studi recenti dimostrano che questi anticorpi si legano alle parti intracellulari della VGKC o alla dendrotossina del veleno di serpente utilizzata nella RIA, e non sono patogeni. Si trovano nelle persone sane o nei pazienti con malattie non autoimmuni, come il morbo di Alzheimer o il morbo di Parkinson. Inoltre, sono rilevabili nei lavoratori sani dei macelli esposti agli aerosol di cervelli animali. Questi dati mostrano che probabilmente è sufficiente determinare solo gli anticorpi contro LGI1 e CASPR2, ma non quelli contro il complesso VGKC.
Anti-GAD
L’enzima glutammato decarbossilasi (GAD) converte il glutammato, il più importante neurotrasmettitore attivante, in acido γ-aminobutirrico (GABA), il più importante neurotrasmettitore inibente, in un solo passaggio. L’enzima si trova nel sistema nervoso e nel pancreas. Anche se il GAD è una molecola intracellulare, viene rilasciato quando le vescicole sinaptiche nel cervello vengono scaricate e può essere riconosciuto dagli autoanticorpi. Gli autoanticorpi contro il GAD si verificano da un lato nel diabete mellito di tipo I e dall’altro nelle malattie neurologiche [10]. Nel diabete mellito, i titoli sono bassi. Nelle malattie neurologiche, i titoli sono molto alti. Le malattie associate sono l’atassia cerebellare, l’encefalite limbica e la sindrome della persona rigida (SPS). La SPS è una condizione rara che può essere spontanea o paraneoplastica. Una caratteristica tipica è l’aumento del tono muscolare che aumenta nel corso degli anni. Si verificano crampi spontanei o innescati. Poiché questi spasmi sono scatenati anche dalle emozioni, dai suoni, dal tatto, eccetera, spesso la condizione viene inizialmente liquidata come psichiatrica. Nell’elettromiogramma, si riscontra un’attività permanente, anche se il paziente cerca di rilassarsi. Se gli anticorpi contro il GAD sono rilevabili, la SPS di solito non è paraneoplastica. Il rilevamento degli anticorpi contro l’anfifisina (Tab. 1) riguarda le donne con carcinoma mammario.
Prospettiva
Gli anticorpi presentati qui sono solo i più importanti. Altri anticorpi saranno sicuramente aggiunti nei prossimi anni. È importante ricordarlo nei pazienti con sintomi neurologici poco chiari, in modo che la diagnosi venga fatta precocemente e al paziente possa essere offerta la migliore terapia possibile.
Messaggi da portare a casa
- Negli ultimi anni, è stato descritto un gran numero di anticorpi rilevanti dal punto di vista diagnostico e prognostico che scatenano malattie immuno-mediate del sistema nervoso centrale e periferico.
- Gli antigeni bersaglio degli anticorpi sono classificati in base alla loro localizzazione in membranosa e intracellulare.
- Gli anticorpi contro gli antigeni intracellulari come Hu, Ri, Yo, CV2, SOX-1 sono anche chiamati onconeuronali, poiché di solito si verificano nel contesto delle neoplasie. Bisogna cercare un tumore. L’immunoterapia è molto promettente solo in misura limitata.
- Gli anticorpi contro gli antigeni di membrana come i recettori e i canali, ad esempio i recettori NMDA o i canali del potassio, scatenano direttamente i sintomi e portano alle encefaliti autoimmuni. I pazienti di solito rispondono bene all’immunoterapia.
Letteratura:
- Rachel L, et al: Test degli autoanticorpi nelle encefalopatie. Neurologia pratica 2012; 12: 4-13.
- Bost C, et al: Encefalite autoimmune negli istituti psichiatrici: prospettive attuali. Malattie e trattamenti neuropsichiatrici 2016; 12: 2775-2787
- Onganer PU, et al: Caratteristiche neuronali del carcinoma polmonare a piccole cellule. British Journal of Cancer; 93: 1197-1201.
- Dalmau JO, et al: Sindromi paraneoplastiche. Arch Neurol 1999; 56: 405-408.
- www.dgn.org/leitlinien/2383-ll-79-2012-paraneoplastische-neurologische-syndrome
- Honnorat J, et al: Encefalopatia limbica autoimmune e anticorpi anti-Hu in bambini senza cancro. Neurologia 2013; 80(24): 2226-2232.
- Gresa-Arribas N, et al: Titoli anticorpali alla diagnosi e durante il follow-up dell’encefalite da recettore anti-NMDA: uno studio retrospettivo. Lancet Neurol 2014; 13(2): 167-177.
- Dalmau J, et al: Encefalite da recettori anti-NMDA: serie di casi e analisi degli effetti degli anticorpi. Lancet Neurol 2008; 7(12): 1091-1098.
- Binks NM, et al: LGI1, CASPR2 e gli anticorpi correlati: un’evoluzione molecolare dei fenotipi. J Neurol Neurosurg Psychiatry 2017; 0: 1-9.
- Saiz A, et al.: Spettro delle sindromi neurologiche associate agli anticorpi della decarbossilasi dell’acido glutammico: indizi diagnostici per questa associazione. Brain 2008; 131: 2553-2563.
InFo NEUROLOGIA & PSICHIATRIA 2018; 16(2): 4-8.