I DOAc sono almeno pari alla terapia standard con VKA per la VCF non valvolare e il tromboembolismo venoso in termini di sicurezza ed efficacia. Il rischio di emorragia intracranica è dimezzato. Di conseguenza, rappresentano una valida alternativa alla VKA. In caso di insufficienza renale, i limiti di utilizzo devono essere attentamente osservati. Con un’emivita breve dei DOAc e quindi un’elevata richiesta di aderenza ai farmaci, la compliance e una buona istruzione giocano un ruolo importante. Ulteriori studi che confrontino direttamente le DOAK tra loro e che verifichino ulteriori indicazioni sono importanti per consentire un trattamento personalizzato.
Per oltre 50 anni, gli antagonisti della vitamina K (VKA) sono stati l’unica forma perorale di anticoagulazione. Nonostante l’eccellente efficacia e l’elevato grado di familiarità, il loro utilizzo è soggetto a diverse limitazioni, come le interazioni con i farmaci e la dieta, l’attento monitoraggio della terapia e gli aggiustamenti della dose. Questi aspetti, insieme al rischio di gravi emorragie, hanno un impatto critico sull’accettazione da parte del paziente e del medico e, in ultima analisi, possono essere in parte responsabili della sottorappresentazione della VKA nella fibrillazione atriale (circa il 50%) [1, 2].
Negli ultimi anni, sono stati introdotti sul mercato gli anticoagulanti orali diretti (DOAC) con una rapida insorgenza d’azione senza la necessità di un ponte parenterale e una farmacocinetica favorevole con una relazione dose-risposta predittiva e senza la necessità di uno stretto monitoraggio terapeutico. A fronte di una buona efficacia e sicurezza di questi preparati, ci sono punti da tenere presenti, come la dipendenza dalla funzione renale, le interazioni farmacologiche e gli antidoti specifici non ancora disponibili nella pratica clinica. Quella che segue è una panoramica degli aspetti clinici dell’anticoagulazione orale dal punto di vista della medicina interna. L’obiettivo è quello di facilitare le crescenti opzioni di selezione della terapia, nel senso della medicina individualizzata.
Nuovo DOAK – Una panoramica (Tab. 1)
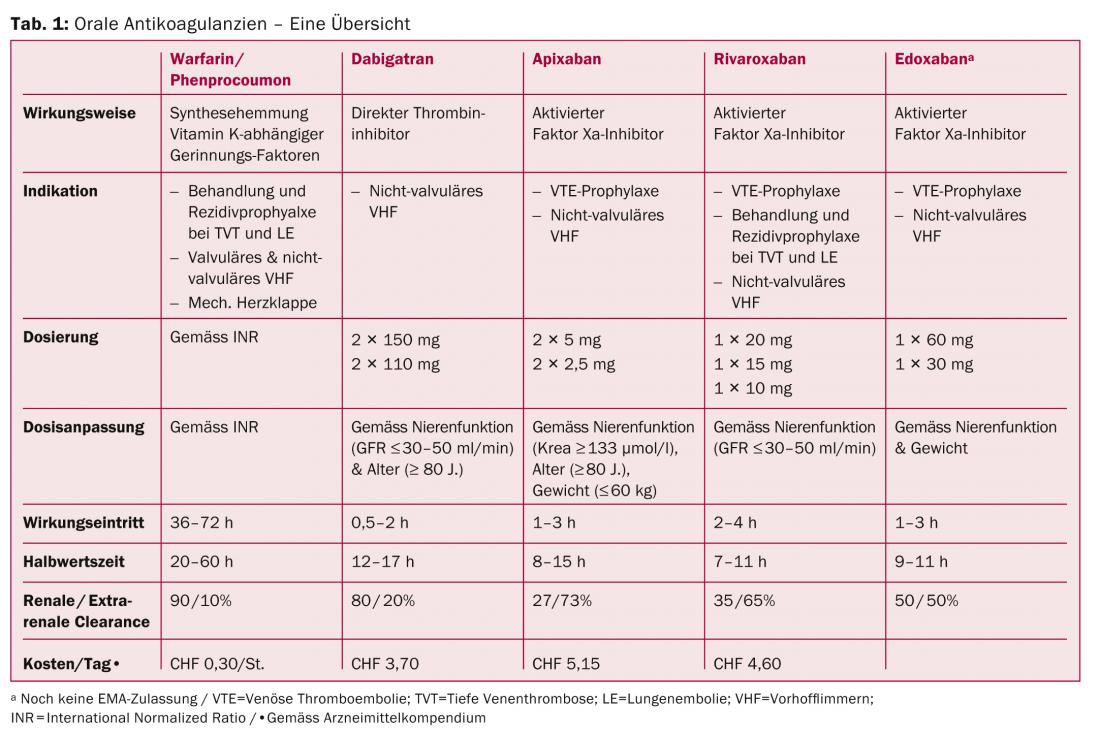
Inibitori diretti del fattore Xa (rivaroxaban; apixaban; edoxaban): L’effetto anticoagulante si esplica attraverso l’inibizione diretta del fattore Xa (Fig. 1) e secondariamente attraverso l’inibizione indiretta della generazione di trombina.
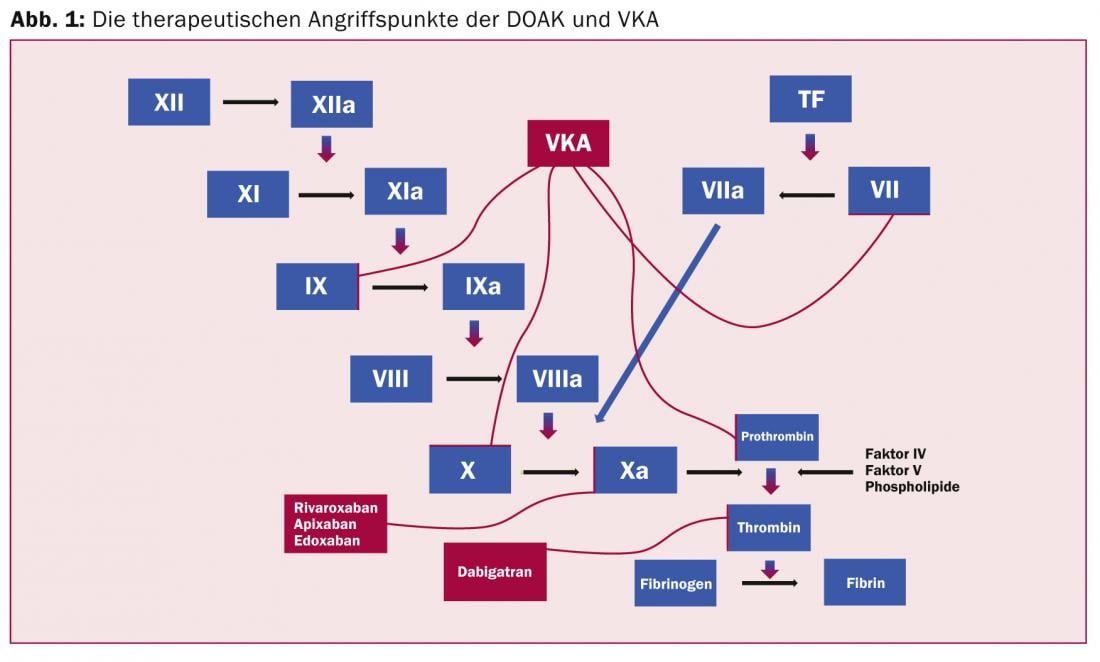
Una molecola di fattore Xa può generare oltre 1000 molecole di trombina nel complesso della protrombinasi.
Inibitore diretto della trombina (dabigatran): L’enzima trombina converte il fibrinogeno in fibrina e amplifica la sua stessa formazione attivando i fattori V, VIII e XI. Inoltre, attiva il fattore XIII stabilizzante il fibrinogeno e le piastrine in modo dipendente dal recettore. L’inibizione indiretta della trombina attraverso l’antitrombina è nota da anni con l’eparina non frazionata. Il meccanismo indiretto, tuttavia, inibisce solo la trombina libera, ma non quella legata alla fibrina, che però svolge un ruolo importante nella crescita del trombo. Gli inibitori diretti della trombina sono in grado di inibire sia la trombina libera che quella legata [3].
Tromboembolismo venoso (VTE) e DOAKs
Fino ad oggi, il trattamento standard per il tromboembolismo venoso (TEV) era la fluidificazione parenterale del sangue con un preparato a base di eparina per almeno cinque giorni, seguito dal trattamento con VKA. Oltre alla necessità di un monitoraggio regolare, questo comportava anche un aumento del rischio di sanguinamento nel contesto della sovrapposizione dell’anticoagulazione.
Gli studi RECORD ed EINSTEIN hanno dimostrato un effetto di rivaroxaban nella prevenzione della trombosi dopo la chirurgia ortopedica (TP dell’anca e del ginocchio) e nel trattamento e nella prevenzione secondaria dell’embolia polmonare, compreso il TEV, equivalente alla terapia standard (recidiva di TEV 2,1% per rivaroxaban e 3% per VKA) con un tasso di emorragia inferiore statisticamente significativo (1,1% contro. 2,2%; HR 0,49, CI 0,31 – 0,79; p=0,003) [4, 5]. La forma di somministrazione diretta per via orale è un vantaggio importante.
Apixaban come tromboprofilassi postoperatoria dopo un intervento di chirurgia ortopedica e come trattamento e profilassi secondaria degli eventi tromboembolici venosi è stato studiato negli studi ADVANCE e AMPLIFY, rispettivamente. Il risultato è stato paritario con la terapia standard in termini di endpoint primari (TEV, morte) con un tasso di sanguinamento inferiore (0,6% vs. 1,8%, HR 0,31; 95% CI 0,17- 0,55) [6, 7].
Negli studi RE-COVER, dabigatran ha avuto un effetto preventivo equivalente sulle TEV ricorrenti (HR 1,08, 95% CI 0,45-1,48) dopo un’anticoagulazione parenterale iniziale di circa nove giorni rispetto a un VKA, con tassi di emorragia maggiore paragonabili (1,6% per dabigatran contro. 1,9% per VKA, HR 0,82; 95% CI 0,45-1,48) e un tasso di sanguinamento complessivo inferiore (16,1% vs. 21,9%, HR 0,71; 95% CI 0,59-0,85).
I tassi di emorragia intracranica sono stati inferiori con tutti i preparati rispetto al VKA.
Tutti e tre i DOAK hanno avuto successo negli studi di estensione, apixaban anche a una dose ridotta di 2×2,5 mg e dabigatran anche rispetto alla VKA.
Attualmente approvato in Svizzera per il trattamento e la profilassi secondaria del TEV è rivaroxaban alla dose di 2×15 mg per tre settimane, seguiti da 1×20 mg. Apixaban e rivaroxaban sono entrambi autorizzati per la tromboprofilassi post-operatoria dopo TP dell’anca e del ginocchio, rispettivamente alla dose di 2×2,5 mg e 1×10 mg.
Fibrillazione atriale e DOAK
La fibrillazione atriale è l’aritmia cardiaca più comune, con una grande rilevanza clinica ed economica per la salute.
Oltre ai VKA, rivaroxaban, dabigatran e apixaban sono ora approvati per la profilassi degli eventi tromboembolici nella VCF non valvolare.
Lo studio ROCKET-AF ha dimostrato che rivaroxaban non è inferiore al trattamento con VKA nella prevenzione dell’ictus e degli eventi embolici sistemici in oltre 14.000 pazienti (tasso di eventi 2,12% vs. 2,42%, HR 0,88), con una superiorità addirittura significativa nell’analisi on-treatment. Inoltre, si è registrato un tasso di emorragia intracerebrale significativamente ridotto (HR 0,67, CI 0,47-0,94, p=0,019) e anche un numero significativamente inferiore di emorragie fatali (HR 0,50, CI 0,31-0,79, p=0,003) con un aumento del rischio di emorragia gastrointestinale (HR 1,25, CI 1,01-1,55, p=0,04) [8].
Lo studio ARISTOTLE ha confrontato apixaban con VKA in oltre 18.000 pazienti con un’efficacia simile contro l’ictus ischemico (0,97% vs. 1,05%, HR 0,92, CI 0,74 -1,13, p=0,42) con una riduzione significativa dell’ictus emorragico (HR 0,51, CI 0,35-0,75, p<0,001) e mortalità (HR 0,89, CI 0,80 – 0,99, p=0,047) [9].
Lo studio RE-LY ha mostrato una riduzione significativa del tasso di ictus ischemico (RR 0,76, CI 0,60 – 0,98, p=0,03, ARR 0,28%/anno-paziente) con una riduzione del rischio di emorragia intracranica per dabigatran alla dose più alta rispetto alla terapia con VKA. Inoltre, c’è stato un leggero aumento del tasso di eventi coronarici (0,82% vs. 0,64%, p=0,09), che è diventato significativo nella meta-analisi, senza influenza sulla mortalità per tutte le cause [10, 11].
Una meta-analisi degli studi di fase III dei quattro DOAK è stata in grado di mostrare un profilo beneficio-rischio favorevole dell’intero gruppo, con una riduzione significativa della mortalità di circa il 10% e del tasso di emorragia intracranica di circa il 50%, con la stessa efficacia contro gli eventi ischemici e, tuttavia, un aumento del tasso di emorragia gastrointestinale.
Allo stesso modo, per i gruppi di rischio clinicamente rilevanti per gli eventi ischemici ed emorragici (età >75 anni, storia di CVI, insufficienza renale), è stato possibile dimostrare la coerenza dell’efficacia e della sicurezza del trattamento DOAK.
[12].

Farmacocinetica e interazioni farmacologiche
Sebbene i DOAK abbiano meno interazioni rispetto ai VKA, ci sono alcune questioni farmacocinetiche che il medico prescrittore deve considerare.
Pertanto, la risecrezione intestinale attraverso il trasportatore P-glicoproteina (P-gp) è significativa con tutti i DOAK, tranne rivaroxaban. L’inibizione competitiva di questo percorso provoca un aumento dei livelli plasmatici. Molti farmaci, spesso utilizzati nei pazienti con VCF, sono substrati della P-gp e devono essere utilizzati con cautela o non utilizzati affatto, soprattutto con dabigatran (verapamil, dronedarone, amiodarone, chinidina).
Il sistema enzimatico CYP3A4 è significativamente coinvolto nell’eliminazione epatica di rivaroxaban e apixaban. In questo senso, le combinazioni con forti inibitori di questa via (claritromicina, eritromicina, ritonavir, ketoconazolo, fluconazolo) e induttori (rifampicina, erba di San Giovanni, carbamazepina, fenitoina, fenobarbital) devono essere evitate se possibile (Tab. 2) [13].
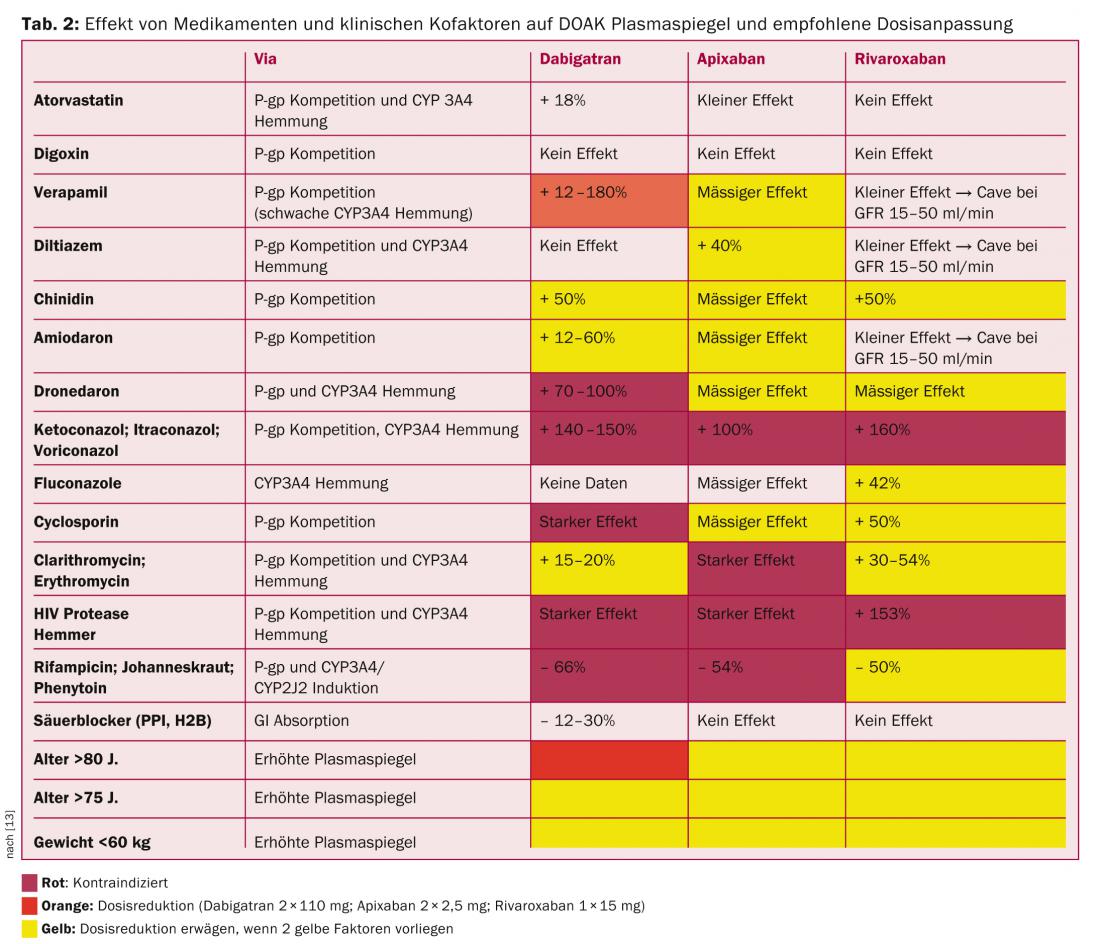
I DOAK stessi non influenzano i sistemi enzimatici menzionati e possono essere combinati con altri substrati (midazolam, atorvastatina, digossina).
La combinazione di tutti i DOAK con agenti antiaggreganti e FANS aumenta il rischio di emorragia di almeno il 60% [14, 15] e deve essere trattata con cautela, con un massimo del 30% di pazienti che assumono agenti antiaggreganti aggiuntivi nei grandi studi.
Se si verifica un aumento del 30-40% della biodisponibilità di rivaroxaban con l’assunzione di cibo, il farmaco deve essere assunto con i pasti.
Controllo della terapia sotto DOAK
Un vantaggio importante del DOAK è che non sono più necessari controlli terapeutici regolari. In alcuni casi, tuttavia, le affermazioni sull’effetto anticoagulante di un trattamento sarebbero di rilevanza clinica. Ad esempio, in caso di grave emorragia, evento tromboembolico, intervento chirurgico urgente, possibile sovradosaggio o compliance problematica.
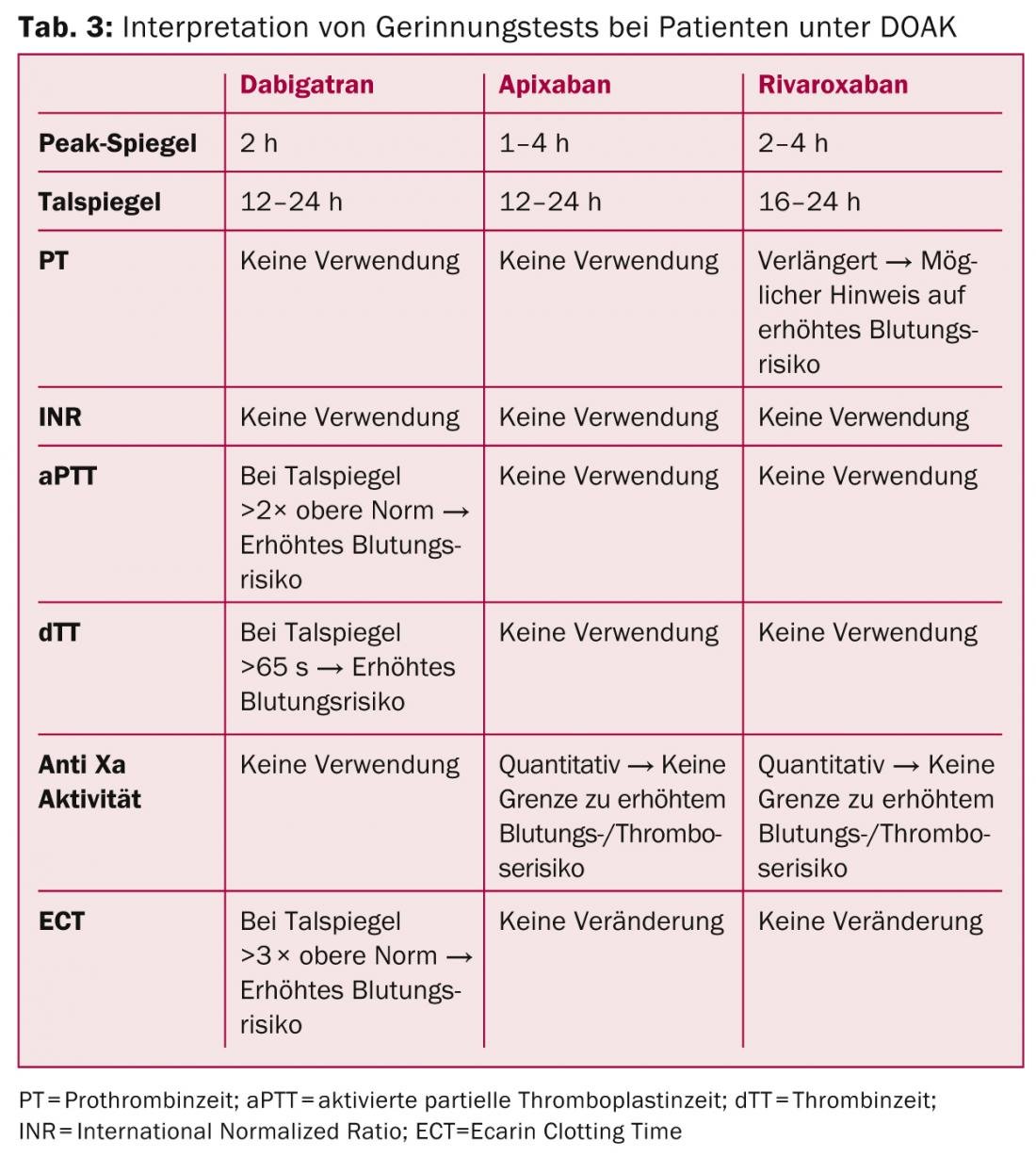
Nel caso degli inibitori della trombina, il “Tempo di coagulazione di Ecarin” (ECT) fornisce informazioni dirette sulla loro attività, anche se con disponibilità limitata. Il prolungamento dell’aPTT fino al raddoppio dopo 12 ore (livello di valle) può indicare un aumento del rischio di sanguinamento con dabigatran. Una misurazione standardizzata del tempo di trombina (ad esempio Hemoclot® per dabigatran) può riflettere più accuratamente lo stato di coagulazione, con un tempo di trombina diretto di >65 secondi e una concentrazione plasmatica di dabigatran di >200 ng/ml (valle) che indica un aumento del rischio di sanguinamento.
Per gli antagonisti del fattore Xa, si verifica un prolungamento del tempo di protrombina (PT) dipendente dalla concentrazione. Inoltre, l’attività del Fattore Xa può essere determinata in modo specifico con l’aiuto del plasma calibrato per il farmaco corrispondente, anche se le associazioni dirette tra i parametri della coagulazione e il rischio di emorragia non sono ancora certe (Tab. 3) [13].
DOAK nell’insufficienza renale
L’insufficienza renale cronica è considerata un fattore di rischio per gli eventi tromboembolici ed emorragici nei pazienti con VCF [16].
In assenza di dati clinici, i DOAc non sono utilizzati nell’insufficienza renale avanzata (GFR <30 ml/min) secondo le attuali linee guida ESC, mentre sembrano essere una valida alternativa ai VKA nella funzione moderatamente compromessa (GFR 30-50 ml/min) a dosi adattate [17]. Personalmente, gli autori sono già cauti a partire da un GFR di 40 ml/min.
In generale, i pazienti con funzione renale compromessa che assumono DOAK devono essere seguiti almeno ogni sei mesi. Ancora più frequente nei pazienti anziani e polimorfi e nei fattori di rischio di deterioramento acuto (ad esempio, infezioni, insufficienza cardiaca).
Complicazioni emorragiche con DOAK
Come tutti gli anticoagulanti, i DOAK comportano anche un aumento del rischio di gravi emorragie. In particolare, la terapia antiaggregante additiva, la combinazione con FANS e la disfunzione renale aumentano il tasso di sanguinamento. Non sono ancora disponibili antidoti specifici (attualmente in fase di sperimentazione II). Oltre alle consuete misure non specifiche, gli esperti raccomandano la somministrazione di concentrato di complesso protrombinico attivato o regolare (PKK, ad esempio Beriplex®; aPKK Feiba®), nonché di fattore VII attivato (Novoseven®).
Se dabigatran è dializzabile, esiste la possibilità di emodialisi terapeutica (soprattutto nell’insufficienza renale).
Malattia coronarica e VHF sotto OAK
La combinazione di VCD e malattia coronarica non è solo comune, ma anche complessa e associata a un aumento significativo della mortalità [18].
Nel contesto acuto, occorre seguire le attuali linee guida e sospendere l’OAC a favore di una duplice terapia antiaggregante con anticoagulazione parenterale.
Nella malattia coronarica stabile, il rapporto beneficio-rischio della terapia combinata deve essere valutato utilizzando i punteggi comuni per il rischio tromboembolico (CHA2DS2-VASc), aterotrombotico (GRACE) e di sanguinamento (punteggio HAS-BLED).
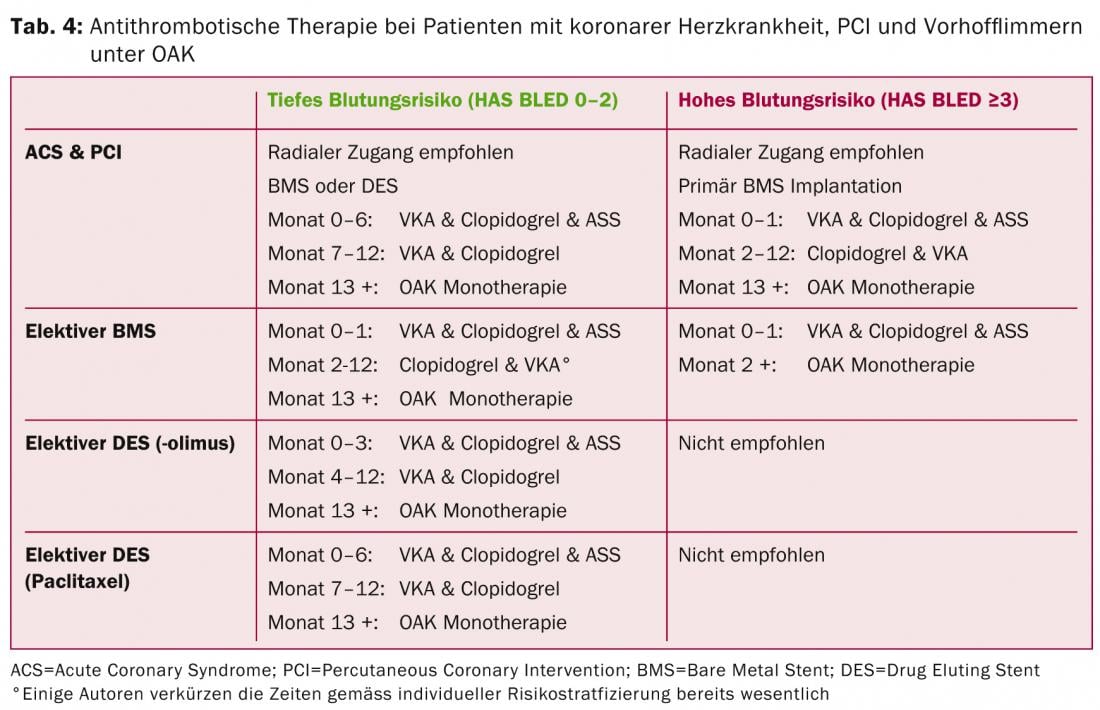
È importante notare che la triplice terapia con doppio antiaggregante e OAK raddoppia almeno il rischio di emorragia e deve essere mantenuta il più breve possibile [19]. I DOAK sono anche un’alternativa ai VKA nella terapia combinata. I nuovi inibitori P2Y12 (prasugrel, ticagrelor) non sono raccomandati nella terapia tripla a causa dell’aumento della tendenza al sanguinamento (eccezione: allergia al clopidogrel, trombosi dello stent sotto clopidogrel). La Tabella 4 offre una panoramica delle attuali raccomandazioni ESC in diversi scenari clinici [20].
Valvole cardiache meccaniche e DOAK
Lo studio RE-ALIGN ha confrontato dabigatran con VKA nei pazienti con valvole protesiche meccaniche.
Lo studio ha dovuto essere interrotto precocemente nella fase II, dopo che è stato dimostrato un aumento del tasso di ictus (5% vs. 0%) e un aumento del tasso di emorragie maggiori (4% vs. 2%; HR 1,76, 95% CI 0,37-8,46) [21].
In questo senso, i VKA rimangono l’unica forma perorale di anticoagulazione nei pazienti con valvole cardiache meccaniche.
Conclusioni
I DOAc sono almeno pari, e in alcuni casi significativamente superiori, alla terapia standard con VKA per la fibrillazione atriale non valvolare e il tromboembolismo venoso in termini di sicurezza ed efficacia, dimezzando contemporaneamente il rischio di sanguinamento intracranico, e rappresentano una valida alternativa ai VKA (raccomandazione ESC di classe IIa, livello di evidenza A). Il controllo di routine dell’effetto anticoagulante viene omesso. In caso di insufficienza renale, i limiti di utilizzo devono essere attentamente osservati. I controlli di laboratorio della funzione renale sono raccomandati annualmente nei pazienti con funzione conservata e almeno ogni sei mesi nei pazienti con funzione compromessa (<40 ml/min; formalmente da GFR 30-60 ml/min). Inoltre, occorre tenere presente i sottogruppi come i pazienti “fragili e anziani”, i pazienti oncologici, gli eventi speciali (infezioni, disidratazione, insufficienza cardiaca, ecc.), l’aumento del rischio di sanguinamento gastrointestinale e le interazioni farmacologiche. Con un’emivita breve dei DOAc e quindi un’elevata richiesta di aderenza ai farmaci, la compliance e una buona istruzione sono particolarmente importanti. Tutti i pazienti devono essere muniti di una scheda di medicazione e di istruzioni per l’uso chiaramente definite. Ulteriori studi con un confronto diretto tra DOAK e test di indicazione in ulteriori gruppi di pazienti (ad esempio, pazienti pediatrici e oncologici) sono importanti per consentire un trattamento personalizzato.
Nicole R. Bonetti
Letteratura:
- Birman-Deych E, et al: Uso ed efficacia del warfarin nei beneficiari di Medicare con fibrillazione atriale. Stroke 2006; 37: 1070-1074.
- Hylek EM, et al: Emorragia maggiore e tollerabilità del warfarin nel primo anno di terapia tra i pazienti anziani con fibrillazione atriale. Circolazione 2007; 115: 2689 -2696.
- Weitz JI, Crowther M: Inibitori diretti della trombina. Ricerca sulla trombosi 2002; 106: V275 – 84.
- Gli sperimentatori EINSTEIN: Rivaroxaban orale per il tromboembolismo venoso sintomatico. N Engl J Med 2010; 363: 2499-2510.
- Gli sperimentatori EINSTEIN: Rivaroxaban orale per l’embolia polmonare sintomatica. N Engl J Med 2012; 366: 1287-1297.
- Agnelli G., et al: Apixaban orale per il trattamento del tromboembolismo venoso acuto. N Engl J Med 2013; 369: 799 – 808.
- Lassen MR, et al: Apixaban rispetto a enoxaparina per la tromboprofilassi dopo la sostituzione dell’anca. N Engl J Med 2010; 363: 2487-2498.
- Patel MR, et al: Rivaroxaban rispetto a warfarin nella fibrillazione atriale non valvolare. N Engl J Med 2011; 365: 883-891.
- Granger CB, et al: Apixaban rispetto a warfarin nei pazienti con fibrillazione atriale. N Engl J Med 2011; 365: 981-992.
- Connolly SJ, et al: Dabigatran rispetto a warfarin nei pazienti con fibrillazione atriale. N Engl J Med 2009; 361: 1139-1151.
- Hohnloser SH, et al: Eventi ischemici miocardici in pazienti con fibrillazione atriale trattati con dabigatran o warfarin nello studio RE-LY. Circolazione 2012; 125: 669-676.
- Ruff CT, et al: Confronto dell’efficacia e della sicurezza dei nuovi anticoagulanti orali con il warfarin nei pazienti con fibrillazione atriale: una meta-analisi di studi randomizzati. The Lancet 2013; DOI: 10.1016/S0140-6736(13)62343-0.
- 13 Heidbuchel H, et al: Guida pratica della European Heart Rhythm Association sull’uso dei nuovi anticoagulanti orali nei pazienti con fibrillazione atriale non valvolare. Società Europea di Cardiologia 2013; doi:10.1093/europace/eut083.
- Mega JL, et al: Rivaroxaban nei pazienti con una recente sindrome coronarica acuta. N Engl J Med 2012; 366: 9-19.
- Alexander JH, et al: Apixaban con la terapia antiaggregante dopo una sindrome coronarica acuta. N Engl J Med 2011; 365: 699 -708.
- Olesen JB, et al: Ictus ed emorragia nella fibrillazione atriale con malattia renale cronica. N Engl J Med 2012; 367: 625-635.
- Fox KA, et al: Prevenzione dell’ictus e dell’embolia sistemica con rivaroxaban rispetto a warfarin nei pazienti con fibrillazione atriale non valvolare e moderata insufficienza renale. Eur Heart J 2011; 32: 2387-2394.
- Lopes RD, et al: Terapia antitrombotica ed esiti dei pazienti con fibrillazione atriale dopo un intervento coronarico percutaneo primario: risultati dello studio APEX-AMI. Eur Heart J 2009; 30: 2019 -2028.
- Lamberts M, et al: Emorragia dopo l’inizio di più farmaci antitrombotici, compresa la tripla terapia, nei pazienti con fibrillazione atriale dopo infarto miocardico e intervento coronarico: uno studio di coorte a livello nazionale. Circolazione 2012; 126: 1185-1193.
- Freek WA Verheugt: Terapia antitrombotica durante e dopo l’intervento coronarico percutaneo nei pazienti con fibrillazione atriale. Circolazione 2013; 128: 2058-2061.
- Eikelboom J, et al: Dabigatran rispetto a Warfarin nei pazienti con valvole cardiache meccaniche. N Engl J Med 2013; 369: 1206-1214.
CARDIOVASC 2014; 13(2): 5-10