L’emicrania è la malattia neurologica più comune e influisce pesantemente sulla qualità di vita delle persone colpite. Per prevenire la cronicizzazione, le misure profilattiche stanno diventando sempre più importanti nella terapia dell’emicrania. Il principio dei nuovi anticorpi contro il peptide legato al gene della calcitonina (CGRP) è quello di iniziare dove inizia il dolore.
Il disturbo da cefalea primaria, caratterizzato da attacchi di cefalea pulsante unilaterale, da moderata a grave, della durata di 4-72 ore e tipicamente associati a sintomi vegetativi, è un disturbo neurologico grave. Tuttavia, spesso è ancora sottodiagnosticata, come ha avvertito il Prof. Messoud Ashina, MD, Copenaghen, in occasione di un simposio satellite iniziato da TEVA al 5° Congresso dell’Accademia Europea di Neurologia (EAN). Tuttavia, i sintomi come gli attacchi di mal di testa, la nausea, la sensibilità alla luce e al suono rappresentano un pesante fardello per le persone colpite e spesso portano a limitazioni significative nella vita quotidiana. Se i sintomi si verificano per almeno 15 giorni al mese, di cui almeno otto giorni soddisfano i criteri diagnostici dell’emicrania, l’emicrania è cronica. Per prevenire questo processo, i pazienti devono ricevere una profilassi adeguata, oltre a una terapia acuta efficace.
Finora, i principali farmaci disponibili per il trattamento preventivo sono stati i beta-bloccanti, i calcio-antagonisti e gli anticonvulsivanti. Tuttavia, poiché non sono stati sviluppati specificamente per la profilassi dell’emicrania, comportano un ampio spettro di effetti collaterali. Pertanto, molti pazienti interrompono la profilassi orale dopo poco tempo. Di conseguenza, è stata condotta una ricerca intensiva su nuove sostanze mirate, efficaci e ben tollerate. Un ruolo chiave nello sviluppo degli attacchi di emicrania è svolto dal peptide legato al gene della calcitonina (CGRP), che induce la vasodilatazione e aumenta il flusso sanguigno cerebrale, ha riferito il Prof. Anthony Dickenson, MD, Londra. Durante un attacco, i livelli di CGRP sono elevati nel cervello e nelle meningi. In questo contesto, sono stati sviluppati gli anticorpi CGRP, che ora vengono trattati come una possibile nuova pietra miliare nella profilassi dell’emicrania, grazie ai dati positivi degli studi.
Gestione dell’emicrania sotto controllo
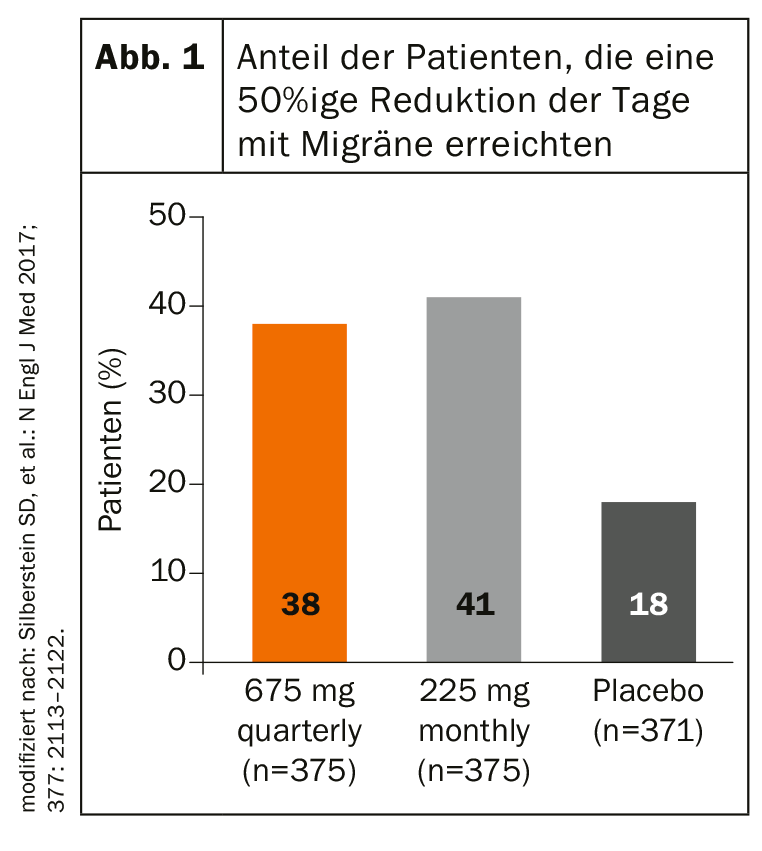
Con fremanezumab, erenumab e galcanezumab, ci sono tre anticorpi che rappresentano la nuova opzione terapeutica. Mentre erenumab blocca il recettore CGRP, fremanezumab e galcanezumab si legano direttamente al neuropeptide. Negli studi di fase III, fremanezumab ha dimostrato un inizio d’azione straordinariamente precoce sia nell’emicrania episodica che in quella cronica. Già alla quarta settimana, c’era una differenza significativa rispetto al placebo. I pazienti con emicrania episodica sono stati trattati con l’iniezione di fremanezumab o placebo una o tre volte a intervalli di quattro settimane durante lo studio di tre mesi. Nei gruppi verum, il numero medio di giorni di mal di testa mensili è diminuito significativamente di più con 2,9 giorni (iniezione sottocutanea al trimestre) e 3,0 giorni (iniezione sottocutanea mensile), rispettivamente, rispetto al placebo con 1,6 giorni. Nello studio sull’emicrania cronica, il numero di giorni mensili con emicrania è diminuito in media di 4,3 e 4,6 nel gruppo verum (placebo: -2,5 giorni). Anche la percentuale di pazienti con una riduzione di almeno il 50% dei giorni di emicrania mensili è stata significativamente più alta con fremanezumab (Fig. 1) . Questi effetti sono rimasti stabili anche a lungo termine per un periodo di 12 settimane, come ha spiegato il Prof. Dr. med. Zaza Katsarava, Unna.
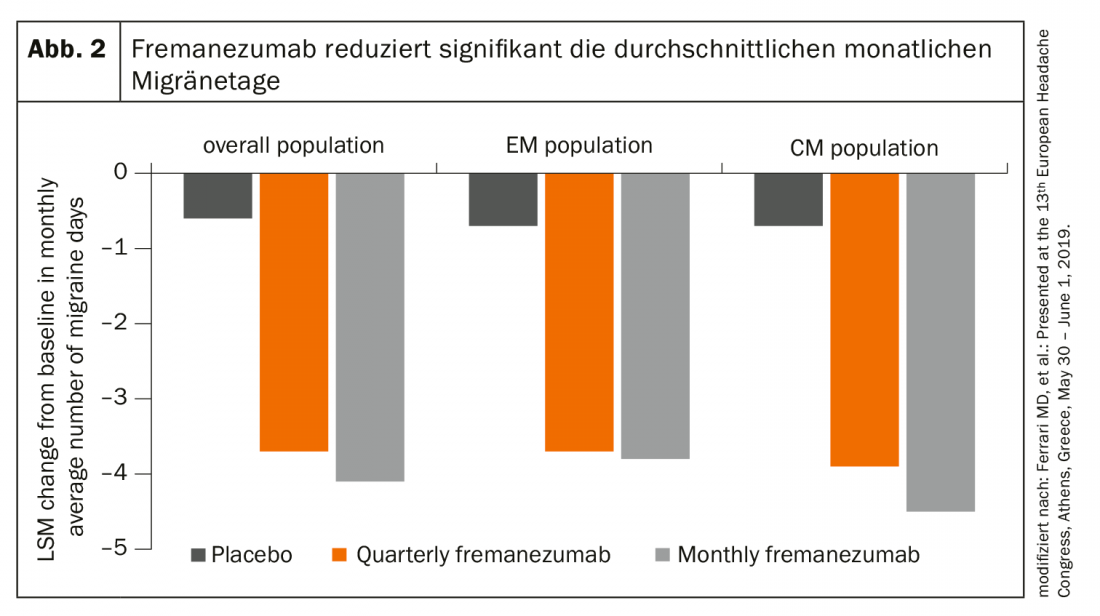
Inoltre, uno studio Focus ha potuto dimostrare che l’anticorpo CGRP riduce in modo significativo sia il numero medio di giorni di emicrania che l’uso di farmaci per l’emicrania acuta dopo una sola settimana di trattamento – nell’emicrania episodica e cronica (Fig. 2). Sono state dimostrate anche una buona sicurezza e tolleranza a lungo termine.
Fonte: TEVA
InFo NEUROLOGIA & PSICHIATRIA 2019; 17(5): 32











