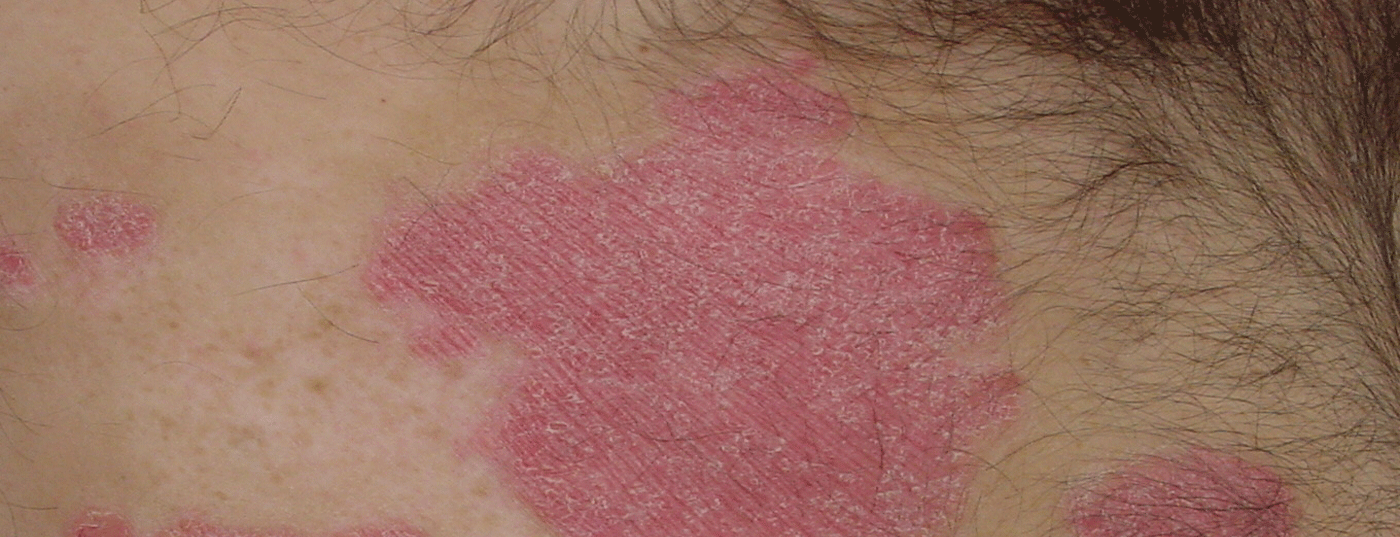
Alla Giornata annuale della psoriasi svizzera a Basilea, sono stati discussi i vantaggi dei registri della psoriasi internazionali e nazionali. Un altro tema era la possibilità di ottimizzare la terapia per la psoriasi a placche grave e moderata. Se non ci sono problemi di sicurezza, il passaggio dai farmaci convenzionali e biologici alle terapie successive non comporta necessariamente un periodo di wash-out. Anche l’ampia gamma di comorbilità, in particolare le condizioni cardiovascolari e artritiche, è stata oggetto del ciclo di conferenze.
Il Prof. Dr. med. Matthias Augustin, di Amburgo, ha parlato dei vantaggi dei registri europei della psoriasi. Un registro dei pazienti è un sistema organizzato,
- che funziona secondo i metodi di uno studio osservazionale.
- che raccoglie dati uniformi (clinici e di altro tipo).
- che valuta i risultati specificati.
- che si riferisce a una popolazione definita da una malattia, una condizione di salute specifica o una terapia.
- che serve uno scopo scientifico, clinico o politico predeterminato.

“Un registro dovrebbe quindi essere in grado di valutare e confrontare l’efficacia clinica o il costo finanziario di una o più terapie diverse. La sicurezza o la nocività a lungo termine di specifici farmaci o trattamenti viene quindi valutata per migliorare la qualità dell’assistenza. Inoltre, un registro può essere valutato per i dati di incidenza e prevalenza, nonché per le tendenze della malattia nel tempo”, ha riassunto il Prof. Augustin. (Tab. 1).

I registri hanno il vantaggio di includere pazienti che non avrebbero potuto partecipare agli studi clinici (RCT). Da un lato, questo limita ovviamente l’importanza dei registri in termini di ricerca, ma corrisponde maggiormente alla vita clinica reale di tutti i giorni [1]. Ad esempio, è stato dimostrato che il rischio di sviluppare effetti collaterali gravi della terapia con sistemi biologici e non biologici per la psoriasi era più alto per i pazienti che facevano parte di registri ma non erano idonei per gli RCT [2]. I registri forniscono quindi informazioni sulla sicurezza e sull’efficacia dei farmaci in un contesto reale.
“Quindi le condizioni degli RCT non corrispondono sempre alla pratica clinica quotidiana. Tuttavia, le raccomandazioni basate sul consenso degli esperti non si basano su dati empirici e le linee guida sono solitamente più orientate verso il paziente non complicato. Sono proprio queste le lacune che i registri possono colmare, ad esempio analizzando i dati del mondo reale e testando le terapie utilizzando endpoint fissi come il punteggio PASI”, ha spiegato il Prof. Augustin. Uno di questi registri internazionali sulla psoriasi è il cosiddetto PSOLAR, che comprende un totale di 12 035 pazienti, di cui 1038 provenienti dall’Europa.
“Sempre più spesso, questi registri forniscono dati che vengono riassunti nelle pubblicazioni. Un esempio è il Biobadaderm spagnolo [2]. Eppure, va notato: Cercando di riunire i registri, ad esempio in una rete europea (PsoNet), non bisogna dimenticare le differenze dei singoli Paesi e dei sistemi sanitari. Rappresentano una sfida per l’interpretazione dei dati [3]. Il numero di pazienti trattati per dermatologo, la terapia precedente, l’uso di biologici – ci sono grandi differenze a livello internazionale”, ha spiegato il Prof. Augustin.
Ottimizzazioni della terapia
Come si può ottimizzare il trattamento della psoriasi a placche da moderata a grave? Questa domanda è stata discussa dal Prof. Dr. med. Ulrich Mrowietz, Kiel: “La psoriasi è una malattia infiammatoria sistemica che deve essere affrontata tenendo conto delle comorbidità e dei fattori scatenanti. I programmi contro l’obesità e il fumo hanno senso in questo caso. L’obiettivo della gestione della psoriasi deve essere quello di migliorare i sintomi della pelle, ma anche le malattie concomitanti. Senza dimenticare la comorbilità nell’area psicologica: i pazienti affetti da psoriasi ne soffrono spesso”.
Le linee guida prevedono una terapia sistemica nelle forme gravi, sia convenzionale “di prima linea” con ciclosporina, esteri dell’acido fumarico, metotrexato, fototerapia e retinoidi, sia con i biologici “di seconda linea” adalimumab, etanercept, infliximab e ustekinumab.
Algoritmo degli obiettivi terapeutici: se il ∆PASI è <50 rispetto al basale, la terapia deve essere adattata. Se è ≥75, può essere mantenuto e continuato. Nella fascia intermedia (∆PASI ≥50 <75), il DLQI è decisivo. Se questo è >5, la terapia deve essere adattata; se è ≤5, può essere continuata [4]. “Le possibilità di aggiustamento della terapia sono un aumento della dose o una riduzione degli intervalli di dosaggio, combinazioni con farmaci topici o sistemici o, infine, un cambio di terapia o di farmaco. Gli scenari di commutazione variano (si veda il riquadro) ed esistono poche prove in letteratura [5].

In ogni caso, i farmaci possono essere cambiati in caso di efficacia insufficiente (fallimento della terapia primaria/secondaria), intolleranza o per motivi di sicurezza (comparsa di effetti collaterali)”, afferma il Prof. Mrowietz. “Tuttavia, non esiste una definizione stabilita di risposta clinica inadeguata. Negli studi clinici pubblicati con gli antagonisti del TNF, la mancata risposta primaria è stata definita come il mancato raggiungimento di un PASI 50”.
Passare dai farmaci convenzionali
Acitretina: nessun successo di trattamento con l’acitretina dopo 24 settimane, nonostante l’aumento della dose. Il passaggio all’anti-TNF o all’ustekinumab può avvenire senza un periodo di washout. L’acitretina può anche essere utilizzata in sovrapposizione o contemporaneamente a questi biologici.
Ciclosporina: nessun successo di trattamento con la ciclosporina dopo 16 settimane, nonostante l’aumento della dose. Il passaggio agli anti-TNF o all’ustekinumab può (probabilmente) essere effettuato senza un periodo di washout. Secondo le attuali conoscenze, una breve sovrapposizione con la ciclosporina sembra ridurre il rischio di una battuta d’arresto della terapia.
Metotrexato: nessun successo di trattamento con il metotrexato dopo 24 settimane, nonostante l’aumento della dose. Il passaggio all’anti-TNF o all’ustekinumab può avvenire senza un periodo di washout. Il metotrexato può anche essere utilizzato in sovrapposizione o contemporaneamente a questi biologici.
Passaggio dai biologici
Efficacia: in linea di principio, l’esperienza dimostra che il primo farmaco biologico rimane efficace più a lungo. Tuttavia, se è necessario passare a un altro biologico perché il primo non è sufficientemente efficace, il cambio viene effettuato al momento normalmente previsto senza un periodo di washout. Questo prima con la dose di induzione, poi con la dose di mantenimento.
Se il farmaco iniziale è adalimumab, il tempo che intercorre fino alla successiva assunzione normalmente programmata o fino al cambio è solitamente di due settimane. Se si tratta di etanercept, la durata è di una settimana. Con infliximab, lo switch può essere preso in considerazione già due o quattro settimane dopo l’ultima dose di infliximab, soprattutto nei casi di fallimento del trattamento. Anche con l’ustekinumab, dove in realtà si otterrebbe un intervallo di otto-dodici settimane, è possibile un cambio già due-quattro settimane dopo l’ultima dose (di nuovo, in caso di fallimento del trattamento).
Sicurezza: se si decide di passare a un altro biologico a causa di considerazioni sulla sicurezza, potrebbe essere necessario un intervallo senza terapia fino a quando il rispettivo parametro di sicurezza si sarà normalizzato o stabilizzato.
Trattamento successivo con lo stesso biologico: “Fondamentalmente, si può affermare che si possono ottenere risultati di efficacia migliori con una terapia biologica continua per un periodo di tempo più lungo, rispetto a una terapia interrotta. Dopo un’interruzione della terapia, può verificarsi una perdita di efficacia con un nuovo trattamento con lo stesso biologico”, afferma il Prof. Mrowietz.
Comorbilità
“La psoriasi raramente si presenta da sola”, ha detto il Prof. Wolf-Henning Boehncke, MD, dell’Ospedale Universitario di Ginevra, introducendo la sua conferenza. “Tra la moltitudine di comorbidità, vorrei individuare due gruppi, ovvero le condizioni cardiovascolari/metaboliche e quelle artritiche. L’artrite psoriasica (PsA) è di per sé una malattia estremamente complessa e presenta diverse manifestazioni. Se la PsA deve essere trattata, è importante rendersi conto che non è semplicemente una sorella minore dell’artrite reumatoide (RA). Questa forma è più diffusa di quanto si pensasse in origine e dovrebbe essere diagnosticata precocemente in presenza di alterazioni dermatologiche”.
Lo screening della PsA può essere integrato, ad esempio, con semplici questionari in cui il paziente indica quali e quante articolazioni gli causano disagio. La PsA periferica viene inizialmente trattata con farmaci antinfiammatori non steroidei; i DMARD possono essere utilizzati per l’artrite/sinovite persistente e gli inibitori del TNF-alfa per l’entesite o la dattilite. Queste terapie TNF con adalimumab [6], etanercept [7] e infliximab [8] mostrano alti tassi di risposta nella PsA. All’EULAR 2012 sono stati presentati anche i risultati di uno studio di fase III su ustekinumab, anch’essi promettenti: Come le terapie TNF, il farmaco ha migliorato i sintomi cutanei e articolari [9].
“Per molto tempo si è pensato che la malattia cardiovascolare nei pazienti affetti da psoriasi fosse causata esclusivamente dai fattori di rischio comuni dei due complessi patologici: ad esempio, l’obesità e la sindrome metabolica [10]. Oggi esistono concetti che vedono la psoriasi insieme all’obesità come origine di un percorso patologico che può portare all’infiammazione sistemica, all’insulino-resistenza, alla disfunzione endoteliale, all’aterosclerosi e all’infarto miocardico. Questo ci darebbe un’idea di come la psoriasi contribuisca alle comorbidità cardiovascolari [11]. In questo caso, è necessario raccogliere ulteriori prove”, afferma il Prof. Boehncke. Questo avrebbe conseguenze anche sulla scelta della terapia: Gli agonisti dell’insulina possono avere un effetto antipsoriasico [12]?
È anche importante conoscere le comorbidità, perché in alcuni casi i farmaci antipsoriasi sistemici possono essere controindicati: La ciclosporina A nell’ipertensione, il metotrexato nella malattia epatica, l’acitretina nella dislipidemia. In sintesi, si può dire quanto segue:
- Le comorbidità influenzano la scelta della terapia.
- I dermatologi sono in grado di diagnosticare precocemente la PsA.
- La psoriasi è un fattore di rischio cardiovascolare indipendente.
- Molte comorbidità continuano ad essere sottovalutate, soprattutto i disturbi d’ansia e la depressione.
Fonte: Giornata annuale della psoriasi in Svizzera, 31 ottobre 2013, Basilea.
Letteratura:
- Zink A, et al: Arthritis & Rheumatism 2006; 54(11): 3399-3407. DOI 10.102/art.22193.
- Garcia-Doval I, et al: Arch Dermatol 2012 Apr; 148(4): 463-470. DOI: 10.1001/archdermatol.2011.2768.
- Ormerod AD, et al: Dermatologia 2012; 224(3): 236-43. DOI: 10.1159/000338572. epub 2012 Jun 1.
- Mrowietz U, et al: Arch Dermatol Res 2011; 303(1): 1-10.
- Mrowietz U, et al: J Eur Acad Dermatol Venerol 2013 Feb 26.
- Mease PJ, et al: Arthritis Rheum 2005 Oct; 52(10): 3279-3289.
- Mease PJ, et al: Arthritis Rheum 2004 Jul; 50(7): 2264-2272.
- Antoni C, et al: Ann Rheum Dis 2005; 64: 1150-1157. DOI:10.1136/ard.2004.032268.
- McInnes IB, et al: EULAR 2012, abstract #OP0158.
- Gisondi P, et al: British Journal of Dermatology 2007; 157(1): 68-73.
- Boehncke WH, et al: BMJ 2010 Jan 15; 340: b5666. DOI: 10.1136/bmj.b5666.
- Hogan AE, et al: Diabetologia 2011 Nov; 54(11): 2745-54. DOI: 10.1007/s00125-011-2232-3. Epub 2011 Jul 9.
PRATICA DERMATOLOGICA 2014; 24(1): 35-37