Gli estratti di iperico sono comprovati per il trattamento dei disturbi depressivi. Tuttavia, alcune preparazioni abbassano i livelli plasmatici di altri farmaci inducendo il CYP3A4 e la P-glicoproteina (ABCB1) e compromettono la loro efficacia. Queste interazioni farmacocinetiche non si osservano con gli estratti a basso contenuto di iperforina. Il trattamento con tali estratti aumenta la sicurezza di questa terapia.
Secondo l’OMS, circa 264 milioni di persone di tutte le categorie di età nel mondo soffrono di depressione. È la principale causa di inabilità al lavoro [1]. Le linee guida internazionali e nazionali sul trattamento raccomandano l’uso della psicoterapia o della farmacoterapia per la depressione lieve, e della psicoterapia e/o della farmacoterapia per la depressione moderata e grave [2]. Oltre agli antidepressivi sintetici come gli SSRI, anche i fitoterapici come l’iperico (Hypericum perforatum) fanno parte della cassetta degli attrezzi terapeutici, dopo che la sua efficacia e la sua buona tollerabilità sono state dimostrate in numerosi studi [3–5]. Tuttavia, l’iperico deve essere assunto sotto la supervisione di un medico esperto [6]: sebbene esistano sul mercato numerosi preparati da banco, oltre a quelli disponibili su prescrizione medica, l’iperico è noto per il suo potenziale di interazione farmacocinetica con un gran numero di farmaci, motivo per cui la sua assunzione non è innocua. Questo fitofarmaco ha raggiunto un livello di notorietà preoccupante dopo che si è saputo che i pazienti sottoposti a trapianto di cuore e trattati con ciclosporina, che erano stati co-somministrati con l’erba di San Giovanni a causa di una comorbidità depressiva, hanno subito il rigetto dell’organo trapiantato [7]. L’estratto di iperico induce l’enzima CYP3A4 responsabile del metabolismo della ciclosporina. L’efficacia di questo immunosoppressore è notevolmente ridotta dalla diminuzione della sua biodisponibilità [8]. Il componente dell’iperico responsabile dell’induzione del CYP3A4 è l’iperforina, anche se gli estratti di iperico disponibili sul mercato differiscono notevolmente nel contenuto di questo composto.
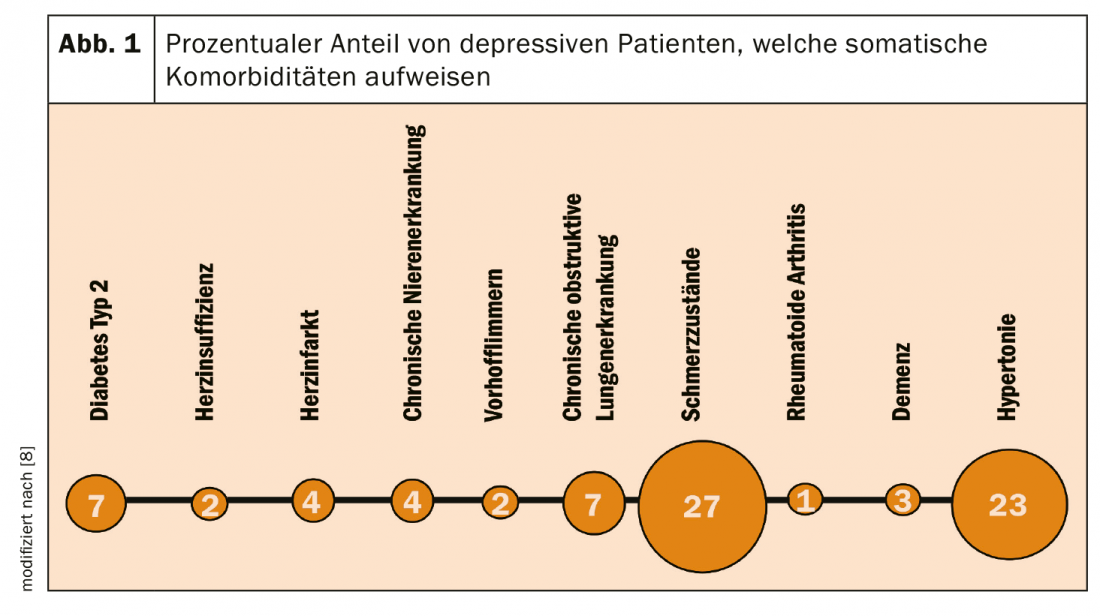
I pazienti depressi non vengono trattati solo da uno specialista in psichiatria e psicoterapia, ma anche da uno specialista in medicina generale o medicina interna. Il rischio di alcune comorbilità è particolarmente elevato nella depressione (Fig. 1), ma i pazienti depressi soffrono anche di altre malattie somatiche e mentali che causano comedicazioni [8]. Fortunatamente, esiste un estratto a bassa iperfornina che è caratterizzato da un basso rischio di interazione con altri farmaci e favorisce le condizioni di una terapia sicura in questi pazienti.
Estratti di iperico e loro indicazioni
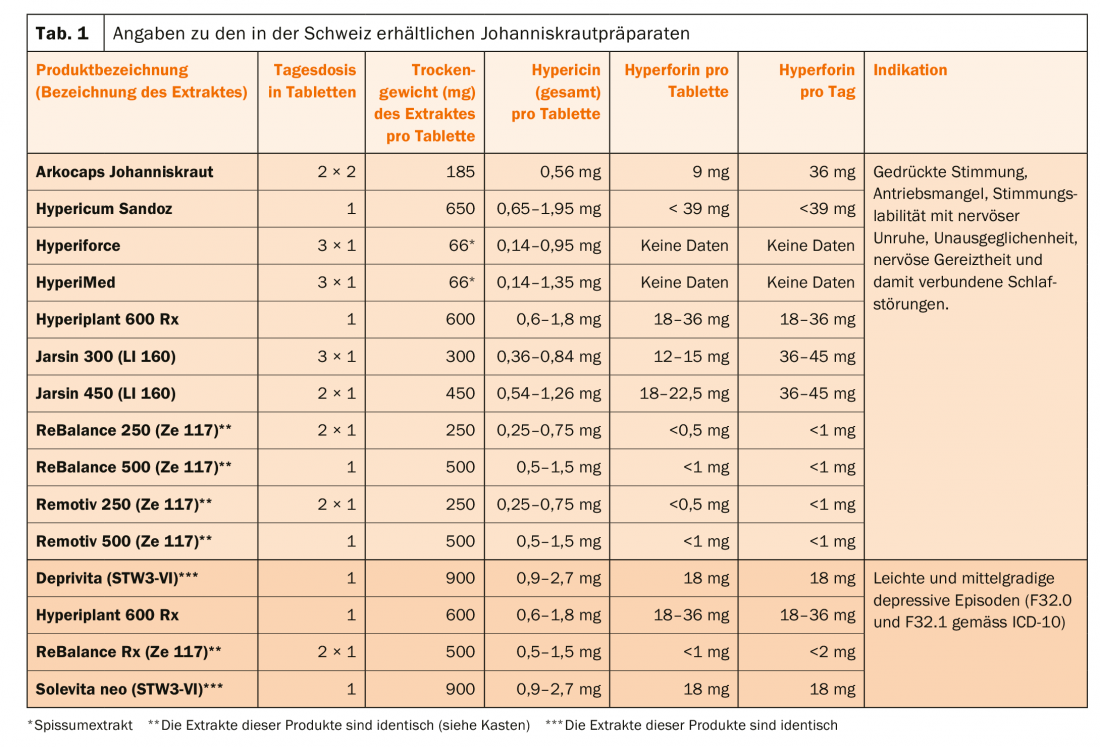
Gli estratti di iperico discussi in questo articolo sono consigliati per due gruppi diagnostici diversi, a seconda della preparazione (Tab. 1):
- Per i pazienti che soffrono di umore depresso, instabilità dell’umore, irrequietezza interiore, stati di tensione e problemi associati ad addormentarsi e a rimanere addormentati. Si tratta di farmaci della categoria di dispensazione D.
- Per i pazienti con diagnosi di episodio depressivo lieve o moderato (F32.0 e F32.1 secondo l’ICD-10). Si tratta di farmaci di categoria B.
Le dosi giornaliere per il trattamento dei pazienti con l’erba di San Giovanni variano in modo significativo (Tab. 1). Ora, però, un’analisi di 28 studi clinici sull’efficacia di diversi estratti di ipericumene nella depressione maggiore mostra che da una dose ≥180 mg/giorno di estratto, si raggiunge un plateau di efficacia, in quanto anche con dosi di 1800 mg/die, non sono stati raggiunti risultati migliori nel trattamento [9].
L’iperico ha relativamente pochi effetti collaterali ed è ben tollerato [10]. Per tutti i fitoterapici a base di Iperico si applica una certa fotosensibilizzazione e si deve evitare una forte esposizione al sole. Tuttavia, il rischio sembra diventare clinicamente significativo solo a dosi giornaliere di >2-4 g di Iperico (corrispondenti a 5-10 mg/giorno di ipericina) [9].
Si devono considerare anche le interazioni farmacodinamiche. L’iperico è anche un inibitore dell’assorbimento della serotonina e pertanto la sua combinazione con gli SSRI comporta un rischio di sindrome da serotonina, anche se nel caso del citalopram, ad esempio, l’induzione prevista del suo metabolismo per un abbassamento della sua biodisponibilità renderebbe tale rischio meno probabile [10].
Meccanismo d’azione
Gli estratti di iperico contengono un gran numero di sostanze attive, le cui concentrazioni variano non solo tra le preparazioni, ma anche nelle singole preparazioni, ad esempio per l’ipericina totale varia tra 0,14-1,35 mg in una compressa rivestita con film Hyperimed® (Tab.1). In passato si riteneva che l’ipericina, la pseudo-ipericina (dove ipericina + pseudo-ipericina sono indicate come ipericina totale) e l’iperforina fossero le principali responsabili degli effetti terapeutici, ma ora è stato dimostrato che anche gli estratti a basso contenuto di iperforina sono efficaci. L’iperico contiene altri composti, come quelli di tipo flavinoide (quercetina, quercetrina, rutina), che possono contribuire all’effetto terapeutico [11]. In generale, gli estratti inibiscono la ricaptazione di serotonina, noradrenalina e dopamina, ma agiscono anche su GABA e glutammato. Il loro profilo di effetto è simile a quello di molti antidepressivi sintetici, compresa la capacità di provocare una downregulation dei recettori β e una upregulation dei recettori 5-HT2 (cioè il numero di recettori diminuisce o aumenta, rispettivamente). L’iperforina favorisce l’ingresso degli ioni Na e Ca nei canali TRPC6 (canali del potenziale recettoriale transitorio). Negli esperimenti sugli animali, a seconda del modello, l’iperforina e/o l’ipericina si dimostrano attive [12,13]. Tuttavia, è difficile trarre conclusioni sul meccanismo della pianta, poiché la standardizzazione degli estratti si basa solo su uno o due composti. Gli estratti che contengono <1 mg/die di iperforina sono chiamati prodotti a bassa iperforina, in contrasto con i prodotti ad alta iperforina (>1 mg/die) (Tab. 1) (Box).
Farmacocinetica clinica e metabolismo
In uno studio farmacocinetico, sono stati misurati un Tmax di 5-10 ore e un’emivita di eliminazione di 12-28 ore per l’ipericina. Misure corrispondenti sono state raccolte anche per la pseudoipericina (1,5-4h; 5-38h), l’iperforina (3-8h; 10-28h) e la quercitina (0,5-6h (con 2 massimi in questo arco di tempo!); 0,8-7h) [14]. Gli studi sul ruolo degli enzimi coinvolti nel metabolismo dell’iperforina e dell’ipericina sono rari. Dall’iperforina si formano almeno 57 metaboliti, nella cui formazione giocano un ruolo le forme di CYP2C e CYP3A. Inibisce il CYP2D6 e il CYP3A in vitro, ma non è chiaro fino a che punto questo risultato sia clinicamente rilevante, poiché l’effetto induttivo predomina dopo una somministrazione prolungata [15]. Quindi, anche altri farmaci come il ritonavir inibiscono il CYP3A4 in una prima fase, prima che si manifesti l’effetto induttivo sullo stesso enzima.
Il CYP3A4 è responsabile del metabolismo di quasi la metà dei farmaci. Condivide numerosi substrati con la glicoproteina P (PgP; ABCB1), che agisce come trasportatore di efflusso per trasportare i farmaci fuori dalla cellula. L’iperforina contenuta negli estratti di iperico si lega al recettore del pregnano X (PXR), dopodiché il CYP3A4 e la PgP vengono indotti nel fegato, nell’intestino e in altri organi attraverso varie fasi [9]. Meno pronunciati e soprattutto non ancora accettati sono i risultati che l’iperforina induce in modo sostanziale anche il CYP1A2, il CYP2C9 e il CYP2C19.
L’induzione del CYP3A4 e della PgP può verificarsi dopo soli 3 giorni di trattamento. Raggiunge il massimo dopo circa 1-2 settimane, anche se può essere osservato per un periodo altrettanto lungo dopo l’interruzione del trattamento, cioè è reversibile dopo tutto [16]! Questa circostanza deve quindi essere presa in considerazione anche quando si passa da una preparazione ricca di iperforina a una povera di iperforina.
Interazioni farmacocinetiche degli estratti di Iperico ricchi di iperforine
Gli estratti di iperico ricchi di iperforina favoriscono quindi il metabolismo di molti farmaci, come è già stato descritto con l’esempio della ciclosporina. Ma impediscono anche il trasporto dei substrati della PgP, ad esempio l’assorbimento della digossina dall’intestino al sangue. Poiché molti steroidi vengono metabolizzati attraverso il CYP3A4, esiste il rischio di emorragia o addirittura di gravidanza con la contraccezione ormonale, ad esempio con etinilestradiolo o desogestrel, nel trattamento concomitante con Iperico ricco di iperforina.
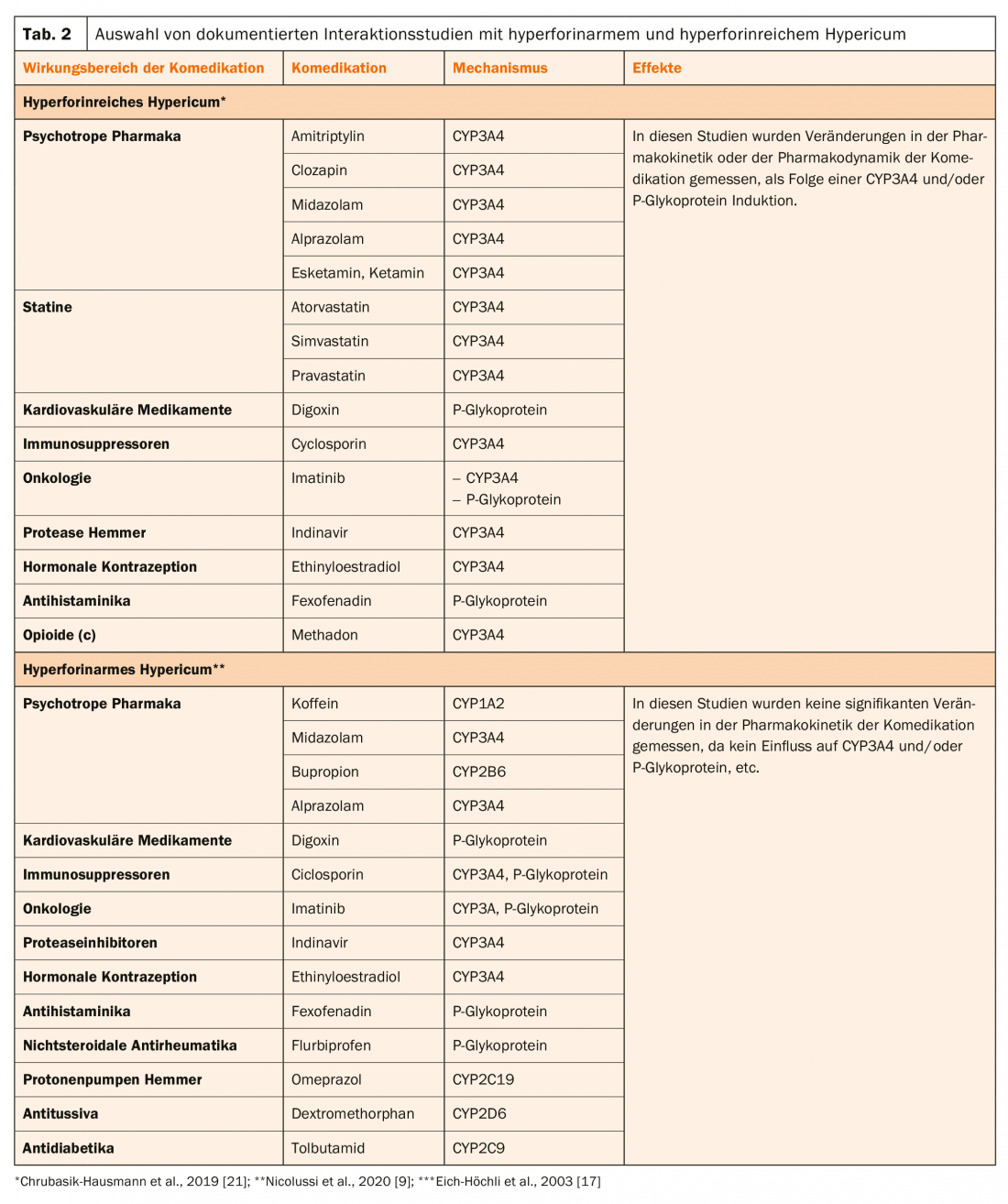
Per esempio, nell’SPC di Hypericum Sandoz® sono elencate come controindicazioni diverse comedicazioni, come alcuni immunosoppressori (ad es. ciclosporina, tacrolimus o sirolimus), farmaci anti-HIV del gruppo degli inibitori non nucleosidici della trascrittasi inversa (ad esempio nevirapina) e degli inibitori delle proteinasi (ad esempio indinavir), alcuni farmaci citostatici (ad esempio imatinib, irinotecan) e anticoagulanti orali di tipo cumarinico (Tab. 2).
Nei pazienti trattati con metadone, un trattamento antidepressivo aggiuntivo con l’iperico ha causato non solo una riduzione dei suoi livelli plasmatici, ma anche sintomi di astinenza, che sono scomparsi solo dopo l’interruzione del trattamento con l’iperico [17].
L’esketamina è stata appena introdotta in Svizzera come antidepressivo aggiuntivo per i pazienti resistenti al trattamento. Poiché viene degradato dal CYP3A4, non sorprende che l’Iperico ricco di iperforina ne riduca i livelli plasmatici di circa la metà [18]. Si può supporre che questo non sia il caso dell’iperfornitore di erba di San Giovanni.
Confronto tra l’iperforina povera e l’iperforina ricca di Hypericum
Le interazioni farmacocinetiche degli estratti di Iperico sono state documentate in numerosi studi e recensioni [9,19–21].
Attualmente è disponibile solo l’estratto Ze 117, che è a basso contenuto di iperforina secondo le linee guida EMA (riquadro, tab. 1) . Pertanto, dopo la somministrazione di questo prodotto, non si osserva una diminuzione dei livelli plasmatici di digossina nei soggetti trattati con questo farmaco [22]. La Tabella 2 mostra gli studi di interazione con Hypericum povero di iperforina e ricco di iperforina. Da ciò risulta chiaro che questi estratti differiscono chiaramente nel loro effetto sul CYP3A4 e/o sulla P-glicoproteina. Pertanto, è probabile che il trattamento con questi estratti comporti rischi maggiori a causa delle interazioni farmacocinetiche, che si manifestano principalmente come una perdita dell’effetto clinico del farmaco.
| L’EMA (Agenzia Europea dei Medicinali) ha approvato nel 2018 che il cosiddetto SPC (Riassunto delle Caratteristiche del Prodotto) non deve più contenere un’avvertenza sulle interazioni farmacocinetiche se nella dose giornaliera di un estratto di iperico il contenuto di iperforina è <1 mg/giorno, come nel caso dell’estratto Ze 117. La Svizzera (Swissmedic) è stato il primo Paese ad adottarlo. Tali avvertenze sono già state rimosse dalle informazioni sul farmaco degli estratti di iperico Ze 117 Remotiv 250/500 e ReBalance 250/500, ma la procedura di riscrittura è ancora in corso per ReBalance Rx, motivo per cui questo prodotto non viene attualmente fornito dall’azienda (a partire da marzo 2020). |
Conseguenze pratiche e conclusioni
La gamma di fitoterapici dell’Iperico è confusa. Ad esempio, nel caso dell’estratto iperforinico Ze 117, vengono offerti tre prodotti identici, ovvero Remotiv®, Rebalance®, Rebalance®Rx. Questi ultimi due prodotti sono rimborsati dalla cassa, mentre Remotiv fa parte della linea OTC e non viene rimborsato. Come già detto, Rebalance® RX (Schedule B) deve essere prescritto da un medico per la depressione lieve o moderata. Rebalance e Remotiv, invece, rientrano nello Schema D e possono quindi essere dispensati da farmacie e drogherie per il trattamento dell’umore depresso, dell’instabilità dell’umore, ecc. Ora, però, le informazioni sul farmaco di Rebalance® RX non specificano ancora che si tratta di un prodotto con un massimo di 0,1 mg di iperforina (per dose giornaliera), ma lo fanno per Remotiv® e Rebalance® (box) . È quindi importante che la collaborazione tra medico – farmacista – paziente sia ottimale, soprattutto perché deve essere chiaro al paziente che l’automedicazione può essere associata a rischi quando, ad esempio, si passa da un estratto di Ze 117 a un altro prodotto, soprattutto perché la maggior parte degli altri prodotti sono ricchi di iperforina. Quando si passa da un estratto ricco di iperforina a uno povero di iperformina, potrebbe essere necessario regolare attentamente la dose del farmaco, nel qual caso si raccomanda il monitoraggio terapeutico dei farmaci [23,24]. Con alcune precauzioni, gli estratti di iperforine a basso contenuto di erba di San Giovanni sono oggi considerati farmaci efficaci e sicuri per il trattamento della depressione lieve o moderata. Non ci sono solo molti pazienti che preferiscono la fitoterapia, ma anche i medici che desiderano utilizzarla in modo specifico, cioè legato al paziente.
Letteratura:
- www.who.int/news-room/fact-sheets/detail/depression (ultimo accesso il 15.4.2020)
- Holsboer-Trachsler E, Hättenschwiler J, Beck J, et al: Il trattamento acuto degli episodi depressivi. Forum medico svizzero. 2016;16(35): 716-725.
- Apaydin EA, Maher AR, Shanman R, et al: Una revisione sistematica dell’erba di San Giovanni per il disturbo depressivo maggiore. Syst Rev. 2016;5(1): 148.
- Rahimi R, Nikfar S, Abdollahi M: Efficacia e tollerabilità dell’Hypericum perforatum nel disturbo depressivo maggiore rispetto agli inibitori selettivi della ricaptazione della serotonina: una meta-analisi. Prog Neuropsychopharmacol Biol Psychiatry. 2009;33(1): 118-127.
- Linde K, Berner MM, Kriston L: L’erba di San Giovanni per la depressione maggiore. Cochrane Database Syst Rev. 2008(4): CD000448.
- Anheyer D, Haller H, Klose P, et al: Farmaci vegetali per i disturbi psichiatrici. Nervenarzt. 2018;89(9): 1009-1013.
- Ruschitzka F, Meier PJ, Turina M, et al: Rigetto acuto del trapianto di cuore dovuto all’erba di San Giovanni. Lancet. 2000;355: 548-549.
- Dumbreck S, Flynn A, Nairn M, et al.: Interazioni farmaco-malattia e farmaco-farmaco: esame sistematico delle raccomandazioni in 12 linee guida cliniche nazionali del Regno Unito. BMJ. 2015;350: h949.
- Nicolussi S, Drewe J, Butterweck V, et al: Rilevanza clinica delle interazioni farmacologiche della parola di San Giovanni rivisitate. Br J Pharmacol. 2020; 177(6): 1212-1226.
- Henderson L, Yue QY, Bergquist C, et al: Erba di San Giovanni (Hypericum perforatum): interazioni farmacologiche ed esiti clinici. British Journal of Clinical Pharmacology. 2002;54(4): 349-356.
- Gurley BJ, Swain A, Hubbard MA, et al.: Valutazione clinica delle interazioni erbe-farmaco mediate dal CYP2D6 nell’uomo: effetti di cardo mariano, cohosh nero, goldenseal, kava kava, erba di San Giovanni ed Echinacea. Mol Nutr Food Res. 2008;52(7): 755-763.
- Muller WE: La ricerca attuale sull’iperico, dalla modalità d’azione all’efficacia clinica. Pharmacol Res. 2003;47(2): 101-109.
- Leuner K, Kazanski V, Muller M, et al.: L’iperforina – un componente chiave dell’erba di San Giovanni attiva in modo specifico i canali TRPC6. FASEB J. 2007;21(14): 4101-4111.
- Schulz HU, Schurer M, Bassler D, Weiser D: Indagine sulla biodisponibilità dell’ipericina, della pseudo-ipericina, dell’iperforina e dei flavonoidi quercetina e isorhamnetina in seguito alla somministrazione orale singola e multipla di una compressa contenente estratto di iperico. Ricerca sui farmaci. 2005;55(1): 15-22.
- Hokkanen J, Tolonen A, Mattila S, Turpeinen M: Metabolismo dell’iperforina, il componente attivo dell’iperico, nei microsomi epatici umani. Eur J Pharm Sci. 2011;42(3): 273-284.
- Johne A, Schmider J, Brockmöller J, et al.: Diminuzione dei livelli plasmatici di amitriptilina e dei suoi metaboliti durante la somministrazione di un estratto di iperico ( Hypericum perforatum ). Giornale di Psicofarmacologia Clinica. 2002;22(1): 46-54.
- Eich-Höchli D, Oppliger R, Powell Golay K, et al.: Trattamento di mantenimento con metadone e erba di San Giovanni – Un rapporto di casi. Farmacopsichiatria. 2003;36: 35-37.
- Peltoniemi MA, Saari TI, Hagelberg NM, et al: L’erba di San Giovanni diminuisce notevolmente le concentrazioni plasmatiche della S-ketamina orale. Fundam Clin Pharmacol. 2012; 26(6): 743-750.
- Soleymani S, Bahramsoltani R, Rahimi R, Abdollahi M: Rischi clinici della co-somministrazione di iperico (Hypericum perforatum). Expert Opin Drug Metab Toxicol. 2017;13(10): 1047-1062.
- Zahner C, Kruttschnitt E, Drewe J, et al.: Nessuna interazione clinicamente rilevante dell’estratto di erba di San Giovanni ze 117 a basso contenuto di iperforina con gli enzimi del citocromo p450 e la p-glicoproteina. Farmacologia clinica e terapeutica. 2019;106(2): 432-440.
- Chrubasik-Hausmann S, Vlachojannis J, McLachlan AJ: Comprendere le interazioni farmacologiche con l’erba di San Giovanni (Hypericum perforatum L.): impatto del contenuto di iperforina. J Pharm Pharmacol. 2019;71(1): 129-138.
- Mueller SC, Uehleke B, Woehling H, et al: Effetto della dose e dei preparati di iperico sulla farmacocinetica della digossina. Clin Pharmacol Ther. 2004; 75(6): 546-557.
- Hiemke C, Bergemann N, Clement HW, et al: Linee guida di consenso per il monitoraggio terapeutico dei farmaci in neuropsicofarmacologia: aggiornamento 2017. Farmacopsichiatria. 2018; 51(1/2): 9-62.
- Klein HG, Haen E: Farmacogenetica e monitoraggio terapeutico dei farmaci. Berlino, Boston: De Gruyter; 2018. 465 p.
InFo NEUROLOGIA & PSICHIATRIA 2020; 18(3): 20-23
PRATICA GP 2020; 15(6): 38-41