La ricerca sui nuovi biologici sta contribuendo a fornire alternative di trattamento per la psoriasi a placche da moderata a grave, quando si verifica una mancanza di risposta o una perdita di efficacia [1]. I dati pubblicati nel 2019 dalla Rete Dermatologica Svizzera delle Terapie Mirate (SDTT) mostrano che il rapido miglioramento dei sintomi cutanei e la libertà dalle lesioni sono tra i criteri più importanti per i pazienti, secondo Julia-Tatjana Maul, MD, Ospedale Universitario di Zurigo [2,3].
Torna a “Notizie su dermatite atopica e psoriasi”.
L’inibitore dell’interleuchina-23 risankizumab (SKYRIZITM) è stato approvato in Svizzera dall’aprile 2019 per la psoriasi a placche da moderata a grave dopo una terapia infruttuosa con il trattamento sistemico convenzionale [4]. Dal 1° agosto 2019, l’anticorpo monoclonale umanizzato è stato approvato anche per l’uso da parte delle casse malattia [5]. Risankizumab viene iniettato per via sottocutanea (150 mg; 2× 75 mg); dopo la prima somministrazione a intervalli di quattro settimane e successivamente a intervalli di dodici settimane ciascuno [4]. L’efficacia elevata e duratura con risposta rapida e la buona tollerabilità sono state confermate clinicamente [6–8].
Dati a lungo termine: Conclusione positiva
L’elevata efficacia, la praticabilità e la tollerabilità contribuiscono al miglioramento della qualità di vita, che è anche un importante obiettivo terapeutico, secondo il Prof. Peter Häusermann, Ospedale Universitario di Basilea. Grazie al rapido tasso di risposta – un significativo sollievo dai sintomi entro 4-8 settimane – è possibile ridurre la fase di compromissione della vita quotidiana legata alla psoriasi. L’esperto ha sottolineato che l’efficacia di risankizumab non diminuisce nemmeno con un uso prolungato [9]. Ciò è confermato anche dai dati di vari studi di fase III [6–8].
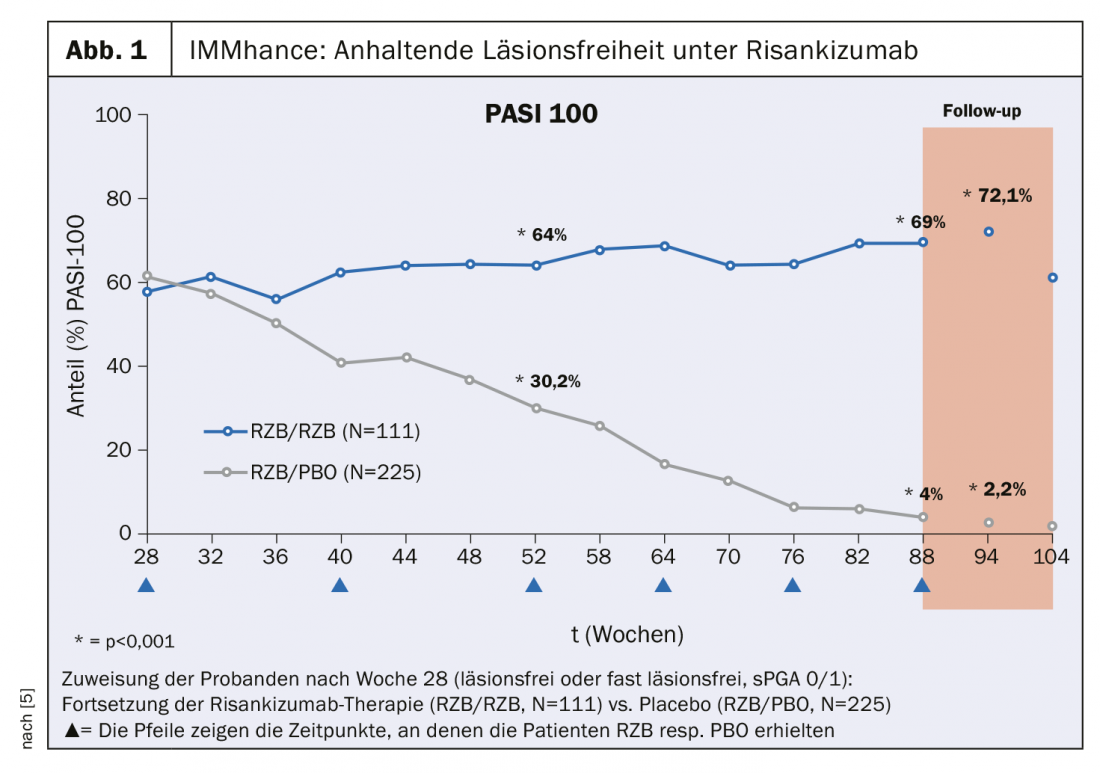
Lo studio IMMhance ha analizzato gli effetti a lungo termine dell’interruzione della terapia con risankizumab nei pazienti con psoriasi a placche da moderata a grave. Coloro che hanno raggiunto uno stato libero da lesioni o quasi libero da lesioni alla settimana 28 dopo l’inizio del trattamento (Static Physician Global Assessment, sPGA 0/1) sono stati assegnati in modo casuale alle condizioni di continuazione della terapia con risankizumab (n=111) vs placebo (n=225). Nel gruppo di partecipanti allo studio ancora in trattamento con risankizumab, oltre il 70% ha ottenuto la guarigione completa della pelle secondo l’indice PASI (Psoriasis Area Severity Index) 100 alla settimana 94 (Fig. 1). Nel gruppo passato al placebo, tuttavia, la risposta PASI 100 è peggiorata dal 61,3% al 2,2% [6]. Negli studi UltIMMa-1 e UltIMMa-2, il 75,1% e l’81,3% dei pazienti trattati con risankizumab (n=598) hanno raggiunto un PASI 90 dopo 16 e 52 settimane di trattamento, rispettivamente, secondo un’analisi integrata di entrambi gli studi. Si tratta di una percentuale significativamente superiore rispetto al gruppo ustekinumab, in cui meno del 50% dei 199 soggetti ha raggiunto un PASI 90 in entrambi i momenti [8].
Controversia economica sulla salute
Risankizumab è indicato per il trattamento della psoriasi a placche da moderata a grave negli adulti che hanno avuto una risposta inadeguata ad altre terapie sistemiche [4]. In particolare, almeno una terapia sistemica convenzionale (ciclosporina, metotrexato, acitretina o UVB e PUVA) deve essere fallita dopo 16 settimane di trattamento [5]. Non c’è consenso su quante prove di terapia sistemica con farmaci non biologici debbano essere provate prima. In generale, tuttavia, viene propagandata una strategia terapeutica personalizzata. L’opportunità di interrompere la terapia quando si raggiunge un PASI di 100 e ciò che viene considerato un criterio per passare a un altro biologico sono valutati in modo diverso. Il Prof. Häusermann ha la visione che in circa cinque anni la classe di sostanze innovative degli inibitori dell’IL-23 sarà utilizzata di routine. Fino ad allora, potrebbe anche essere possibile ridurre il divario di prezzo rispetto alle terapie sistemiche convenzionali, che attualmente rappresenta un dilemma economico sanitario di questi farmaci altamente efficaci [9].
Torna a “Notizie su dermatite atopica e psoriasi”.
Letteratura:
- Birchler T: Risankizumab come opzione di trattamento per la psoriasi. Presentazione diapositive. Thomas Birchler, AbbVie AG, Consulente medico, Tavola rotonda con i media, Iaculis GmbH & AbbVie AG, 29.10.2019, Zurigo.
- Maul JT: Risankizumab come opzione di trattamento per la psoriasi. Presentazione diapositive. Julia-Tatjana Maul, MD, Tavola rotonda con i media, Iaculis GmbH & AbbVie AG, 29.10.2019, Zurigo.
- Maul JT e altri. Il genere e l’età determinano in modo significativo le esigenze dei pazienti e gli obiettivi di trattamento nella psoriasi – una lezione per la pratica. J Eur Acad Dermatol Venereol, 2019. 33(4): p. 700-708.
- Informazioni tecniche attuali di SKYRIZITM su www.swissmedicinfo.ch.
- Elenco delle specialità 2019 dell’Ufficio federale della sanità pubblica UFSP. www.spezialitaetenliste.ch, ad agosto 2019.
- Blauvelt A, Leonardi, C., Gooderham, M., Papp, K. Efficacia e sicurezza di Risankizumab Q12W continuo rispetto all’interruzione del trattamento: risultati in doppio cieco a 2 anni dello studio di fase 3 IMMhance. presentato al 24° Congresso Mondiale di Dermatologia. Milano, Italia, 10-15 giugno 2019.
- Gordon KB e altri. Efficacia e sicurezza di risankizumab nella psoriasi a placche da moderata a grave (UltIMMa-1 e UltIMMa-2): risultati di due studi di fase 3 in doppio cieco, randomizzati, controllati con placebo e ustekinumab. Lancet, 2018. 392(10148): p. 650-661.
- Lebwohl M e altri. Efficacia e sicurezza di Risankizumab nella psoriasi a placche da moderata a grave: un’analisi integrata di UltIMMa-1 e UltIMMa-2. P8108, presentato al Meeting annuale dell’American Academy of Dermatology, Washington DC, 1-5 marzo 2019.
- Häusermann P: Risankizumab come opzione di trattamento per la psoriasi. Presentazione diapositive. Prof. Dr. med. Peter Häusermann, Tavola rotonda con i media, Iaculis GmbH & AbbVie AG, 29.10.2019, Zurigo.
Adattato da: DERMATOLOGIE PRAXIS 2019; 29(6): 26











