Una volta che il danno articolare si è verificato nel corso dell’artrite reumatoide, non può più essere invertito con i farmaci. Pertanto, è importante utilizzare le terapie di base il prima possibile. Se le sostanze convenzionali non funzionano a sufficienza o non sono tollerate, entrano in gioco i biologici. Il seguente articolo offre una panoramica delle strategie terapeutiche.
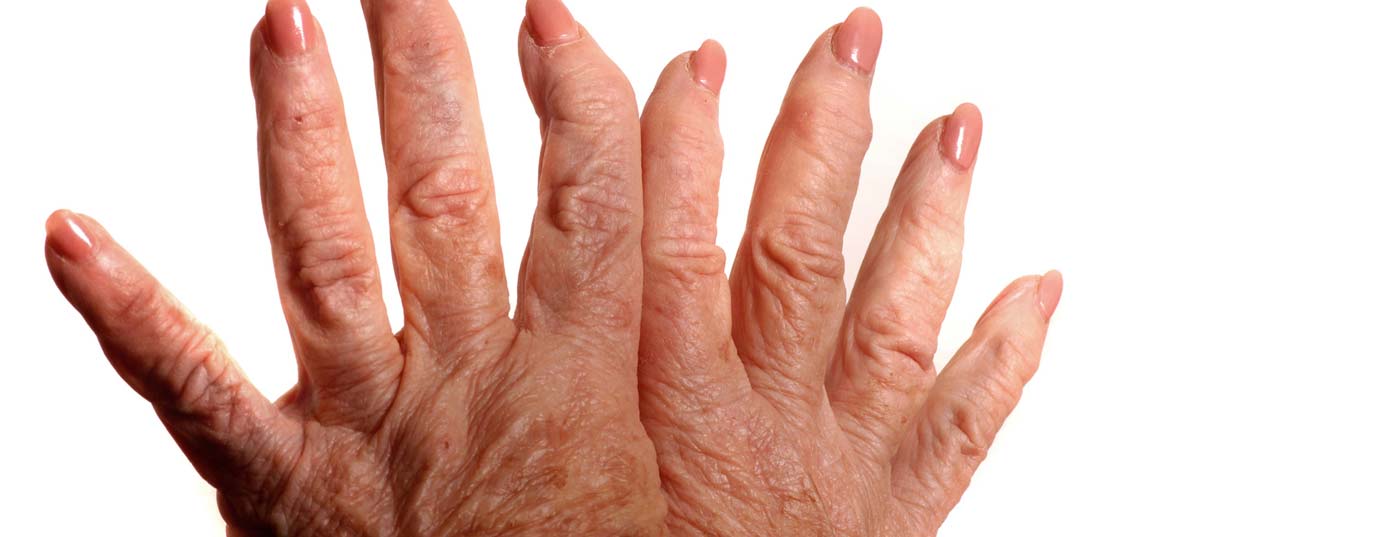
La distruzione delle articolazioni dovuta all’infiammazione nell’artrite reumatoide (RA) inizia molto presto nel corso della malattia, di solito nei primi mesi. Il danno articolare o artrosi secondaria (Fig. 1) è irreversibile e non può essere invertito con i farmaci. Quanto più precocemente si utilizzano le terapie di base, tanto migliore è la risposta.
Per una buona gestione, è essenziale la collaborazione interdisciplinare con la fisioterapia, la terapia occupazionale e, talvolta, la chirurgia reumatologica. Il coordinamento delle misure terapeutiche all’interno di queste aree deve essere fatto con attenzione, soprattutto nell’interazione tra il fornitore di cure primarie e il reumatologo.

Diagnosi precoce
Oggi, la remissione completa è un obiettivo abbastanza realistico e può essere raggiunta più facilmente all’inizio che alla fine del ciclo di vita. Poiché la terapia di base dovrebbe essere idealmente iniziata entro i primi tre mesi dalla comparsa dei sintomi, la diagnosi precoce è fondamentale. All’inizio della malattia, ci vuole molta esperienza per fare una diagnosi corretta attraverso i sintomi tipici, il modello di coinvolgimento articolare e gli esami supplementari (laboratorio con autoanticorpi, artrosonografia, radiografie).
Approcci al trattamento
Farmaci di base: I farmaci di base sono essenziali per un controllo adeguato dell’attività della malattia nella maggior parte dei casi. A lungo termine, sono molto meno tossici dei glucocorticoidi, a condizione che vengano utilizzati in modo appropriato. Non solo riducono i sintomi dell’infiammazione, ma idealmente rallentano e arrestano il processo erosivo-distruttivo. Con le sostanze sintetiche convenzionali, l’effetto di solito si manifesta con una latenza di circa due o tre mesi.
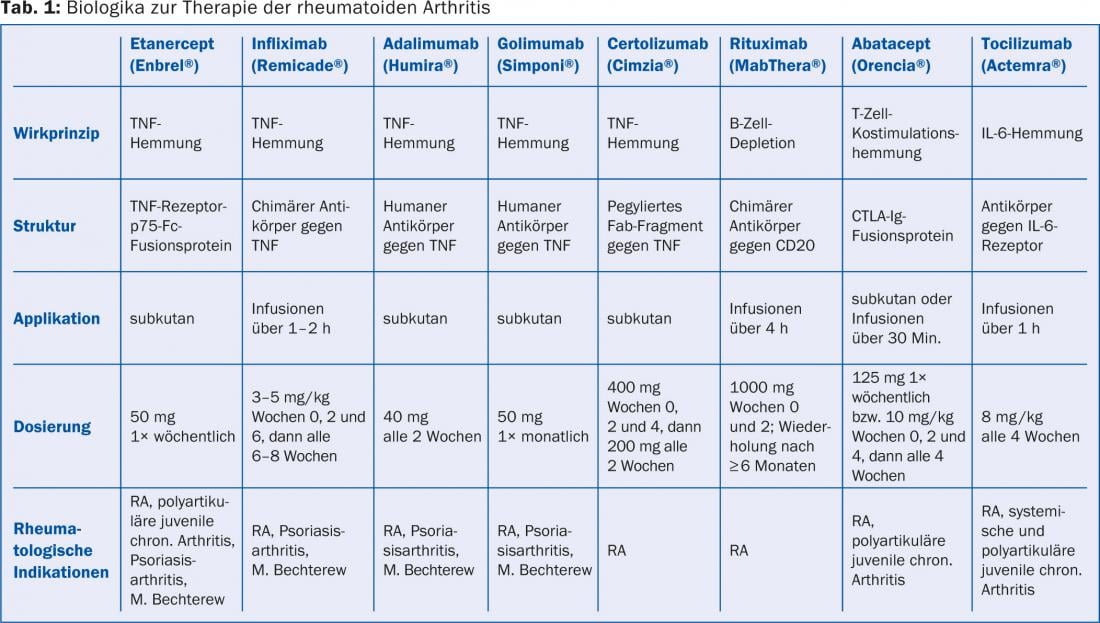
La gamma di terapie di base è in costante aumento. I farmaci di base sintetici comunemente utilizzati sono il metotrexato, la leflunomide (Arava® e generici), la sulfasalazina (Salazopyrin® EN) e l’idrossiclorochina (Plaquenil®). Recentemente è stato reso disponibile il farmaco sintetico selettivo tofacitinib (Xeljanz®), che inibisce gli enzimi intracellulari, ovvero le cosiddette Janus chinasi. Viene utilizzato per via perorale con o senza farmaci di base convenzionali (ad esempio, il metotrexato). Inoltre, ci sono i biologici (Tabella 1) , che hanno portato a una vera e propria rivoluzione nel trattamento dell’AR negli ultimi 15 anni: Oggi è possibile trovare un farmaco ben efficace e tollerabile per la maggior parte dei pazienti, ma spesso sono necessarie delle combinazioni. Oggi, raggiungere la remissione è un obiettivo abbastanza realistico.
Adattare la terapia alle esigenze individuali dei pazienti è impegnativo. Richiede molta esperienza. Pertanto, il trattamento deve essere sempre eseguito in collaborazione con uno specialista in reumatologia.
Il metotrexato è di solito la prima scelta, anche se è meglio somministrarlo insieme, ad esempio, a idrossiclorochina, leflunomide o biologici (combinazioni di due farmaci). Sono possibili anche combinazioni di tre o addirittura quattro. I diversi meccanismi d’azione delle singole sostanze ottengono un effetto additivo e talvolta persino sinergico, che consente di mantenere il dosaggio delle singole sostanze più basso (meno effetti collaterali). Le terapie combinate richiedono molta esperienza, compreso il monitoraggio.
Metotrexato, leflunomide, tofacitinib e tutti i biologici hanno un effetto immunosoppressivo. Per evitare un aumento eccessivo del rischio di infezione, le terapie combinate non devono contenere più di due di questi immunosoppressori o più di un biologico. Anche le dosi elevate di steroidi devono essere evitate. È essenziale istruire il paziente a riferire tempestivamente se si sospettano sintomi di infezione e a sospendere qualsiasi farmaco biologico. Se un’infezione sospetta è confermata da un aumento della CRP, è consigliabile un ricovero immediato se il focolaio dell’infezione rimane poco chiaro o se è necessaria una terapia antibiotica parenterale o un monitoraggio.
I biologici intervengono in modo specifico nel processo infiammatorio a livello molecolare. I possibili trattamenti includono l’inibizione del TNF (inibitori del TNF) o della costimolazione delle cellule T (Abatacept), la riduzione dell’attività dell’interleuchina-6 (Tocilizumab) e la deplezione delle cellule B (Rituximab). L’esperienza più lunga è stata quella degli inibitori del TNF. Dal punto di vista clinico, sono solo marginalmente migliori del metotrexato in monoterapia, ma il loro inizio d’azione è molto più rapido: l’attività infiammatoria sistemica (umorale) viene soppressa in soli due giorni, il che spesso si manifesta con un brusco miglioramento dei sintomi generali (stanchezza, spossatezza e inappetenza).
L’effetto antierosivo degli inibitori del TNF è chiaramente superiore a quello del metotrexato. Possono anche essere combinati molto bene con farmaci di base sintetici e soprattutto con il metotrexato, che in media porta a un effetto clinico e antierosivo ancora migliore.
Gli inibitori del TNF vengono iniettati per via sottocutanea o infusi per via endovenosa. Nella maggior parte dei casi sono ben tollerati. Gli effetti collaterali più importanti includono reazioni cutanee nel sito di iniezione o reazioni all’infusione. Il rischio di infezione è circa raddoppiato con l’inibizione del TNF e sono possibili infezioni opportunistiche, soprattutto con patogeni intracellulari. Poiché può verificarsi una riattivazione della tubercolosi, è necessario uno screening preventivo della tubercolosi. Le vaccinazioni contro lo pneumococco e l’influenza annuale sono utili. I possibili siti di ingresso, come la parodontite o le lesioni cutanee (anch’esse micosi), devono essere eliminati prima di iniziare la terapia.
Dopo il fallimento della terapia di base convenzionale, abatacept e tocilizumab possono essere considerati al posto degli inibitori del TNF. Un’altra indicazione di queste due sostanze e del rituximab è l’effetto insufficiente della terapia anti-TNF. Abatacept ha un eccellente profilo di tollerabilità. Il tocilizumab sopprime l’attività infiammatoria sistemica (umorale) più di tutti i biologici. Il rituximab ha il vantaggio che i cicli di trattamento non devono essere più frequenti di sei mesi e funziona meglio nei pazienti positivi al fattore reumatoide e agli anticorpi anti-CCP. Per abatacept, tocilizumab e rituximab, si applicano precauzioni simili a quelle degli inibitori del TNF, ma le infezioni opportunistiche si verificano con minore frequenza. Da notare: Un aumento della CRP correlato all’infezione può essere inibito da tocilizumab (CAVE sottovaluta la gravità dell’infezione).
I biologici sono costosi a causa della loro complessa produzione, motivo per cui vengono approvati solo se una precedente terapia con sostanze convenzionali si è dimostrata insufficiente. È necessario ottenere preventivamente un’approvazione dei costi da parte della compagnia di assicurazione sanitaria.
Glucocorticoidi: gli steroidi sono indicati solo come ponte a breve termine fino all’inizio dell’azione dei farmaci di base e per l’uso a lungo termine a basso dosaggio (ad esempio, prednisone ≤ 7,5 mg/d) se l’efficacia dei farmaci di base è insufficiente. Recentemente è stata resa disponibile una forma di prednisone a rilascio prolungato (Lodotra®). Viene assunto prima di andare a letto e rilascia il prednisone con un ritardo di diverse ore, in modo che sia già pienamente efficace quando ci si alza al mattino. Il rapido e forte effetto antinfiammatorio invoglia le persone a utilizzare i glucocorticoidi in dosi più elevate per periodi di tempo più lunghi. La monoterapia con glucocorticoidi è oggi obsoleta, tuttavia, perché l’uso a lungo termine in dosi più elevate è associato a una grave tossicità (ad esempio, l’osteoporosi). Se le singole articolazioni sono dominanti, sono appropriate le iniezioni di steroidi intra-articolari.
Monitoraggio per l’ottimizzazione della terapia
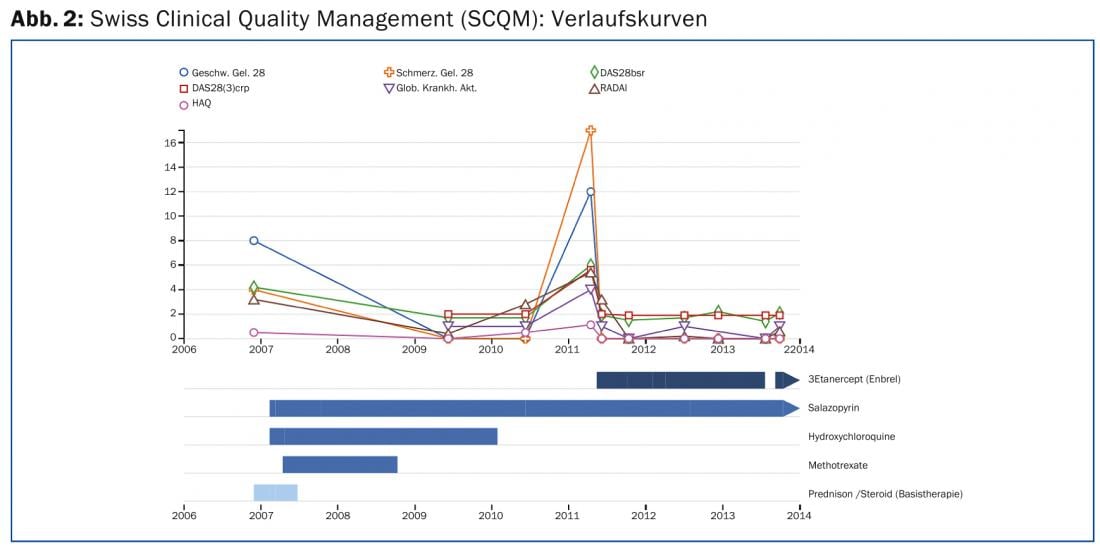
In ogni caso, è necessario monitorare e regolare continuamente i farmaci insieme a uno specialista in reumatologia, il che è meglio fare nell’ambito della gestione della qualità. In Svizzera, il registro SCQM (Swiss Clinical Quality Management in Rheumatic Diseases) è disponibile a questo scopo (www.scqm.ch). Come sistema di miglioramento delle misurazioni, l’SCQM è ben utilizzabile nella pratica e fornisce preziosi dati di registro della “vita reale”. Attraverso i questionari, che vengono regolarmente compilati dal paziente e dal reumatologo su internet o su carta, è possibile registrare in modo standardizzato il decorso dell’attività infiammatoria, il danno articolare e gli effetti della malattia. Anche le radiografie e gli esami di laboratorio fanno parte della valutazione. Le valutazioni centralizzate consentono di ottimizzare continuamente la terapia (Fig. 2) . Le linee guida della Società Svizzera di Reumatologia (www.rheuma-net.ch/Richtlinien) forniscono una sintesi delle misure di monitoraggio necessarie per i singoli farmaci di base.
Comorbilità
L’osteoporosi e l’arteriosclerosi sono le malattie concomitanti più significative. I bifosfonati sono già utilizzati in caso di terapia steroidea continua quando c’è un’osteopenia da moderata a grave, cioè non solo quando c’è un’evidenza di osteoporosi (raccomandazioni “Osteoporosi da steroidi” su www.rheuma-net.ch/Richtlinien). Nella RA, c’è un’accelerazione dell’arteriosclerosi. Gli eventi cardiovascolari si verificano con una frequenza circa doppia rispetto alla popolazione normale, motivo per cui i fattori di rischio (diabete, fumo, ipertensione e ipercolesterolemia) devono essere presi di mira e affrontati in modo aggressivo.
Adrian Forster, MD
Letteratura:
- Schneider M, Krüger K: Artrite reumatoide – diagnosi precoce e gestione della malattia. Dtsch Ärztebl Int 2013; 110: 477-484.
- Smolen JS, et al: Raccomandazioni EULAR per la gestione dell’artrite reumatoide con farmaci antireumatici sintetici e biologici modificanti la malattia: aggiornamento 2013. Ann Rheum Dis 2014; 73: 492-509.
- Bykerk VP, Schoels MM: Strategie di trattamento per l’artrite reumatoide precoce. Curr Opin Rheumatol 2013; 25: 375-383.
- Gramling A, O’Dell JR: Gestione iniziale dell’artrite reumatoide. Rheum Dis Clin North Am 2012; 38: 311-325.
CONCLUSIONE PER LA PRATICA
- Iniziare la terapia di base il prima possibile è fondamentale per la prognosi. L’obiettivo del trattamento è la remissione.
- Se i farmaci di base convenzionali non sono abbastanza efficaci, sono indicati i biologici o il tofacitinib.
- La monoterapia con steroidi è da escludere.
- È fondamentale che il rischio di malattie concomitanti, come l’osteoporosi o l’arteriosclerosi, venga individuato e ridotto precocemente.
A RETENIR
- Un trattamento di base instaurato il più presto possibile è fondamentale per la diagnosi. L’obiettivo del trattamento è la remissione.
- Se i farmaci di base classici non sono sufficientemente efficaci, vengono indicati gli agenti biologici o il tofacitinib.
- La monoterapia da parte di stéroïdes non è più di attualità.
- È fondamentale valutare e ridurre il rischio di comorbidità, come l’osteoporosi o l’artrite.
PRATICA GP 2014; 9(4): 12-15