Il diabete è associato a un aumento del rischio cardiovascolare. La terapia multifattoriale dei quattro principali fattori di rischio glicemia, peso, ipertensione e dislipidemia nelle persone con diabete di tipo 2 rappresenta una sfida. Tuttavia, è stato dimostrato che i diabetici possono trarre grandi benefici dalle moderne opzioni di trattamento. Per la riduzione dei lipidi, sono disponibili efficaci opzioni terapeutiche “add-on” con ezetimibe e inibitori PCSK-9. I dati degli studi dimostrano che gli inibitori di PCSK-9 contribuiscono a ridurre ulteriormente i lipidi nei pazienti con e senza diabete.
I diabetici adulti hanno una probabilità da due a quattro volte maggiore di avere un evento cardiovascolare, come un ictus ischemico o un infarto miocardico non fatale, rispetto alle persone sane, e le malattie cardiovascolari rappresentano fino al 50% dei decessi associati al diabete [1,2]. I livelli elevati di colesterolo LDL sono uno dei principali fattori di rischio, insieme al controllo glicemico inadeguato, all’obesità e all’ipertensione [3]. Il fatto che i livelli di colesterolo siano un fattore rilevante e che i pazienti diabetici possano trarre beneficio dalla riduzione dei lipidi è dimostrato dai dati di vari studi prospettici e randomizzati, spiega il Prof. Gottfried Rudofsky, MD, Responsabile del Centro Metabolico, Ospedale Cantonale di Olten [4].
Quali sono gli obiettivi terapeutici raccomandati dall’ESC?
L’obiettivo del trattamento lipidico è quello di ridurre il più possibile il rischio di eventi cardiovascolari. Gli studi degli ultimi anni dimostrano che più basso è l’LDL-C, più basso è il rischio cardiovascolare. Di conseguenza, non esiste un limite minimo di concentrazione di LDL-C al di sotto del quale il rischio cardiovascolare non diminuisce ulteriormente. Questo è stato incorporato nelle linee guida ESC/EAS riviste nel 2019, con raccomandazioni di esperti che si concentrano sui pazienti ad alto rischio [5]. La maggior parte dei diabetici sono considerati pazienti ad alto rischio per quanto riguarda la terapia ipocolesterolemizzante, per i quali si dovrebbe puntare a un intervallo target di <1,8 mmol/l secondo le attuali linee guida (Tab. 1) [4,6,7]. Solo in un piccolo gruppo di diabetici con un rischio moderato è sufficiente un intervallo target di LDL <2,6 mmol/l. Se, oltre al diabete, c’è anche una malattia arteriosclerotica manifesta, il rischio aumenta a “molto alto” e si deve puntare a un intervallo target LDL di <1,4 mmol/l. Se si verifica un secondo evento vascolare nell’arco di 2 anni in terapia con statine al massimo della tolleranza, il rischio del paziente aumenta in modo massiccio – in questa costellazione, si raccomanda un’ulteriore riduzione delle LDL a <1,0 mmol/l.
Terapia statinica a dosaggio iniziale, eventualmente combinata con ezetimibe
Una volta stabilito l’obiettivo terapeutico, il primo passo nel trattamento è il dosaggio massimo tollerato di statine, dice il Prof. Rudofsky. (Fig. 1). Al momento del dosaggio, si deve prendere in considerazione la “regola del sei”, che afferma che la massima riduzione dell’LDL-C può essere ottenuta con la prima dose iniziale e che ogni ulteriore raddoppio della dose porta solo a una riduzione aggiuntiva del 6% del colesterolo [8]. D’altra parte, bisogna anche considerare che una dose iniziale più bassa è associata a tassi di effetti collaterali/intolleranza alla statina più bassi. In una seconda fase, può avvenire il dosaggio. Questo approccio a tappe evita che il paziente venga erroneamente classificato come intollerante alle statine, il che complica l’ulteriore corso della terapia. Potrebbe essere necessario prendere in considerazione l’uso di una delle statine meno potenti, che tuttavia sono spesso più tollerabili.
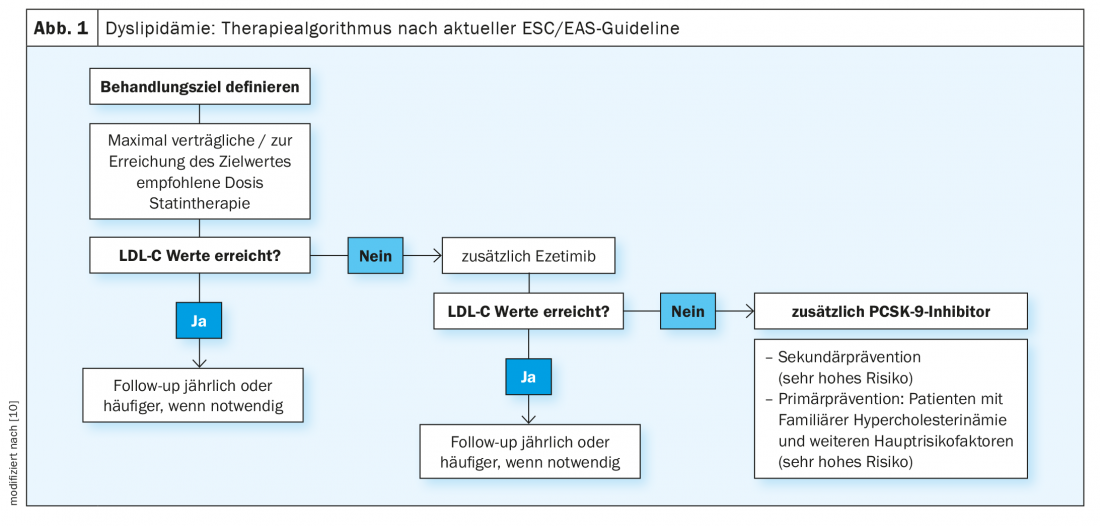
Se l’obiettivo LDL viene raggiunto con questa strategia di trattamento, il Prof. Rudofsky raccomanda controlli regolari dopo un anno o a seconda della situazione clinica [4]. Se non si raggiunge l’intervallo target, si può ottenere un’ulteriore riduzione delle LDL combinandola con l’ezetimibe, che ora è disponibile anche in combinazioni fisse con statine altamente potenti. Ezetimibe si attacca al bordo a spazzola dell’intestino tenue, inibisce i trasportatori del colesterolo nella membrana delle cellule della mucosa e quindi il suo assorbimento. Se il trasporto del colesterolo dall’intestino al fegato viene ridotto, la quantità di colesterolo immagazzinata è minore e l’eliminazione del colesterolo dal sangue aumenta. Per quanto riguarda l’ezetimibe, lo studio IMPROVE-IT è uno studio con endpoint cardiovascolare che mostra differenze statisticamente significative nell’endpoint primario di morbilità rispetto al trattamento con la sola simvastatina [9]. In base a ciò, ezetimibe ha un beneficio aggiuntivo per la profilassi secondaria. 18.144 pazienti dopo una sindrome coronarica acuta con un livello di LDL-C di 50-125 mg/dl sono stati randomizzati a 40 mg di ezetimibe/simvastatina o 40 mg di placebo/simvastatina. Tra i 4933 diabetici che hanno partecipato allo studio, la maggiore riduzione relativa è stata ottenuta in termini di infarto miocardico (24%) e ictus ischemico (39%) [12].
Se i valori target non vengono raggiunti: utilizzare gli inibitori di PCSK-9.
Come fase finale di escalation, gli inibitori della PCSK-9 sono disponibili come “add-on”, che possono ottenere un’ulteriore riduzione del 50-60% dei livelli di LDL, un effetto considerevole (Fig. 1) [10]. Alirocumab ed Evolocumab aumentano il numero di recettori LDL nel fegato legandosi a PCSK-9 e abbassano l’LDL-C in aggiunta a statine ed ezetimibe fino a livelli di 0,2 mmol/l. Nello studio ODYSSEY-OUTCOMES, multinazionale e in doppio cieco, l’inibitore della PCSK-9 Praluent® (alirocumab) ha ridotto la morte, l’infarto miocardico, l’ictus e l’angina instabile del 15% e la sola mortalità del 15% nei pazienti ad alto rischio cardiovascolare entro 2,8 anni [11]. 18 924 pazienti ad alto rischio che avevano avuto una sindrome coronarica acuta nei 12 mesi precedenti la randomizzazione hanno partecipato allo studio. Si trattava di un collettivo di pazienti in cui, nonostante la terapia con statine ad alto dosaggio e massima tolleranza, con ulteriori farmaci combinati per la riduzione dei lipidi nella fase di run-in, non era stato raggiunto un controllo lipidico soddisfacente. Il Prof. Rudofsky sottolinea che il valore LDL al basale era di circa 1,8 mmol/l, cioè già basso, e che è possibile ottenere un’ulteriore riduzione. Poiché i pazienti con diabete hanno un rischio cardiovascolare maggiore rispetto ai non diabetici, la riduzione del rischio assoluto in questa sottopopolazione è doppia rispetto ai pazienti senza diabete, afferma il Prof. Rudofsky e aggiunge: “I pazienti con diabete di tipo 2 ne traggono un beneficio particolare”, per cui l’effetto della terapia sembra essere maggiore in quelli con un danno vascolare più pronunciato.
Fonte: Sanofi-Aventis
Letteratura:
- Dal Canto E, et al: European Journal of Preventive Cardiology 2019; 26(2), Suppl, 25-32.
- International Diabetes Federation: Atlante del diabete IDF 9ª edizione 2019. www.diabetesatlas.org, (ultimo accesso 18.10.2021)
- Wong K, et al: J Diabetes Complications 2012; 26: 169-174.
- Il paziente metabolico: “Alimentare la conoscenza”, Sanofi-Aventis AG, conferenza web, 26.08.2021
- Riesen WF, et al: Swiss Med Forum 2020; 20(0910): 140-148.
- Rudofsky G, Hellige G, Arenja N: Il paziente diabetico cardiovascolare – una sfida interdisciplinare . HAUSARZT PRAXIS 2021; 16(7): 10-16.
- Mach F, et al: Eur Heart J 2020; 41: 111-188.
- Knopp RH: N Engl J Med 1999; 431: 498-511.
- Cannon CP, et al: N Engl J Med 2015; 372: 2387-2397.
- Autori/Membri della task force; Comitato ESC per le linee guida pratiche (CPG); Società cardiache nazionali ESC. Linee guida ESC/EAS 2019 per la gestione delle dislipidemie: modifica dei lipidi per ridurre il rischio cardiovascolare. Aterosclerosi. 2019; 290: 140-205.
- Schwartz GG, et al; N Engl J Med. 2018;379(22): 2097-2107.
- Giugliano RP, et al: Circulation 2018; 137(15): 1571-1582.
PRATICA GP 2021; 16(10): 36-37