Diversi studi hanno dimostrato che gli ultrasuoni possono essere utilizzati per rilevare i carcinomi in aggiunta alla mammografia, soprattutto nel seno denso. Nella diagnosi precoce del cancro nelle donne asintomatiche, l’ecografia mammaria non ha attualmente uno status indipendente riconosciuto. Nelle donne sottoposte a screening intensificato, l’ecografia è anche parte integrante del programma di esami multimodali. Se è indicata una biopsia, questa viene effettuata preferibilmente sotto guida ecografica.
Gli ultrasuoni sono noti per essere un metodo di esame pratico e facilmente accessibile, con una buona sensibilità, anche se dipendente dall’esaminatore. Nella diagnostica del carcinoma mammario, occorre distinguere tra l’uso degli ultrasuoni nel contesto della diagnosi precoce e l’uso nei casi di sospetto carcinoma mammario o di carcinoma già confermato.
Aspetti tecnici
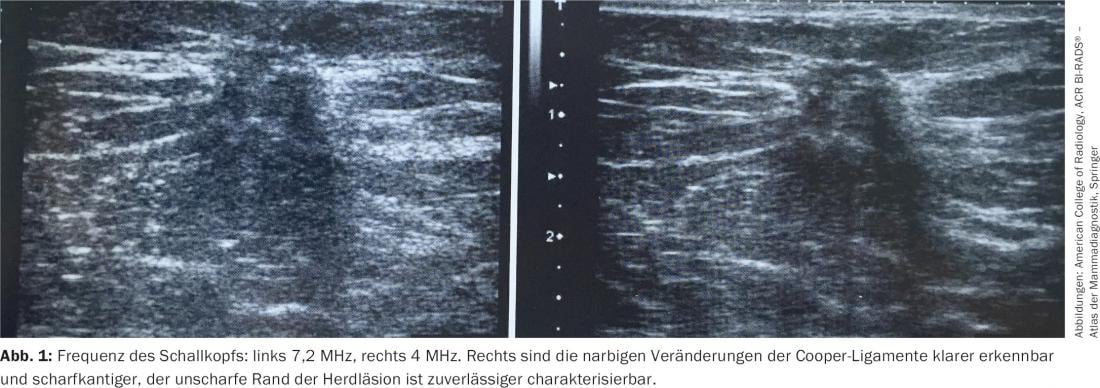
Il requisito principale di un’ecografia mammaria è quello di fornire un’immagine ad alto contrasto e ad alta risoluzione con una buona rappresentazione anatomica. La scarsa qualità dell’immagine ecografica può portare a gravi errori di diagnosi, ad esempio confondere un carcinoma con una cisti. La linea guida pratica dell’ACR per l’esecuzione di un esame ecografico del seno (2011) raccomanda l’uso di un trasduttore lineare ad ampia larghezza di banda con una frequenza centrale di almeno 10 MHz [1]. All’estremità superiore della scala delle alte frequenze (tra 12 e 18 MHz), questi trasduttori forniscono immagini ad alta risoluzione (Fig. 1) . Nella gamma di frequenze più basse, è possibile raggiungere una profondità di penetrazione nel tessuto fino a 5 cm.
La zona focale deve essere impostata nella regione di interesse nel terzo anteriore e medio tra la pelle e la parete toracica. Quando si valuta una lesione, la zona focale è posizionata in modo ottimale al centro della lesione.
La più antica tecnica di esame sistematico è il tracciato trasversale e longitudinale a meandri del torace. Con l’aumento della risoluzione spaziale nelle ecografie della mamma, il sistema dei dotti si è offerto come struttura di guida, per cui la guida antiradiografica del trasduttore nelle sezioni segmentali trasversali e longitudinali si sta diffondendo come alternativa.
Tecniche come il Doppler, le analisi 3D e 4D e l’elastografia aumentano la quantità di informazioni diagnostiche, ma non sono ancora state definite come necessarie per la diagnostica di base. La tecnologia più recente in questo campo è l’ecografia mammaria automatizzata, che consente di ottenere esami ecografici a tutto campo rapidi e indipendenti dall’utente.
Diagnostica a ultrasuoni per la diagnosi precoce
La mammografia è l’unico metodo di screening per il cancro al seno che è stato in grado di mostrare un effetto positivo sulla riduzione della mortalità specifica per cancro al seno in diversi studi basati sulla popolazione [2]. Anche in tempi di concetti terapeutici più moderni, le dimensioni del tumore e soprattutto lo stato linfonodale alla diagnosi rimangono un parametro prognostico essenziale e indiscusso [3]. Ciò significa che il ruolo dell’imaging nella diagnosi precoce del tumore al seno rimane centrale. Di undici studi randomizzati sulla mammografia, solo quelli che hanno mostrato anche una diminuzione dei casi di cancro al seno avanzato e un aumento dei casi di cancro al seno nodale-negativo hanno mostrato una riduzione della mortalità per cancro al seno [4,5].
Nelle donne con tessuto mammario denso, il carcinoma mammario può essere mascherato e, di conseguenza, non essere notato alla mammografia; questo porta ad un eccesso di carcinomi mammari avanzati e di nuova diagnosi [6]. Dopo una mammografia di screening normale, le donne con una densità mammaria estremamente elevata hanno quasi 18 volte più probabilità di ricevere una diagnosi di cancro al seno a causa di sintomi clinici, rispetto alle donne con tessuto ghiandolare coinvolto [7]. Questi carcinomi di intervallo (cioè quelli diagnosticati prima dello screening successivo) tendono ad essere più grandi, più aggressivi e con una prognosi peggiore rispetto ai carcinomi rilevati al momento dello screening. Di conseguenza, un basso tasso di carcinomi di intervallo è una misura dell’efficacia dello screening.
La densità mammaria elevata gioca un ruolo non solo in termini di mascheramento del cancro al seno, ma aumenta il rischio di cancro al seno in sé. Le meta-analisi hanno dimostrato un rischio da quattro a cinque volte maggiore di sviluppare il cancro al seno quando le donne con una densità mammaria molto bassa sono state confrontate con le donne con una densità mammaria molto alta [8].
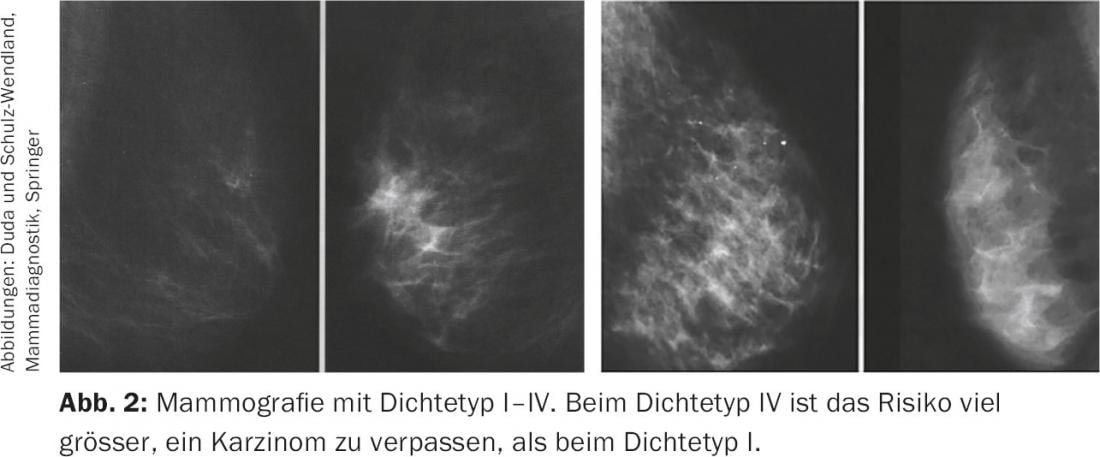
Diversi studi hanno dimostrato che gli ultrasuoni possono essere utilizzati per rilevare i carcinomi in aggiunta alla mammografia, soprattutto nel seno denso. (Fig.2). La linea guida S3 per il carcinoma mammario richiede quindi l’uso regolare dell’ecografia mammaria nei seni mammograficamente densi (densità ACR 3,4) già nella linea guida per la diagnosi precoce del 2008 [9]. L’ecografia è anche raccomandata come misura complementare per i seni densi nell’ultima raccomandazione della linea guida del Gruppo di lavoro sull’oncologia ginecologica [10]. Poiché la densità del seno ha un impatto così significativo sulla certezza di escludere il cancro al seno, nel 2011 negli Stati Uniti è stata addirittura approvata una legge che impone alle strutture che eseguono mammografie di fornire sia al medico di riferimento che alla paziente informazioni scritte sulla densità del seno individuale.
Nella diagnosi precoce del cancro nelle donne asintomatiche, l’ecografia mammaria non ha attualmente uno status indipendente riconosciuto. Il suo ruolo in questo senso è piuttosto quello di integrare la mammografia, con la qualità della mammografia e dell’ecografia che si influenzano a vicenda.
Un team internazionale di ricercatori ha voluto sapere se l’ecografia è adatta anche per lo screening del cancro al seno [11]. A questo scopo, circa 2700 donne sono state esaminate tre volte a intervalli di un anno ciascuna, mediante mammografia ed ecografia. Sono stati rilevati in totale 111 casi confermati di cancro al seno. I tassi di rilevamento erano comparabili per entrambi i metodi di esame. Per rilevare un caso di cancro al seno, 129 donne dovevano essere sottoposte a ecografia. Nella mammografia, questo valore era 127. Tuttavia, il successo degli ultrasuoni sembrava migliore con l’aumento della densità del seno. Inoltre, sono stati rilevati ecograficamente più tumori invasivi e linfonodi-negativi. I ricercatori valutano l’ecografia come alternativa nei Paesi in cui non viene offerto uno screening mammografico strutturato.
Non bisogna dimenticare che l’aumento del tasso di rilevamento del cancro dovuto all’ecografia mammaria additiva è compensato da un aumento del tasso di biopsia. Fortunatamente, il chiarimento interventistico di un reperto ecografico non chiaro, che può essere effettuato senza indugio, consente un tempo di attesa significativamente più breve rispetto ai metodi alternativi (stereotassia, tomosintesi o persino chiarimento guidato dalla risonanza magnetica).
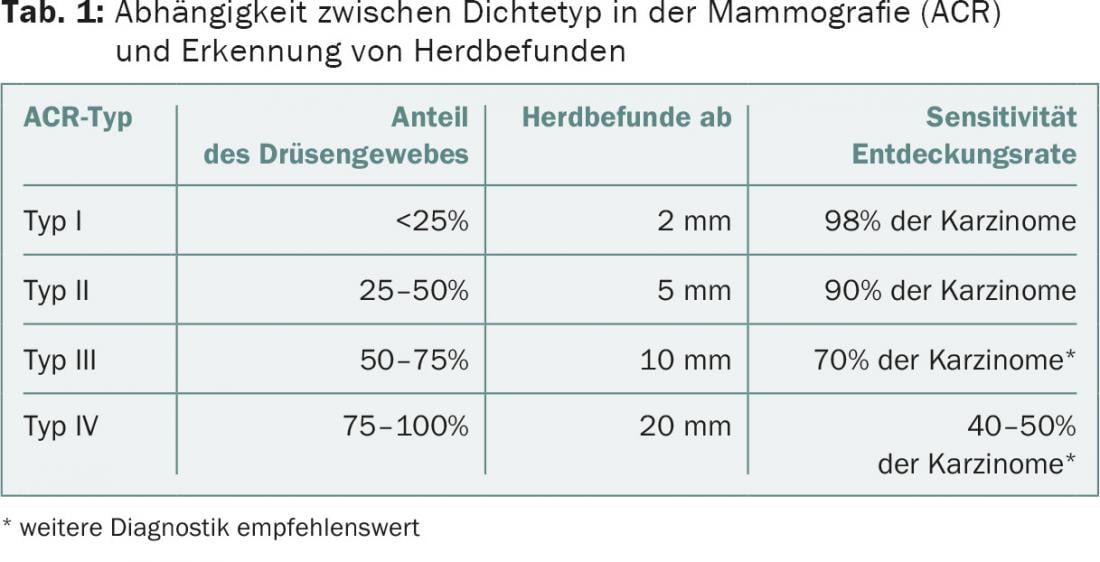
In sintesi, l’ecografia mammaria è obbligatoria nella situazione di diagnosi precoce come metodo aggiuntivo alla mammografia nei seni densi (densità ACR 3.4) (Tab. 1) . Questo significa anche che l’ecografia mammaria svolge un ruolo più importante nella donna più giovane (con tessuto ghiandolare fisiologicamente denso) rispetto alla paziente più anziana. I risultati sonografici hanno un valore maggiore nelle donne più giovani rispetto a quelle più anziane e possono persino superare la mammografia nelle donne di età inferiore ai 40 anni in termini di diagnosi positive di malignità.
Nelle donne sottoposte a screening intensificato (portatrici di mutazioni dei geni BRCA1 o BRCA2, rischio eterozigote ≥20% o rischio residuo nell’arco della vita ≥30% secondo un modello di previsione standardizzato, nonché sopravvissute a tumori infantili con radioterapia terapeutica della parete toracica), anche l’ecografia è parte integrante del programma di esami multimodali (raccomandati ogni sei mesi a partire dai 25 anni).
Diagnostica a ultrasuoni nel paziente sintomatico
Poiché l’ecografia mammaria è un metodo di esame pratico e facilmente accessibile, viene spesso utilizzata nella paziente sintomatica all’inizio del processo diagnostico. L’ecografia integra le altre tecniche di imaging e permette di differenziare i risultati cistici da quelli solidi. Anche se il correlato mammografico di un reperto alla palpazione è già visibile, è importante caratterizzare ecograficamente la massa, per documentare l’estensione del tumore ed escludere la multifocalità/centricità e il coinvolgimento ascellare. Nelle pazienti con reperti anormali alla risonanza magnetica mammaria e con un’ecografia mammaria inizialmente non rilevante, si deve assolutamente eseguire un’ecografia target. Se il reperto sospetto descritto nella risonanza magnetica può essere rappresentato anche ecograficamente, è possibile eseguire una chiarificazione bioptica ecografica anziché guidata dalla risonanza magnetica. Il chiarimento interventistico di un risultato ecografico poco chiaro può essere effettuato senza ritardi e riduce significativamente il tempo di attesa rispetto ai metodi alternativi. Questo significa meno stress psicologico per il paziente.
È quindi comprensibile che una chiarificazione bioptica venga effettuata preferibilmente su guida ecografica, a condizione che i risultati possano essere ben rappresentati dagli ultrasuoni. Un’indicazione particolarmente valida è la presenza di più linfonodi palpabili con sospetto carcinoma. L’ecografia è anche al primo posto nella cascata diagnostica del seno durante la gravidanza e l’allattamento. A differenza della biopsia guidata dalla stereotassi, dalla tomosintesi o dalla risonanza magnetica, la biopsia guidata dall’ecografia richiede anche meno personale, attrezzature e sforzi organizzativi.
L’ecografia mammaria viene utilizzata anche per monitorare la risposta del tumore durante la chemioterapia neoadiuvante. In questi pazienti, di solito è indicato marcare il tumore con una clip durante la chemioterapia neoadiuvante, in modo che il sito da operare possa essere ancora tracciato se c’è una risposta tumorale completa al termine della chemioterapia. L’inserimento della clip può avvenire di solito con guida ecografica senza problemi. Gli ultrasuoni vengono utilizzati anche per monitorare le dimensioni del tumore durante la terapia endocrina primaria di un carcinoma mammario non operato in precedenza (ad esempio, in una paziente anziana o se l’operazione consigliata viene rifiutata). Inoltre, l’ecografia nel contesto preoperatorio aiuta a marcare l’incisione esatta e a eseguire la marcatura a filo del tumore, se il carcinoma non è palpabile ma può essere visualizzato ecograficamente.
Letteratura:
- American College of Radiology: Linee guida pratiche ACR per l’esecuzione dell’esame ecografico del seno.
- Broeders M, et al: L’impatto dello screening mammografico sulla mortalità per cancro al seno in Europa: una revisione degli studi osservazionali. J Med Screen 2012; 19: 14-25.
- Saadatmand S, et al: Influenza dello stadio tumorale al momento della diagnosi del cancro al seno sulla sopravvivenza nei tempi moderni: studio basato sulla popolazione di 173797 pazienti. BMJ 2015; 351: h4901.
- Smith RA, et al: Gli studi randomizzati sullo screening del cancro al seno: cosa abbiamo imparato? Radiol Clin North Am 2004; 42: 793-806.
- Tabár L, et al.: Approfondimenti dagli studi sullo screening del cancro al seno: come lo screening influisce sulla storia naturale del cancro al seno e implicazioni per la valutazione dei programmi di screening. Breast J 2015; 21:13-20.
- Gierach GL, et al: Relazione tra densità mammografica e morte per cancro al seno nel Breast Cancer Surveillance Consortium. J Natl Cancer Inst 2012; 104: 1218-1227.
- Boyd NF, et al: Densità mammografica e rischio di cancro al seno: comprensione attuale e prospettive future. Breast Cancer Res 2011; 13: 223.
- Sickles EA: L’uso dell’imaging mammario per lo screening delle donne ad alto rischio di cancro. Radiol Clin North Am 2010; 48: 859-878.
- Albert US (editore): Linea guida di livello 3 per la diagnosi precoce del cancro al seno in Germania. 1° aggiornamento 2008. Germering/Monaco: W. Zuckschwerdt Verlag GmbH, Industriestrasse 1, D-82110ISBN 978-3-88603-931-9.
- Schreer I, Albert US: Diagnosi precoce e diagnosi. In: Comitato per il seno dell’AGO. Diagnosi e trattamento delle pazienti con cancro al seno primario e metastatico. Raccomandazioni 2015. www.ago-online.de.
- Berg WA, et al: Stato attuale dello screening supplementare nei seni densi. JNCI J Natl Cancer Inst 2016; prima online.
InFo ONCOLOGIA & EMATOLOGIA 2016; 4(6): 11-15
PRATICA GP 2017; 12(2): 26-30