I disturbi respiratori legati al sonno sono comuni. L’apnea ostruttiva del sonno (OSA) ha il carattere di una malattia diffusa. La prevalenza dell’apnea ostruttiva del sonno è in costante aumento nei Paesi industrializzati occidentali, a causa della crescente prevalenza dell’obesità, dell’invecchiamento e dell’uso diffuso di metodi diagnostici. Il 40% della popolazione soffre di apnea ostruttiva del sonno con un Indice di Ipopnea (AHI) >5, dove l’AHI descrive il verificarsi di eventi respiratori per ora di sonno.
I disturbi respiratori legati al sonno sono comuni. L’apnea ostruttiva del sonno (OSA) ha il carattere di una malattia diffusa. La prevalenza dell’apnea ostruttiva del sonno è in costante aumento nei Paesi industrializzati occidentali, a causa della crescente prevalenza dell’obesità, dell’invecchiamento e dell’uso diffuso di metodi diagnostici. Il 40% della popolazione tedesca soffre di apnea ostruttiva del sonno con un indice di apnea e ipopnea (AHI) >5, dove l’AHI descrive il verificarsi di eventi respiratori per ora di sonno.
La malattia è più comune negli uomini e negli anziani oltre i 60 anni. La sindrome OSA, la combinazione di OSA e sonnolenza diurna concomitante, è segnalata con una prevalenza del cinque per cento della popolazione tedesca (al momento non sono disponibili indagini attuali dalla Svizzera) [1]. I disturbi respiratori legati al sonno non trattati portano a complicazioni cardiovascolari, a una pronunciata sonnolenza diurna e quindi a un aumento del rischio di incidenti. Anche la funzione cognitiva della persona colpita può essere compromessa.
La respirazione disturbata dal sonno è suddivisa in quattro gruppi principali secondo l’ICSD-3: SA ostruttiva, SA centrale, ipossiemia legata al sonno, ipoventilazione legata al sonno [2]. Nell’OSA, si verifica un collasso ripetitivo delle vie aeree superiori. A causa dell’abbassamento del tono muscolare, si verifica più frequentemente nel sonno profondo e in quello REM. Se si verifica un collasso delle vie aeree superiori sotto forma di apnea, la persona colpita cerca di contrastare l’apnea con un maggiore sforzo respiratorio. Questo sforzo maggiore è seguito da una reazione di eccitazione nervosa centrale, il cosiddetto arousal. Se il paziente riesce a riaprire le vie respiratorie, si produce un forte russare irregolare. L’apnea centrale del sonno è causata da un disturbo nella regolazione centrale della respirazione. L’ipossiemia e l’ipoventilazione legate al sonno derivano da una riduzione persistente dell’attività respiratoria. Ciò che hanno in comune è l’interruzione della normale architettura del sonno, vale a dire che il sonno è costantemente interrotto da reazioni di risveglio, la proporzione di sonno profondo e REM diminuisce, dando luogo a un sonno non ristoratore con conseguente stanchezza o sonnolenza diurna.
Sintomi e diagnosi
Le pause respiratorie, il russare e la sonnolenza diurna sono segnalati come sintomi frequenti dei disturbi respiratori legati al sonno; in questo caso, è particolarmente necessario ottenere informazioni da altri pazienti, poiché i pazienti affetti spesso non riferiscono alcun disturbo soggettivo. I disturbi insonni sono indicati dalla frammentazione dell’architettura del sonno. Nei casi di apnea pronunciata, viene descritto un risveglio con respiro corto. I questionari possono essere utilizzati per valutare la sonnolenza diurna derivante dalla SBAS (respirazione disturbata dal sonno). La Scala della sonnolenza di Epworth viene spesso utilizzata a questo scopo. Qui si chiede ai pazienti la probabilità di addormentarsi in otto situazioni tipiche della vita quotidiana. I singoli risultati vengono sommati per ottenere un valore totale compreso tra zero e 24. Un valore superiore a dieci è considerato patologico. L’esame clinico deve includere un’ispezione delle vie aeree superiori. È necessario esaminare la cavità nasale, il rinofaringe, la cavità orale, la faringe profonda e la laringe. In questo caso, l’ostruzione anatomica nell’area della cavità orale, in particolare l’ipertrofia delle tonsille palatine e della base della lingua, gioca un ruolo speciale nello sviluppo della respirazione disturbata dal sonno nel senso dell’OSA.
Occorre valutare anche la posizione della mascella superiore rispetto a quella inferiore e lo stato dei denti. Sia la poligrafia cardio-respiratoria che la polisonnografia sono disponibili come strumenti diagnostici. Come procedura diagnostica di base, la poligrafia viene inizialmente eseguita in regime ambulatoriale, vale a dire che il paziente può dormire con il sistema diagnostico nel suo ambiente familiare a casa. Il dispositivo PG è un apparecchio di misurazione portatile che misura o registra il flusso respiratorio nasale, le escursioni respiratorie del torace e dell’addome, la frequenza cardiaca, il russamento, la saturazione di ossigeno e la posizione del paziente. I dati vengono registrati continuamente per almeno 6 ore e poi elaborati o sincronizzati con un software, in modo che il medico curante possa fare una valutazione individuale dell’intera notte. Se la diagnosi di respirazione disturbata dal sonno non è possibile durante una poligrafia cardiorespiratoria ambulatoriale, il paziente interessato deve essere indirizzato a un laboratorio del sonno per ulteriori diagnosi, in questo caso una polisonnografia.
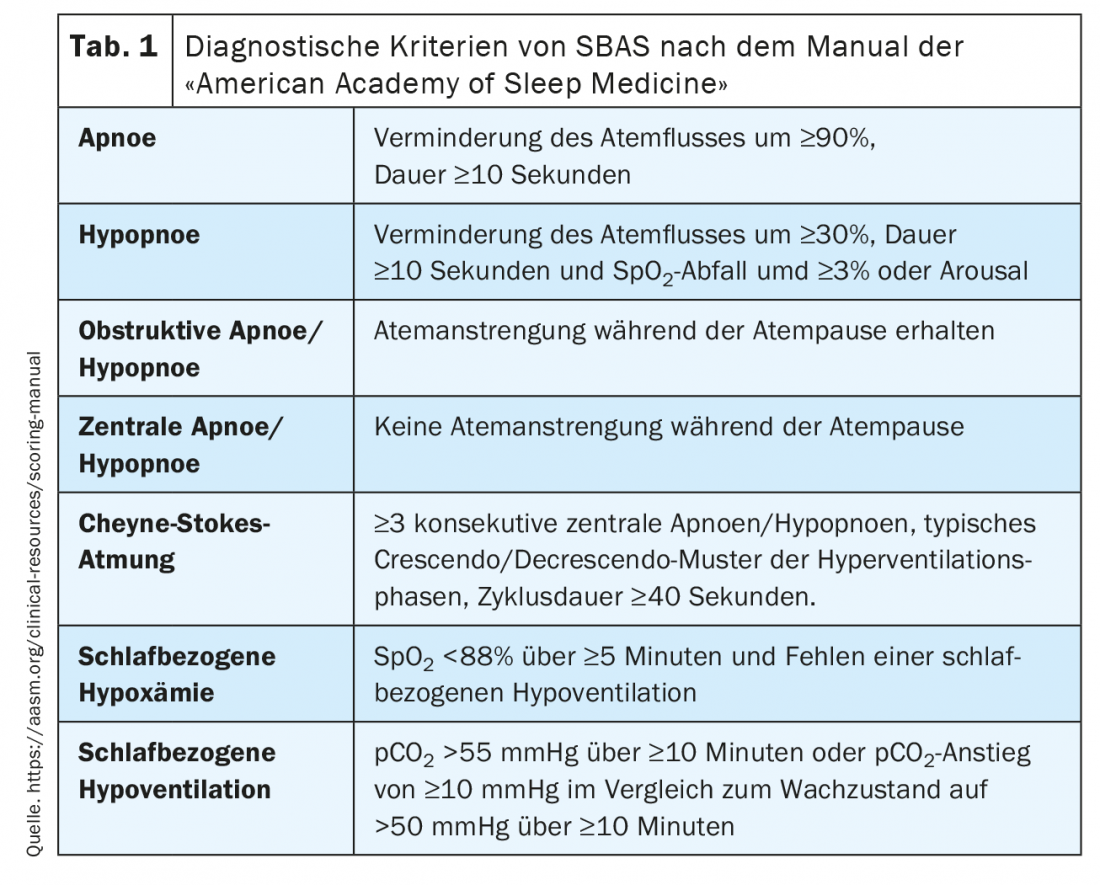
I criteri diagnostici della SBAS nel contesto della PG/PSG sono definiti in base al manuale dell’Accademia Americana di Medicina del Sonno [3] e sono riassunti nella Tabella 1 .
Apnea ostruttiva del sonno
L’OSA deriva dall’ostruzione delle vie aeree superiori nella regione (oro)faringea posteriore durante il sonno. Oltre alla cosiddetta fessurazione pronunciata del palato molle con archi palatali profondi e un’ugola possibilmente allargata e allungata, la causa può essere l’ipertrofia delle tonsille palatine o l’ipertrofia della base della lingua. Allo stesso modo, si verificano malposizioni della mandibola o fattori non anatomici, come la debolezza del muscolo genioglosso, che ha una funzione di dilatazione della porzione faringea delle vie aeree superiori. Il restringimento delle vie aeree è più comunemente associato all’obesità, con un maggiore accumulo di grasso nelle pareti laterali della faringe. L’obesità è il principale fattore di rischio dell’OSA, insieme all’aumento dell’età e al sesso maschile. Di conseguenza, i pazienti con sindrome metabolica sono particolarmente colpiti dall’OSA [4]. L’OSA è la causa più comune di ipertensione arteriosa secondaria e influenza lo stato metabolico dei diabetici aumentando la resistenza all’insulina. La relazione tra iperlipidemia e OSA non è ancora stata stabilita in modo definitivo. In generale, il rischio cardiovascolare aumenta nei pazienti con OSA non trattata [5].
I pazienti con OSA grave, in particolare, sviluppano un’ipertensione arteriosa con non-dipping (mancanza di riduzione della pressione sanguigna durante la notte). Anche i pazienti che presentano solo un’ostruzione delle vie aeree superiori nel sonno REM, a causa del rilassamento muscolare che si verifica in quel momento, mostrano la sintomatologia dell’ipertensione arteriosa (6). Esiste una stretta associazione tra l’OSA non trattata e le aritmie cardiache, in particolare la fibrillazione atriale [7], le malattie cardiache come la CHD e l’infarto del miocardio [8] e l’insorgenza di ictus [9]. Se c’è un’eccessiva sonnolenza diurna dovuta all’OSA, si può ipotizzare anche un aumento del rischio cardiovascolare [10]. A causa della possibile comparsa di sonnolenza diurna fino all’eccessiva sonnolenza diurna nel contesto dell’OSA, il rischio di infortunio dei pazienti affetti è particolarmente elevato, soprattutto se si svolgono professioni con attività di controllo e monitoraggio. Il medico non ha l’obbligo di segnalarlo, ma è obbligatorio informare la persona interessata di questa circostanza; le informazioni fornite devono essere documentate per iscritto e controfirmate dal paziente.
Eseguendo una poligrafia cardiorespiratoria, si può determinare la gravità dell’OSA. A tale scopo, viene determinato l’indice di apnea-ipopnea (AHI) della persona colpita. L’AHI comprende il numero di apnee e ipopnee per ora di sonno. I risultati lievi corrispondono a un AHI di 5-15, i risultati moderati a un AHI di 15-30/h e i risultati gravi a un AHI superiore a 30/h.
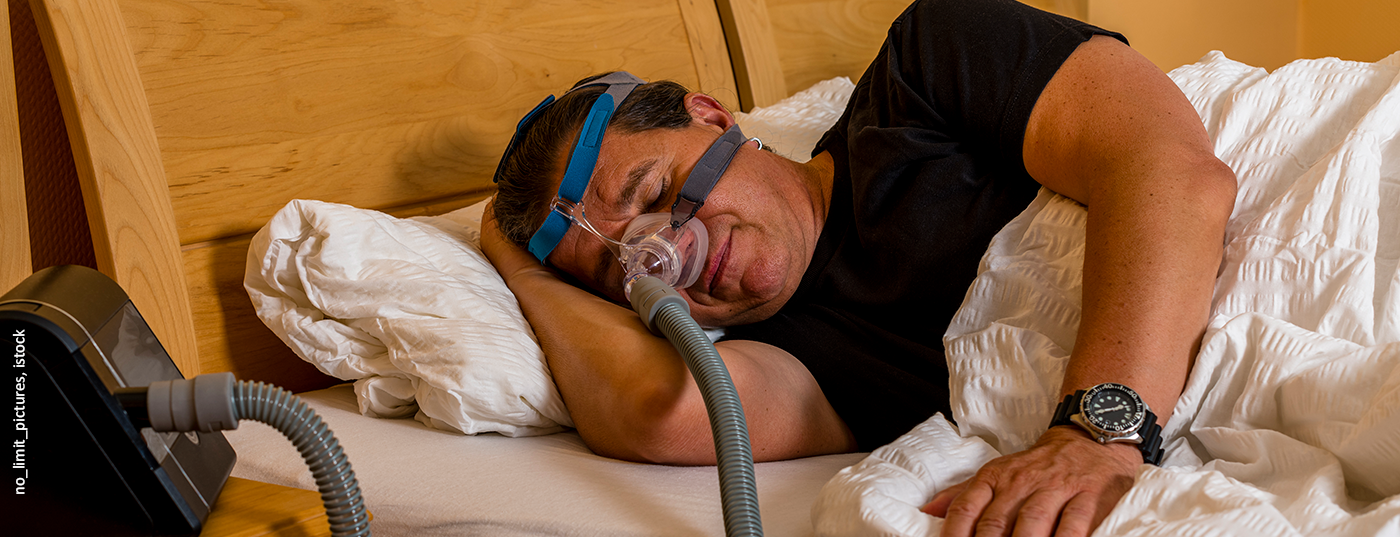
Terapia cPAP: il gold standard della terapia per l’OSA è lo splintaggio pneumatico continuo delle vie aeree superiori, utilizzando la pressione positiva delle vie aeree applicata tramite una maschera nasale/bocca/nasale (Fig. 1). La terapia con pressione positiva continua delle vie aeree (cPAP) è il trattamento più comunemente utilizzato. Lo splintaggio pneumatico elimina l’ostruzione delle vie aeree superiori e quindi, idealmente, tutte le apnee e le ipopnee e quindi anche l’ipossia notturna. Eliminando i risvegli indotti dall’ipossia, si migliora l’architettura del sonno e quindi il riposo del sonno, che porta a una riduzione della stanchezza diurna che lo accompagna. Come effetto collaterale, il russare viene eliminato in modo significativo, eliminando ciò che spesso viene indicato dal partner di letto come socialmente disturbante, il che aumenta la compliance alla terapia cPAP. Migliorando la funzione endoteliale [10] e abbassando la pressione arteriosa [11], si riducono i fattori di rischio cardiovascolare [12]. La terapia iperbarica notturna comporta effetti collaterali indesiderati in molti pazienti.
Spesso si lamenta una secchezza delle membrane mucose del tratto respiratorio superiore al mattino. Gli umidificatori ad aria calda, che oggi sono integrati in modo permanente nella maggior parte dei dispositivi cPAP e possono essere regolati individualmente dal paziente, possono fornire un rimedio in questo caso. Altrettanto frequentemente, durante la terapia viene descritta un’ostruzione nasale, che non di rado porta all’interruzione della terapia durante la notte. La vestibilità della maschera deve essere controllata e cambiata con un altro modello, se necessario. Occasionalmente, può essere utile ridurre leggermente la sovrapressione positiva del trattamento, soprattutto per alleviare le vie respiratorie nasali. La riduzione della pressione terapeutica deve essere almeno monitorata con la poligrafia cardio-respiratoria durante il corso della terapia; non deve compromettere in modo significativo l’efficacia del trattamento.
I pazienti affetti spesso utilizzano da soli i congestionanti nasali, come gocce o spray nasali contenenti xilometazolina, per evitare che il naso si gonfi a causa dell’aumento del flusso sanguigno nel turbinato inferiore. È noto che si verifica un’assuefazione, che gradualmente porta a una maggiore frequenza di utilizzo delle gocce.
spruzzi. Per non compromettere la terapia cPAP, si devono assolutamente prendere in considerazione misure chirurgiche del turbinato inferiore. La conchotomia assistita da radiofrequenza, ovvero la riduzione del turbinato inferiore, rende i trattamenti più rispettosi dei tessuti e di grande successo. Nonostante la moltitudine di opzioni per ottimizzare la terapia cPAP, la compliance al trattamento a lungo termine è solo del 60-70%. In questo contesto, è utile collegare i pazienti a gruppi di auto-aiuto, che possono migliorare significativamente l’accettazione del trattamento tra le persone colpite, grazie a uno scambio regolare tra di loro.
Esistono alcune alternative alla terapia con cPAP nel trattamento dell’OSA, ma la loro efficacia comparativa è ridotta. I più utilizzati sono gli splint di avanzamento mandibolare (UPS), che negli ultimi anni sono stati notevolmente migliorati in termini di comfort grazie all’uso di nuovi materiali e metodi di adattamento. Avanzando la mandibola, si riduce l’ostruzione orofaringea, soprattutto nella regione della base della lingua. Il prerequisito per il montaggio di un UPS è uno stato dentale sufficiente, una protrusione sufficiente della mascella inferiore e l’assenza di malattie dell’articolazione temporo-mandibolare. Grazie ai miglioramenti tecnici dell’UPS negli ultimi anni, questo trattamento è ora considerato equivalente alla terapia cPAP per i pazienti con OSA da lieve a moderata, se i requisiti anatomico-funzionali sopra citati sono soddisfatti nella persona interessata.
Nell’OSA grave, l’UPS deve essere utilizzato solo dopo il fallimento della terapia cPAP iniziale. Gli effetti collaterali tipici del trattamento UPS sono i fastidi all’articolazione della mandibola, per cui si raccomanda di sottoporsi a regolari controlli dentistici o ortodontici. Nell’OSA dipendente dalla posizione supina, spesso in combinazione con l’OSA di grado lieve, può essere appropriato l’uso di un gilet di prevenzione supina. Non è raro che le persone trovino scomodo indossare questi ausili durante la notte, quindi la compliance a lungo termine tende ad essere bassa. Le misure chirurgiche in alternativa alla terapia con cPAP includono l’uvulopalatofarnigoplastica in combinazione con la tonsillectomia bds. (TE-UPPP) [13], l’avanzamento maxillomandibolare [14] e la stimolazione del nervo ipoglosso (HGNS). [15] sono considerati. L’indicazione per una di queste procedure chirurgiche richiede una selezione precisa del paziente in relazione all’anatomia e alla funzione delle vie aeree superiori. L’indicazione per l’UPPP-TE richiede la presenza di un’ipertrofia della tonsilla palatina bds. che si trova anche nell’area distale a livello della base della lingua, oltre a una fessurazione pronunciata, cioè una posizione profonda del palato molle con un’ugola ipertrofica.
L’intervento è caratterizzato da un alto grado di invasività; le possibili complicanze non solo si presentano nell’immediato decorso post-operatorio, ma possono anche portare a un disagio a lungo termine a causa del profondo cambiamento della struttura anatomica dell’orofaringe. Si può anche osservare che il successo terapeutico iniziale diminuisce nel tempo, per cui la UPPP-TE dovrebbe essere eseguita solo dopo un’indicazione molto rigorosa e un’accurata selezione preoperatoria dei pazienti. In presenza di una malposizione della mandibola nei pazienti con OSA, si può prendere in considerazione un avanzamento maxillomandibolare, in cui si esegue un’osteotomia della mascella e della mandibola per farle avanzare e quindi rimuovere l’ostruzione orofaringea, soprattutto lo spazio delle vie aeree posteriori, in modo molto efficace.
In linea di principio, anche i pazienti senza malposizioni scheletriche della mascella superiore/inferiore sono idonei per questa procedura, ma anche in questo caso si deve tenere conto della natura altamente invasiva dell’intervento e dell’alterazione esterna della regione maxillomandibolare del viso. La HGNS è un’altra alternativa chirurgica per il trattamento dell’OSA. L’aggregato pacemaker viene impiantato in modo analogo ai pacemaker cardiaci conosciuti, l’elettrodo di stimolazione del nervo ipoglosso viene posizionato all’estremità distale del nervo e un altro elettrodo per valutare la respirazione viene inserito in uno spazio intercostale. Come per le altre procedure chirurgiche, è necessaria una diagnosi preoperatoria precisa. In particolare, si raccomanda un esame endoscopico delle vie aeree superiori indotto da farmaci, per escludere un’ostruzione concentrica a livello dell’orofaringe.
Apnea centrale del sonno
L’apnea centrale del sonno (CSA) è meno comune dell’OSA ed è caratterizzata da una mancanza di sforzo respiratorio durante la pausa respiratoria, dovuta a una disfunzione dell’impulso nervoso centrale che controlla la respirazione. Oltre all’insorgenza idiopatica, la ZSA si verifica nel contesto di modelli di malattia neurologica dovuti a lesioni del centro respiratorio situato nel midollo allungato. Anche i farmaci che deprimono l’apparato respiratorio, come l’uso di oppiacei, possono causare ZSA. Tuttavia, il sottotipo più comune è la respirazione di Cheyne-Stokes, che si verifica fino alla metà dei pazienti con insufficienza cardiaca sistolica grave [16]. Caratteristicamente, gli episodi di iperventilazione in crescendo-decrescendo si verificano tra le apnee centrali. I fattori di rischio sono il sesso maschile, l’età avanzata, l’ipocapnia e la presenza di fibrillazione atriale [17]. A causa dell’ipossia ricorrente e della conseguente attivazione del sistema nervoso simpatico, nei pazienti colpiti si verificano frequentemente aritmie cardiache maligne, che riducono di conseguenza la sopravvivenza complessiva di questo gruppo di pazienti [18].
Oltre al trattamento della rispettiva malattia di base, è possibile un approccio terapeutico basato sull’apparecchio, come nel trattamento dell’OSA. La terapia cPAP è meno efficace rispetto all’OSA; il trattamento basato sull’apparecchio può essere esteso con l’uso di dispositivi biPAP-ST, in base ai quali questi dispositivi generano un livello di pressione diverso durante l’inspirazione e l’espirazione e viene memorizzata una frequenza respiratoria minima; se questa frequenza minima non viene raggiunta, i dispositivi attivano il respiro successivo. La servoventilazione adattiva (ASV) è una forma speciale utilizzata nel trattamento della respirazione di Cheyne-Stokes. L’ecocardiografia per determinare la frazione di eiezione ventricolare sinistra (LVEF) è obbligatoria prima di iniziare l’ASV, in quanto l’ASV deve essere utilizzata solo nei pazienti che hanno una LVEF >45% [19]. La stimolazione frenica transvenosa [20] è un’altra procedura per trattare la ZSA. Analogamente all’HGNS, viene impiantato un pacemaker che stimola il nervo frenico tramite un elettrodo; la respirazione viene rilevata tramite un altro elettrodo nella vena azygos.
Ipossiemia e ipoventilazione legate al sonno
L’ipossiemia e l’ipoventilazione legate al sonno sono caratterizzate da periodi prolungati di riduzione ventilatoria durante il sonno, che si verificano principalmente nelle fasi REM con desaturazioni di ossigeno prolungate (ipossiemia SB) e un’ipercapnia di accompagnamento (ipoventilazione SB) dovuta a un sovraccarico simultaneo della pompa respiratoria. Tipico è il mal di testa mattutino dovuto all’ipercapnia, accompagnato da vertigini, problemi di concentrazione e stanchezza diurna. Oltre alla BPCO, le malattie neuromuscolari e le deformità toraciche svolgono un ruolo significativo nello sviluppo della malattia. Una forma particolare è la sindrome da ipoventilazione da obesità (OHS), che è definita da un’ipercapnia superiore a 45 mmg/Hg di pCO2 durante il giorno e da un IMC superiore a 30. Molti pazienti hanno un’OSA concomitante.
Oltre al trattamento della malattia di base, il dispositivo più comunemente utilizzato per il trattamento è un dispositivo biPAP-ST. Se la causa è una BPCO clinicamente rilevante, di solito è necessario un trattamento con ventilazione domiciliare non invasiva (NIV) [21] e un trattamento con ossigeno a lungo termine per almeno 16 ore al giorno. Analogamente al trattamento dell’OSA con la cPAP, il successo terapeutico a lungo termine delle suddette opzioni terapeutiche è limitato dalla mancanza di compliance da parte dei pazienti.
Messaggi da portare a casa
- L’apnea ostruttiva del sonno (OSA), l’apnea centrale del sonno (ZSA) e l’ipossiemia e l’ipoventilazione legate al sonno appartengono ai disturbi respiratori legati al sonno (SBAS).
- Il russare eccessivo combinato con le pause respiratorie e la conseguente sonnolenza o sonnolenza diurna sono i sintomi tipici dell’OSA, che è la SBAS più comune.
- L’insufficienza cardiaca può portare a un tipico modello di respirazione notturna, la respirazione di Cheyne-Stokes, che è una forma di ZSA.
- L’ipossiemia e l’ipoventilazione legate al sonno si verificano con l’insufficienza respiratoria, l’esaurimento della pompa respiratoria o la compromissione della funzione polmonare.
- Oltre all’anamnesi e all’esame clinico, la poligrafia cardiorespiratoria o polisonnografia costituisce il nucleo della diagnostica.
Letteratura:
- Fietze I, Laharnar N, Obst A, et al: Analisi della prevalenza e dell’associazione dell’apnea ostruttiva del sonno con differenze di sesso e di età – Risultati di SHIP Trend. J Sleep Res 2019; 28(5): e12770; doi: 10.1111/jsr12770; Epub 2018 Oct 1.
- Stuck BA, Weeß HG: La nuova “Classificazione internazionale dei disturbi del sonno” – Una valutazione critica dei criteri diagnostici per i disturbi respiratori legati al sonno. Somnologia 2015; 19: 126-132.
- Rodenbeck A: Manuale dell’Accademia Americana di Medicina del Sonno. Panoramica dell’aggiornamento versione 2.0. Somnologia 2013; 17: 122-130.
- Schulz R, Eisele HJ, Reichenberger F, Seeger W: Apnea ostruttiva del sonno e sindrome metabolica. Pneumologia 2008; 62(2): 88-91.
- Schulz R, Eisele HJ, Weissmann N, Seeger W: Apnea ostruttiva del sonno: un importante fattore di rischio cardiovascolare. Deutsches Ärzteblatt 2006; 103: 775-781.
- Aurora RN, Crainiceanu C, Gottlieb DJ, et al: Apnea ostruttiva durante il sonno REM e malattie cardiovascolari. AM J Respir Crit Care Med 2018; 197(5): 653-660; doi: 10.1164/rccm.201706-1112OC.
- Gami AS, Pressman G, Caples SM et al: Associazione tra fibrillazione atriale e apnea ostruttiva del sonno. Circulation 2004; 110(4): 364-367; doi: 10.1161/01.CIR.0000136587.68725.8E; Epub 2004 Jul12.
- Gottlieb DJ, Yenokyan G, Newman AB, et al: Studio prospettico sull’apnea ostruttiva del sonno e sull’insorgenza di malattia coronarica e insufficienza cardiaca: lo studio sleep heart health. Circolazione 2010; 122(4): 352-360; doi 10.1161/CIRCULATIONHA.109.901801; Epub 2010 Jul 12.
- Arzt M, Young T, Finn L, et al: Associazione tra la respirazione disturbata dal sonno e l’insorgenza di ictus. Am J Respir Crit Care Med 2005; 172(11): 1447-1451; doi: 10.1164/rccm.200505-7020C; Pubblicato il 1° settembre 2005.
- Mazzotti DR, Keenan BT, Lim DC, et al: I sottotipi di sintomi dell’apnea ostruttiva del sonno predicono l’incidenza di esiti cardiovascolari. Am J Respir Crit Care Med 2019; 200(4): 493-506; doi: 10.1164/rccm.201808-1509OC.
- Becker HF, Jerrentrup A, Ploch T, et al: Effetto del trattamento con pressione positiva continua nasale delle vie aeree sulla pressione sanguigna nei pazienti con apnea ostruttiva del sonno. Circolazione 2003; 107(1): 68-73; doi: 10.1161/01.cir.0000042706.47107.7a.
- McEvoy RD, Antic NA, Heeley E, et al: CPAP per la prevenzione degli eventi cardiovascolari nell’apnea ostruttiva del sonno. N Engl J Med 2016; 375(10): 919-931; doi: 10.1056/NEJMoa1606599.
- Fujita S, Conway WA, Zorick F, Roth T: Correzione chirurgica delle anomalie anatomiche nella sindrome delle apnee ostruttive del sonno: uvulopalatofaringoplastica. Otolaryngol Head Neck Surg 1981; 89: 923-934.
- Hochban W, Brandenburg U, Peter JH.: Trattamento chirurgico dell’apnea ostruttiva del sonno mediante avanzamento maxillomandibolare. Sonno 1994; 17: 624-629.
- Strollo PJ Jr, Soose RJ, Maurer JT, et al: Stimolazione delle vie aeree superiori per l’apnea ostruttiva del sonno. N Engl J Med 2014; 370(2): 139-149; doi: 10.1056/NEJMoa1308659.
- Schulz R, Blau A, Börgel J e altri: Apnea notturna nell’insufficienza cardiaca. Eur Respir J 2007; 29(6): 1201-1205; doi: 10.1183/09031036.00037106.
- Sin DD, Fitzgerald F, Parker JD, et al: Fattori di rischio per l’apnea del sonno centrale e ostruttiva in 450 uomini e donne con insufficienza cardiaca congestizia. Am J Respir Crit Care Med 1999; 160(4): 1101-1106; doi: 10.1164/ajrccm.160.4.9903020.
- Hanly PJ, Zuberi-Khokhar NS: Aumento della mortalità associato alla respirazione Cheyne-Stokes nei pazienti con insufficienza cardiaca congestizia. Am J Respir Crit Care Med 1996; 153(1): 272-276; doi: 10.1164/ajrccm.153.1.8542128.
- Cowie MR, Woehrle H, Wegscheider K, et al: Servoventilazione adattiva per l’apnea centrale del sonno nell’insufficienza cardiaca sistolica. N Engl J Med 2015; 373(12): 1095-1105; doi: 10.1056/NEJMoa1506459.
- Ponikowski P, Javaheri S, Michalkiewicz D, et al: Stimolazione transvenosa del nervo frenico per il trattamento dell’apnea centrale del sonno nell’insufficienza cardiaca. Eur Heart J 2012; 33(7): 889-894; doi: 10.1093/eurheartj/ehr298.
- Köhnlein T, Windisch W, Köhler D, et al: Ventilazione positiva non invasiva per il trattamento della broncopneumopatia cronica ostruttiva stabile grave: uno studio clinico prospettico, multicentrico, randomizzato e controllato. Lancet Respir Med 2014; 2(9): 698-705; doi: 10.1016/S2213-2600(14)70153-5.
InFo PNEUMOLOGIA & ALLERGOLOGIA 2021; 3(3): 11-15.