Il problema principale dell’angioplastica è la stenosi ricorrente, di cui una grande percentuale è dovuta allo sviluppo di iperplasia neointimale (NIH). Questo fenomeno può essere efficacemente soppresso applicando farmaci antiproliferativi agli stent e ai palloncini. Gli studi iniziali sull’argomento mostrano risultati incoraggianti, con ulteriori studi randomizzati che dovrebbero fornire maggiori informazioni sui potenziali effetti collaterali, sulla selezione dei pazienti e anche sul rapporto costi-benefici.
Numerosi studi epidemiologici che utilizzano tecniche di esame oggettivo mostrano una prevalenza di malattia arteriosa periferica (PAVD) del 3-10% e, a partire dai 70 anni, del 15-20%. Clinicamente, la PAOD si presenta in fasi diverse, dai pazienti asintomatici all’ischemia critica dell’arto (CLI). Dopo la diagnosi di CLI, il 30% dei pazienti subisce un’amputazione nel primo anno, il 20% ha dolore e ulcerazioni persistenti [1]. Il tasso di mortalità a un anno è del 20%, con eventi cardiaci e cerebrali che dominano il destino dei pazienti. La rivascolarizzazione è quindi un obiettivo terapeutico primario. Il successo tecnico dell’angioplastica percutanea transluminale (PTA) è generalmente molto elevato. Per gli eventi acuti, come le dissezioni che limitano il flusso e il “contraccolpo elastico” dell’arteria, lo stent offre una soluzione meccanica nel senso di un supporto del vaso. Il problema principale del metodo è il verificarsi di stenosi ricorrenti, che si verificano nel 30-50%/anno a seconda della lunghezza e della posizione della lesione. La causa principale della stenosi ricorrente è lo sviluppo dell’iperplasia neointimale (NIH). Questo può essere efficacemente soppresso con l’applicazione topica di farmaci antiproliferativi. Nell’angioplastica coronarica percutanea, questo concetto è stato applicato con successo per quasi un decennio ed è ampiamente supportato da diversi studi randomizzati. Al contrario, l’evidenza di questo metodo nell’area del flusso periferico è significativamente inferiore. Un articolo di revisione sull’argomento è stato già pubblicato in VASA 02/2012 [2]. Di seguito, sono stati aggiunti i risultati dello studio attuale.
Stenosi ricorrente dopo l’angioplastica
La NIH è il risultato di una cascata vasoproliferativa che inizia nel trauma vascolare da PTA con danno endoteliale e attivazione piastrinica. I complessi meccanismi biochimici coinvolti nello sviluppo della NIH non sono ancora del tutto compresi. Eventi secondari come lo stress ossidativo e l’infiammazione causano l’espressione di varie metalloproteinasi di matrice (MMP) attraverso un aumento dei radicali liberi, che contribuiscono alla degradazione del collagene e dell’elastina nella parete arteriosa e quindi permettono la migrazione delle cellule nell’intima vascolare. Il paradigma secondo cui queste cellule sono esclusivamente cellule muscolari lisce vascolari che hanno perso l’espressione della desmina e la contrattilità e ora esprimono la vimentina è stato messo in discussione dalla ricerca di diversi gruppi. È stato dimostrato che dopo l’angioplastica coronarica o l’intervento di bypass, i fibroblasti migrano anche dall’avventizia attraverso la media nell’intima e acquisiscono l’espressione della SMA (“actina muscolare liscia”), trasformandosi così in miofibroblasti [3–5]. Dopo la PTA degli shunt di dialisi, sono state rilevate anche cellule muscolari lisce e cellule endoteliali derivate da cellule staminali circolanti provenienti dal midollo osseo [6]. Dal punto di vista terapeutico, qui si sta creando una base promettente per nuovi approcci terapeutici.
Una volta nell’intima vascolare, i miofibroblasti proliferano e sintetizzano le proteine della matrice extracellulare. Questo processo termina in genere circa tre o quattro mesi dopo il trauma vascolare con uno strato cellulare neointimale che, a seconda del suo spessore, può restringere il lume del vaso a tal punto da provocare una stenosi ricorrente. L’applicazione di farmaci antiproliferativi inibitori del ciclo cellulare a palloncini e stent (paclitaxel, sirolimus, everolimus) sopprime efficacemente la formazione dello strato neointimale. La somministrazione topica consente di ottenere elevate concentrazioni di farmaco a livello locale, senza causare effetti collaterali sistemici.
Il sirolimus (rapamicina) è un macrolide naturale con effetti immunosoppressivi. È in grado di aumentare la concentrazione della proteina inibitoria del ciclo cellulare p27, che inibisce la transizione dalla fase G1 alla fase S della cellula. L’Everolimus, che è un derivato del sirolimus, ha lo stesso meccanismo d’azione. Il principio attivo Paclitaxel (PTX) è stato originariamente isolato dalla corteccia del tasso del Pacifico (Taxus brevifolia). Recentemente, può essere parzialmente sintetizzato dal tasso europeo. Il paclitaxel si lega in modo irreversibile alla beta-tubulina e quindi impedisce la degradazione dei microtubuli, motivo per cui la cellula non può più dividersi mitoticamente. Il paclitaxel è altamente lipofilo e quindi viene assorbito rapidamente dalla parete vascolare.
Situazione dello studio
Negli studi sugli stent a rilascio di farmaco (DES) e sui palloncini rivestiti di farmaco (DCB), viene fatta una distinzione generale tra le applicazioni sulle arterie femoropoplitee (tabella 1) e sulle arterie sotto il ginocchio (BTK), corrispondentemente più strette ( tabella 2).
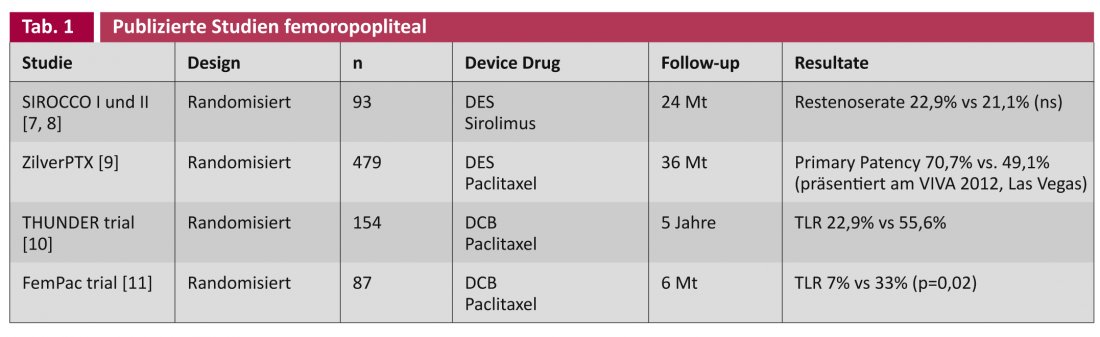
Gli studi SIROCCO sono stati condotti rispettivamente nel 2002 e nel 2002. Nel 2006, uno stent a rilascio di sirolimus è stato confrontato in modo casuale con lo stesso stent non rivestito nel trattamento dell’arteria femorale superficiale [7, 8]. Dopo due anni, non è stata riscontrata alcuna differenza nel verificarsi di stenosi ricorrenti, forse a causa della concentrazione di sirolimus troppo bassa (90 μg/cm2). Il recente studio prospettico randomizzato multicentrico sullo stent ZilverPTX® ha confrontato uno stent al nitinolo a rilascio di paclitaxel (3 μg/mm2) con l’angioplastica con palloncino semplice (POBA) e lo stesso stent in metallo nudo non rivestito (BMS) in 479 pazienti. Lo studio è stato concepito per cinque anni, con i risultati intermedi che sono stati riportati continuamente ai congressi: Dopo tre anni, lo stent rivestito mostra una netta superiorità statisticamente significativa nella pervietà primaria (= “assenza angiografica o duplex sonografica di stenosi ricorrente”) del 70,7% rispetto al 49,1% (presentato a VIVA 2012, Las Vegas).
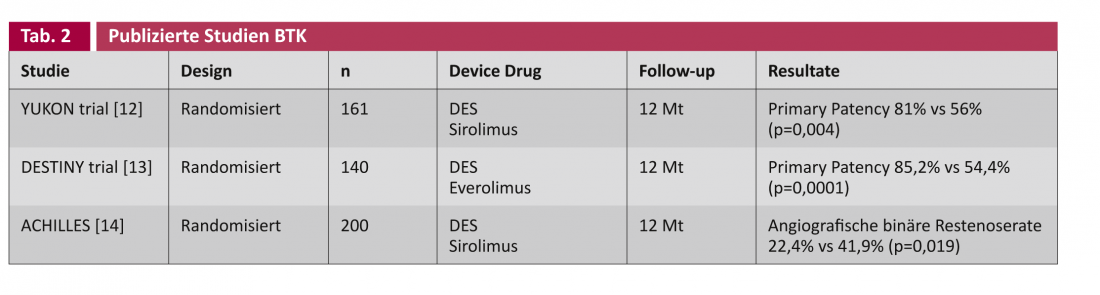
In linea di principio, nel trattamento delle lesioni vascolari è auspicabile che non rimanga alcun materiale estraneo, come uno stent. Il concetto di DCB ne tiene conto. Nello studio THUNDER, c’è un vantaggio significativo per il DCB per quanto riguarda il tasso di reintervento (“rivascolarizzazione della lesione bersaglio”, TLR) anche dopo cinque anni, sebbene solo con lesioni vascolari brevi (Corso Interventistico di Lipsia 2012). La domanda chiave rimane se c’è un posto per il DCB anche nelle lesioni lunghe e fortemente calcificate. Sono in corso studi che analizzano la DCB in combinazione con altre tecnologie come l’aterectomia, oltre a tutta una serie di studi sulla DCB nell’uso primario (Tab. 3).
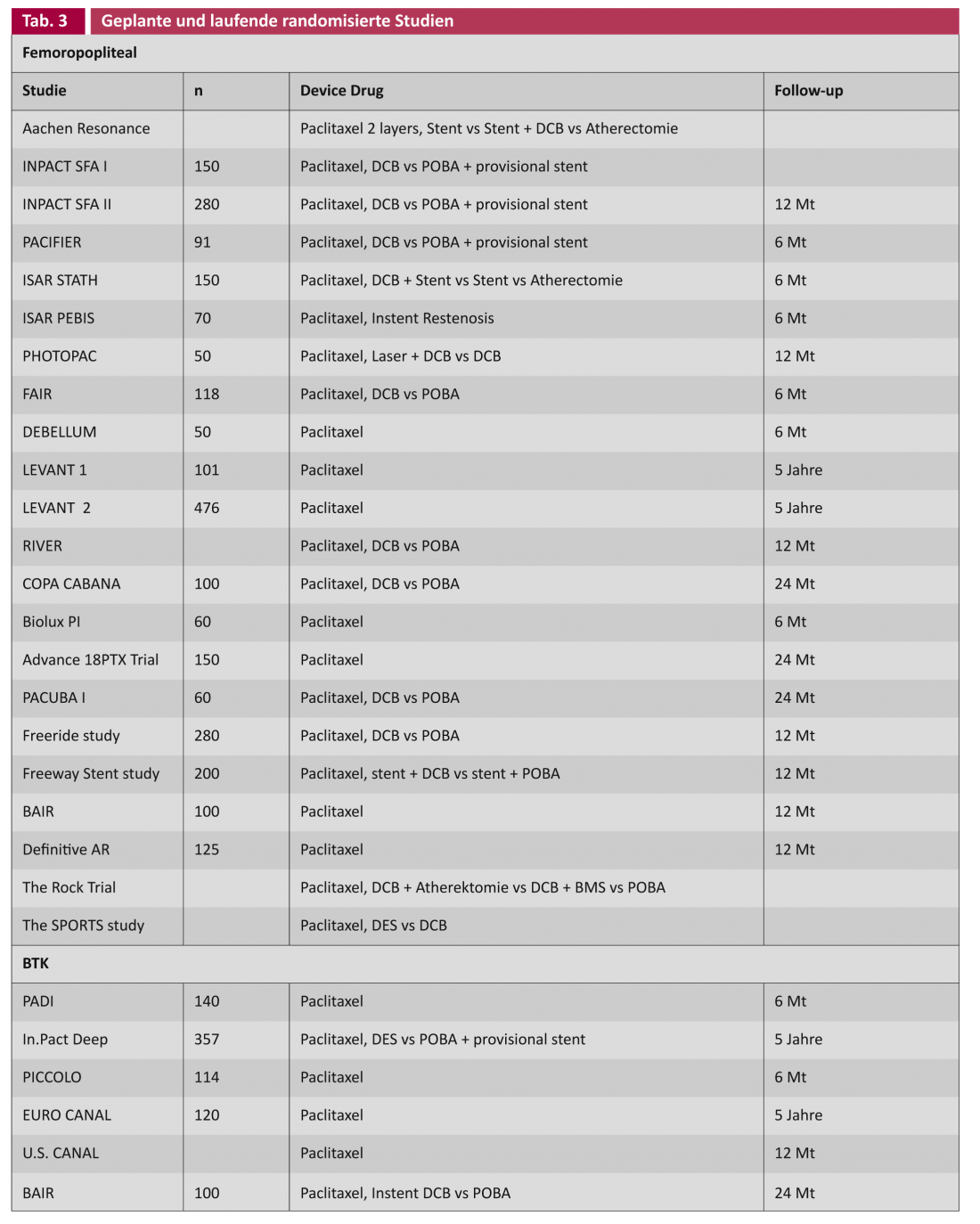
L’uso della tecnologia a rilascio di farmaco nel segmento arterioso infrapopliteo richiede una considerazione separata. I pazienti con ischemia critica degli arti di solito presentano ostruzioni multiple delle arterie della parte inferiore della gamba, come nei diabetici e nei pazienti con grave insufficienza renale. Assicurando almeno un vaso aperto verso il piede (“flusso in linea retta”), si dovrebbe migliorare la guarigione della ferita e ridurre il tasso di amputazione. Tuttavia, l’angioplastica sulle arterie della gamba inferiore da sola spesso produce un risultato di dilatazione non sufficientemente buono, non da ultimo a causa della lunghezza delle occlusioni dei vasi. Qui si verificano spesso la dissezione e il contraccolpo, che potenzialmente possono portare a un’occlusione precoce nelle arterie di calibro sottile.
Scheinert et al. sono stati i primi a inserire uno stent coronarico a rilascio di farmaco per via infrapoplitea in 30 pazienti nel 2006. Dopo sei mesi, non è stata trovata alcuna stenosi ricorrente [15]. Lo studio YUKON-BTK ha randomizzato questo stent con uno stent a eluizione di sirolimus e ha anche rilevato una superiorità statisticamente significativa del DES nella pervietà primaria (81% vs 56%, p=0,004) [12]. Altri studi randomizzati pubblicati sull’argomento includono DESTINY [8] e ACHILLES [14], che trovano anche questa paternità primaria statisticamente migliore per il DES.
Tuttavia, per quanto riguarda gli importanti endpoint clinici dell’amputazione e della morte, la tecnologia non apporta ancora alcun vantaggio dimostrabile, come hanno dimostrato Rastan et al. in una revisione dei dati raggruppati di 1039 pazienti negli studi sopra citati [16].
Discussione
Oltre agli studi randomizzati sopra elencati, esiste tutta una serie di dati di registro [2]. L’interpretazione dei risultati suggerisce che il rivestimento farmacologico, analogo all’angioplastica coronarica, è un metodo promettente nel trattamento della PAVK. Sempre più evidenze dimostrano che il tasso di stenosi ricorrente, e quindi potenzialmente di reinterventi, può essere ridotto sia per via femoropoplitea che infrapoplitea. Tuttavia, è prematuro formulare un gold standard a partire da questo, soprattutto perché gli studi randomizzati con i criteri di inclusione non sempre riflettono le normali condizioni quotidiane. I risultati dei grandi studi in corso forniranno maggiori informazioni sui potenziali effetti collaterali, sulla giusta selezione dei pazienti e anche sul rapporto costo-beneficio. (Tab. 3). Quest’ultimo aspetto richiede un’attenzione particolare, poiché si spera che la potenziale riduzione del tasso di reintervento porti a una riduzione dei costi, come è stato dimostrato in modo comparativo negli studi di cardiologia grazie all’uso dei DES. [17].
Non ci sono dati prospettici randomizzati sul post-trattamento con l’antiaggregazione duale. Secondo il consenso svizzero, la doppia antiaggregazione viene generalmente effettuata per un mese dopo l’impianto di BMS periferici [18]. A causa della ritardata reendotelializzazione dopo l’impianto di DES/DCB, questo viene effettuato per un tempo più lungo, analogamente alla cardiologia. Negli studi citati, questo periodo era compreso tra uno e sei mesi, a seconda della regione vascolare trattata.
Letteratura:
- Norgren L, et al; gruppo di lavoro TASC II: J Vasc Surg 2007; 45 Suppl: S5-67.
- Buechel R, Stirnimann A, Zimmer R, Keo H, Groechenig E: VASA 2012; 41(4): 248-261.
- Scott NA, et al: Circulation 1996; 93(12): 2178-2187.
- Shi Y, et al: Circulation 1996; 94(7): 1655-1664.
- Shi Y, et al: Circulation 1997; 95(12): 2684-2693.
- Sata M, et al: Nat Med 2002; 8(4): 403-409.
- Duda SH, et al: Circulation 2002; 106(12): 1505-1509.
- Duda SH, et al: J Endovasc Ther 2006; 13(6): 701-710.
- Dake MD, et al; a nome degli Investigatori Zilver PTX: Circ Cardiovasc Intervent 2011; 4(5): 495-504.
- Tepe G, et al: NEJM 2008; 358(7): 689-699.
- Werk M, et al: Circulation 2008; 118(13): 1358-1365.
- Rastan A, et al: Eur Heart J 2011; 32: 2274-2281.
- Bosiers M, et al: J Vasc Surg 2012; 55(2): 390-398.
- Scheinert D, et al; ACHILLES Investigators: J Am Coll Cardiol 2012; 60(22): 2290-2295.
- Scheinert D, et al: EuroIntervention 2006; 2(2): 169-174.
- Rastan A, Noory E, Zeller T: Vasa 2012; 2: 90-95.
- Filion KB, et al: Am J Cardiol 2009; 103(3): 338-344.
- Jäger K, et al: Schweiz Med Forum 2009; 9(39): 690.
CARDIOVASC 2013; 12(1), 15-19