Il metilfenidato viene utilizzato da decenni nel trattamento dell’ADHD. Esistono diverse ipotesi su come esattamente questo psicostimolante dispieghi i suoi effetti. Una di queste riguarda il metilfenidato che influenza la neurotrasmissione dopaminergica nel nucleo accumbens e le reti neuronali associate. Per saperne di più, un team di ricerca ha condotto uno studio di imaging.
Il metilfenidato (MPH) è il farmaco di scelta per il trattamento del disturbo da deficit di attenzione e iperattività (ADHD) clinicamente rilevante [1]. Ritalin® è il nome del marchio del preparato MPH più vecchio e più comune. Altri farmaci utilizzati in Svizzera che contengono anche il principio attivo MPH sono Medikinet MR®, Equasym®, Focalin® e Concerta® [2]. Si distingue tra preparati a breve e a lunga durata d’azione. Spesso, all’inizio del trattamento viene utilizzato un preparato MPH a breve durata d’azione, ad esempio la compressa di Ritalin® da 10 mg. L’MPH in questa forma viene assorbito rapidamente dall’organismo e inizia a fare effetto dopo circa 30 minuti. Dopo 3-4 ore, l’effetto svanisce rapidamente. Inoltre, esiste la possibilità di somministrare stimolanti in forma a lunga durata d’azione. In questo caso, il principio attivo viene rilasciato dalla compressa con un ritardo e l’effetto viene mantenuto da 7 a un massimo di 14 ore, a seconda della preparazione. Tuttavia, le informazioni sulla durata d’azione sono solo una linea guida; la terapia può essere adattata al meglio alle esigenze del bambino [3].
Esame di risonanza magnetica in un disegno crossover
I ricercatori hanno condotto uno studio crossover randomizzato, controllato con placebo e in doppio cieco presso l’Ospedale Universitario di Fukui (Giappone) [4]. L’età media dei 27 bambini con ADHD era di 10,6 anni (SD 1,8; range di età: 7,3-15,5 anni). Nei 49 soggetti di controllo senza ADHD, l’età media era di 11,1 anni (SD 2,3; range di età 6,1-15,6 anni). I criteri di inclusione sono riportati nel riquadro. I bambini con ADHD sono stati scansionati due volte con la risonanza magnetica funzionale a riposo in condizioni di metilfenidato e placebo. Durante il primo appuntamento, è stato loro somministrato MPH (1,0 ± 0,1 mg/kg) o placebo (lattosio) con rilascio osmotico (OROS), come negli studi precedenti in doppio cieco. Da cinque a otto ore dopo la somministrazione, quando la concentrazione di MPH nel sangue è massima, i bambini sono stati sottoposti a un esame fMRI allo stato di riposo e hanno eseguito un test di prestazione continuo standardizzato fuori dallo scanner MRI. Al secondo appuntamento (da 1 a 6 settimane dopo il primo appuntamento), i bambini con ADHD sono stati sottoposti a una scansione fMRI allo stato di riposo e hanno eseguito il test di performance dopo aver assunto il secondo farmaco: i bambini che avevano assunto OROS-MPH al primo appuntamento hanno ricevuto il placebo al secondo appuntamento in condizioni di doppio cieco e viceversa.
Il gruppo di controllo, cioè i partecipanti allo studio senza ADHD, ha completato la stessa scansione fMRI a riposo una volta senza OROS-MPH o placebo.

Il metilfenidato ha dimostrato di modulare l’attività neuronale
È stato dimostrato che il metilfenidato (MPH) aumenta l’attività neuronale spontanea nel nucleo accumbens e nelle reti della salienza e della modalità predefinita [4].
- Nel test di performance, l’MPH ha ridotto significativamente gli errori di omissione, il tempo di reazione medio e la variabilità di risposta intraindividuale durante un compito (IIRV) nel gruppo ADHD (ciascuno p<0,001).
- La modulazione indotta dal metilfenidato dell’attività neuronale spontanea nella rete di modalità predefinita ha previsto l’effetto del trattamento in termini di variabilità della risposta intraindividuale (IIRV) (r=-0,46, p=0,016).
- Per quanto riguarda gli effetti dell’MPH sull’attività neuronale spontanea nel nucleo accumbens, l’ampiezza delle fluttuazioni a bassa frequenza (ALFF) nel nucleo accumbens destro era significativamente più alta nella condizione ADHD-MPH rispetto alla condizione ADHD-placebo (p<0,05, correzione di Bonferroni, Cohen’s d=0,55).
- L’ALFF era significativamente più alto nelle reti di salienza (SN) e nella rete di modalità predefinita (DMN) nella condizione ADHD-MPH rispetto alla condizione ADHD-placebo (SN: p<0,05, Cohen’s d=0,57; DMN: p<0,01, Cohen’s d=0,66; Bonferroni corretto in ogni caso). Non c’era alcuna differenza significativa nella rete frontoparietale sinistra e destra (p>0,05). L’analisi di regressione lineare multipla ha rivelato che solo la modulazione dell’MPH del modello di somiglianza ALFF all’interno della rete di modalità predefinita era significativamente associata agli effetti del farmaco sulla variabilità della risposta intraindividuale (Tabella 1) . Ciò indica che si tratta di un meccanismo d’azione neurobiologico cruciale.
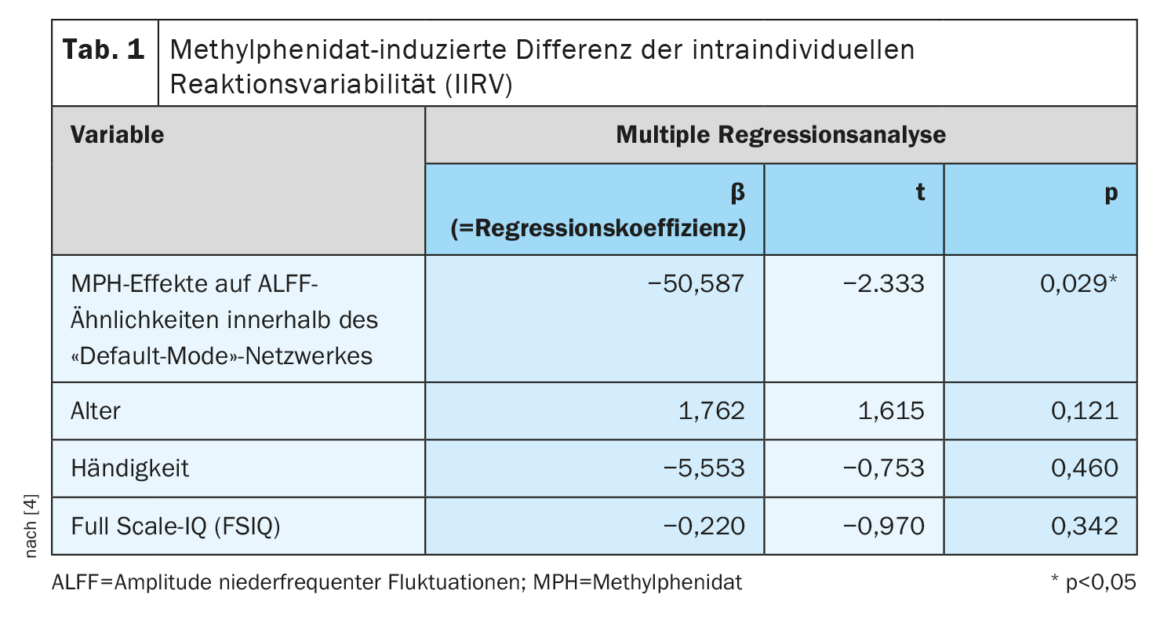
Questi risultati ampliano l’attuale comprensione dei meccanismi neurobiologici alla base del trattamento con MPH nei bambini con ADHD e, secondo gli autori dello studio, in futuro potrebbero consentire di ricavare biomarcatori clinicamente utili per valutare il successo del trattamento.
Letteratura:
- Praxis Suchtmedizin Schweiz, www.praxis-suchtmedizin.ch/praxis-suchtmedizin/index.php/de/medikamente/einleitung-mh, (ultimo accesso 10.02.2023)
- Swissmedic: Informazioni sui medicinali, www.swissmedicinfo.ch,(ultimo accesso 10.02.2023)
- «Die medikamentöse Behandlung von Kindern und Jugendlichen mit einer Aufmerksamkeitsdefizit-Hyperaktivitätsstörung ADHS», März 2022,
www.pukzh.ch/sites/default/assets/File/
Informationen%20Stimulanzien%20und%20Ritalin.pdf, (ultimo accesso 10.02.2023) - Mizuno Y, et al.: Methylphenidate Enhances Spontaneous Fluctuations in Reward and Cognitive Control Networks in Children With Attention-Deficit/Hyperactivity Disorder. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, available online 23 October 2022, www.sciencedirect.com/science/article/pii/S2451902222002476, (ultimo accesso 10.02.2023)
HAUSARZT PRAXIS 2023; 18(2): 24–25
InFo NEUROLOGIE & PSYCHIATRIE 2023; 21(2): 30–31











