Un paziente con diabete di tipo 2 ha una probabilità 2-3 volte maggiore di avere un infarto del miocardio o un ictus rispetto alle persone senza diabete. Le malattie cardiovascolari rappresentano fino al 50% dei decessi associati al diabete. È quindi indicato un trattamento ottimale dei quattro principali fattori di rischio: glicemia, peso, pressione alta e livelli di lipidi nel sangue.
Anche se la mortalità per malattia coronarica nei pazienti con diabete di tipo 2 è diminuita costantemente negli ultimi 2 decenni, la probabilità di subire un infarto miocardico o un ictus è da 2 a 3 volte superiore rispetto alle persone senza diabete [1]. Le malattie cardiovascolari rappresentano quindi fino al 50% dei decessi associati al diabete [2]. Nonostante questo aumento del rischio, la maggior parte delle persone colpite non viene ancora trattata adeguatamente per quanto riguarda i quattro principali fattori di rischio: glicemia, peso, pressione alta e livelli di lipidi nel sangue, e solo circa un paziente diabetico su 300 raggiunge i propri valori target individuali [3]. È proprio questa terapia multifattoriale di tutti i fattori di rischio che rende la terapia adeguata di un paziente con diabete di tipo 2 una sfida quotidiana nella pratica. Il seguente articolo intende fornire un aggiornamento sulle attuali raccomandazioni terapeutiche in materia.
Inibizione dell’aggregazione piastrinica
Per molto tempo, la somministrazione di acido acetilsalicilico (ASA) 100 mg è stata considerata una misura sensata nella prevenzione primaria del diabete di tipo 2, perché la somministrazione era associata a una riduzione degli eventi ischemici. In una meta-analisi che includeva pazienti con e senza diabete, il trattamento ha comportato una riduzione relativa degli eventi cardiaci avversi maggiori (MACE) del 12% (0,51% vs. 0,57%, p≤0,0001) nei soggetti a basso rischio in prevenzione primaria, principalmente riducendo gli infarti miocardici non fatali, ma senza ridurre i tassi di ictus o la mortalità [4]. Tuttavia, questa riduzione è accompagnata da un aumento altrettanto significativo degli eventi di sanguinamento rilevanti, per cui il beneficio netto appare discutibile. Questi risultati coincidono con gli studi di follow-up, per cui il trattamento profilattico primario con l’acido acetilsalicilico dovrebbe ora essere preso in considerazione nelle attuali linee guida ESC solo nei pazienti con diabete e un rischio elevato o molto elevato di eventi cardiovascolari e in assenza di controindicazioni. (Tab. 1). In questi casi, è necessario somministrare contemporaneamente un inibitore della pompa protonica [6].
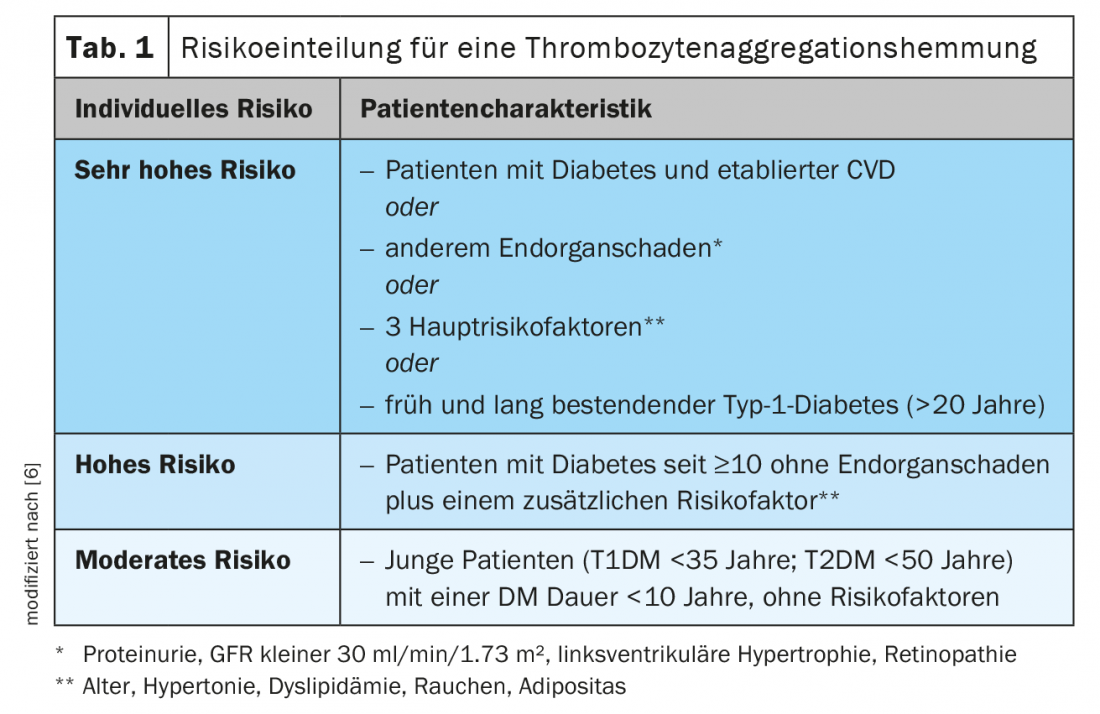
Nella profilassi secondaria, come nel caso di studio, il rapporto rischio-beneficio dei farmaci antiaggreganti è chiaramente positivo, per cui dovrebbero essere somministrati su base obbligatoria [6].
Nei pazienti con sindrome coronarica acuta (SCA), l’uso aggiuntivo di nuovi agenti antiaggreganti come ticagrelor (Brilique®) o prasugrel (Efient®) si è dimostrato superiore al trattamento con clopidogrel [7,8] nel primo anno dopo una sindrome coronarica acuta. La scelta dei farmaci antiaggreganti è analoga a quella dei non diabetici e dipende dal tipo di ACS. Nei pazienti a rischio (età >50 anni e un fattore di rischio aggiuntivo come l’età >60 anni, il diabete di tipo 2 con trattamento farmacologico o l’insufficienza renale cronica con una clearance della creatinina <60 ml/min/1,73m2), la doppia terapia antiaggregante può essere somministrata per più di 12 mesi dopo un infarto miocardico, se necessario [9]. Nel determinare la durata della terapia e i prodotti utilizzati, è importante una stretta e buona interazione tra gli specialisti coinvolti e il medico di base.
Terapia anti-iperglicemica
Dal 2006, la gamma terapeutica per il trattamento dell’iperglicemia si è ampliata in modo significativo. È incoraggiante che tutte e tre le forme di terapia più recenti, gli inibitori DPP4, gli agonisti del recettore GLP1 e gli inibitori SGLT2, da un lato non abbiano un potenziale ipoglicemico endogeno, cioè non possano scatenare da soli l’ipoglicemia. D’altra parte, sono neutri dal punto di vista del peso (inibitori della DPP4) o possono addirittura avere un effetto di riduzione del peso (GLP1-RA > SGLT2 inibitori) [10].
In primo luogo e prima del trattamento farmacologico, viene determinato l’intervallo target individuale di HbA1c per il rispettivo paziente [11]. Questo si basa sulla durata della malattia, sull’età e sull’aspettativa di vita del paziente, ma anche sulle circostanze che accompagnano la terapia. Se non ci sono malattie concomitanti e la motivazione del paziente è alta, un intervallo target di HbA1c inferiore di <Il 6,5% può essere mirato o accettato se il farmaco da utilizzare ha un basso rischio ipoglicemico o non ha un potenziale ipoglicemico endogeno (Tabella 2) . Se si utilizzano sostanze come l’insulina o le sulfoniluree, è sufficiente un intervallo target di HbA1c superiore al 7,0%.

In ogni caso, però, la terapia farmacologica deve essere iniziata precocemente e, se necessario, anche in combinazione, in quanto può portare a un migliore controllo a lungo termine rispetto alla terapia anti-iperglicemica sequenziale [12]. Tuttavia, gli approcci terapeutici devono essere integrati da un’adeguata educazione di base del paziente affetto e da un’adeguata modifica della dieta e dello stile di vita, che, combinata con la riduzione del peso, migliora in modo sostenibile il controllo del diabete in ogni fase della malattia [10,11].
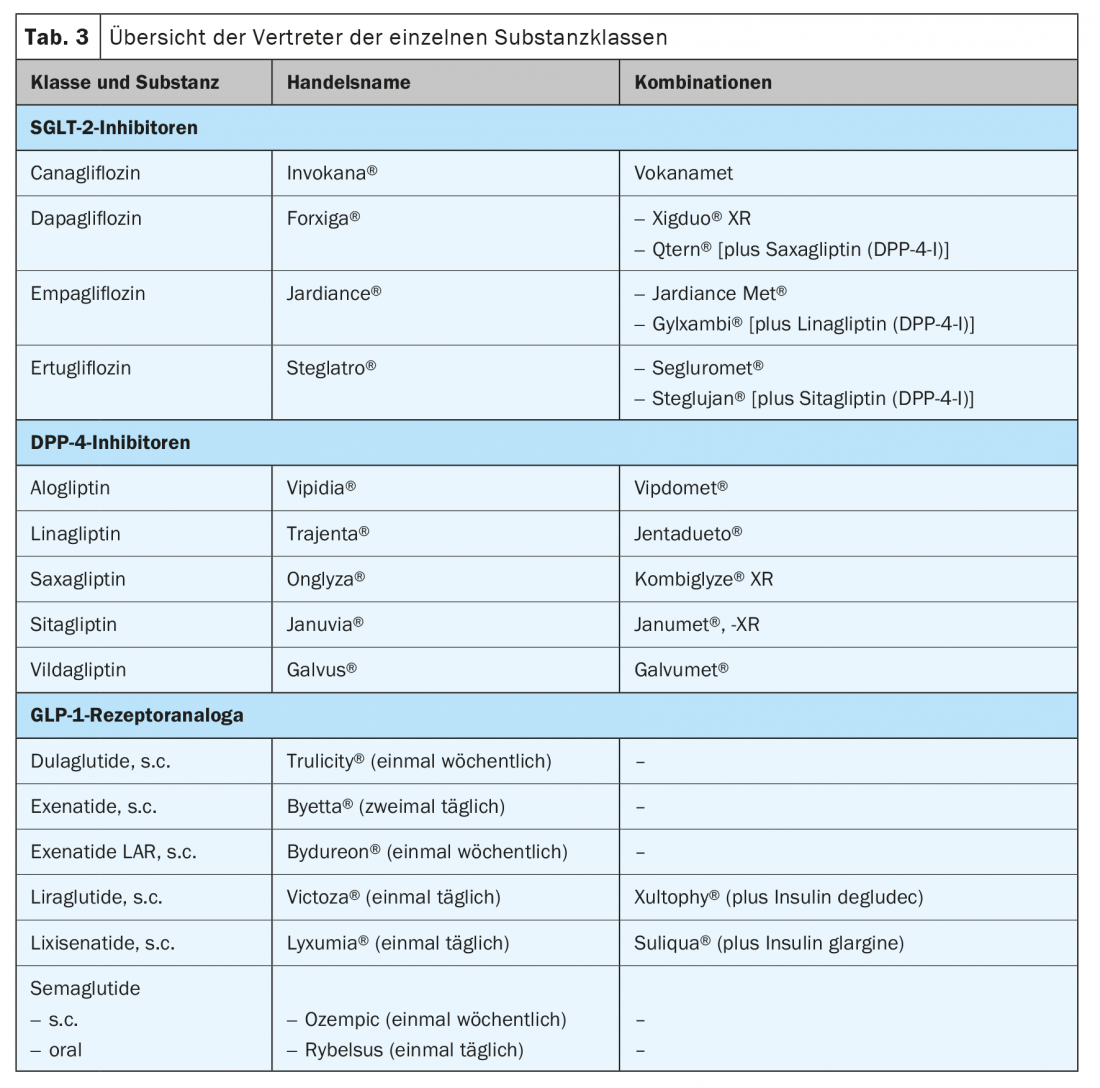
Di seguito, verranno discusse le tre classi terapeutiche più recenti, poiché negli ultimi anni sono stati raccolti numerosi dati scientifici su di esse, che aiutano a caratterizzare più da vicino le sostanze e aiutano nella selezione per il rispettivo paziente (Tab. 3).
Terapia anti-iperglicemica – Inibitori della dipeptidil peptidasi 4 (inibitori DPP4):
La classe degli inibitori della dipeptidil peptidasi (DPP)4 comprende oggi cinque diverse sostanze (Tab. 3). Le sostanze hanno circa lo stesso effetto anti-iperglicemico. Con un’HbA1c basale di circa l’8%, si può prevedere una riduzione dello 0,5-0,7%. Inoltre, sono neutrali rispetto al peso [13]. Di solito sono molto ben tollerati dai pazienti e sono una delle poche classi di sostanze che possono essere utilizzate nei casi di compromissione della funzione renale [14]. In questo caso, il dosaggio della maggior parte dei preparati deve essere adattato alla rispettiva funzione renale. Solo linagliptin non richiede ulteriori aggiustamenti per l’insufficienza renale e viene somministrato a 5 mg al giorno. Il farmaco non ha un effetto sulla conservazione della funzione renale, ma sembra possibile ridurre in una certa misura la progressione dell’albuminuria [15]. Questa classe di sostanze non sembra avere un effetto che vada oltre la pura riduzione del glucosio per quanto riguarda la riduzione del rischio cardiovascolare del paziente. I quattro studi sugli endpoint pubblicati sui preparati non mostrano alcuna riduzione dei tassi di eventi [16–19]. Al contrario, il saxagliptin può addirittura aumentare leggermente il tasso di ricoveri per insufficienza cardiaca scompensata [19].
Grazie alla sua buona tollerabilità, è un farmaco ideale per l’uso nei pazienti anziani, quando il controllo glicemico è l’obiettivo principale e un altro effetto sui reni e sul cuore è meno prioritario [20].

Terapia anti-iperglicemica – Inibitori del trasportatore 2 del sodio legato al glucosio (inibitori SGLT2)
La classe più giovane di farmaci non insulinici è il gruppo degli inibitori del trasportatore sodio-glucosio (SGLT) 2 (Tab. 3). Questo gruppo di farmaci sfrutta un meccanismo fisiologico di recupero degli zuccheri nel rene come principio terapeutico. Bloccando questi trasportatori, gran parte del glucosio precedentemente filtrato liberamente nel glomerulo viene escreto nelle urine. Questo comporta una perdita giornaliera di circa 60-70 g di glucosio [21]. Quindi, con un’HbA1c basale dell’8%, ci si può aspettare una riduzione dell’HbA1c dello 0,7-0,8%. Inoltre, il peso si riduce di circa 2-3 kg e la pressione sanguigna di 3-5 mmHg sistolica. Un vantaggio particolare è la buona efficacia in ogni fase della malattia del paziente, poiché il principio attivo non dipende dalla presenza o dal mantenimento della secrezione di insulina. Pertanto, può essere utilizzato in modo sensato in combinazione precoce con la metformina, ma anche nella terapia insulinica. I principali effetti collaterali sono l’aumento dell’incidenza di infezioni fungine genitali e una certa poliuria, che di solito si attenua nel corso del trattamento [21].
A seconda del preparato, la somministrazione è possibile fino a una funzione renale di 45 ml/min/1,73m2 (canagliflozin, dapagliflozin, empagliflozin) o 60 ml/min/1,73m2 (ertugliflozin) [21]. Al di sotto di questo livello, l’effetto di riduzione del glucosio non è significativo. Mentre l’effetto anti-iperglicemico diminuisce con la diminuzione della funzione renale, questo non si osserva per gli effetti benefici sul rene o sul cuore, che sono ancora presenti anche con un GFR ridotto [22].
Oltre agli effetti glicemici, gli inibitori SGLT2 sembrano avere effetti particolari nei diabetici con insufficienza renale e con insufficienza cardiaca e ridotta funzione di pompa (HFrEF). Per quanto riguarda gli effetti renali, le sostanze di questa classe di farmaci sembrano migliorare il rene e mantenerne la funzione in ogni fase. Questo è vero nella prevenzione primaria, ma anche nella prevenzione secondaria, dove l’albuminuria di qualsiasi gravità viene influenzata favorevolmente e anche la funzione renale è protetta [23,24]. Questo ha fatto sì che all’inibizione del SGLT2 sia stato assegnato un posto pari a quello degli ACE-inibitori nelle linee guida per il trattamento della malattia renale diabetica [25]. È interessante notare che questi effetti sono ancora presenti quando la funzione renale è già così gravemente compromessa che non si verifica un abbassamento significativo del glucosio. Canagliflozin è il primo rappresentante del gruppo di sostanze che è stato anche in grado di dimostrare l’efficacia con un GFR <30 ml/min/1,73m2 nei pazienti con albuminuria (ACR >300 mg/g) e di conseguenza può ancora essere trasmesso qui [22]. È quindi interessante chiedersi in che misura gli effetti siano presenti anche indipendentemente dal diabete o dalla nefropatia diabetica. I risultati iniziali di dapagliflozin dimostrano che questo può essere presente anche nell’insufficienza renale dei pazienti non diabetici [26].
Il trattamento dei pazienti con diabete e insufficienza cardiaca è emerso come il secondo dominio indipendente dall’abbassamento della glicemia. Già nel primo studio con endpoint cardiovascolare, EMPAREG, in cui sono stati studiati principalmente pazienti diabetici con malattia cardiovascolare conclamata, è stata osservata una riduzione significativa della mortalità del 33%, accompagnata da una riduzione altrettanto forte degli eventi di insufficienza cardiaca [23]. Anche gli effetti sull’insufficienza cardiaca sembrano essere un effetto di classe e possono quindi essere descritti da tutti e quattro i rappresentanti, mentre la riduzione della mortalità cardiovascolare non ha potuto essere provata al di là di ogni dubbio da tutte le sostanze. Di nuovo, ci si chiede se questi effetti sull’insufficienza cardiaca siano indipendenti dal diabete. Sono disponibili due studi per l’HFrEF, che sono stati in grado di dimostrare lo stesso effetto benefico nella popolazione non diabetica [27,28]. Se questo si verifichi anche nell’HFpEF, cioè nell’insufficienza cardiaca con funzione di pompa sistolica conservata, è oggetto di indagini attuali e si attende con interesse.
Va sottolineato che, sulla base di questi dati cardiaci e renali, le ultime raccomandazioni terapeutiche raccomandano l’uso di questo farmaco nei pazienti con malattia cardiovascolare accertata, insufficienza cardiaca o problemi renali, indipendentemente dall’HbA1c-Si deve prendere in considerazione il valore, cioè anche nei pazienti che in realtà sono già nel range target, ad esempio con una monoterapia di metformina, si deve utilizzare in aggiunta un inibitore SGLT2.
Terapia anti-iperglicemica – Agonisti del recettore del peptide glucagone-simile 1 (GLP1-RA)
La classe di terapia più forte in termini di riduzione della glicemia, oltre all’insulina, è quella degli agonisti del recettore GLP1. Fino a poco tempo fa, i rappresentanti di questo gruppo di sostanze venivano iniettati esclusivamente per via sottocutanea, per cui la frequenza può variare da prodotto a prodotto. Dall’estate 2020, tuttavia, è disponibile anche Rybelsus® (semaglutide), il primo rappresentante che può essere somministrato come compressa. Quando si somministra il semaglutide per via orale, è importante prendere in considerazione le modalità di assunzione che consentono al peptide di essere assorbito e di avere effetto in primo luogo. Sono simili a quelli dei preparati tiroidei: min. 30 minuti prima del primo pasto, senza altri farmaci o integratori alimentari, con un massimo di 120 ml di acqua dopo almeno un pasto. Fase di digiuno di 8 ore.
L’effetto di questo gruppo di sostanze si esplica essenzialmente attraverso un aumento della secrezione di insulina dipendente dal glucosio da parte delle cellule beta del pancreas, in combinazione con l’inibizione dell’appetito attraverso il ritardo dello svuotamento gastrico e un effetto diretto sul centro della fame [29]. Questo spiega anche buona parte degli effetti collaterali osservati, che devono essere interpretati piuttosto come un effetto eccessivo: Nausea fino al vomito. Questo è minore quando la dose viene aumentata lentamente e spesso diminuisce con la durata della terapia [29]. A seconda dell’HbA1c iniziale, ci si può aspettare una riduzione compresa tra lo 0,8% e l’1,6%, anche se le differenze individuali sono molto marcate. Questo vale anche per l’effetto sul peso corporeo, che diminuisce di 2-6 kg durante la terapia. Ulteriori effetti benefici derivano dalla riduzione della pressione sanguigna e dei lipidi [29]. In linea di massima, sono quattro i preparati più utilizzati in Svizzera: liraglutide, exenatide LAR, dulaglutide e semaglutide. La scelta del preparato da utilizzare può dipendere dalle preferenze del paziente (applicazione quotidiana o una volta alla settimana; somministrazione orale o sottocutanea). Nei pazienti ad alto rischio cardiovascolare con aterosclerosi conclamata, si può ipotizzare un effetto benefico per tutti e quattro gli agenti, che è meglio dimostrato per liraglutide e dulaglutide [21,30].
Anche per questa classe di sostanze, l’uso indipendente dal valore di HbA1c è raccomandato nei pazienti con malattie cardiovascolari o problemi renali noti.
Nei pazienti con insufficienza renale, queste sostanze possono essere somministrate. Sono sicuri da usare e sembrano rallentare un po’ la progressione nell’insufficienza renale compromessa. Nei pazienti con un GFR <30 ml/min/1,73m2, tuttavia, il farmaco deve essere interrotto in caso di aumento del vomito, poiché la deplezione di volume potrebbe plausibilmente peggiorare la situazione fino all’insufficienza renale acuta.
Terapia antipertensiva
L’ipertensione arteriosa è una delle comorbidità più comuni del diabete, che colpisce più del 60% [31]. In una meta-analisi, è stato dimostrato che una riduzione della pressione arteriosa di oltre 10 mmHg nei diabetici di tipo 2 riduce significativamente la mortalità (RR 0,87, 95% CI 0,78-0,96), gli eventi cardiovascolari (RR 0,89, 95% CI 0,83-0,95) e soprattutto gli ictus (RR 0,73, 95% CI 0,64-0,83) [31]. Allo stesso tempo, anche le complicanze microvascolari a lungo termine, come la retinopatia e l’albuminuria, sono state significativamente ridotte. D’altra parte, c’è eterogeneità di effetti quando la pressione arteriosa viene abbassata a una sistolica inferiore a 130 mmHg, poiché in questo caso solo il rischio di ictus viene ulteriormente ridotto, senza fornire ulteriori benefici sugli esiti cardiaci o microvascolari. Al contrario, un abbassamento troppo aggressivo aumenta il rischio di effetti collaterali gravi [31]. Si raccomanda di trattare l’ipertensione arteriosa nei diabetici con farmaci a partire da una pressione arteriosa di >140/90 mmHg. Si deve puntare a valori target di sistolica inferiori a 130 mmHg, ma non inferiori a 120 mmHg. Per l’età >65 anni, si dovrebbe scegliere un intervallo target moderatamente più alto >130-139 mmHg. Per la diastolica è stato definito un intervallo target inferiore a 80 mmHg, ma non inferiore a 70 mmHg (Tab. 4) [6]. La base di qualsiasi trattamento è, come sempre, la modifica dello stile di vita. Il trattamento farmacologico deve iniziare principalmente con una terapia combinata. I pazienti con diabete traggono beneficio dagli ACE-inibitori e dagli antagonisti del recettore dell’angiotensina-1, che dovrebbero essere utilizzati soprattutto in caso di microalbuminuria, albuminuria, proteinuria o ipertrofia LV [6]. Buoni partner di combinazione sono i calcio antagonisti o i diuretici tiazidici (simili). La compliance può essere promossa utilizzando la combinazione di 3 pillole in una sola, che sono disponibili in numero sempre maggiore. Va sottolineato che la pressione arteriosa può essere ancora una volta influenzata favorevolmente dalla scelta appropriata del farmaco antidiabetico. Quando si utilizza un agonista del recettore GLP1, come liraglutide, si può osservare una riduzione di 1-2 mmHg o un inibitore SGLT-2, come empagliflozin, una riduzione di 4 mmHg [23,30].
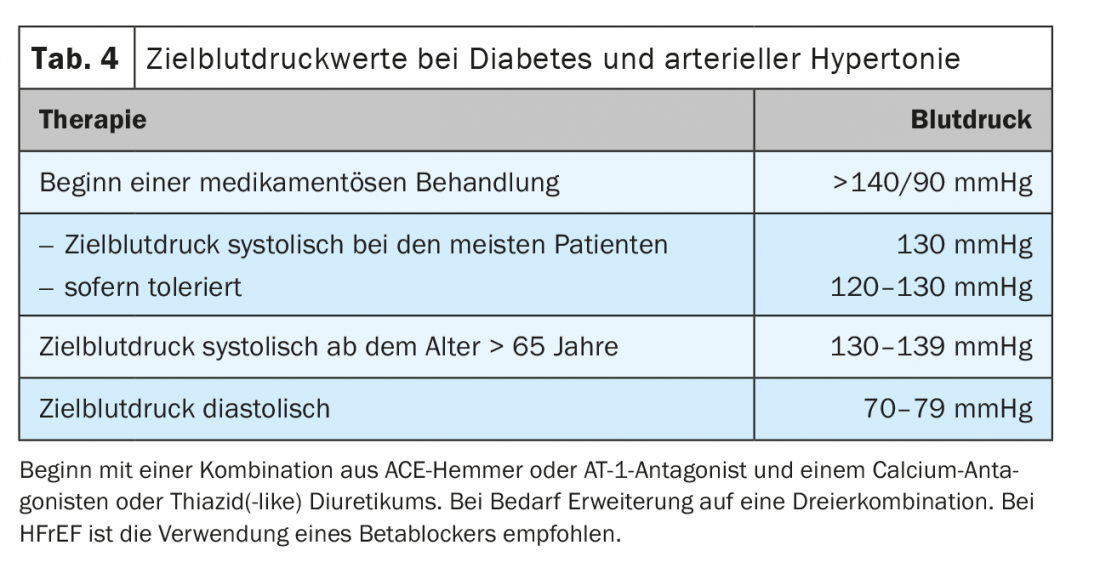
Se contemporaneamente esiste un’insufficienza cardiaca con ridotta funzione di pompa (HFrEF), si raccomanda anche l’uso di un beta-bloccante nei diabetici per ridurre la mortalità [6]. La combinazione di sacubitril e valsartan (Entresto®) è stata anche in grado di ridurre significativamente l’endpoint primario di mortalità o di prima ospedalizzazione per peggioramento dell’insufficienza cardiaca nel sottogruppo dei diabetici, anche se in misura leggermente inferiore rispetto ai non diabetici. Nei pazienti con HFrEF, occorre prestare attenzione a massimizzare il dosaggio possibile e tollerabile dei farmaci per l’insufficienza cardiaca e a non limitarsi agli obiettivi di pressione sanguigna sopra menzionati.
Terapia ipocolesterolemizzante
I dati degli studi degli ultimi cinque anni mostrano in modo impressionante che con un’ulteriore riduzione del colesterolo LDL, è possibile abbassare il rischio cardiovascolare rimanente. Questo ha senso soprattutto se il rischio del paziente è corrispondentemente aumentato rispetto alla popolazione generale. La maggior parte dei pazienti con diabete è considerata di per sé ad alto rischio per quanto riguarda la terapia ipocolesterolemizzante, per i quali si dovrebbe puntare a un intervallo target di <1,8 mmol/l, secondo le attuali linee guida. Solo in un piccolo gruppo di diabetici con un rischio moderato è adeguato un intervallo target di LDL <2,6 mmol/l (Fig. 1) . In questa situazione, non è necessario calcolare il rischio individuale con il calcolatore AGLA, altrimenti così prezioso, [32].

Se il diabete è associato a una malattia arteriosclerotica manifesta, il rischio aumenta a “molto alto” e si deve puntare a un intervallo target di LDL <1,4 mmol/l. Se si verifica un secondo evento vascolare entro 2 anni di terapia con statine tollerate al massimo, il rischio del paziente sembra essere estremamente aumentato. Si raccomanda un’ulteriore riduzione delle LDL in un intervallo <1,0 mmol/l. Un secondo evento aterosclerotico non include una stenosi in-stent che deve essere trattata.
Il primo passo della terapia è la somministrazione di una statina altamente potente (rosuva o atorvastatina). Per raggiungere i valori target, spesso è necessario un dosaggio elevato. Tuttavia, la nostra raccomandazione è di iniziare con una dose bassa (ad esempio 10 o 20 mg), in quanto presenta un tasso inferiore di effetti collaterali e raggiunge comunque la maggior parte della riduzione dell’LDL. In una seconda fase, deve avvenire il dosaggio. In questo modo si evita che un paziente venga erroneamente classificato come intollerante alle statine a causa dell’intolleranza a dosi più elevate, il che complica l’ulteriore corso della terapia.
Se tuttavia dovessero verificarsi effetti collaterali con atorva e rosuvastatina, l’uso di fluva o pravastatina, che sono meno potenti ma spesso meglio tollerati, può essere utile in questo gruppo a rischio.
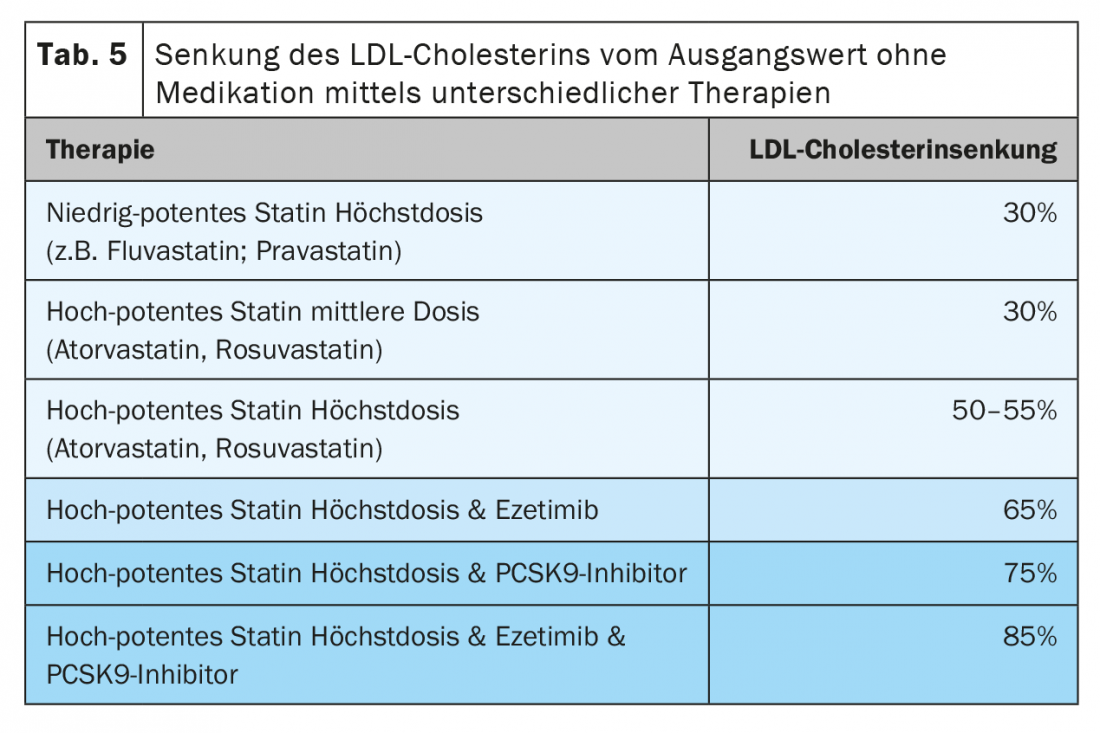
Un’ulteriore riduzione dell’LDL si ottiene combinandola con l’ezetimibe, che ora è disponibile anche in combinazioni fisse con entrambe le statine altamente potenti. Si possono ottenere riduzioni di circa il 65% rispetto alla linea di base iniziale. Se questa combinazione viene dosata, circa l’80% dei pazienti può essere portato nel range target. Come fase finale di escalation, sono poi disponibili gli inibitori di PCSK-9, che ottengono un’ulteriore riduzione del 50-60% del livello di LDL già raggiunto con la combinazione (Tab. 5) [32].
Conclusione
In sintesi, si può affermare che la cura dei pazienti con diabete, soprattutto quando si è manifestata la malattia arteriosclerotica, rappresenta una sfida nella pratica clinica quotidiana, in quanto occorre tenere presenti diverse sfaccettature terapeutiche e, se necessario, coordinare e concordare l’interazione di diverse discipline per garantire la migliore assistenza possibile a questi pazienti ad alto rischio. Con questo articolo abbiamo cercato di coprire i vari argomenti, che per loro natura possono essere affrontati solo in modo sommario.
Messaggi da portare a casa
- La prevenzione primaria con acido acetilsalicilico deve essere presa in considerazione solo nei pazienti con diabete e rischio elevato o addirittura molto elevato di eventi cardiovascolari. D’altra parte, il trattamento secondario con acido acetilsalicilico è obbligatorio.
- Le nuove forme di terapia per l’iperglicemia includono: Inibitori DPP4, antagonisti del recettore GLP1 e inibitori SGLT2. Tutte e tre le classi di sostanze non hanno un potenziale ipoglicemizzante e sono neutre o riducono il peso.
- Gli inibitori della DPP4 sono particolarmente indicati per i pazienti anziani senza insufficienza cardiaca, grazie alla loro buona tollerabilità e alla loro applicabilità in caso di compromissione della funzione renale.
- Gli inibitori SGLT2 sono il trattamento di scelta per i diabetici con funzione renale compromessa e/o insufficienza cardiaca con funzione di pompa compromessa.
- I GLP1-RA hanno il più forte effetto di abbassamento della glicemia, contribuiscono alla perdita di peso e hanno una prognosi favorevole nei pazienti ad alto rischio cardiovascolare.
- Il trattamento antipertensivo è consigliato nel diabete a partire da una pressione arteriosa di >140/80 mmHg con un obiettivo di pressione arteriosa di <130/80 mmHg.
- I valori target per il colesterolo LDL nei pazienti con diabete dipendono dal profilo di rischio complessivo e sono definiti da <2,6 a <1,0 mmol/l.
Letteratura:
- Almdal T, et al: L’effetto indipendente del diabete mellito di tipo 2 sulla cardiopatia ischemica, l’ictus e la morte: uno studio basato sulla popolazione di 13.000 uomini e donne con 20 anni di follow-up. Arch Intern Med 2004; 164: 1422-1426.
- International Diabetes Federation: Atlante del diabete IDF 9ª edizione 2019. www.diabetesatlas.org
- Wong K, et al: Confronto dei fattori demografici e del controllo dei fattori di rischio cardiovascolare tra gli adulti statunitensi con diabete di tipo 2 in base alla classificazione del trattamento insulinico. J Diabetes Complications 2012; 26: 169-174.
- Baigent C, Blackwell L, Collins R, et al: Aspirina nella prevenzione primaria e secondaria delle malattie vascolari: meta-analisi collaborativa dei dati dei singoli partecipanti agli studi randomizzati. Lancet 2009;373: 1849-1860.
- ASCEND Study Collaborative Group, Bowman L, Mafham M, Wallendszus K, et al: Effetti dell’aspirina per la prevenzione primaria nelle persone con diabete mellito. N Engl J Med 2018;379: 1529-1539
- Cosentino F, Grant PJ, Aboyans V, et al: Linee guida ESC su diabete, pre-diabete e malattie cardiovascolari sviluppate in collaborazione con l’EASD 2019 European Heart Journal (2020) 41: 255-323.
- Investigatori PLATO, Wallentin L, Becker RC, Budaj A, et al: Ticagrelor rispetto a clopidogrel nei pazienti con sindromi coronariche acute. N Engl J Med 2009;361: 1045-1057.
- Ricercatori TRITON-TIMI 38, Wiviott SD, Braunwald E, McCabe CH, et al: Prasugrel rispetto a clopidogrel nei pazienti con sindromi coronariche acute. N Engl J Med 2007; 357: 2001-2015.
- Comitato direttivo e sperimentatori di PEGASUS-TIMI 54, Bonaca MP, Bhatt DL, Cohen M, et al: Uso a lungo termine di ticagrelor in pazienti con infarto miocardico precedente. N Engl J Med 2015; 372: 1791-1800.
- Lehmann R, Gastaldi G, Czock A, et al.: Raccomandazioni svizzere della Società di Endocrinologia e Diabetologia (SGED/SSED) per il trattamento del diabete mellito di tipo 2 (2020).
- Buse JB, Wexler DJ, Tsapas A, et al: Aggiornamento 2019 a: Gestione dell’iperglicemia nel diabete di tipo 2, 2018. Un rapporto di consenso dell’American Diabetes Association (ADA) e dell’Associazione Europea per lo Studio del Diabete (EASD). Diabetologia. 2020 Feb;63(2): 221-228.
- Gruppo di studio VERIFY; Matthews DR, Paldánius PM, Proot P, et al.: Durabilità glicemica di una terapia combinata precoce con vildagliptin e metformina rispetto alla monoterapia sequenziale con metformina nel diabete di tipo 2 di nuova diagnosi (VERIFY): uno studio di 5 anni, multicentrico, randomizzato, in doppio cieco Lancet. 2019 Oct 26; 394(10208): 1519-1529.
- Craddy P, Palin HJ, Johnson KI: Efficacia comparativa degli inibitori della dipeptidil peptidasi-4 nel diabete di tipo 2: una revisione sistematica e un confronto di trattamenti misti. Diabetes Ther 5: 1-41, 2014.
- Davis TM: Inibitori della dipeptidil peptidasi-4: farmacocinetica, efficacia, tollerabilità e sicurezza nell’insufficienza renale. Diabetes Obes Metab 16: 891-899, 2014.
- Gli investigatori di CARMELINA; Perkovic V, Toto R, Cooper ME, et al: Effetti di Linagliptin sugli esiti cardiovascolari e renali in persone con funzione renale normale e ridotta: analisi secondaria dello studio randomizzato CARMELINA. Diabetes Care 2020 Aug; 43(8): 1803-1812.
- Green JB, Bethel MA, Armstrong PW, et al: Effetto di Sitagliptin sugli esiti cardiovascolari nel diabete di tipo 2. N Engl J Med. 2015 Jul 16;373(3): 232-242.
- Investigatori EXAMINE; White WB, Cannon CP, Heller SR, et al: Alogliptin dopo la sindrome coronarica acuta nei pazienti con diabete di tipo 2. N Engl J Med. 369: 1327-1335, 2013.
- Investigatori CARMELINA; Rosenstock J, Perkovic V, Johansen OE, et al: Effect of Linagliptin vs Placebo on Major Cardiovascular Events in Adults With Type 2 Diabetes and High Cardiovascular and Renal Risk: The CARMELINA Randomized Clinical Trial JAMA 321: 69-79, 2019.
- Comitato direttivo e sperimentatori SAVOR-TIMI 53; Scirica BM, Bhatt DL, Braunwald E, et al: Saxagliptin ed esiti cardiovascolari in pazienti con diabete mellito di tipo 2. N Engl J Med 369: 1317-1326, 2013.
- Avogaro A, Dardano A, de Kreutzenberg SV, Del Prato S: Gli inibitori della dipeptidil peptidasi-4 possono minimizzare il carico ipoglicemico e migliorare la sicurezza nelle persone anziane con diabete. Diabetes Obes Metab 17: 107-115, 2015.
- Scheen AJ: Inibitori del cotrasportatore di sodio-glucosio di tipo 2 per il trattamento del diabete mellito di tipo 2. Nat Rev Endocrinol 16: 556-577, 2020.
- Investigatori dello studio CREDENCE; Perkovic V, Jardine MJ, Neal B, et al: Canagliflozin ed esiti renali nel diabete di tipo 2 e nella nefropatia. N Engl J Med 380:2 295-2306, 2019.
- Zinman B, Wanner C, Lachin JM, et al: Empagliflozin, esiti cardiovascolari e mortalità nel diabete di tipo 2. N Engl J Med. 2015 Nov 26;373(22): 2117-2128.
- Investigatori DECLARE-TIMI 58; Wiviott SD, Raz I, Bonaca MP, et al: Dapagliflozin e gli esiti cardiovascolari nel diabete di tipo 2. N Engl J Med. 2019 Jan 24;380(4): 347-357.
- Gruppo di lavoro Diabete di Kidney Disease: Improving Global Outcomes (KDIGO). Linea guida di pratica clinica KDIGO 2020 per la gestione del diabete nella malattia renale cronica.Kidney Int. 2020 Oct; 98(4S): S1-S115.
- Comitati e sperimentatori dello studio DAPA-CKD; Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al: Dapagliflozin nei pazienti con malattia renale cronica. N Engl J Med. 2020 Oct 8;383(15): 1436-1446.
- Comitati e sperimentatori dello studio DAPA-HF; McMurray JJV, Solomon SD, Inzucchi SE, et al: Dapagliflozin nei pazienti con insufficienza cardiaca e frazione di eiezione ridotta. N Engl J Med. 2019 Nov 21;381(21): 1995-2008.
- Investigatori dello studio EMPEROR-Reduced; Packer M, Anker SD, Butler J, et al: Esiti cardiovascolari e renali con Empagliflozin nello scompenso cardiaco. N Engl J Med. 2020 Oct 8;383(15): 1413-1424.
- Davidson JA: Effetti differenziali degli agonisti del recettore GLP-1 prandiale e non prandiale nella terapia del diabete di tipo 2. Postgrad Med 127: 827-841, 2015.
- Marso SP, Daniels GH, Brown-Frandsen K, et al: Liraglutide e gli esiti cardiovascolari nel diabete di tipo 2. N Engl J Med. 2016 Jul 28;375(4): 311-322.
- Emdin CA, Rahimi K, Neal B, et al: Riduzione della pressione sanguigna nel diabete di tipo 2: una revisione sistematica e una meta-analisi. JAMA 2015;313: 603-615.
- Autori/Membri della task force; Comitato ESC per le linee guida pratiche (CPG); Società cardiache nazionali ESC. Linee guida ESC/EAS 2019 per la gestione delle dislipidemie: modifica dei lipidi per ridurre il rischio cardiovascolare. Aterosclerosi. 2019 Nov; 290: 140-205.
CARDIOVASC 2021; 20(1): 10-16