La prognosi del carcinoma gastrico avanzato è ancora estremamente sfavorevole. Sono quindi urgentemente necessari nuovi approcci terapeutici. I risultati attuali suggeriscono che la terapia con gli inibitori del checkpoint potrebbe diventare più importante nel prossimo futuro.
Finora, la terapia con inibitori del checkpoint per il cancro gastrico è stata approvata in Svizzera solo per i casi molto avanzati. Per esempio, l’approvazione di nivolumab è limitata alla terapia di terza linea e quella di pembrolizumab al trattamento di tumori metastatici con elevata instabilità microsatellitare (MSI-H) o riparazione difettosa del DNA mismatch (dMMR) senza opzioni terapeutiche alternative [2]. I risultati di vari studi danno ora motivo di sperare che queste indicazioni vengano presto ampliate.
Lo stato delle cose
Fino ad oggi, il cancro gastrico in stadio IV è stato il dominio della chemioterapia (Fig. 1) . Sebbene la chemioterapia possa migliorare il tempo di sopravvivenza rispetto al trattamento puramente di supporto, migliora la sopravvivenza solo di circa 6,7 mesi [3]. Un mese in più può essere guadagnato utilizzando combinazioni di chemioterapia, ma queste comportano anche un aumento delle tossicità [3]. Le chemioterapie doppie basate sul platino e una fluoropirimidina sono lo standard raccomandato, mentre il beneficio delle combinazioni triple è valutato in modo controverso [4].
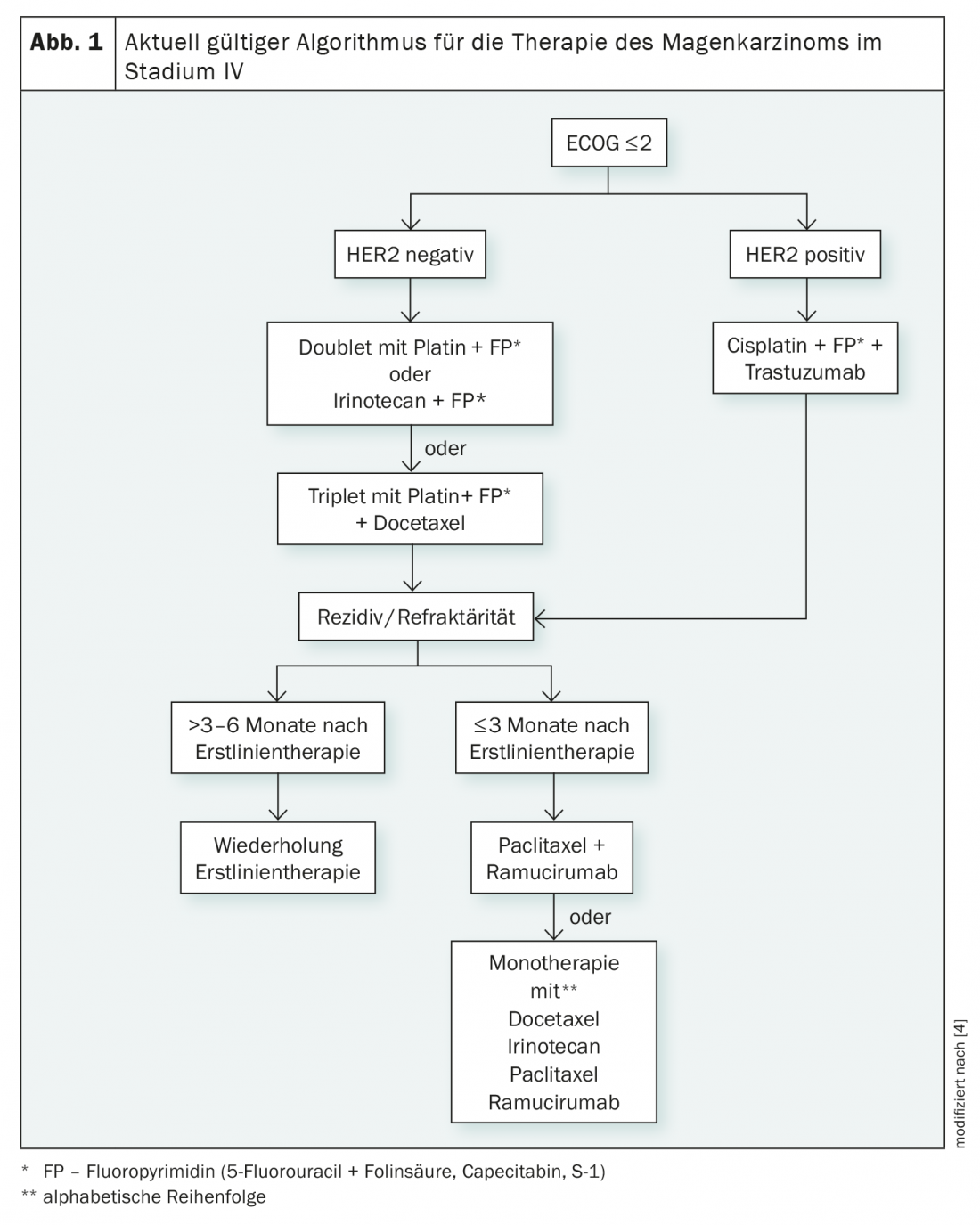
Mentre le terapie mirate sono disponibili per i tumori HER2-positivi, questa opzione non esiste attualmente per i casi HER2-negativi. L’aggiunta di trastuzumab alla chemioterapia porta ad un aumento del tasso di risposta e della sopravvivenza libera da progressione e complessiva nei tumori HER2-positivi, che rappresentano il 10-15% dei tumori gastrici. L’effetto è rilevabile, con un aumento della sopravvivenza mediana di poco più di due mesi, ma è piccolo [5]. Quindi siamo lontani da una cura, indipendentemente dallo stato di HER2.
Se la chemioterapia di prima linea con o senza trastuzumab fallisce, si può utilizzare l’anticorpo ramucirumab diretto contro il VEGFR-2 (recettore del fattore di crescita endoteliale vascolare 2). Questo provoca un prolungamento della sopravvivenza di circa 1,5 mesi rispetto al placebo [6]. In alternativa, la chemioterapia è possibile anche in seconda linea. I loro esiti sono paragonabili a quelli del trattamento con ramucirumab. I risultati migliori si ottengono con le combinazioni di paclitaxel e anticorpo anti-VEGFR-2 [4].
Per quanto riguarda tutte le altre linee di terapia, attualmente non esistono linee guida chiare. Le opzioni includono ramucirumab, chemioterapia, trifluridina/tipiracil (TAS-102) e vari inibitori del checkpoint. Oltre a migliorare le opzioni terapeutiche per il trattamento di prima e seconda linea del carcinoma gastrico in stadio IV, è quindi importante stabilire uno standard terapeutico per la terza linea nel corso dei prossimi anni.
Gli inibitori del checkpoint come opzione
Non solo per questo standard di cura in terza linea, gli inibitori del checkpoint potrebbero presto svolgere un ruolo di supporto, ma anche per integrare le opzioni nelle fasi precedenti del trattamento. Attualmente sono in corso diversi studi che stanno testando l’uso di nivolumab, pembrolizumab e altri in tutte le linee di terapia (Tab. 1). I risultati ottenuti finora indicano che il trattamento con gli inibitori del checkpoint non è almeno inferiore alla chemioterapia. Ad esempio, lo studio KEYNOTE-062 ha riportato un’efficacia comparabile del bloccante PD-1 pembrolizumab come monoterapia di prima linea, con una tollerabilità significativamente migliore [7]. Sembra importante considerare diversi sottogruppi nell’analisi dell’efficacia. Con un’alta espressione di PD-L1, c’è stata una chiara tendenza verso una sopravvivenza globale più lunga con il trattamento con pembrolizumab.
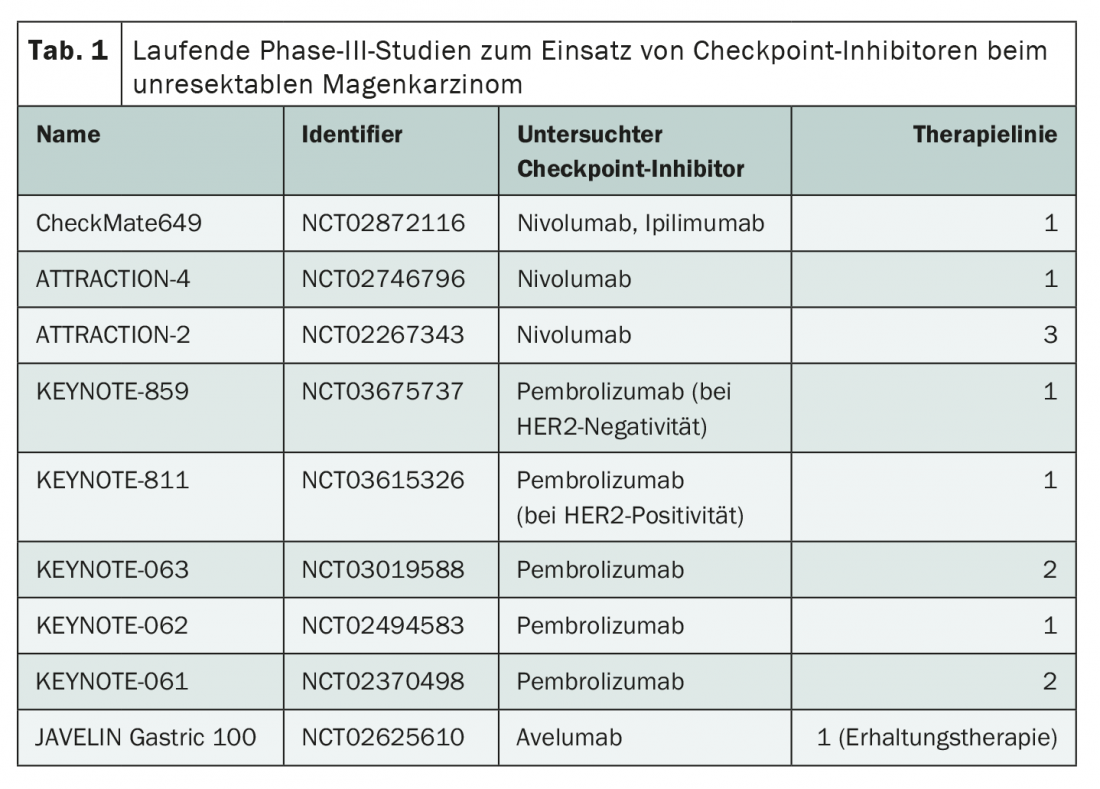
I risultati di numerosi altri studi sull’uso degli inibitori del checkpoint nella terapia di prima linea sono in attesa, ma in vari congressi del 2020 sono stati forniti spunti interessanti. Al Congresso della Società Europea di Oncologia Medica (ESMO), Markus Moehler ha presentato i primi promettenti dati dello studio CheckMate649, che comprende 1581 pazienti [8]. Rispetto alla sola chemioterapia, l’espressione di PD-L1 con l’aggiunta di nivolumab ha mostrato un miglioramento significativo della sopravvivenza globale e della sopravvivenza libera da progressione. Un effetto minore, ma significativo, era presente anche nel gruppo totale.
Inoltre, sono stati presentati i primi risultati dello studio ATTRACTION-4, che studia anche la somministrazione aggiuntiva di nivolumab in prima linea, ma in 724 pazienti esclusivamente asiatici [9]. Narikazu Boku ha riportato un aumento significativo della sopravvivenza libera da progressione e del tasso di risposta con l’aggiunta di nivolumab alla chemioterapia. Tuttavia, la sopravvivenza globale non è stata significativamente prolungata secondo questa prima analisi.
Mentre la somministrazione aggiuntiva di immunoterapici viene solitamente studiata per la terapia di prima linea, la terapia con il solo inibitore del checkpoint è in discussione anche nelle linee successive. Nello studio ATTRACTION-2, ad esempio, è stato già osservato un miglioramento significativo della prognosi con l’uso di nivolumab nella terapia di terza linea. La sopravvivenza mediana è aumentata da 4,14 a 5,26 mesi [10].
Uno sguardo al futuro
Anche se si devono ancora attendere dati a più lungo termine, l’uso di immunoterapici nel carcinoma gastrico avanzato è un’opzione valida. Nel frattempo, sono in corso numerosi studi di grandi dimensioni su questo approccio, alcuni dei quali hanno già prodotto dei risultati, alcuni dei quali sono speranzosi. La somministrazione di inibitori del checkpoint potrebbe presto diventare di routine nella terapia di prima linea del carcinoma gastrico non resecabile, soprattutto nei casi di espressione di PD-L1 e come aggiunta alla chemioterapia standard. Nelle linee di trattamento successive, è in discussione anche l’uso esclusivo di immunoterapici, che ha dimostrato di essere superiore alla somministrazione di placebo. Nel complesso, la tollerabilità sembra essere superiore a quella della chemioterapia.
L’identificazione di biomarcatori adatti faciliterebbe la selezione dei pazienti giusti per l’immunoterapia. Questo tema, che riguarda anche numerose malattie oltre al carcinoma gastrico, probabilmente ci accompagnerà ancora per molto tempo. I candidati promettenti sono attualmente l’espressione di PD-L1 nel tumore e nello stroma (punteggio di positività combinato), l’associazione con il virus di Epstein-Barr e l’instabilità microsatellitare [11,12]. Anche su questo sono in corso diversi studi.
Molte domande rimangono senza risposta, come l’applicazione esatta, la selezione ideale dei pazienti e l’efficacia stessa. Tuttavia, presto potrebbe essere impossibile immaginare un trattamento per il carcinoma gastrico senza immunoterapia, a condizione che l’approvazione venga estesa. Sulla base dei dati disponibili finora, non ci si può aspettare una grande svolta, ma piccoli passi nella giusta direzione sono a portata di mano.
Letteratura:
- Smyth EC, et al: Cancro gastrico: Linee guida di pratica clinica ESMO per la diagnosi, il trattamento e il follow-up. Annali di Oncologia. 2016; 27: v38-v49.
- Informazioni sui farmaci di swissmedic. www.swissmedicinfo.ch (ultimo accesso 17.01.2021)
- Wagner AD, et al: Chemioterapia per il cancro gastrico avanzato. Cochrane Database Syst Rev. 2017; 8: CD004064.
- Lordick F, et al.: Onkopedia – Carcinoma gastrico. www.onkopedia.com/de/onkopedia/guidelines/magenkarzinom (ultimo accesso 17.01.2021)
- Bang YJ, et al: Trastuzumab in combinazione con la chemioterapia rispetto alla sola chemioterapia per il trattamento del carcinoma gastrico o della giunzione gastro-esofagea (ToGA) in stadio avanzato HER2-positivo: uno studio controllato randomizzato di fase 3, in aperto. Lancet. 2010; 376(9742): 687-697.
- Fuchs CS, et al: Monoterapia con Ramucirumab per l’adenocarcinoma gastrico o della giunzione gastro-esofagea avanzato precedentemente trattato (REGARD): uno studio internazionale, randomizzato, multicentrico, controllato con placebo, di fase 3. Lancet. 2014; 383(9911): 31-39.
- Shitara K, et al: Efficacia e sicurezza di Pembrolizumab o Pembrolizumab più chemioterapia rispetto alla sola chemioterapia per i pazienti con cancro gastrico avanzato di prima linea: lo studio clinico randomizzato di fase 3 KEYNOTE-062. JAMA Oncol. 2020; 6(10): 1571-80.
- Moehler M, et al.: Nivolumab (nivo) più chemioterapia (chemio) rispetto alla chemio come trattamento di prima linea (1L) per il cancro gastrico avanzato/cancro della giunzione gastroesofagea (GC/GEJC)/adenocarcinoma esofageo (EAC): Primi risultati dello studio CheckMate 649. Annali di Oncologia. 2020; 31: S1142-1215.
- Boku N, et al: Nivolumab più chemioterapia rispetto alla sola chemioterapia nei pazienti con cancro gastrico/giunzione gastroesofagea (G/GEJ) avanzato o ricorrente, precedentemente non trattato: studio ATTRACTION-4 (ONO-4538-37). Annali di Oncologia. 2020; 31: S1142-1215.
- Chen L-T, et al: Uno studio di fase 3 di nivolumab nel carcinoma gastrico o della giunzione gastroesofagea avanzato precedentemente trattato (ATTRACTION-2): dati aggiornati a 2 anni. Cancro gastrico: rivista ufficiale dell’Associazione Internazionale del Cancro Gastrico e dell’Associazione Giapponese del Cancro Gastrico. 2020; 23(3): 510-519.
- Shitara K, et al: Pembrolizumab rispetto a paclitaxel per il carcinoma gastrico o della giunzione gastro-esofagea in stadio avanzato, precedentemente trattato (KEYNOTE-061): uno studio randomizzato, in aperto, controllato, di fase 3. Lancet. 2018; 392(10142): 123-133.
- Kim ST, et al: Caratterizzazione molecolare completa delle risposte cliniche all’inibizione di PD-1 nel carcinoma gastrico metastatico. Nat Med. 2018; 24(9): 1449-1458.
- ClinicalTrials.gov. www.clinicaltrials.gov (ultimo accesso 17.01.2021)
InFo ONCOLOGIA & EMATOLOGIA 2021; 9(1): 18-19