Il fatto che gli inibitori dell’IL17 siano caratterizzati da una rapida insorgenza dell’azione è stato più volte dimostrato empiricamente e si riflette anche in un attuale studio testa a testa. Guardando al futuro, ci sono sviluppi interessanti nella pipeline, tra cui il nuovo anticorpo Bimekizumab, che ha come bersaglio le subunità IL-17A e IL-17F e che ha mostrato risultati promettenti in studi recenti.
I primi biologici approvati per il trattamento della psoriasi sono stati gli inibitori del TNF-alfa adalimumab, etanercept e infliximab. Sebbene questo abbia già significato un notevole miglioramento delle opzioni terapeutiche, la maggior parte dei pazienti non ha raggiunto la completa liberazione dai sintomi. Nel frattempo, però, ci sono stati enormi progressi in questo senso.
anti-IL17: rapida insorgenza d’azione come marchio di fabbrica
L’inibitore dell’IL12/23 ustekinumab è stato seguito dai due inibitori dell’IL17A secukinumab e ixekinumab, nonché dall’antagonista del recettore dell’IL17 brodalumab (attualmente non approvato in Svizzera) [1]. Il blocco dell’IL17 si è rivelato molto efficace e ha permesso di ottimizzare i tassi di risposta. L’ultima generazione di biologici altamente efficaci comprende anche gli inibitori dell’IL23, guselkumab, tildrakizumab e risankizumab. Ci sono alcune differenze tra le classi di sostanze. “La terapia anti-IL17 funziona rapidamente, molto rapidamente”, sottolinea il Prof. Dr. med. Diamant Thaci, Istituto e Centro di Eccellenza dell’Università di Lubecca [2]. Questo era già evidente nello studio CLEAR pubblicato nel 2015, in cui l’inibitore dell’IL17A secukinumab ha mostrato una risposta PASI75 precoce, alla settimana 4 dal basale [3]. Dopo 16 settimane di terapia, il secukinumab si è dimostrato superiore all’inibitore dell’IL12/23 ustekinumab in termini di risposta PASI90 (79% vs 57,6%; p<0,0001) e ha ottenuto un miglioramento maggiore e più duraturo della condizione cutanea alla settimana 52.
La scoperta di una rapida insorgenza dell’azione è stata replicata più volte e i dati di uno studio testa a testa pubblicato nel 2020 lo confermano ancora una volta. Lo studio IXORA è uno studio randomizzato, in doppio cieco, che ha incluso pazienti con psoriasi a placche da moderata a grave (PASI ≥12, sPGA ≥3 e ≥10% di superficie corporea interessata) [4]. L’endpoint primario era PASI100 a 12 settimane e gli endpoint secondari includevano altri punteggi PASI e sPGA. Dei 1027 pazienti inclusi nello studio, 520 hanno ricevuto ixekizumab e 507 guselkumab. Il 41% dei pazienti con ixekizumab ha raggiunto PASI100 dopo 12 settimane, rispetto a solo il 25% con guselkumab. Nel complesso, ixekizumab si è dimostrato superiore a guselkumab. L’insorgenza dell’azione è stata più rapida e un maggior numero di pazienti ha ottenuto una pelle senza aspetto, mentre i profili di sicurezza erano comparabili. Questi risultati sottolineano la risposta rapida, ma non fanno alcuna dichiarazione sull’effetto a lungo termine, che è oggetto di altri studi.

Posto del secukinumab nel trattamento della PsA
Nelle attuali raccomandazioni terapeutiche dell’EULAR, gli inibitori del TNF-alfa e gli inibitori dell’IL17 sono indicati come biologici equivalenti di prima linea dopo il fallimento dei DMARDS convenzionali [5]. Questa valutazione si basa sui risultati dello studio comparativo EXCEED sulla terapia di prima linea per l’artrite psoriasica. Lo studio multicentrico in doppio cieco di fase IIIb ha incluso 853 pazienti adulti con artrite psoriasica attiva. 426 pazienti hanno ricevuto 300 mg di secukinumab per via sottocutanea al basale, alle settimane 1, 2, 3, 4 e poi ogni 4 settimane fino alla settimana 48. Adalimumab è stato somministrato per via sottocutanea ogni 2 settimane a 427 pazienti. Con il secukinumab, il 67% e con l’adalimumab il 62% dei partecipanti allo studio ha raggiunto l’ACR20 dopo 52 settimane [6]. Il profilo di sicurezza di secukinumab e adalimumab è stato ampiamente in linea con i segnali di sicurezza precedentemente noti. Le caratteristiche individuali del paziente (ad esempio le comorbidità) sono suggerite come criteri decisionali per l’utilizzo di secukinumab o adalimumab dopo il fallimento di un csDMARDS.
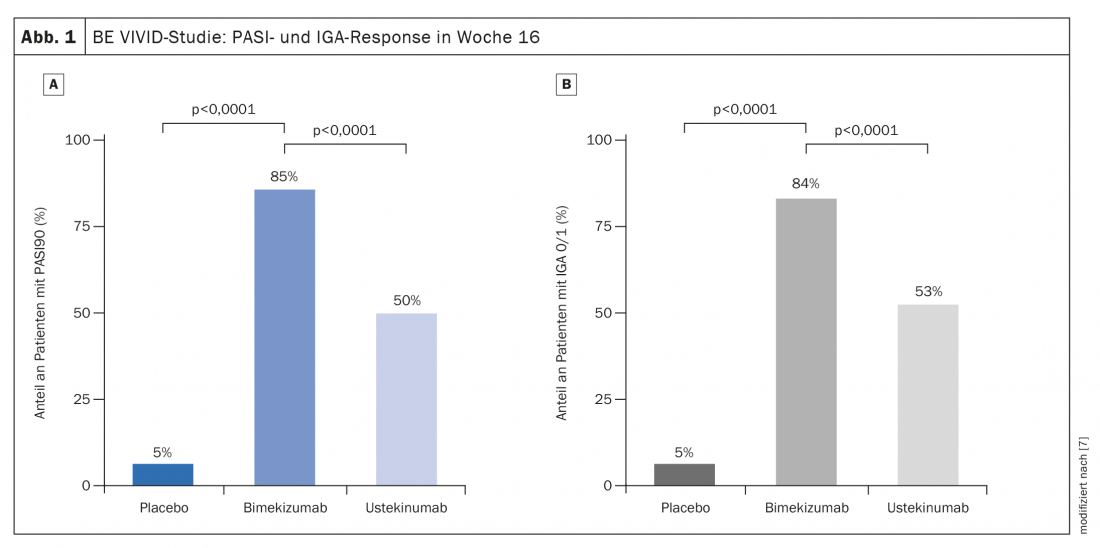
Prospettive: risultati promettenti del blocco di IL-17A/F
In uno studio comparativo pubblicato nel 2021, l’inibitore anti-IL17A/F bimekizumab ha dimostrato di avere un’insorgenza d’azione molto rapida e una scarsa perdita di effetto nel corso dello studio. Bimekizumab ha raggiunto questo obiettivo per quanto riguarda PASI75 entro 4 settimane, che è stato raggiunto da ustekinumab solo dopo 4 mesi, ha riassunto il Prof. Thaci. Lo studio multicentrico comparativo BE VIVID, randomizzato, in doppio cieco, attivo e controllato con placebo, ha incluso 567 adulti [7]. 321 partecipanti allo studio hanno ricevuto bimekizumab 320 mg ogni 4 settimane e 163 soggetti sono stati trattati con ustekinumab 45 mg o 90 mg (in base al peso) ogni 12 settimane; 83 pazienti hanno ricevuto placebo ogni 4 settimane. Alla settimana 16 dal basale, l’85% dei pazienti nel braccio bimekizumab ha raggiunto PASI90, rispetto al 50% nel braccio ustekinumab (differenza di rischio 35 [95%-KI 27–43]; p<0,0001) (Fig. 1A). Nel gruppo placebo, questa percentuale era del 5% (differenza di rischio 80 [95%-KI 74–86]; p<0,0001). Circa l’84% dei pazienti con bimekizumab aveva un punteggio IGA di 0 o 1, rispetto al 53% con ustekinumab (differenza di rischio 30 [95%-KI 22–39]; p<0,0001) e al 5% con placebo (differenza di rischio 79 [95%-KI 73-85] p<0,0001) (Fig. 1B). Anche il bimekizumab ha ottenuto una risposta più rapida. Alla settimana 4, dopo una singola dose, è stato osservato un punteggio PASI75 nel 77% dei pazienti del gruppo bimekizumab, rispetto a solo il 15% di ustekinumab (OR 18,2; 95% CI 11-30,1, p<0,0001). È stato anche notevole che i valori PASI90 non solo erano significativamente migliori dopo 4 mesi, ma che non c’è stata quasi nessuna perdita di efficacia con bimekizumab nel prosieguo dello studio. Questo indica un potenziale promettente per la terapia anti-IL17 a lungo termine, ha detto il relatore.
Congresso: Conferenza DDG 2021
Letteratura:
- Sawyer LM, et al: Valutazione dell’efficacia relativa dei trattamenti mirati con interleuchina-17 e interleuchina-23 per la psoriasi a placche da moderata a grave: revisione sistematica e meta-analisi di rete della risposta PASI. PLoS One 2019; 14(8): 1-31.
- Thaci D: I biologici attraverso i secoli – approcci terapeutici ieri, oggi e domani. Prof. Dr. med. Diamant Thaci, S09: Traccia Infiammazioni: Dermatite atopica e psoriasi come malattie sistemiche, Conferenza DDG 2021, 17.04.2021.
- Thaci D, et al: Il secukinumab è superiore all’ustekinumab nella schiaritura della pelle dei soggetti con psoriasi a placche da moderata a grave: CLEAR, uno studio randomizzato controllato. JAAD 2015; 73(3): 400-409.
- Blauvelt A, et al: Gruppo di studio IXORA-R. Confronto testa a testa tra ixekizumab e guselkumab nei pazienti con psoriasi a placche da moderata a grave: efficacia, sicurezza e velocità di risposta a 12 settimane da uno studio randomizzato, in doppio cieco. Br J Dermatol 2020; 182(6): 1348-1358.
- Gossec L, et al: Raccomandazioni EULAR per la gestione dell’artrite psoriasica con terapie farmacologiche: aggiornamento 2019. Ann Rheum Dis 2020; 79(6): 700-712.
- McInnes IB, et al: Secukinumab versus adalimumab per il trattamento dell’artrite psoriasica attiva (EXCEED): uno studio di fase 3b, in doppio cieco, a gruppi paralleli, randomizzato, con controllo attivo. The Lancet 2020; 395(10235): 1496-1505.
- Reich K, et al: Bimekizumab versus ustekinumab per il trattamento della psoriasi a placche da moderata a grave (BE VIVID): efficacia e sicurezza di uno studio di fase 3 di 52 settimane, multicentrico, in doppio cieco, con comparatore attivo e controllato con placebo. Lancet 2021; 397(10273): 487-498.
- NCT03440736, https://clinicaltrials.gov/ct2/show/NCT03440736
DERMATOLOGIE PRAXIS 2021; 31(3): 20-22 (pubblicato il 1.6.21, prima della stampa).