Il diabete è la causa più comune di malattia renale cronica (CKD).
L’organizzazione internazionale Kidney Disease: Improving Global Outcomes (KDIGO) ha recentemente pubblicato nuove linee guida sulla gestione del diabete di tipo 2 nelle persone con CKD. Viene diffuso un approccio terapeutico che si basa su diversi pilastri. Uno dei messaggi chiave: la progressione della malattia renale può essere rallentata con nuovi farmaci, in modo che molte persone possano essere risparmiate dalla dialisi per lungo tempo.
Mentre in passato erano disponibili solo poche opzioni terapeutiche in grado di arrestare la progressione della CKD associata al diabete, attualmente esistono diverse classi moderne di farmaci che possono rallentare in modo significativo la perdita della funzione renale, se vengono utilizzati in tempo. È quindi importante che le persone colpite ricevano un’assistenza tempestiva da parte di un nefrologo [1]. “I criteri per presentare la persona con diabete mellito al nefrologo sono, ad esempio: calo nuovo o significativo dell’eGFR, eGFR ≤60 ml/min/1,73 m², eritrocituria o albuminuria di grado 2 o 3”, ha spiegato la Prof.ssa Dr med. Julia Weinmann-Menke, Mainz, addetta stampa della Società tedesca di nefrologia [1,3].
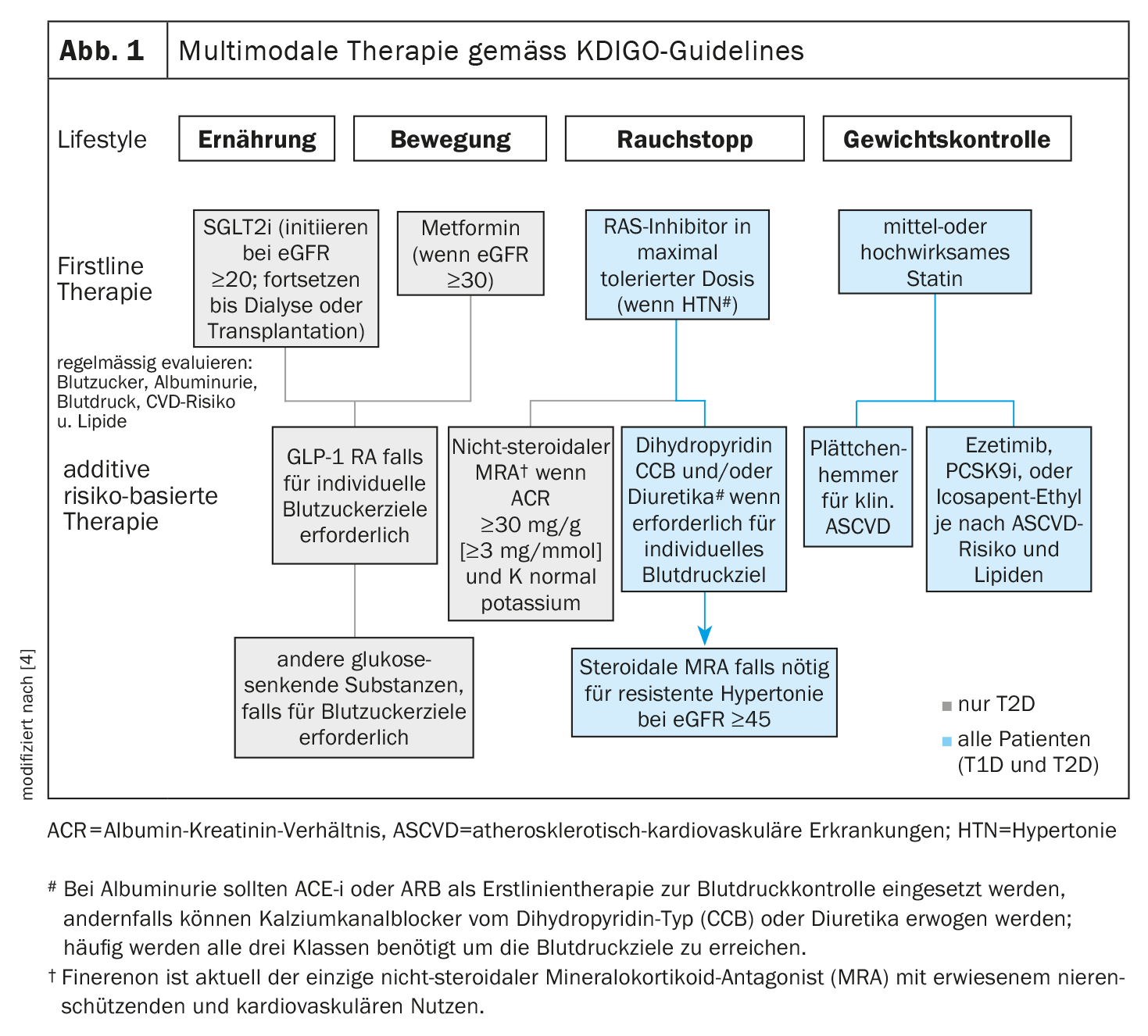
Il fatto che le linee guida KDIGO emesse nel 2020 siano già disponibili in una versione rivista nel 2022 riflette il rapido progresso nel campo del trattamento della nefropatia associata al diabete [4]. La KDIGO propone un approccio terapeutico multimodale (Fig. 1).
- Tutti i pazienti devono prestare attenzione ai fattori dello stile di vita: esercizio fisico, dieta e cessazione del fumo. Le terapie farmacologiche di prima linea devono essere selezionate in base alle caratteristiche cliniche individuali.
- Il controllo della glicemia nel diabete di tipo 2 (T2D) si basa su una combinazione di metformina e di inibitori del cotrasportatore sodio-glucosio 2 (SGLT-2-i). Per i pazienti in cui SGLT-2-i e metformina non sono efficaci nel raggiungere gli obiettivi di glucosio nel sangue, gli agonisti del recettore del peptide-1 simile al glucagone (GLP-1 RA) sono i farmaci preferiti per abbassare il glucosio.
- Nei pazienti con albuminuria e ipertensione (HTN), si consiglia l’inibizione del sistema renina-angiotensina (RAS). Una statina è consigliata a tutti i pazienti con T1D o T2D e CKD.
- Un antagonista non steroideo del recettore mineralcorticoide (ns-MRA) può essere aggiunto alla terapia di prima linea nei pazienti con T2D e un elevato rischio residuo di progressione della CKD e di eventi cardiovascolari**.
- L’aspirina è generalmente utilizzata per la prevenzione secondaria a vita nei pazienti con malattia cardiovascolare conclamata, a meno che non esistano controindicazioni, e può essere presa in considerazione per la prevenzione primaria nei pazienti ad alto rischio di malattia cardiovascolare aterosclerotica (ASCVD).
** Indicatore di alto rischio residuo di progressione della CKD e di eventi cardiovascolari: albuminuria persistente (>30 mg/g [>3 mg/mmol])

SGLT-2-i: la soglia dell’eGFR è stata abbassata
I pazienti con T2D, CKD e un eGFR ≥20 ml/min per 1,73 m² sono stati ampiamente studiati negli RCT su SGLT-2-i. Sulla base di questi studi, si ribadisce la forte raccomandazione di trattare i pazienti con T2D e CKD con un SGLT-2-i, indipendentemente dall’albuminuria. Un cambiamento importante è la soglia di eGFR più bassa a cui iniziare il trattamento con SGLT-2-i. La linea guida 2022 raccomanda l’introduzione di un SGLT-2-i per i pazienti con T2D e CKD che hanno un eGFR ≥20 ml/min per 1,73 m², rispetto a ≥30 ml/min per 1,73 m² della linea guida 2020 [4].

Gli studi Dapagliflozin e prevenzione degli esiti avversi nella malattia renale cronica (DAPA-CKD) e Effetto di Sotagliflozin sugli eventi cardiovascolari e renali nei pazienti con diabete di tipo 2 e compromissione renale moderata, che sono a rischio cardiovascolare. (SCORED) ha arruolato pazienti con CKD con un eGFR fino a 25 ml/min per 1,73 m². [5,6].
Lo studio sulla protezione del cuore e dei reni con Empagliflozin (EMPA-KIDNEY), condotto esclusivamente con popolazioni affette da CKD e interrotto precocemente a causa dei benefici, includeva anche partecipanti con un eGFR ≥20 ml/min per 1,73 m² [7]. Le analisi di sottogruppo di singoli studi e le meta-analisi hanno dimostrato benefici renali e cardiovascolari in tutte le categorie di eGFR, compresi i partecipanti con eGFR <30 ml/min per 1,73 m² e quelli senza albuminuria [8,9].

Agonisti del recettore GLP-1: nuove intuizioni
Nel 2021, sono stati pubblicati i risultati di un nuovo grande studio endpoint su efpeglenatide, che sono stati incorporati nelle nuove linee guida KDIGO. Lo studio AMPLITUDE-O (Effect of Efpeglenatide on Cardiovascular Outcomes) ha sostenuto l’evidenza dei benefici cardiovascolari del GLP-1 RA e ha rafforzato l’ipotesi che il GLP-1 RA possa migliorare anche gli esiti renali [2]. Di conseguenza, il GLP-1 RA rimane la terapia di seconda linea raccomandata per abbassare i livelli di glucosio nel sangue nella T2D e nella CKD. Il comprovato beneficio cardiovascolare di GLP-1 RA è stato dimostrato per tutte le categorie di eGFR ed è servito come motivazione principale per raccomandare GLP-1 RA come farmaco di scelta per abbassare la glicemia nei pazienti con T2D e CKD che non hanno raggiunto i loro obiettivi di glicemia nonostante l’uso di SGLT-2-i e metformina (o nei quali non è stato possibile utilizzare SGLT-2-i e/o metformina).
Finerenone – antagonista non steroideo dei mineralocorticoidi come ultimo giocatore
Efficace nel prevenire la progressione della malattia renale diabetica è anche il nuovo antagonista selettivo dei recettori mineralocorticoidi, non steroideo, finerenone [1]. Questo è stato dimostrato dai due grandi studi clinici FIDELIO-DKD (Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease) [10] e FIGARO-DKD (Finerenone in Reducing Cardiovascular Mortality and Morbidity in Diabetic Kidney Disease) [11] nonché dall’analisi combinata FIDELITY [12] basata su di essi. I risultati più importanti in un colpo d’occhio:
Nello studio FIDELIO-DKD, il finerenone ha ridotto significativamente l’incidenza di entrambi gli esiti renali compositi primari (insufficienza renale, declino sostenuto dell’eGFR di ≥40% o morte per malattia renale; hazard ratio [HR]0,82; 95% CI: 0,73-0,93) e l’esito cardiovascolare composito secondario (morte per cause cardiovascolari, infarto miocardico non fatale, ictus non fatale o ricovero per insufficienza cardiaca; HR: 0,86; 95% CI: 0,75-0,99). [10].
In FIGARO-DKD, il finerenone ha ridotto significativamente l’endpoint cardiovascolare combinato (HR: 0,87; 95% CI: 0,76-0,98) [11].
Nello studio FIDELITY, gli esiti cardiovascolari complessivi sono stati ridotti nei pazienti trattati con finerenone (HR: 0,86; 95% CI: 0,78-0,95), senza alcuna eterogeneità significativa nelle caratteristiche dei pazienti al basale [12].
I pazienti trattati con finerenone avevano anche meno probabilità di andare incontro a insufficienza renale, a una diminuzione dell’eGFR superiore al 57% o a morte renale (HR: 0,77; 95% CI: 0,67-0,88), e meno probabilità di andare incontro a insufficienza renale definita come inizio di dialisi cronica o trapianto renale (HR: 0,80; 95% CI: 0,64-0,99).
Letteratura:
- “Giornata mondiale del diabete: la dialisi non è un destino inevitabile per le persone con diabete mellito!”, Società tedesca di nefrologia, 11.11.2022
- Gerstein HC, et al: N Engl J Med 2021; 385: 896-907.
- Position paper Cooperazione Diabetologia/Nefrologia. Società Tedesca di Diabetologia/Società Tedesca di Nefrologia/Associazione dei Nefrologi Ospedalieri Senior 2018. www.ddg.info,(ultimo accesso 10.01.2023)
- Rossing P, et al: Sintesi della Linea Guida di Pratica Clinica KDIGO 2022 per la Gestione del Diabete nella Malattia Renale Cronica: un aggiornamento basato su nuove evidenze rapidamente emergenti. Kidney Int 2022; 102(5): 990-999.
- Bhatt DL, et al: N Engl J Med 2021; 384: 117-128.
- Heerspink HJL, et al: N Engl J Med 2020; 383: 1436-1446.
- Gruppo collaborativo EMPA-Kidney: Nephrol Dial Transplant 2022; 37; 1317-1329.
- Bakris G, et al: Clin J Am Soc Nephrol 2020; 15: 1705-1714.
- Chertow GM, et al: J Am Soc Nephrol 2021; 32: 2352-2361.
- Bakris GL, et al: N Engl J Med 2020; 383: 2219-2229.
- Pitt B, et al: N Engl J Med 2021; 385: 2252-2263.
- Rossing P, et al.: Ricercatori FIDELIO-DKD e FIGARO-DKD: Diabetes Care. Pubblicato online, 15 agosto (2022), 10.2337/dc22-0294
- Seidu S, et al: Aggiornamento 2022 alla dichiarazione di posizione di Primary Care Diabetes Europe: un approccio allo stato di malattia per la gestione farmacologica del diabete di tipo 2 nell’assistenza primaria. Prim Care Diabetes 2022; 16(2): 223-244.
- “Prurito associato alla malattia renale cronica: dall’epidemiologia al trattamento”, 25 novembre 2021, www.emjreviews.com,(ultimo accesso 14 dicembre 2022).
- Sukul N, et al: Kidney Med 2020; 3(1): 42-53.e1
- Yan B, et al: J Am Heart Assoc 2021; 10(7): e016201.
- “CHMP Meeting Highlights February 2022”, 17/03/2022, www.basg.gv.at, (ultimo accesso 14/12/2022).
- Fishbane S; KALM-1 Trial Investigators: N Engl J Med 2020; 382(3): 222-232.
- American Society of Nephrology: Abstract FR-OR24, www.asn-online.org (ultimo accesso 14 dicembre 2022).
PRATICA GP 2023; 18(1): 20-21











