Il punteggio focale (FS) nelle biopsie delle ghiandole salivari minori labiali è uno dei due criteri più importanti (con la positività anti-SSA) per la diagnosi della sindrome di Sjögren primaria (pSS). Per ridurre i tassi di errore nella diagnostica, gli algoritmi di apprendimento profondo che utilizzano le reti neurali artificiali potrebbero essere utilizzati per supportare i patologi in futuro.
Secondo i criteri ACR/EULAR per la pSS, la classificazione del focus score (FS) è uno dei tre criteri di classificazione, ma richiede una competenza che non è sempre disponibile nella pratica. Il 53% dei casi porta a una revisione della diagnosi quando viene valutata da esperti.
L’ apprendimento automatico coinvolge famiglie di algoritmi in grado di raccogliere una grande quantità di dati e di utilizzarli per prevedere qualcosa, ad esempio. L’apprendimento profondo è un sottoinsieme di questo campo che si concentra su una sola famiglia di algoritmi ed è chiamato “reti neurali profonde”, ha spiegato Louis Basseto, Scienta Lab, Dipartimento di Ricerca, Parigi, a titolo di introduzione [1].
L’apprendimento profondo viene già utilizzato nella patologia medica, ad esempio nel cancro al seno, dove già utilizza algoritmi per riconoscere le metastasi nei campioni di tessuto provenienti dai linfonodi in modo molto accurato e con prestazioni migliori rispetto ai patologi. “Il nostro gruppo ha anche dimostrato che l’apprendimento automatico può essere utilizzato nell’artrite reumatoide per prevedere la risposta al metotrexato e agli inibitori del TNF”. Ora i ricercatori si sono posti il compito di applicare il deep learning alla sindrome di Sjögren e di scoprire se può aiutare nella categorizzazione del punteggio di attenzione e nella diagnosi di pSS?
Apprendimento profondo basato sulle biopsie delle ghiandole salivari
A tal fine, hanno sviluppato due reti di apprendimento profondo utilizzando biopsie di ghiandole salivari labiali digitalizzate di pazienti per prevedere il punteggio focale (FS ≥1 o FS <1) e la diagnosi di sindrome di Sjögren primaria basata solo sull’istologia (pSS+ o pSS-). Lo studio ha incluso 325 pazienti (145 dell’Università di Parigi-Saclay, Ospedale Bicêtre, 71 della Queen Mary University di Londra e 109 dell’Università di Birmingham), utilizzando biopsie prelevate nella pratica clinica di routine. I partecipanti sono stati divisi in tre gruppi:
- pSS e FS <1 (32%, sintomi di sicca)
- pSS+ e FS ≥1 (47%)
- pSS+ e FS <1 (21%)
Tutte le FS sono state precedentemente confermate da patologi e le diagnosi di pSS da esperti.
Una o più immagini della biopsia vengono utilizzate per fare una previsione. Ciascuna immagine viene suddivisa in piastrelle e l’algoritmo assegna un punteggio di rischio a ciascuna di queste piastrelle in modo indipendente. Tutte queste informazioni vengono poi combinate per fare una previsione del punteggio di attenzione o della diagnosi, a seconda dell’algoritmo utilizzato.
“Utilizziamo due set di dati diversi”, ha spiegato Basseto: un set di formazione (70% dei pazienti) e un set di validazione (30% dei pazienti). I due insiemi contengono la stessa proporzione di classi positive e negative (pSS+/pSS- o FS ≥1/FS <1) und die verschiedenen Zentren, aus denen sich die Teilnehmer zusammensetzen, sind im Training und in der Validierung gemischt. Diese beiden Aufgaben nennt man «semi-supervised learning», also halbüberwachtes Lernen. «Das ist der Schlüssel zum Verständnis der Arbeit: Halbüberwachtes Lernen bedeutet, dass wir dem Modell im Training zwar Informationen geben – z.B. sagen wir ihm, wenn ein Patient einen FS>1. Tuttavia, non diciamo quali parti dell’imaging porterebbero un patologo a credere questo. Il modello lo determina dai dati stessi”.
Nuovi potenziali biomarcatori
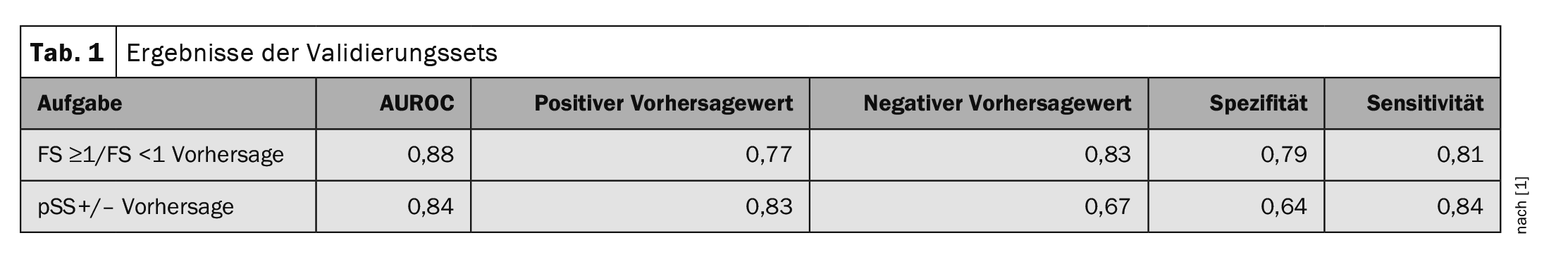
Le prestazioni dell’algoritmo sono state misurate utilizzando l’area sotto la curva ROC (AUROC). Per quanto riguarda il punteggio di focalizzazione (FS ≥1/FS <1), l’algoritmo ha raggiunto un AUROC di 0,88. Il 77% delle previsioni positive erano in realtà pazienti con un punteggio di focalizzazione ≥1. Nel caso del valore di predizione negativo, l’83 percento dei dati ha indicato correttamente che si trattava di un FS<1. Nel caso della previsione della diagnosi, l’AUROC era di 0,84. L’83% dei pazienti con una previsione positiva dell’algoritmo erano effettivamente positivi alla Sjögren (pSS+) e il 67% dei pazienti con una previsione negativa erano effettivamente negativi alla Sjögren (pSS-) (Tabella 1).
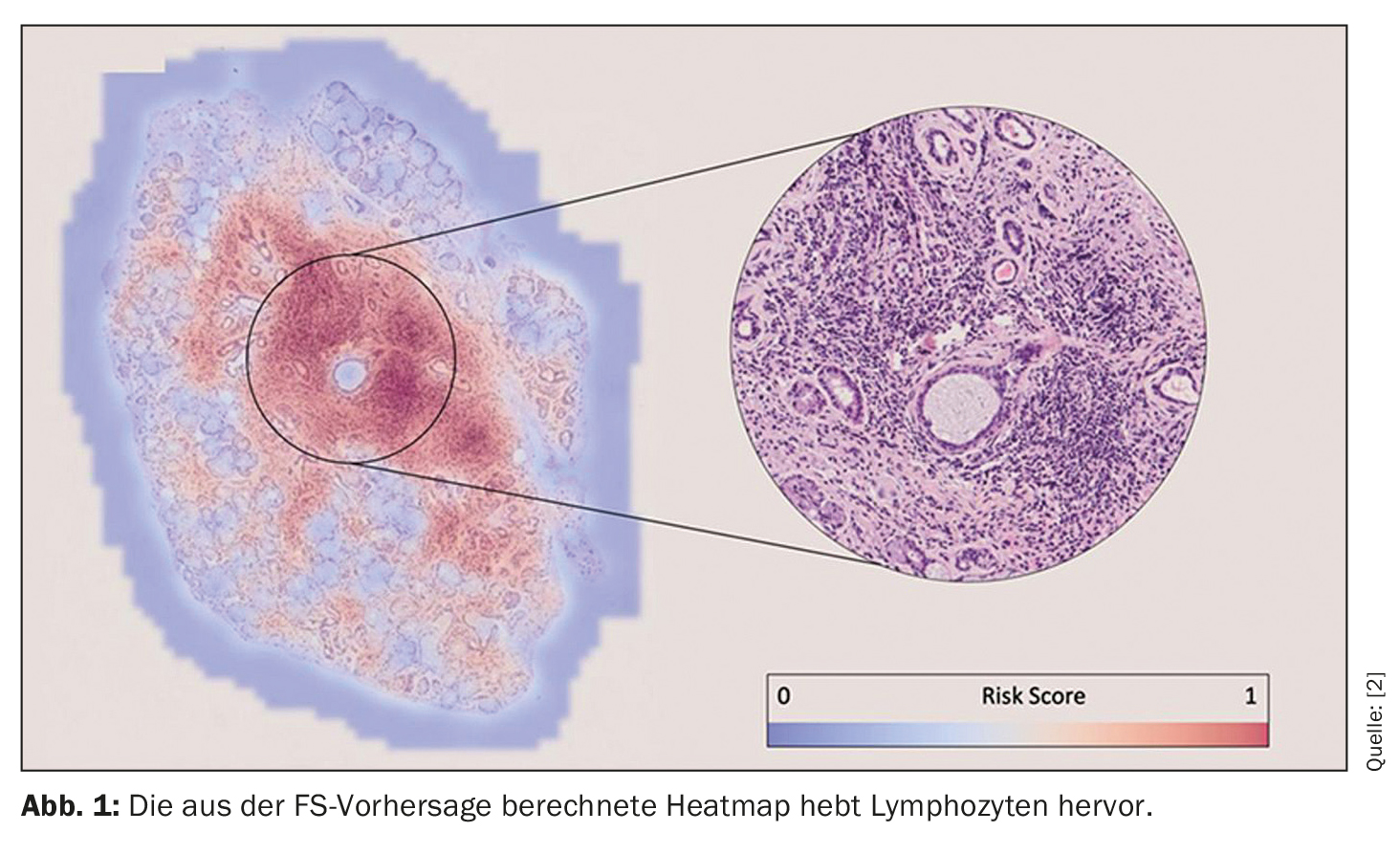
“Queste previsioni sono state fatte esclusivamente sulla base delle immagini. Non abbiamo detto all’algoritmo dove guardare per prendere la sua decisione – ma dopo l’addestramento, possiamo rivedere gli algoritmi per vedere su quale base hanno fatto le loro previsioni”. La scoperta dei ricercatori è stata che l’algoritmo per il punteggio di focalizzazione ha identificato i focolai linfocitari per fare una previsione. (Fig. 1). Questo garantisce la spiegabilità e consente al patologo di confermare visivamente i risultati della predizione. Questo è quindi rassicurante per la FS, dice Basseto, “ma ciò che è rassicurante per la FS è molto eccitante per la diagnosi, in quanto potrebbe portare alla potenziale identificazione di nuovi biomarcatori istologici che sono di interesse solo per la popolazione pSS+ e FS<1)”. Questo aspetto è di particolare interesse per il lavoro futuro del gruppo di ricerca.
Messaggi da portare a casa
- L’apprendimento profondo predice con precisione il punteggio di attenzione e la diagnosi di sindrome di Sjögren primaria sulla base di biopsie di ghiandole salivari labiali.
- L’apprendimento profondo potrebbe potenzialmente ridurre il tasso di errore nella diagnosi di ~2,5 volte. Il tasso di errore dovuto al deep learning è del 19,7% rispetto al 53% dei centri non esperti.
Prospettive:
- Sono necessarie ulteriori valutazioni cliniche per convalidare gli algoritmi nella pratica clinica reale.
- Ulteriore convalida su una coorte più ampia.
- Il lavoro in corso mira a identificare nuovi biomarcatori istologici associati alla diagnosi di pSS.
Congresso: EULAR 2023
Fonte:
- Basseto L: Vortrag «Deep Learning Accurately Predicts Focus Score and Diagnosis of Primary Sjögren Syndrome using Labial Salivary Gland Biopsies»; EULAR 2023, Mailand, 2.6.2023 (online).
- Basseto L: Scientific Abstract OP0232, EULAR 2023; doi: 10.1136/annrheumdis-2023-eular.418.
InFo RHEUMATOLOGIE 2023: 5(2): 20–21