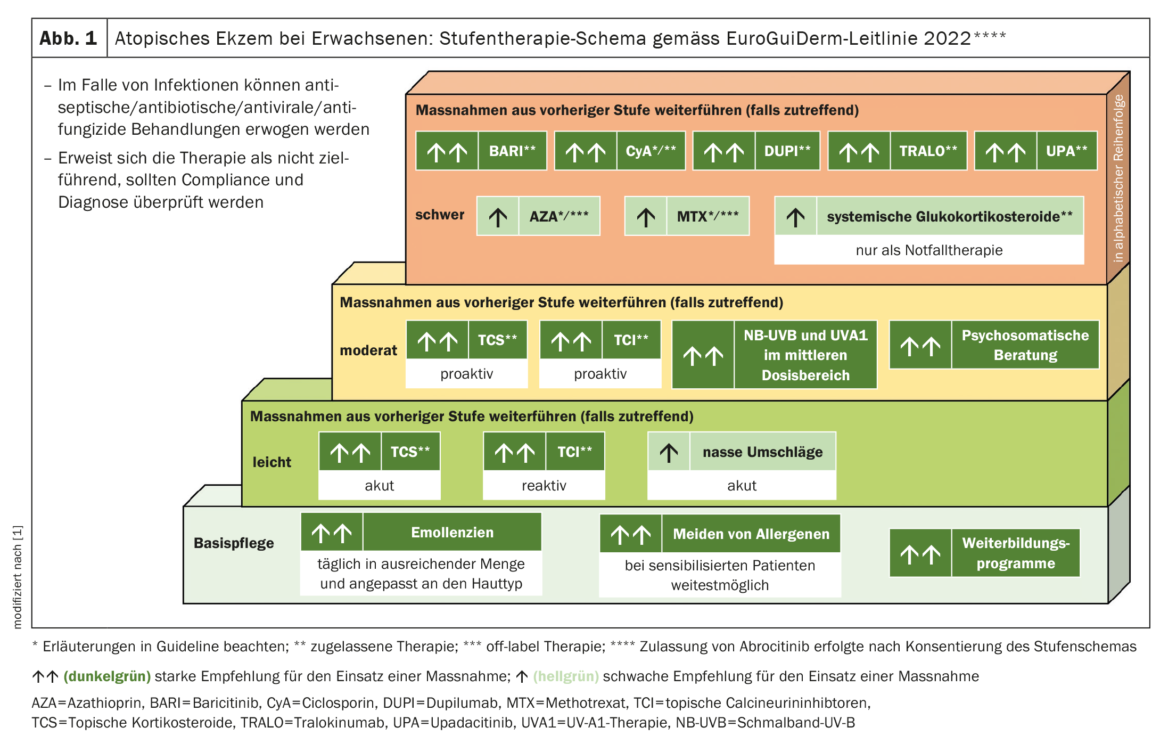
Negli ultimi tempi sono stati compiuti progressi significativi nel trattamento della dermatite atopica, comprese diverse nuove opzioni terapeutiche sistemiche che hanno superato gli ostacoli normativi. Questo è stato anche incorporato nella linea guida EuroGuiDerm sul trattamento dell’eczema atopico, pubblicata lo scorso anno. Quindi, contiene anche informazioni dettagliate sull’uso dei biologici e degli inibitori della JAK.
Le linee guida basate sull’evidenza forniscono una panoramica completa delle prove più recenti e sono una base decisionale importante per la scelta del trattamento adeguato. Il Forum Europeo di Dermatologia (EDF) è impegnato a migliorare l’assistenza sanitaria per i pazienti dermatologici in tutta Europa e ha lanciato il Centro Europeo per lo Sviluppo di Linee Guida qualche anno fa. La linea guida europea per l’eczema atopico pubblicata nel 2022 è stata sviluppata secondo gli standard EuroGuiDerm, descritti sul sito web dell’EDF. In generale, la terapia sistemica è indicata quando l’eczema atopico da moderato a grave non può essere controllato adeguatamente con i farmaci topici e la terapia con luce UV. La terapia sistemica può anche essere utile per ridurre la quantità di TCS somministrata ai pazienti che richiedono corticosteroidi topici (TCS) prolungati per controllare l’eczema atopico [1].
Sostanze innovative altamente efficaci: cosa è importante considerare?
Nel caso dei due biologici dupilumab e tralokinumab, non solo l’efficacia ma anche la tollerabilità è valutata come vantaggiosa. Non sono richiesti controlli di laboratorio regolari o altre misure di monitoraggio [2]. A differenza degli inibitori della janus chinasi (JAK), che sono caratterizzati da un inizio d’azione molto rapido, dupilumab e tralokinumab richiedono diverse settimane per sviluppare la loro piena efficacia [1]. Gli inibitori della JAK sono anche opzioni terapeutiche altamente efficaci e sicure, tenendo conto delle controindicazioni, degli effetti collaterali e degli esami di laboratorio necessari. Mentre i due biologici vengono applicati per via sottocutanea con intervalli di dosaggio di 2-4 settimane, gli inibitori della JAK sono disponibili in forma di dosaggio orale, con assunzione giornaliera raccomandata.
Biologici: altamente efficaci e mirati – non è necessario un monitoraggio di routine.
L’approvazione del primo farmaco biologico – Dupilumab – ha rappresentato un’importante pietra miliare e ha stabilito nuovi standard per il trattamento della dermatite atopica. In Svizzera, dupilumab (Dupixent®) è stato approvato per il trattamento della dermatite atopica (AD) da moderata a grave negli adulti dal 2019, seguito dall’estensione dell’indicazione per gli adolescenti e, da giugno 2022, dupilumab può essere utilizzato anche per i bambini a partire dai 6 anni di età [3]. Dupilumab si lega alla subunità α del recettore dell’IL-4, che fa parte dei complessi recettoriali dell’IL-4 e dell’IL-13. Negli adulti, la dose iniziale raccomandata è di 600 mg di dupilumab (due iniezioni da 300 mg) e la dose di mantenimento è di 300 mg ogni due settimane. Per i bambini e gli adolescenti dai 6 ai 17 anni, il dosaggio consigliato dipende dal peso corporeo.
La linea guida EuroGuiDerm indica che il trattamento con dupilumab è generalmente ben tollerato e non sono necessari esami ematici di laboratorio di routine [1]. La congiuntivite si sviluppa in circa un terzo dei pazienti. Tuttavia, questo può essere trattato bene. Nella maggior parte dei casi, l’uso di colliri antinfiammatori è sufficiente e il trattamento con dupilumab non deve essere interrotto [4–6].
Anche il tralokinumab (Adtralza®) è un anticorpo monoclonale umano, ma a differenza del dupilumab, neutralizza specificamente l’IL-13. In Svizzera, il tralokinumab è stato approvato per i pazienti adulti con AD da moderata a grave dal giugno 2022 [3]. La dose iniziale per gli adulti è di 600 mg (4 iniezioni da 150 mg ciascuna), seguita da una dose di mantenimento di 300 mg (2 iniezioni da 150 mg ciascuna), con un intervallo di dosaggio di 2 settimane ciascuna. Dalla 16esima settimana, l’intervallo può essere esteso a 4 settimane. Come per dupilumab, la linea guida EuroGuiDerm menziona la congiuntivite come possibile effetto collaterale, anche se questo si verifica in una percentuale minore di pazienti con tralokinumab [1,7]. Come per dupilumab, anche gli esami di laboratorio chimici di routine non sono necessari [1].
Inibitori della JAK: somministrabili per via orale e rapida insorgenza d’azione.
La linea guida EuroGuiDerm raccomanda gli stessi esami per lo screening basale e il monitoraggio del trattamento per tutti gli inibitori della JAK attualmente approvati [1]. La linea guida sottolinea che l’approvazione di abrocitinib ha seguito il consenso dello schema terapeutico graduale, motivo per cui questo inibitore JAK non è elencato, ma nella linea guida ci sono spiegazioni dettagliate anche su questa opzione terapeutica. Comune a tutti gli inibitori della JAK è la raccomandazione di uno screening di base, che comprende l’emocromo completo, il profilo renale/fegato/lipidico e i livelli di creatinina fosfochinasi, nonché lo screening dell’epatite e della tubercolosi (compresa la radiografia del torace). Per il monitoraggio, si raccomanda di eseguire un emocromo completo, un profilo renale/fegato/lipidico e un livello di creatinina fosfochinasi dopo quattro settimane di trattamento, oppure ogni tre mesi durante la terapia.
Baricitinib (Olumiant®) è un inibitore orale selettivo di JAK1 e JAK2, approvato in Svizzera dal febbraio 2021 per il trattamento di pazienti adulti con AD da moderata a grave [3]. Il dosaggio standard è di 4 mg (1×/d p.o.). La dose di 2 mg (1×/d p.o.) è considerata nei pazienti di 75 anni e più o nei pazienti con infezioni croniche/recidivanti o con una clearance della creatinina di 30-60 ml/min. La linea guida EuroGuiDerm elenca le infezioni del tratto respiratorio superiore, il mal di testa e l’aumento del colesterolo LDL come gli effetti collaterali più comuni di baricitinib negli studi clinici [1]. L’acne si verifica meno frequentemente rispetto ad altri inibitori di JAK. Non sono state segnalate neoplasie nei pazienti trattati con baricitinib durante il periodo controllato con placebo, e non sono stati segnalati perforazioni gastrointestinali, eventi cardiovascolari positivi o casi di tubercolosi.
L’upadacitinib (Rinvoq®) è un inibitore della JAK biodisponibile per via orale, selettivo e reversibile, che inibisce principalmente la JAK1 [3]. In Svizzera, upadacitinib è stato approvato per il trattamento dell’AD da moderato a grave negli adulti dal novembre 2021. La dose orale raccomandata è di 15 mg di upadacitinib una volta al giorno. Secondo la linea guida EuroGuiDerm, le infezioni del tratto respiratorio superiore e l’acne sono stati gli effetti collaterali più comuni con upadacitinib negli studi clinici [1]. I tassi di incidenza cumulativa degli eventi avversi gravi sono stati dello 0% per 30 mg, del 2,4% per 15 mg, del 4,8% per 7,5 mg e del 2,4% per il placebo.
Abrocitinib (Cibinqo®) è un inibitore orale selettivo di JAK-1. In Svizzera, abrocitinib è stato approvato per il trattamento dell’AD negli adulti dall’aprile 2022 [3]. Nella linea guida EuroGuiDerm, gli eventi avversi correlati alla dose (200 mg, 100 mg, placebo) sono stati nausea (14,6%, 6,1%, 2,0%), mal di testa (7,8%, 5,9%, 3,5%) e acne (4,7%, 1,6%, 0%). Nei gruppi di abrocitinib da 200 mg e 100 mg, i tassi di incidenza delle infezioni gravi sono stati rispettivamente di 2,33/100 anni-paziente (PY) e 2,65/100 PY. Per l’herpes zoster, i tassi di incidenza sono stati rispettivamente 4,34/100 PJ e 2,04/100 PJ, e per l’herpes simplex, 11,83/100 PJ e 8,73/100 PJ, rispettivamente [1,8].
| Lo sviluppo della linea guida EuroGuiDerm, pubblicata nel Journal of the European Academy of Dermatology and Veneorology , ha coinvolto 26 esperti di 12 Paesi europei, nominati dalle società nazionali partner o dai due coordinatori della linea guida. Inoltre, tre rappresentanti dei pazienti hanno partecipato allo sviluppo della linea guida. La parte 1 riassume le raccomandazioni per la terapia sistemica, mentre la parte 2 tratta le opzioni terapeutiche non sistemiche. Per la Parte 1 della linea guida, oltre alle raccomandazioni del gruppo di esperti, i risultati del documento di revisione di Drucker et al. considerato. Si sottolinea che quando si applicano le raccomandazioni terapeutiche, bisogna prestare attenzione alle condizioni e alle circostanze locali di licenza. a [1,9] |
Altri principi attivi menzionati nella linea guida
Oltre alle opzioni di terapia sistemica convenzionali e nuove, la linea guida EuroGuiDerm menziona anche i due candidati farmaci lebrikizumab e nemolizumab – entrambi biologici che sono attualmente in fase di studio per l’uso nell’AD in studi di fase III [1]. Il lebrikizumab è un anticorpo monoclonale che si lega specificamente all’IL-13 liberamente circolante. Il nemolizumab blocca la subunità α del recettore IL-31. Altri agenti menzionati nella linea guida includono l’anticorpo monoclonale anti-IgE omalizumab, che è approvato per il trattamento dell’asma e dell’orticaria cronica spontanea, ma non per l’eczema atopico. La base di evidenza per omalizumab nell’eczema atopico è controversa. Un altro principio attivo citato è l’alitretinoina, che è approvata in alcuni Paesi europei per il trattamento dell’eczema cronico delle mani. L’alitretinoina è un principio attivo del gruppo dei retinoidi.
Letteratura:
- Wollenberg A, et al: Linea guida europea (EuroGuiDerm) sull’eczema atopico: parte I – terapia sistemica. J Eur Acad Dermatol Venereol 2022; 36(9): 1409-1431.
- Worm M, et al.: Terapia moderna della dermatite atopica: biologici e farmaci a piccole molecole. J Dtsch Dermatol Ges 2020; 18(10): 1085-1093.
- Informazioni sui farmaci, www.swissmedicinfo.ch,(ultimo accesso 08.03.2022).
- Wollenberg A, et al: Sicurezza di laboratorio di dupilumab nella dermatite atopica da moderata a grave: risultati di tre studi di fase III (LIBERTY AD SOLO 1, LIBERTY AD SOLO 2, LIBERTY AD CHRONOS). Br J Dermatol 2020; 182: 1120-1135.
- Akinlade B, et al: Congiuntivite negli studi clinici su dupilumab. Br J Dermatol 2019; 181: 459-473.
- Wollenberg A, et al: Congiuntivite che si verifica in pazienti con dermatite atopica trattati con dupilumab – caratteristiche cliniche e trattamento. J Allergy Clin Immunol Pract 2018; 6: 1778-1780.e1
- Wollenberg A, et al: Tralokinumab per la dermatite atopica da moderata a grave: risultati di due studi di fase III, randomizzati, in doppio cieco, multicentrici, controllati con placebo, della durata di 52 settimane (ECZTRA 1 e ECZTRA 2). Br J Dermatol 2021; 184: 437-449.
- Simpson EL, Silverberg JI, Nosbaum A, et al: Analisi integrata della sicurezza di abrocitinib per il trattamento della dermatite atopica da moderata a grave, dal programma di studi clinici di fase II e di fase III. Am J Clin Dermatol 2021; 22: 693-707.
- Drucker AM, et al: Trattamenti immunomodulatori sistemici per i pazienti con dermatite atopica: una revisione sistematica e una meta-analisi di rete. JAMA Dermatology, 01 giu 2020; 156(6): 659-667.
PRATICA DERMATOLOGICA 2023; 33(2): 32-33











