L’interleuchina-23 e l’interleuchina-17A svolgono un ruolo importante nel processo infiammatorio della psoriasi a placche. Un confronto tra due agenti diretti contro questi bersagli nella psoriasi a placche da moderata a grave ha portato a risultati interessanti.
Torna a “Notizie su dermatite atopica e psoriasi”.
Come l’azienda farmaceutica AbbVie Inc. in un comunicato stampa, l’inibitore dell’IL23 risankizumab (Skyrizi™) [1] si è dimostrato superiore all’inibitore dell’IL17A secukinumab (Cosentyx®) [2] in questo studio multicentrico di fase III, in doppio cieco, randomizzato, controllato attivo, in aperto, per quanto riguarda vari endpoint primari e secondari dopo un periodo di trattamento di 52 settimane [3]. I soggetti sono stati randomizzati 1:1 alla condizione Skyrizi™ 150 mg* (n=164) o Cosentyx® 300 mg** (n=163) come iniezioni sottocutanee. I due endpoint primari sono stati definiti come non inferiorità alla settimana 16 e superiorità alla settimana 52 rispetto al PASI90. Gli endpoint secondari erano i valori dei seguenti parametri alla settimana 52: PASI 100, sPGA 0/1 e PASI 75.
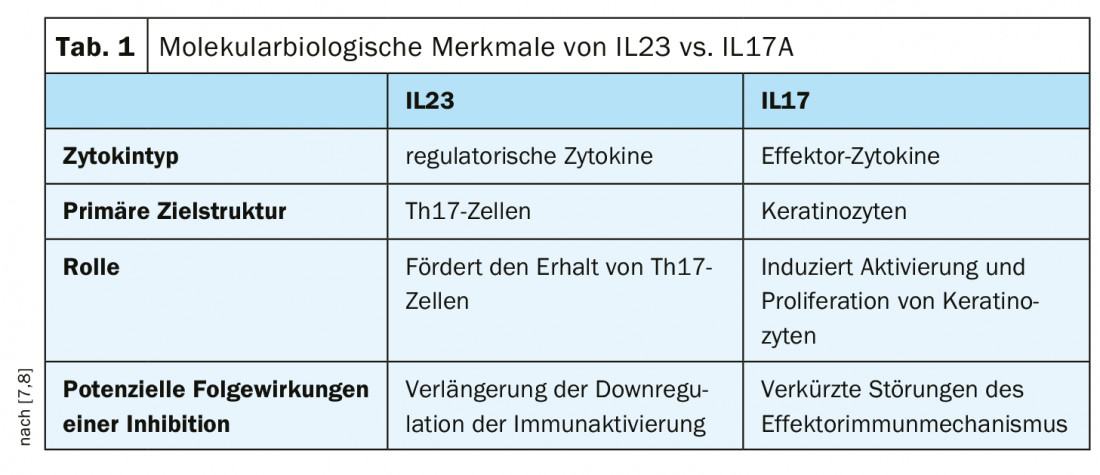
In trattamento con risankizumab, il 74% dei pazienti ha raggiunto PASI90 alla settimana 16, rispetto al 66% della condizione con secukinumab [3]. Risankizumab ha soddisfatto anche il secondo endpoint primario (87% di risposta PASI 90 rispetto al 57% con secukinumab, p<0,001) [3]. L’inibitore dell’IL23 risankizumab si è dimostrato superiore anche all’inibitore dell’IL17A secukinumab in tutti gli endpoint secondari misurati in questo studio, compresi PASI 100, PASI 75 e sPGA 0/1 alla settimana 52 (p<0,001) [3]. Il profilo di sicurezza di Skyrizi™ è stato coerente con quello degli studi precedenti, senza nuovi segnali di sicurezza segnalati nel periodo di studio di 52 settimane (4-6). I biologici Skyrizi™ (risankizumab) [1] e Cosentyx® (secukinumab) [2] sono approvati in Svizzera per il trattamento della psoriasi a placche da moderata a grave negli adulti. Si tratta di due delle opzioni terapeutiche antagoniste dell’interleuchina, successivamente ampliate negli ultimi anni, per i pazienti affetti da psoriasi. Le due citochine IL-23 e IL17A differiscono per quanto riguarda varie caratteristiche biologiche molecolari (Tab. 1).
* Condizione Skyrizi™ 150 mg: 2 iniezioni sottocutanee da 75 mg ciascuna alle settimane 0, 4 e 12; successivamente a intervalli di 12 settimane.
** Condizione Cosentyx® 300 mg: 2 iniezioni sottocutanee da 150 mg ciascuna alla settimana 0,1,2,3,4; successivamente a intervalli di 4 settimane.
Fonte: AbbVie Inc.
Letteratura:
- Skyrizi [Summary of Product Characteristics]. AbbVie Ltd. Disponibile su: www.ema.europa.eu.
- Cosentyx: https://compendium.ch, ultimo accesso 12.02.2020
- Comunicato stampa di AbbVie: https://news.abbvie.com/news/press-releases/new-head-to-head-phase-3-data-show-skyrizi-risankizumab-superior-to-cosentyx-secukinumab-across-primary-and-all-ranked-secondary-endpoints-in-adults-with-moderate-to-severe-plaque-psoriasis-at-52-weeks.htm
- Gordon K, et al: Efficacia e sicurezza di risankizumab nella psoriasi a placche da moderata a grave (UltIMMa-1 e UltIMMa-2): risultati di due studi di fase 3 in doppio cieco, randomizzati, controllati con placebo e controllati con ustekinumab. The Lancet 2018; 25; 392(10148): 650-661.
- Reich K, et al: Risankizumab rispetto ad adalimumab in pazienti con psoriasi a placche da moderata a grave (IMMvent): uno studio di fase 3 randomizzato, in doppio cieco, controllato con comparatore attivo. Lancet 2019; 394(10198): 576-586.
- Blauvelt A, et al: Efficacia e sicurezza di Risankizumab Q12W continuo rispetto alla sospensione del trattamento: risultati in doppio cieco a 2 anni dello studio di Fase 3 IMMhance. Poster #478. 24° Congresso Mondiale di Dermatologia. 2019.
- Gooderham MJ, et al: Spostare l’attenzione – il ruolo primario dell’IL-23 nella psoriasi e in altri disturbi infiammatori. J Eur Acad Dermatol Venereol 2018; 32: 1111-1119.
- Girolomoni G, et al: Il ruolo dell’IL-23 e dell’asse immunitario IL-23/TH17 nella patogenesi e nel trattamento della psoriasi. J Eur Acad Dermatol Venereol 2017; 31: 1616-1626.
DERMATOLOGIE PRAXIS 2020; 30(1): 27 (pubblicato il 22.2.20, prima della stampa).











