La BPCO è associata a un’elevata morbilità e mortalità. Attualmente è la quarta causa di morte a livello mondiale e, secondo una previsione del Global Burden of Disease Study, sarà la terza causa entro il 2020. C’è un’alta prevalenza e un alto tasso di ricovero e, di conseguenza, una grande perdita di giorni lavorativi. Quindi, a che punto siamo attualmente con la terapia, quando l’ORO porta costantemente nuovi cambiamenti?
“Queste modifiche sono generalmente giustificate. Dopo tutto, ci portano anche a migliorare il tutto”, ha dichiarato il Prof. Dr. Michael Dreher, Clinica di Pneumologia e Medicina Interna Intensiva, Clinica Medica V, Ospedale Universitario RWTH Aachen, in occasione del 60° Congresso della DGP a Monaco. Tuttavia, l’esperto ha anche ammesso che, quando ha esaminato per la prima volta l’ORO 2019, ha pensato che molte cose sarebbero tornate ad essere complicate, che molte cose sarebbero cambiate e che i pazienti avrebbero dovuto di nuovo sentirsi dire cosa fare. “Ma in realtà non è così difficile e non è così lontano dalla routine clinica e da ciò che facciamo comunque”. Sulla base delle raccomandazioni GOLD, il Prof. Dreher ha classificato l’importanza dei corticosteroidi per via inalatoria (ICS) nel trattamento della BPCO, non senza sottolineare che nulla di tutto ciò è definitivo, perché sono sempre le decisioni individuali a dover essere prese dai medici.
In sostanza, quando un paziente con BPCO si presenta per la prima volta e non ha ancora effettuato alcuna terapia, viene comunque suddiviso in gruppi di rischio: Nel gruppo A e B i pazienti sintomatici e nel gruppo C e D i pazienti con frequenti esacerbazioni. In base a ciò, si valuta il modo migliore per adattare la terapia. Nella terapia iniziale, solo pochi pazienti possono trarre beneficio dagli steroidi inalatori. Sono utilizzati solo nel gruppo D nella combinazione ICS/LABA. Lo studio IMPACT, uno dei più ampi studi sulla BPCO, ha confrontato la triplice terapia LAMA/LABA/ICS con quella di un farmaco a base di acido folico. Nel tasso di esacerbazioni gravi e moderate, la triplice terapia è risultata significativamente migliore rispetto alla broncodilatazione massima. Ma anche i LABA/ICS sono risultati migliori rispetto alla broncodilatazione massima. Una critica mossa in passato è stata quella di includere principalmente pazienti con un certo grado di reversibilità. Ma d’altra parte, dice l’esperto, è molto probabile che siano proprio questi pazienti nella presentazione iniziale a dover pensare allo steroide inalatorio. “Se non siamo sicuri al 100% se si tratta di asma o di BPCO, se il paziente ha una reversibilità, allora l’ICS ha certamente un ruolo nella BPCO”.
Molte strade portano alla triplice terapia
Ciò che si deve evitare, tuttavia, è che il paziente riceva una tripla terapia nella terapia iniziale. Nel 2016, lo studio FLAME ha confrontato LAMA/LABA vs ICS/LABA e ha dimostrato che LAMA/LABA era significativamente meno associato alle esacerbazioni rispetto alla combinazione ICS/LABA. Pertanto, è certamente giustificato effettuare una doppia broncodilatazione in prima battuta per un paziente del gruppo D. La maggior parte dei pazienti in FLAME ha avuto meno di due esacerbazioni moderate o gravi nell’ultimo anno, nel qual caso i pazienti hanno probabilmente tratto beneficio. IMPACT, invece, aveva una popolazione di pazienti significativamente più malati e con un tasso più elevato di esacerbazioni, il che significa che gli ICS sono certamente ben indicati in questo caso. Quando si confrontano FLAME e IMPACT, non c’è differenza tra la broncodilatazione massima e la combinazione LABA/ICS, ma c’è una differenza quando ci sono due o più esacerbazioni moderate o una grave. “Quindi è sempre una domanda cruciale: di che tipo di paziente stiamo parlando? Se poi facciamo l’indicazione giusta, possiamo anche aiutare molto bene queste persone con un ICS”.
Il Prof. Dreher non ha voluto lasciar correre l’accusa che in Germania vengono prescritti troppi ICS. Nella sua argomentazione ha citato i dati del registro DACCORD, che comprende quasi 6000 pazienti. Gli ICS sono prescritti in oltre il 30% dei pazienti qui, il che non è molto secondo lo pneumologo. Il problema è piuttosto che l’ICS viene spesso applicato anche in ORO A o B. “E in realtà ha relativamente poco a che fare con l’ORO A”. Il 30% citato è un dato della Germania. Se si valutano i tre grandi studi tripli IMPACT, TRIBUTE e KRONOS in base al numero di pazienti che assumevano ICS prima di essere randomizzati, i numeri vanno dal 60 (IMPACT, TRIBUTE) al 70% (KRONOS).
Lo studio KRONOS ha confrontato il dosaggio fisso triplo vs LABA/ICS vs LAMA/LABA. I criteri di inclusione erano la BPCO da moderata a molto grave, FEV1 inferiore a 80 e superiore al 25%; i pazienti dovevano essere sintomatici, ma non era necessaria una storia di esacerbazioni. Quindi la domanda era: la terapia tripla funziona nei pazienti sintomatici che non hanno una storia di esacerbazioni? “Al contrario, si può anche dire: funziona per tutti i pazienti con BPCO?”, ha sottolineato l’esperto. Perché: il registro DACCORD elenca solo il 3% del totale di 6000 pazienti come asintomatici.
Quando è indicato, tuttavia, l’ICS funziona molto bene anche in KRONOS. Anche in questo caso, le esacerbazioni sono state significativamente inferiori rispetto alle combinazioni LAMA/LABA e LABA/ICS. Tuttavia, non solo la storia delle esacerbazioni dovrebbe essere inclusa nella domanda su quando i pazienti con BPCO beneficiano degli steroidi inalatori, ma anche il numero di eosinofili. GOLD ha definito 2 soglie chiare: Al di sotto di 100 eosinofili ha relativamente poco senso pensare a una ICS, mentre al di sopra di 300 EOS è certamente giustificata.
Tenere sotto controllo gli eosinofili
Quindi i pazienti che si esacerbano frequentemente e che hanno un’eosinofilia nel sangue hanno maggiori probabilità di beneficiare di uno steroide inalatorio. Ma un numero maggiore di pazienti potrebbe beneficiare di un ICS? Nella pratica quotidiana, come suggeriscono i dati DACCORD, ci si trova molto raramente di fronte a pazienti con BPCO esacerbata. Almeno in questa coorte, il tasso di riacutizzazione era solo dello 0,38. Si tratta di un valore molto basso e inferiore a quello degli studi prospettici. (Per TRIBUTE 0,5-0,6, KRONOS 0,5-0,95 e IMPACT 0,9-1,2). Si può certamente sospettare, dice il Prof. Dreher, che le esacerbazioni si perdano nella vita clinica quotidiana. Il problema di base: se a un paziente esacerbante viene somministrato del cortisone e nota che lo fa sentire bene, la prossima volta potrebbe non andare dal medico, ma prendere le compresse da solo.
Infine, ma non meno importante, il pneumologo ha incoraggiato il principio che meno è meglio: “Se ho una BPCO lieve/moderata e pochi ricoveri, devo essere equo e mettere in dubbio anche il senso dell’ICS”. Non solo l’escalation, ma anche la de-escalation può portare al successo in alcuni casi. Lo studio SUNSET ha incluso proprio questa popolazione di pazienti. Il FEV1 era pari al 40-80% dell’obiettivo, non c’era più di un’esacerbazione moderata/grave nell’ultimo anno e almeno 6 mesi di tripla terapia. Lo studio è stato randomizzato alla tripla terapia o a indacaterolo/glicopirronio e placebo; l’endpoint primario era la non inferiorità della funzione polmonare. Questo non è stato mostrato. Quando l’ICS è stato eliminato, il paziente ha perso una media di 26 ml di FEV1, ma non ci sono state più esacerbazioni (endpoint secondario). E ancora una volta è emerso chiaramente: le esacerbazioni senza ICS sono più frequenti nei pazienti che hanno un’elevata eosinofilia nel sangue, cioè 300 o più.
Cosa c’è di nuovo nell’asma?
L’utilità dell’uso dei corticosteroidi per via inalatoria è stata anche al centro della conferenza del Prof. Dr. Andreas R. Koczulla, dell’Ospedale Universitario di Marburgo, con un focus particolare sull’asma. L’esperto ha innanzitutto ricordato alla platea la nuova Linea Guida Nazionale per l’Assistenza Sanitaria (NVL) sull’asma, che è stata pubblicata nel settembre 2018 e che contiene il noto schema a tappe che elenca i dosaggi bassi, medi e alti.
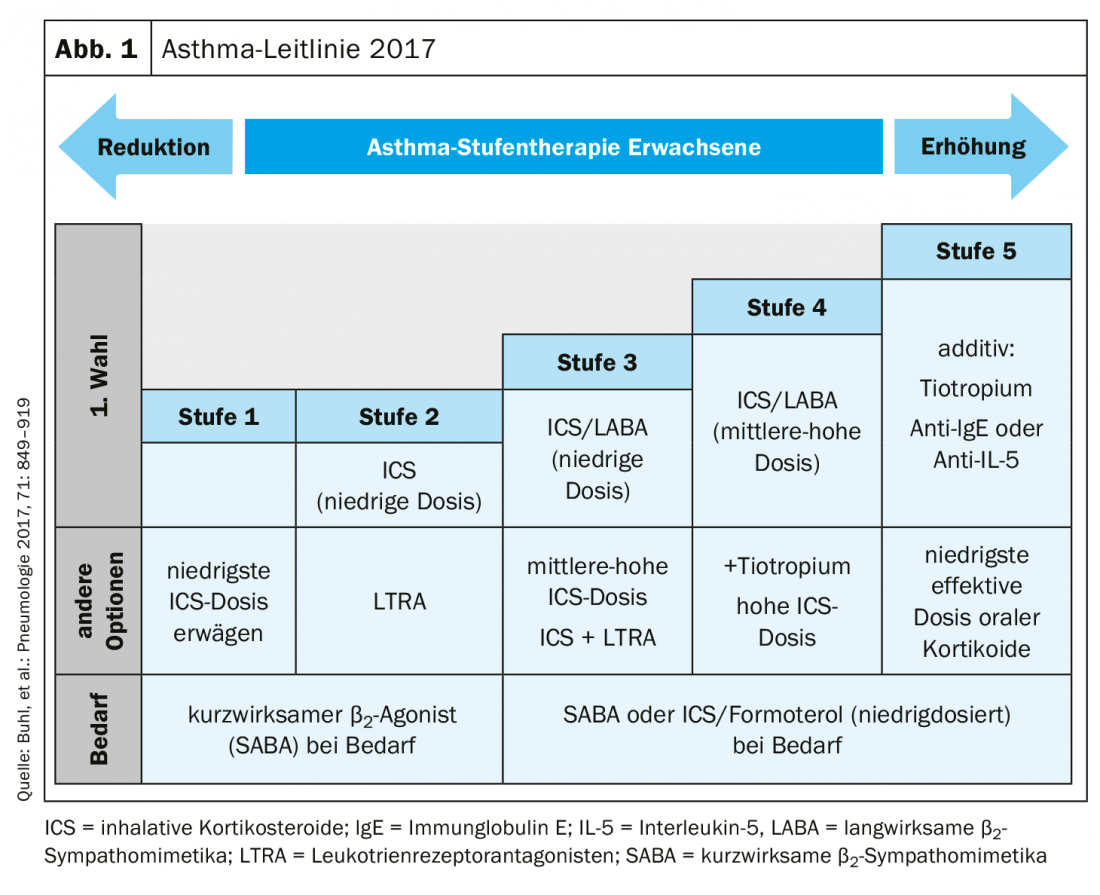
Ha definito gli obiettivi terapeutici dell’uso degli ICS come segue: spegnere le citochine proinfiammatorie e upregolare i geni antinfiammatori; ridurre le cellule infiammatorie e, in ultima analisi, migliorare i sintomi clinici del paziente; anche il rilievo epiteliale, che può diventare disregolato nel contesto dell’asma, dovrebbe tornare ad essere armonizzato. Tuttavia, la strada per raggiungere questi obiettivi può essere difficile, soprattutto se si considerano i possibili effetti collaterali.
Il fluticasone propionato ha una raccomandazione di dose ICS bassa di 100-250, media di 250-500 e alta di oltre 500, secondo GINA. La NVL prevede una forma di dose massima a ≥1000 µg. Un recente lavoro ha analizzato la quantità di dose necessaria per raggiungere il massimo del FEV1. “Si raggiunge l’80% del massimo con 146 µg di fluticasone propionato. Se vuole arrivare al 90%, aumenti la dose a 209 µg. Tuttavia, più alto è il dosaggio, più gravi sono gli effetti collaterali sistemici. Questi includono l’insufficienza surrenale, la cataratta, le fratture e il diabete”.
Il paziente fa quello che vuole – è un bene!
I pazienti spesso agiscono più in base ai loro sintomi e, se i sintomi non sono particolarmente pronunciati, spesso assumono un po’ meno farmaci, quindi regolano la loro terapia da soli. Il Prof. Koczulla ha espresso preoccupazione per il fatto che solo il 3,3% di tutti i pazienti affetti da asma viene incluso nei classici studi controllati randomizzati. “Davvero copriamo la nostra vita quotidiana con questi studi?”. Il relatore ha quindi presentato un altro studio reale, il cosiddetto studio di Salford, che ha confrontato una terapia standard con una combinazione ICS/LABA. Sono state osservate più risposte con la combinazione ICS/LABA (fluticasone furoato/vilanterolo) (71%) rispetto alla terapia standard (56%). Un responder era un paziente con un miglioramento dell’ACT di tre o più punti o di un totale di 20 o più punti. “Quindi ha funzionato bene in questo caso e certamente vale la pena menzionare che non ci sono state differenze significative tra la FF/VI e la terapia standard in termini di esacerbazioni ed effetti collaterali”, ha riassunto il pneumologo.
Alla luce dei risultati, il collega Dreher ha aggiunto che stiamo per dividere i pazienti in due gruppi: quelli che stanno bene e con i quali si possono sviluppare concetti terapeutici individuali per vedere se si può anche salvare qualcosa. E l’altro gruppo con quelli più gravi, dove bisogna considerare gli anticorpi e dove il medico deve assicurarsi che il paziente sia fuori dal trattamento prima di parlare di alternative. Il Prof. Koczulla è d’accordo: “Sta andando chiaramente nella direzione dell’individualizzazione. E forse quelli che stanno andando bene possono essere interrogati digitalmente, poi inviano uno smiley e non li si vede più per altri sei mesi”.
Sommario
- Gli ICS sono raramente appropriati al momento della diagnosi iniziale, ma probabilmente non sono così rari più avanti nel decorso della malattia. Vale a dire, quando un paziente si esacerba frequentemente.
- Se vengono coinvolti anche gli eosinofili, sono ora disponibili gruppi di sostanze buone per ridurre le esacerbazioni.
- Tuttavia, non bisogna limitarsi all’escalation, ma anche porsi sempre delle domande: forse la de-escalation ha più senso.
- L’aumento delle dosi di ICS aumenta anche il tasso di effetti collaterali.
- La terapia basata sui bisogni porta a effetti di risparmio.
- Ci sono pochi dati per il range di dosi massime (i dati degli studi controllati randomizzati dimostrano che è possibile una terapia basata sul bisogno, lo studio della vita reale ha anche dimostrato che la combinazione ICS/LABA funziona relativamente bene).
Fonte: Simposio industriale “ICS nell’asma e nella BPCO – terapia in tempi di cambiamento”, nell’ambito del 60° Congresso della DGP; Organizzatore: Berlin Chemie
InFo PNEUMOLOGIA & ALLERGOLOGIA 2019, 1(1): 26-27.











