L’asportazione delle metastasi epatiche del colon-retto è rilevante per la prognosi. Per valutare la resecabilità si utilizzano criteri oncologici e tecnico-chirurgici.
Il cancro del colon-retto (CRC) è il terzo tumore più comune nel mondo occidentale. Il 50% di tutti i pazienti con carcinoma colorettale sviluppa metastasi epatiche; il fegato è l’organo più frequentemente colpito. Il 14-20% dei pazienti presenta già metastasi epatiche al momento della diagnosi; nel resto dei pazienti, queste vengono diagnosticate solo nel corso della malattia. Le metastasi epatiche sono classificate come malattia da cancro colorettale in stadio IV e hanno un tasso medio di sopravvivenza a 5 anni del 10-15%. Nei pazienti con tumori che rispondono bene alla chemioterapia consolidata e che possono essere rimossi con le moderne tecniche chirurgiche e radiologiche interventistiche, questo tasso di sopravvivenza è significativamente più alto, pari al 25-40%. Il vantaggio di sopravvivenza di oltre il 20% si applica anche ai pazienti con metastasi epatiche estese, inizialmente classificate come non resecabili e divenute asportabili solo dopo una chemioterapia aggressiva.
L’invio tempestivo di un paziente con metastasi epatiche colorettali estese a un centro specializzato è un fattore importante per mettere in pratica questi risultati in Svizzera.
Qual è la strategia oncologica per le metastasi epatiche?
L’obiettivo del trattamento dei pazienti con metastasi epatiche è il controllo a lungo termine del tumore. La resezione chirurgica delle metastasi epatiche aiuta a raggiungere questo obiettivo. La selezione dei pazienti che si qualificano per la chirurgia potenzialmente curativa è un processo interdisciplinare. L’idoneità di un paziente alla resezione si basa su diversi criteri: Condizioni generali del paziente, appropriatezza oncologica e resecabilità tecnica.
Quali pazienti possono essere resecati?
Da un punto di vista tecnico-chirurgico, è importante mantenere una riserva sufficiente di parenchima epatico funzionale durante la chirurgia epatica. La resezione di una quantità eccessiva di tessuto epatico porta a un’insufficienza d’organo post-operatoria, che ha un’alta mortalità e deve essere evitata a tutti i costi. La valutazione della resecabilità tecnica comporta un’analisi sfaccettata dell’anatomia, dell’istologia e della funzione del fegato, eseguita al meglio da un team di chirurghi epatobiliari, radiologi, epatologi e patologi. In caso di resecabilità tecnica, è importante garantire, secondo i criteri moderni, che il volume futuro del fegato (“futuro residuo epatico”, FLR) e la funzione epatica dopo la resezione siano sufficienti. La volumetria del fegato consente di quantificare esattamente il volume previsto della FLR. Per i pazienti con un parenchima epatico normalmente funzionante, la linea guida prevede che possa essere tollerata una riduzione del volume epatico fino al 20-25% (corrispondente a circa due segmenti epatici). I pazienti con danni al fegato dovuti a un precedente trattamento chemioterapico necessitano di un volume FLR di almeno il 30-35%, e quelli con cirrosi epatica ancora di più. Un’importante innovazione degli ultimi anni è la tendenza alla chirurgia parenchima-sparing, il che significa che la pianificazione della resezione spesso non è guidata dai confini anatomici dei singoli segmenti epatici, ma piuttosto vengono eseguite resezioni non anatomiche. In questo modo, si può ottenere il massimo risparmio di tessuto epatico sano.
Come viene valutata la funzionalità epatica prima dell’intervento?
Ci sono solo alcuni esami comuni che aiutano a valutare meglio la funzione del fegato. I “valori epatici” facilmente determinabili negli esami del sangue (ad esempio, la bilirubina) non sono abbastanza sensibili per mappare i sottili cambiamenti funzionali dopo la chemioterapia. Il test al verde di indocianina ha una sensibilità maggiore, ma è poco utilizzato in Europa nei Paesi di lingua tedesca. A Winterthur, consideriamo il gold standard la scintigrafia epatica, chiamata anche HIDA scan. Fornisce informazioni molto sensibili sulla funzione proprio di quelle aree del fegato che rimangono dopo la resezione, la cosiddetta “riserva epatica”. Inoltre, una biopsia del fegato non affetto da tumore può anche fornire indicazioni importanti sulla presenza di un rimodellamento fibrotico o addirittura di cirrosi, che limiterebbe fortemente la capacità rigenerativa del fegato e renderebbe impossibile una resezione epatica estesa.
Il fegato rimanente può essere ingrandito?
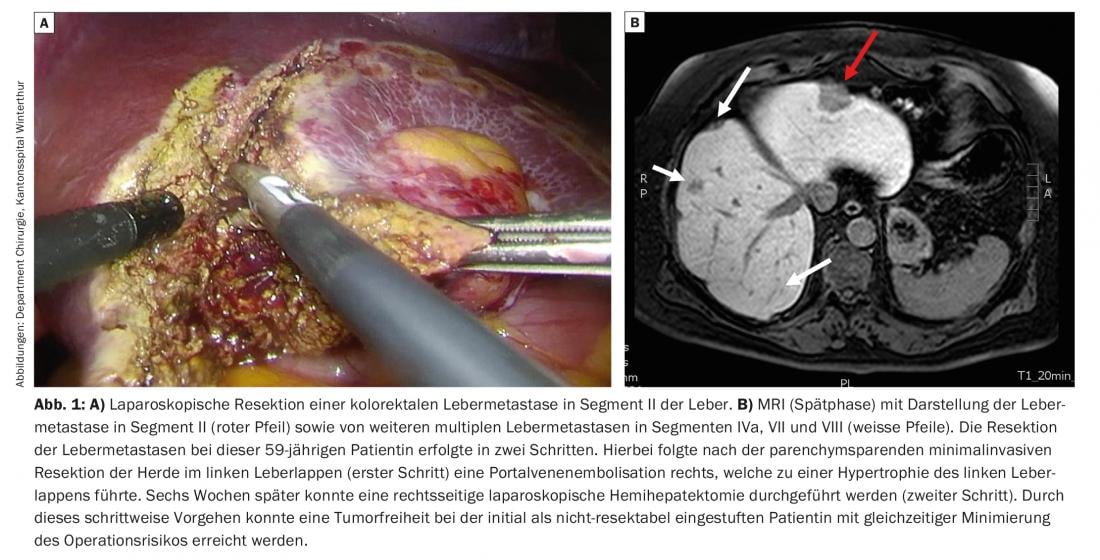
La maggior parte dei pazienti non presenta un coinvolgimento tumorale esteso del fegato (ad esempio, metastasi di piccolo volume) e la resezione di tutti i focolai può spesso essere eseguita in modo sicuro ed efficace; nell’80% dei casi ciò è possibile anche per via laparoscopica. (Fig. 1). La procedura minimamente invasiva ha il particolare vantaggio di un recupero più rapido per il paziente e provoca anche meno aderenze intra-addominali, il che rappresenta un vantaggio per il paziente se l’intervento viene ripetuto. Se la riserva epatica non risulta essere abbastanza grande, il fegato può essere fatto crescere con alcuni metodi prima della resezione. Ciò comporta l’interruzione del flusso della vena porta mediante embolizzazione (embolizzazione percutanea della vena porta, PVE) o legatura chirurgica (legatura della vena porta, PVL), con conseguente crescita del lato opposto del fegato.
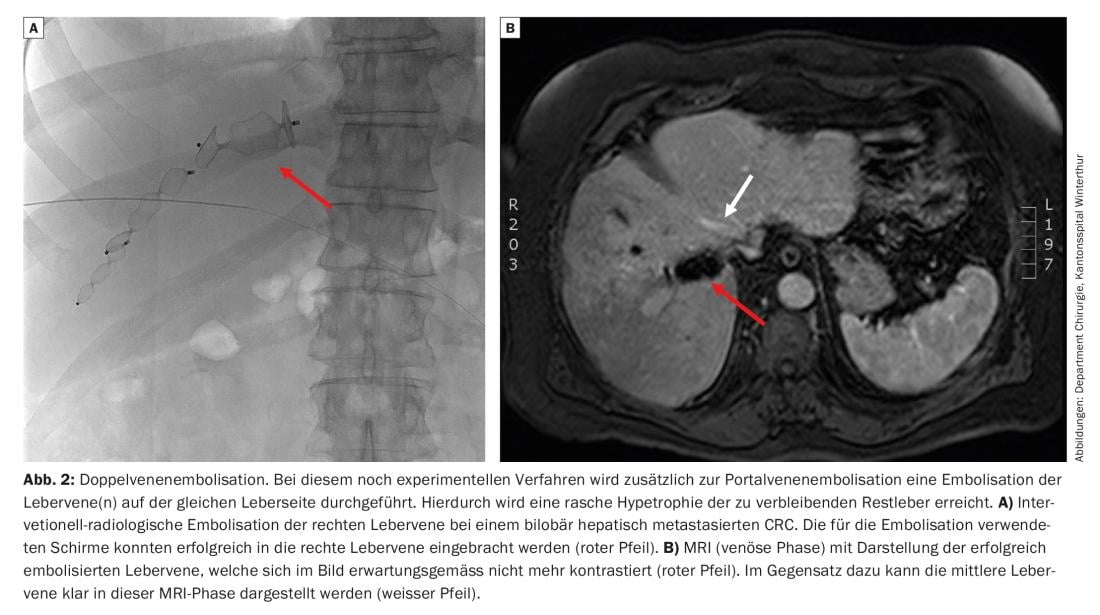
Come funziona un PVE?
Nella PVE, speciali preparati o bobine di plastica vengono inseriti nei rami della vena porta che alimentano la parte del fegato da resecare. L’occlusione delle vene portali porta all’ipertrofia dei segmenti da lasciare (cioè la FLR). Nel caso di metastasi colorettali bilobari, spesso vengono eseguiti due interventi in successione. Nel primo intervento, le metastasi nel futuro parenchima epatico rimanente vengono rimosse (Fig. 1) – seguite dalla PVE percutanea e poi, in un secondo intervento, dalla resezione delle aree epatiche embolizzate ancora interessate dal tumore. Queste procedure consentono di eseguire una resezione epatica estesa nei pazienti che sono stati classificati come tecnicamente non resecabili a causa di una FLR insufficiente alla valutazione iniziale. Questa procedura chirurgica in due fasi riduce il rischio di insufficienza epatica post-operatoria. La sopravvivenza a lungo termine nei pazienti trattati con due interventi è uguale a quella dei pazienti trattati con un solo intervento.
Che cos’è l’ALPPS?
Oltre alla PVE, sono in discussione altre strategie per stimolare la rigenerazione del fegato. Ad esempio, la modifica dell’FLR può essere realizzata operativamente in un’operazione in due fasi chiamata “ALPPS”. Nella prima fase, il parenchima epatico viene tagliato oltre alla legatura di un ramo della vena porta. Di conseguenza, la futura frazione di fegato conservato (FLR) si ipertrofizza molto più rapidamente rispetto alla sola occlusione della vena porta. Il secondo passo è il completamento dell’epatectomia. Il vantaggio di questa tecnica è principalmente che la probabilità di resezione completa del tumore è ancora più alta con questa strategia rispetto ai metodi convenzionali PVE e PVL. Tuttavia, ci sono prove che il tessuto epatico a crescita rapida non funziona altrettanto bene del tessuto epatico a crescita lenta. Inoltre, c’è una certa preoccupazione per il tasso di complicanze ancora piuttosto elevato di questa operazione.
Ulteriori sviluppi per la manipolazione del tessuto epatico sono attualmente in fase di ricerca. Queste includono, ad esempio, l’innovativa doppia embolizzazione della vena, in cui la vena epatica omolaterale viene embolizzata per via percutanea oltre alla PVE (Fig. 2) . Con questo metodo, si può ottenere un’ipertrofia della FLR altrettanto rapida, simile a quella dell’ALPPS, senza dover eseguire due interventi.
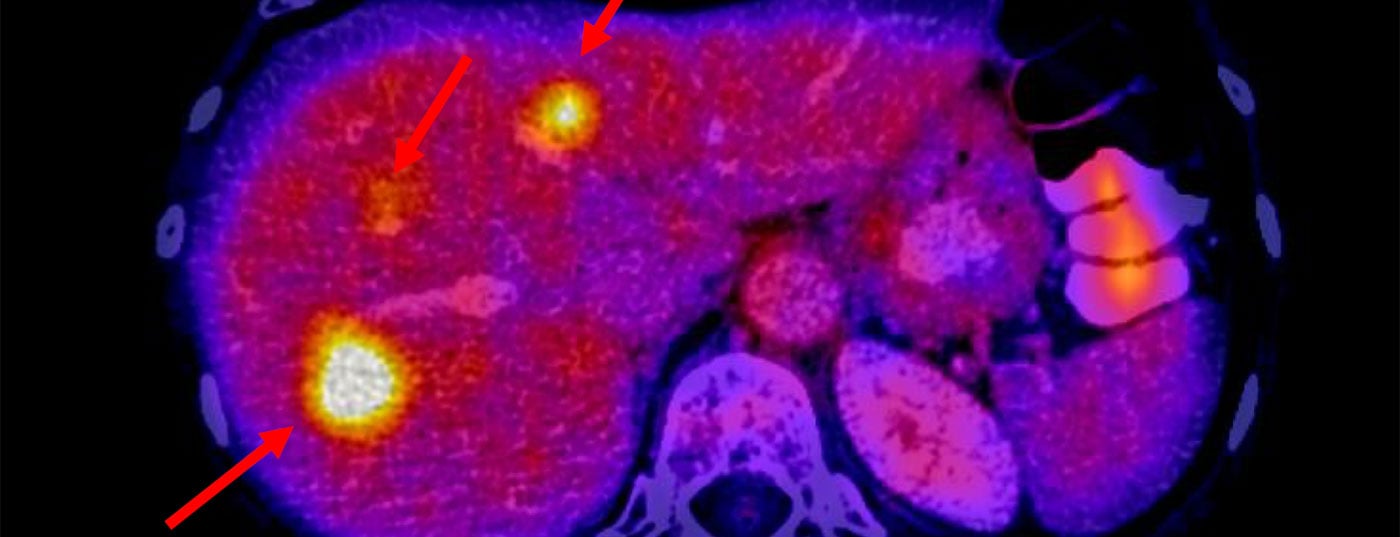
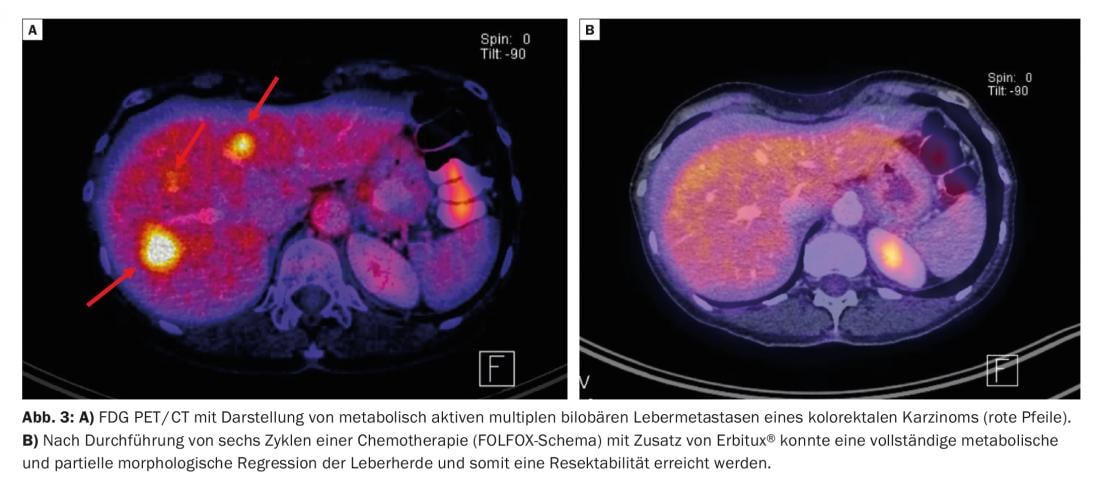
Le metastasi possono essere ridotte?
I pazienti con metastasi estese sono spesso candidati inadatti alla resezione epatica a causa dell’estensione e della distribuzione anatomica dei focolai epatici. Oltre a manipolare il volume del fegato, la chemioterapia può portare a un’impressionante riduzione delle dimensioni (il cosiddetto downsizing) del carico tumorale iniziale. Le terapie combinate oncologiche utilizzate in questo caso, come il regime FOLFOX, sono spesso combinate con anticorpi per i fattori di crescita tumorale, come cetuximab e bevacizumab (Fig. 3). Queste terapie fanno sì che più del 50% dei pazienti inizialmente non resecabili diventino poi resecabili grazie a questo ridimensionamento.
Messaggi da portare a casa
- L’asportazione delle metastasi epatiche del colon-retto può essere curativa e prolunga la sopravvivenza. La determinazione della resecabilità si basa su criteri oncologici e tecnico-chirurgici.
- Dal punto di vista oncologico, la possibilità di un’asportazione completa di tutte le aree tumorali vitali, sia intra che extraepatiche, deve essere data con intento curativo.
- Da un punto di vista tecnico, la resecabilità è data se tutte le metastasi vitali possono essere rimosse con margini di resezione microscopicamente negativi e un volume epatico residuo sufficiente. In questo caso, il team interdisciplinare curante ha a disposizione una serie di procedure consolidate, che mirano sia a manipolare la riserva epatica che a ridurre l’infestazione tumorale. Anche in caso di metastasi estese al fegato, si cerca una terapia curativa.
Ulteriori letture:
- Adams RB, et al: Selezione per la resezione epatica delle metastasi epatiche colorettali: dichiarazione di consenso degli esperti. HPB (Oxford) 2013 Feb; 15(2): 91-103.
- Folprecht G, et al: Risposta tumorale e resecabilità secondaria delle metastasi epatiche del colon-retto dopo la chemioterapia neoadiuvante con cetuximab: lo studio randomizzato di fase 2 CELIM. Lancet Oncol 2010 Jan; 11(1): 38-47.
- Guiu B, et al: La deprivazione venosa epatica prolungata prima dell’epatectomia maggiore induce un aumento marcato e molto rapido della futura funzione del residuo epatico. Eur Radiol 2017 Aug; 27(8): 3343-3352.
- Ironside N, et al: Revisione sistematica degli esiti perioperatori e di sopravvivenza delle resezioni epatiche con e senza embolizzazione preoperatoria della vena porta per le metastasi colorettali. HPB (Oxford) 2017 Jul; 19(7): 559-566.
- Jones RP, et al: Effetto del processo decisionale specialistico sulle strategie di trattamento delle metastasi epatiche colorettali. Br J Surg 2012 Sep; 99(9): 1263-1269.
- Nordlinger B, et al: Chemioterapia perioperatoria con FOLFOX4 e chirurgia rispetto alla sola chirurgia per le metastasi epatiche resecabili da cancro del colon-retto (studio 40983 dell’Intergruppo EORTC): uno studio randomizzato controllato. Lancet 2008; 371: 1007-1016.
- Olthof PB, et al: Scintigrafia epatobiliare per valutare la funzione epatica nell’associazione della divisione del fegato e della legatura della vena porta per l’epatectomia stadiata: il volume del fegato sovrastima la funzione epatica. Chirurgia 2017 ottobre; 162(4): 775-783.
- Ruers T, et al; EORTC Gastro-Intestinal Tract Cancer Group: Ablazione con radiofrequenza combinata con trattamento sistemico rispetto al solo trattamento sistemico nei pazienti con metastasi epatiche colorettali non resecabili: uno studio randomizzato di fase II dell’Intergruppo EORTC (EORTC 40004). Ann Oncol 2012 Oct; 23(10): 2619-2626.
- Tomlinson JS, et al: La sopravvivenza effettiva a 10 anni dopo la resezione delle metastasi epatiche colorettali definisce la cura. J Clin Oncol 2007 Oct 10; 25(29): 4575-4580.
- Schadde E, et al: Epatectomia ALPPS monosegmento: estensione della resecabilità mediante ipertrofia rapida. Chirurgia 2015; 157: 676-689.
- Schadde E, et al: Previsione della mortalità dopo lo stadio 1 dell’ALPPS: un’analisi di 320 pazienti del Registro Internazionale ALPPS. Annali di chirurgia 2015; 262: 780-785.
PRATICA GP 2018; 13(1): 20-23
InFo ONCOLOGIA & EMATOLOGIA 2019; 7(6): 17-19.