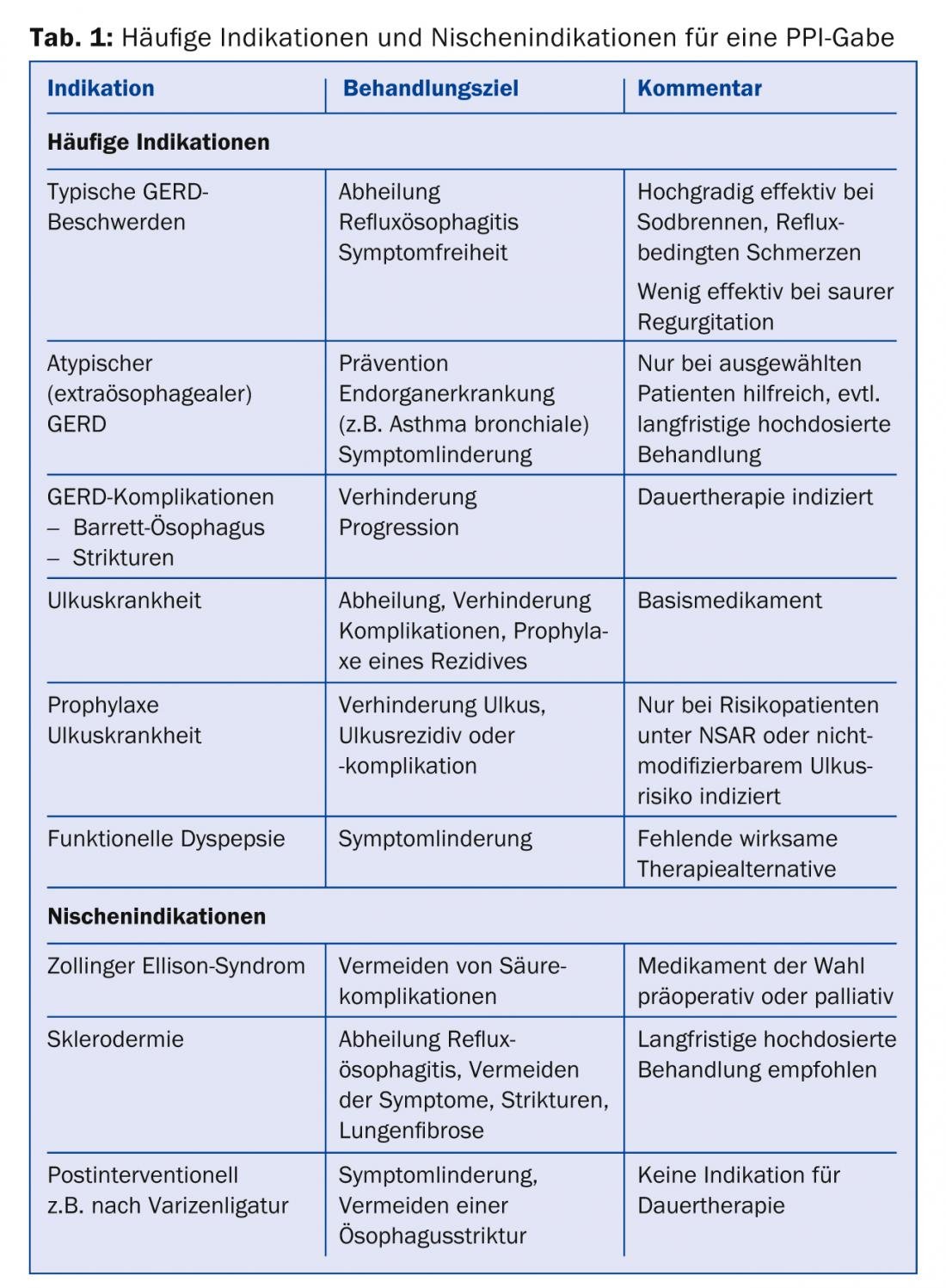
Gli inibitori della pompa protonica (IPP) sono la terza classe di farmaci più utilizzata nella pratica clinica attuale in tutto il mondo, dopo gli antibiotici e le statine (Tab. 1). Questi inibitori acidi altamente potenti curano e migliorano efficacemente i sintomi della malattia da reflusso gastro-esofageo e di altre patologie causate dai succhi gastrici. Tuttavia, con l’uso diffuso e spesso a lungo termine degli IPP, anche i piccoli rischi per la salute sono rilevanti. Il compito del medico di famiglia è quello di evitare l’uso inutile degli IPP senza privare i pazienti con buone indicazioni di questo farmaco efficace. Il seguente articolo offre una panoramica delle indicazioni e dei rischi in uso.
Qual è il ruolo dei PPI nel trattamento della malattia da reflusso gastroesofageo (GERD)? Gli IPP sono la classe di farmaci più efficace per la GERD. Grazie alla disponibilità degli IPP, la maggior parte dei pazienti con i sintomi tipici del reflusso (ad esempio, bruciore di stomaco, rigurgito acido) può essere trattata bene dal medico di famiglia o addirittura con l’automedicazione con gli IPP [1,2]. Ulteriori chiarimenti o il rinvio a un gastroenterologo sono necessari solo per il trattamento dei sintomi di reflusso refrattari. È inoltre importante verificare sempre l’indicazione per la terapia a lungo termine con gli IPP nei pazienti senza sintomi. Spesso la dose può essere ridotta e fino al 40% dei pazienti rimane libero da sintomi per mesi, anche dopo aver interrotto gli IPP [3]. Questa percentuale può essere ulteriormente aumentata somministrando farmaci su richiesta (ad esempio, antiacidi, alginati come Gaviscon®) [2].
Con i PPI, l’esofagite da reflusso e le stenosi peptiche, che sono complicazioni della GERD, possono guarire o essere prevenute [4]. L’esofago di Barrett è un’altra conseguenza clinicamente importante della GERD e può portare all’adenocarcinoma dell’esofago in circa lo 0,2% all’anno [5]. Studi caso-controllo suggeriscono che i PPI possono prevenire la progressione verso il carcinoma in questo caso [6]. I risultati del grande studio ASPECT, prospettico e randomizzato, saranno presto disponibili per chiarire definitivamente questa domanda [7]. A nostro avviso, la terapia a lungo termine con un PPI è già indicata per l’esofago di Barrett.
Le manifestazioni extra-esofagee della GERD comprendono tosse cronica, raucedine e sensazione di globus. In questi pazienti, la relazione tra il reflusso e i sintomi è meno chiara e i disturbi ORL (sinusite cronica, ‘gocciolamento post-nasale’) e le malattie pneumologiche possono contribuire alla patogenesi [1]. I tassi di successo del trattamento con PPI sono di conseguenza più modesti [8].
Se i sintomi persistono, il medico di base ha due opzioni: il trattamento empirico con PPI al doppio della dose standard per otto-dodici settimane, e la misurazione oggettiva del pH per determinare la gravità dell’esposizione all’acido esofageo e la relazione tra reflusso e sintomi extra-esofagei [8]. Il paziente deve essere coinvolto in questa decisione. È importante che in caso di trattamento con IPP non riuscito o di misurazione negativa del pH, l’IPP venga interrotto.
Indicazione ulcera peptica
Gli IPP sono i farmaci di base per il trattamento dell’ulcera peptica e delle sue complicanze. Pertanto, nella situazione di emorragia, la neutralizzazione del pH gastrico può attivare la coagulazione del sangue e limitare il sanguinamento [9]. Inoltre, la maggior parte delle ulcere gastriche o duodenali guarisce entro poche settimane dalla terapia con PPI [10]. I PPI fanno anche parte della terapia di eradicazione dell’H. pylori. Anche in questo caso, l’IPP deve essere interrotto dopo che l’ulcera è guarita e il fattore di rischio è stato eliminato. La terapia continua con PPI per la profilassi dello sviluppo dell’ulcera o della recidiva è indicata nei pazienti ad alto rischio che assumono FANS e nei pazienti che hanno già avuto un’ulcera e presentano fattori di rischio non modificabili [11].
Indicazione dispepsia funzionale
I PPI sono efficaci nel trattamento della dispepsia funzionale (FD) in alcuni casi e possono anche essere somministrati empiricamente in assenza di sintomi di allarme e dopo aver escluso l’infezione da H. pylori. Purtroppo, il tasso di successo dei PPI per questa indicazione è basso (“number needed to treat”, NNT: 10, rispetto a NNT 2-3 per i sintomi tipici del reflusso) [12].
Mancata risposta alla somministrazione di PPI
Non tutti i sintomi del GERD rispondono al trattamento con PPI. Ad esempio, i sintomi del reflusso gastrico possono essere ridotti con i farmaci, nel migliore dei casi. Anche per i pazienti con i sintomi tipici del GERD (Fig. 1), l’effetto degli IPP non è perfetto.

Sebbene fino al 90% di tutti i pazienti risponda al trattamento, circa un terzo di tutti i pazienti in terapia con PPI a lungo termine non diventa completamente libero dai sintomi [1,2]. Inoltre, un gran numero di pazienti con GERD assume farmaci da banco oltre agli IPP [13]. Suggeriamo un approccio sequenziale in caso di risposta insoddisfacente alla PPI (Fig. 2) .

Se i sintomi sono tipici con gli IPP, si dovrebbe provare un preparato a base di alginato (ad esempio Gaviscon®). Gli alginati formano uno strato viscoso davanti all’ingresso dell’esofago e possono quindi prevenire il reflusso acido e non acido [14]. Inoltre, il PPI potrebbe essere cambiato e/o la dose aumentata.
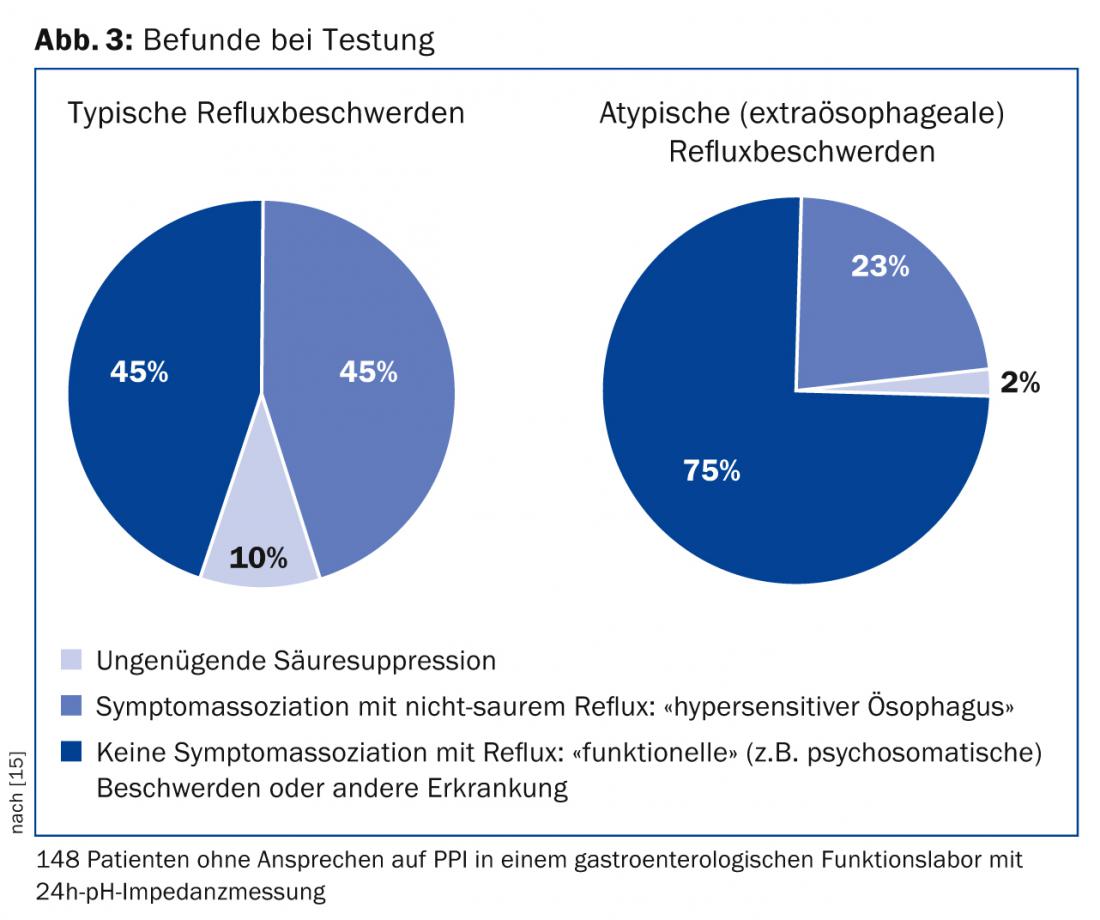
In caso di sintomi atipici o di mancata risposta agli IPP nonostante le misure citate, è necessario eseguire ulteriori diagnosi gastroenterologiche. La prima indicazione è una gastroscopia per escludere un’ulcera peptica o una neoplasia. Se i risultati sono normali, è necessario eseguire una manometria e una misurazione dell’impedenza del pH per identificare la causa dei disturbi [1,2]. Per esempio, solo circa la metà di tutti i pazienti con “disturbi da reflusso” che vengono indirizzati a un laboratorio funzionale gastroenterologico hanno una malattia da reflusso oggettivabile (Fig. 3) [15]. Per esempio, i pazienti che soffrono di acalasia vengono inizialmente diagnosticati erroneamente come pazienti con GERD in circa il 40% dei casi e trattati con PPI [16].
Una diagnosi esatta dei disturbi refrattari consente poi un trattamento mirato (figg. 2 e 3) . Se il reflusso acido viene confermato come causa del disturbo, la soppressione dell’acido deve essere ulteriormente ottimizzata. In assenza di reflusso patologico, ma in presenza di un’associazione sintomatica tra reflusso e bruciore di stomaco o dolore toracico (il cosiddetto “esofago sensibile”), gli alginati possono essere somministrati in aggiunta ai PPI. Inoltre, la sensibilità viscerale può essere modulata con antidepressivi a basso dosaggio (ad esempio, amitriptilina 25 mg nocté). In assenza di malattia da reflusso e di associazione di sintomi, il PPI può essere interrotto. Al contrario, si deve trattare un disturbo della motilità o un disturbo psicosomatico, se necessario, oppure si devono fare ulteriori diagnosi.
Rischio di rimbalzo acido
Secondo l’esperienza clinica, il bruciore di stomaco spesso peggiora brevemente dopo la sospensione di un PPI. I sintomi del reflusso possono scatenarsi dopo la somministrazione di PPI a breve termine anche in soggetti precedentemente privi di sintomi [17]. Questo effetto di rimbalzo può rendere difficile per i pazienti interrompere gli IPP e contribuire alla somministrazione inutile di IPP [18]. Se si verificano sintomi di rimbalzo dopo l’interruzione, l’IPP deve essere ridotto gradualmente (ad esempio, una settimana di dose singola standard, una settimana di dose dimezzata standard). Inoltre, consigliamo gli antiacidi o gli alginati, se necessario, durante lo svezzamento.
Altri rischi di un PPI
Contrariamente ai timori iniziali, i PPI non aumentano il rischio di cancro gastrico [19]. Molti studi caso-controllo hanno trovato un’associazione del rischio di cancro con l’indicazione al trattamento con PPI (GERD, ulcera gastrica, ecc.) ma non con l’uso di PPI [20]. D’altra parte, un IPP può mascherare i sintomi del cancro gastrico. Pertanto, la gastroscopia è obbligatoria in caso di sintomi di allarme prima del trattamento empirico con IPP e deve sempre essere presa in considerazione di nuovo se l’effetto degli IPP è insufficiente.
La perdita dell’effetto antibatterico dell’acido gastrico aumenta il rischio di enterite infettiva con shigella e salmonella, tra gli altri [21]. Soprattutto per i pazienti ospedalizzati o bisognosi di cure, l’aumento del rischio di infezioni da Clostridium difficile (HR 2,5) o di polmonite (HR 1,4) è probabilmente rilevante [22]. Nei pazienti con cirrosi epatica, gli IPP non sono in grado di arrestare l’emorragia da varici esofagee, ma possono aumentare il rischio di peritonite batterica spontanea, per cui in genere non dovrebbero essere somministrati in questo gruppo di pazienti [23].
Le considerazioni fisiologiche suggeriscono anche una riduzione dell’assorbimento di vitamina B12, calcio, magnesio e ferro con l’uso di IPP [24]. Con l’attuale abbondanza di alimenti con quantità sufficienti di vitamine e minerali, questo rischio è raramente rilevante [24]. Tuttavia, in caso di disturbi compatibili con la malnutrizione di queste sostanze citate, il monitoraggio deve essere generoso. Gli studi di associazione hanno anche identificato l’osteoporosi come possibile complicazione dell’uso di PPI a lungo termine (HR per il rischio di frattura 1,25) [25]. È importante notare che tutti questi rischi sono stati riscontrati in studi caso-controllo, ma non in grandi studi prospettici randomizzati, e quindi non sono esenti dall’influenza di possibili confondenti.
Le interazioni farmacologiche degli IPP e gli altri rischi sono riassunti nella Tabella 2. Un’interazione farmacologica inizialmente temuta tra IPP e clopidogrel è stata smentita da studi recenti. Gli IPP, ad esempio, comportano il rischio teorico di blocco del clopidogrel, in quanto possono bloccare il citocromo CYP2C19, importante per l’attivazione del clopidogrel. Tuttavia, in un ampio studio in cui i pazienti hanno ricevuto clopidogrel da solo o insieme a un IPP dopo l’inserimento di uno stent coronarico, il rischio di eventi avversi cardiaci era esattamente lo stesso in entrambi i bracci di studio, con un minor numero di eventi avversi gastrointestinali con l’IPP [26]. Pertanto, l’interazione farmacologica tra IPP e clopidogrel non è rilevante nella pratica. Questo discorso mostra come le considerazioni fisiologiche possano occasionalmente trarre in inganno e come il confonditore “morbilità” possa fingere interazioni rilevanti negli studi caso-controllo.

Un’indicazione adeguata è fondamentale
Nonostante tutti i vantaggi, è importante mettere in guardia dall’uso acritico di questi farmaci: Le stime indicano che il 25-75% di tutti i pazienti trattati con gli IPP non ha un’indicazione adeguata. In una serie di casi tipici di pazienti ricoverati, il 20% assume PPI al momento del ricovero, il 40% inizia a prendere un PPI durante il ricovero e il 50% trova un PPI nella cartella clinica di dimissione [27]. Questo avviene quasi sempre senza un’indicazione adeguata e senza che nella lettera di dimissione venga suggerito un momento per la revisione dei farmaci. È quindi probabile che i pazienti ricoverati frequentemente vengano trattati frequentemente con gli IPP anche in ambito ambulatoriale [28]. È proprio questo gruppo di pazienti che è vulnerabile ai problemi sopra menzionati.
CONCLUSIONE PER LA PRATICA
- L’introduzione degli IPP come inibitori sicuri ed efficaci della secrezione acida ha avuto un grande impatto positivo sul trattamento di molte malattie gastro-esofagee.
- Tuttavia, bisogna mettere in guardia da un uso acritico di questi farmaci.
- Resta il compito responsabile del medico di famiglia di interrompere l’IPP “non necessario”, di continuare l’IPP “necessario”, utile, alla dose efficace più bassa e, soprattutto, di distinguere con certezza le due situazioni.
A RETENIR
- L’introduzione sul mercato degli IPP come inibitori sicuri ed efficaci della secrezione di acidi ha avuto un importante effetto positivo sul trattamento di diverse malattie dell’intestino e dell’esofago.
- Tuttavia, è necessario adottare una misura di protezione contro l’uso irrazionale di questi farmaci.
- C’è un alto livello di responsabilità da parte del medico di famiglia nell’interrompere i PIP “inutili”, nel continuare i PIP “necessari” alle dosi più efficaci e, soprattutto, nel differenziare con precisione le due situazioni.
Prof. Dr. med. Mark Fox
PD Dr. med. Benjamin Misselwitz
Daniel Pohl, MD
Letteratura:
- Fox M, Forgacs I: Malattia da reflusso gastro-esofageo. BMJ 2006; 332: 88-93.
- Tytgat GN, et al: Nuovo algoritmo per il trattamento della malattia da reflusso gastro-esofageo. Aliment Pharmacol Ther 2008 Feb 1; 27(3): 249-256.
- Schwizer W, et al: L’effetto dell’infezione e dell’eradicazione dell’Helicobacter pylori nei pazienti con malattia da reflusso gastroesofageo: uno studio multicentrico a gruppi paralleli, in doppio cieco, controllato con placebo. United European Gastroenterology Journal 2013; 1(4): 226-235.
- Castell DO, et al: Esomeprazolo (40 mg) rispetto a lansoprazolo (30 mg) nel trattamento dell’esofagite erosiva. Am J Gastroenterol 2002; 97(3): 575-583.
- de Jonge PJ, et al: L’esofago di Barrett: epidemiologia, rischio di cancro e implicazioni per la gestione. Gut 2014 Jan; 63(1): 191-202.
- Singh S, et al: Farmaci acido-soppressivi e rischio di adenocarcinoma esofageo nei pazienti con esofago di Barrett: una revisione sistematica e una meta-analisi. Gut 2013 Nov 12.
- Jankowski J, Sharma P: Articolo di revisione: approcci al trattamento dell’esofago di Barrett – il ruolo degli inibitori della pompa protonica e altri interventi. Aliment Pharmacol Ther 2004 Feb; 19 Suppl 1: 54-59.
- Sifrim D, Barnes N: Tosse cronica correlata a GERD: come identificare i pazienti che risponderanno alla terapia antireflusso? J Clin Gastroenterol. 2010 Apr; 44(4): 234-236.
- Sung JJ, et al: Esomeprazolo per via endovenosa per la prevenzione del sanguinamento ricorrente da ulcera peptica: uno studio randomizzato. Ann Intern Med 2009 Apr 7; 150(7): 455-464.
- Leodolter A, et al: Una meta-analisi che confronta i tassi di eradicazione, guarigione e recidiva nei pazienti con ulcera gastrica o duodenale associata all’Helicobacter pylori. Aliment Pharmacol Ther 2001 dic; 15(12): 1949-1958.
- Chan FK, Sung JJ: Ruolo dei soppressori di acidi nella profilassi dei danni da FANS. Best Pract Res Clin Gastroenterol 2001 Jun; 15(3): 433-445. PubMed PMID: 11403537.
- Wang WH, et al: Effetti degli inibitori della pompa protonica sulla dispepsia funzionale: una meta-analisi di studi randomizzati controllati con placebo. Clin Gastroenterol Hepatol. 2007 Feb; 5(2): 178-185; quiz 40.
- Hungin AP, et al: Revisione sistematica: Modelli di utilizzo degli inibitori della pompa protonica e aderenza nella malattia da reflusso gastroesofageo. Clin Gastroenterol Hepatol 2012 Feb; 10(2): 109-116.
- Sweis R, et al: Soppressione del reflusso postprandiale da parte di un alginato che forma zattere (Gaviscon Advance) rispetto ad un semplice antiacido, documentata dalla risonanza magnetica e dal monitoraggio della pH-impedenza: valutazione meccanicistica in volontari sani e studio randomizzato, controllato, in doppio cieco in pazienti con reflusso. Aliment Pharmacol Ther 2013 Jun; 37(11): 1093-1102.
- Mainie I, et al: Reflusso acido e non acido nei pazienti con sintomi persistenti nonostante la terapia soppressiva dell’acido: uno studio multicentrico che utilizza il monitoraggio combinato impedenza-pH ambulatoriale. Gut. 2006 ottobre; 55(10): 1398-1402.
- Kessing BF, Bredenoord AJ, Smout AJ: Errata diagnosi di malattia da reflusso gastroesofageo nell’acalasia. Clin Gastroenterol Hepatol. 2011 Dic; 9(12): 1020-1024.
- Reimer C, et al.: La terapia con inibitori della pompa protonica induce sintomi correlati all’acido in volontari sani dopo la sospensione della terapia. Gastroenterologia 2009; 137(1): 80-87.
- Howden CW, Kahrilas PJ: Editoriale: quanto è “difficile” interrompere il trattamento con gli IPP? Am J Gastroenterol 2010 Jul; 105(7): 1538-1540.
- Klinkenberg-Knol EC, et al: Trattamento a lungo termine con omeprazolo nella malattia da reflusso gastroesofageo resistente: efficacia, sicurezza e influenza sulla mucosa gastrica. Gastroenterologia 2000 Apr; 118(4): 661-669.
- Tamim H, et al.: Associazione tra uso di farmaci acido-soppressivi e rischio di cancro gastrico. Uno studio caso-controllo nidificato. Drug Saf 2008; 31(8): 675-684.
- Leonard J, Marshall JK, Moayyedi P: Revisione sistematica del rischio di infezione enterica nei pazienti che assumono soppressione acida. Am J Gastroenterol 2007 Sep; 102(9): 2047-2056; quiz 57.
- Howell MD, et al: Soppressione iatrogena dell’acido gastrico e rischio di infezione nosocomiale da Clostridium difficile. Arch Intern Med. 2010 10 maggio; 170(9): 784-790.
- Goel GA, et al: Aumento del tasso di peritonite batterica spontanea nei pazienti cirrotici che ricevono la soppressione farmacologica dell’acido. Clin Gastroenterol Hepatol 2012 Apr; 10(4): 422-427.
- Pohl D, et al.: Abbiamo bisogno di acido gastrico? Digestione 2008; 77(3-4): 184-197.
- Gray SL, et al: Uso di inibitori della pompa protonica, frattura dell’anca e variazione della densità minerale ossea nelle donne in postmenopausa: risultati della Women’s Health Initiative. Arch Intern Med 2010 10 maggio; 170(9): 765-771.
- Bhatt DL, et al: Clopidogrel con o senza omeprazolo nella malattia coronarica. N Engl J Med 2010 Nov 11; 363(20): 1909-1917.
- Yachimski PS, et al: Inibitori della pompa protonica per la profilassi del sanguinamento nosocomiale del tratto gastrointestinale superiore: effetto delle linee guida standardizzate sulla pratica di prescrizione. Arch Intern Med. 2010 10 maggio; 170(9): 779-783.
- Arasaradnam RP, et al: Audit della prescrizione di inibitori della pompa protonica (PPI): vengono seguite le linee guida NICE? Clin Med 2003 luglio-agosto; 3(4): 387-388.
PRATICA GP 2014; 9(6): 26-31