[1-3]Lo studio comparativo SEQUENCE, recentemente pubblicato sul New England Journal of Medicine (NEJM), ha confrontato i due inibitori dell’interleuchina (IL)-23 e dell’IL-12/-23, risankizumab (SKYRIZI®) e ustekinumab, in pazienti affetti da malattia di Crohn (CD). [4-6] Analisi supplementari post-hoc sono state presentate alla Settimana Europea di Gastroenterologia (UEGW ) che si terrà dal 12 al 15 ottobre 2024 a Vienna. [4-6] I risultati mostrano, tra l’altro, che risankizumab raggiunge tassi di efficacia numericamente superiori rispetto a ustekinumab, indipendentemente dalla durata della malattia, porta a una maggiore normalizzazione dei biomarcatori e migliora significativamente la qualità della vita.
Nello studio SEQUENCE, oltre 500 pazienti affetti da CD con fallimento del trattamento sono stati randomizzati a uno o più inibitori del TNF e trattati in aperto per 48 settimane con risankizumab (N=255) o ustekinumab (N=265) [1]. < Entrambi gli endpoint primari sono stati raggiunti: con la remissione clinica dopo 24 settimane (CDAI 150) Risankizumab non era inferiore a ustekinumab (58,6% contro 39,5%). < Per quanto riguarda il secondo endpoint primario, la remissione endoscopica (SES-CD ≤ 4 e ≥ 2 punti più bassi rispetto al basale) dopo 48 settimane, risankizumab era significativamente superiore a ustekinumab (31,8% vs. 16,2%, p 0,001) [1]. Inoltre, il tasso complessivo di eventi avversi legati al trattamento (TEAEs) è stato basso in entrambi i gruppi (27,9% vs. 21,9%) e non sono stati identificati nuovi segnali di sicurezza con risankizumab rispetto agli studi pivotal [1, 7, 8]. Analisi supplementari post-hoc dello studio comparativo sono state presentate alla UEGW 2024.
Tassi di efficacia numericamente più elevati con risankizumab, indipendentemente dalla durata della malattia, con il massimo beneficio dopo aver iniziato il trattamento il più presto possibile [4].
Il trattamento precoce con terapie avanzate come i biologici può rallentare o interrompere la progressione della CD, migliorando così la qualità di vita dei pazienti ed evitando ulteriori complicazioni come fistole, ricoveri e interventi chirurgici [9, 10].<2 Jahre, 2-5 Jahre, 5-10 Jahre,>L’efficacia di risankizumab rispetto a ustekinumab in pazienti con diversa durata della malattia ( 10 anni) è stata ora analizzata in un’analisi post-hoc dello studio SEQUENCE [4]. Il risultato: indipendentemente dalla durata della malattia, una percentuale numericamente maggiore di pazienti ha raggiunto la remissione clinica ed endoscopica dopo 24 e 48 settimane con risankizumab, nonché la risposta endoscopica e la remissione clinica ed endoscopica senza steroidi dopo 48 settimane [4]. In particolare, nella risposta endoscopica a 48 settimane, più pazienti con risankizumab hanno raggiunto l’endpoint* rispetto al gruppo ustekinumab( <2 anni: 52,8 % vs. 25,6 %, P <0,5 %). 25,6 %, P < 0,05; 2-5 anni: 40,7 % vs. 12,9 %, P < 0,001; 5-10 anni: 46,3 % vs. 25,4 %, P < 0,05; >10 anni: 44,1 % vs. 23,6 %, P < 0,01). I pazienti con risankizumab e una durata della malattia di ≤2 anni hanno tratto i maggiori benefici, il che supporta un intervento precoce nei pazienti con CD [4].

Fig. 1: Tassi di normalizzazione più elevati dei biomarcatori hs-CRP e FC con risankizumab. Analisi post-hoc, tutti i valori p sono nominali e non controllati per molteplicità. FC = calprotectina fecale; hs-CRP = proteina C-reattiva ad alta sensibilità; Q8W = ogni 8 settimane; RZB = risankizumab; s.c. = sottocutaneo; UST = ustekinumab. Adattato da [5]
I biomarcatori sottolineano la superiorità di risankizumab rispetto a ustekinumab [5]
Nell’analisi dei dati primari dello studio SEQUENCE, i pazienti con risankizumab hanno mostrato una maggiore riduzione della calprotectina fecale (FC) e della proteina C-reattiva (CRP) rispetto a ustekinumab [1]. [11] La FC e la CRP sono i due biomarcatori più comunemente utilizzati nella CD e servono come marcatori oggettivi dell’infiammazione intestinale. [11] La normalizzazione di FC e CRP è pertanto raccomandata come obiettivo terapeutico a medio termine nelle linee guida STRIDE II. Un’analisi post-hoc dello studio SEQUENCE presentato all’UEGW mostra che questo obiettivo è raggiungibile per un numero maggiore di pazienti con risankizumab rispetto a ustekinumab: in questo caso, una percentuale maggiore di pazienti con risankizumab con FC elevata (>1) ha raggiunto la normalizzazione di FC e CRP:Nei pazienti con FC elevata (>250 mg/kg) o CRP (>5 mg/L) all’inizio dello studio, una percentuale maggiore di pazienti con risankizumab ha raggiunto la normalizzazione del valore di CRP alle settimane 24 e 48 e la normalizzazione del valore di FC alle settimane 8, 24 e 48 (p nominale < 0,01) (Fig. 1). 1) [5]. Inoltre, un numero maggiore di pazienti con risankizumab ha raggiunto la normalizzazione dei biomarcatori in combinazione con la remissione clinica e la risposta endoscopica rispetto ai pazienti che hanno ricevuto ustekinumab (Fig. 2) [5].
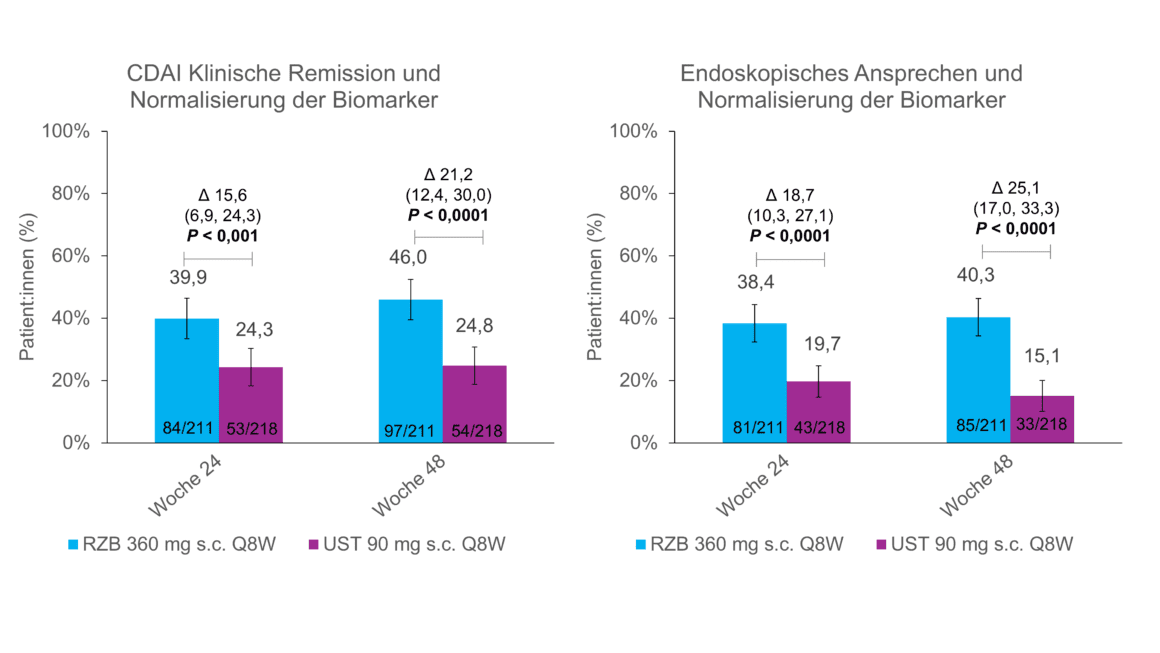
Fig. 2: Remissione clinica o risposta endoscopica + normalizzazione dei biomarcatori più frequente con risankizumab. Analisi post-hoc, tutti i valori p sono nominali e non controllati per molteplicità. CDAI = Crohn’s Disease Activity Index; Q8W = ogni 8 settimane; RZB = risankizumab; s.c. = sottocutaneo; UST = ustekinumab. Adattato da [5]
Miglioramento della qualità di vita e dei sintomi psicologici con risankizumab [6]
Un’ulteriore analisi post-hoc ha esaminato il miglioramento della qualità di vita e ha analizzato vari risultati riferiti dai pazienti (PRO), come IBDQ e SF-36v2 [6]. Una percentuale significativamente maggiore di pazienti trattati con risankizumab ha mostrato miglioramenti clinicamente significativi nella remissione dell’IBDQ (settimana 24: 52,5% vs. 30,9%; settimana 48: 49,8% vs. 33,2%) e miglioramenti nel SF-36v2 fisico e mentale, rispetto al gruppo ustekinumab [6]. Inoltre, una percentuale significativamente inferiore di pazienti del gruppo risankizumab ha riportato sintomi come affaticamento, depressione o ansia alle settimane 24 e 48 rispetto ai pazienti con ustekinumab [6].
Conclusione
[4-6]Lo studio SEQUENCE è il primo studio testa a testa in CD a dimostrare la superiorità di un biologico rispetto a un altro biologico [1]. Le analisi approfondite post-hoc qui presentate sottolineano ora anche la migliore efficacia di risankizumab in pazienti con diverse durate della malattia, in termini di biomarcatori e qualità di vita. Questi risultati sottolineano il potenziale beneficio di un intervento precoce con risankizumab per migliorare ulteriormente il controllo della malattia e la qualità della vita dei pazienti.
*Analisi post-hoc, tutti i valori p sono nominali e non controllati per molteplicità.
Abbreviazioni: CDAI = Crohn’s Disease Activity Index; IBDQ = Inflammatory Bowel Disease Questionnaire; PRO = Patient-reported outcome (esito riferito dal paziente); SES-CD = Simple Endoscopic Score for Crohn’s Disease (punteggio endoscopico semplice per la malattia di Crohn); SF-36v2 = Short Form-36versione 2; TEAE = Treatment-emergent adverse events (eventi avversi emergenti dal trattamento).
Fonte:
Settimana Europea di Gastroenterologia (UEGW) 2024, dal 12 al 15 ottobre 2024, Vienna (Austria). Relazione: Dr. sc. nat. Stefanie Jovanovic
Brevi informazioni tecniche SKYRIZI®

CH-SKZG-240100 11/2024 Questo articolo è stato realizzato con il sostegno finanziario di AbbVie AG, Alte Steinhauserstrasse 14, Cham.
Questo articolo è stato pubblicato in tedesco.
Letteratura
1 Peyrin-Biroulet, L., et al, Risankizumab versus ustekinumab per la malattia di Crohn da moderata a grave. N Engl J Med, 2024. 391(3): p. 213-223.
2. riassunto attuale delle caratteristiche del prodotto di SKYRIZI® (risankizumab) Malattia di Crohn su www.swissmedicinfo.ch.
3. riassunto attuale delle caratteristiche del prodotto di ustekinumab su www.swissmedicinfo.ch.
4 Peyrin-Biroulet, L., et al. Efficacia di Risankizumab rispetto a Ustekinumab in base alla durata della malattia nei pazienti con malattia di Crohn da moderata a grave: un’analisi post-hoc dello studio di fase 3 SEQUENCE . PP0589. Poster presentato alla UEGW; Vienna, 12-15 ottobre 2024.
5 Colombel JF, et al: Riduzione dei biomarcatori infiammatori e miglioramento dei risultati clinici ed endoscopici con Risankizumab rispetto a Ustekinumab nei pazienti con malattia di Crohn da moderata a grave: un’analisi post-hoc dello studio SEQUENCE di fase 3. PP0588. Poster presentato alla UEGW; Vienna, 12-15 ottobre 2024.
6 Loftus EV, et al: Miglioramento della qualità di vita correlata alla salute nei pazienti con malattia di Crohn da moderata a grave trattati con Risankizumab rispetto a Ustekinumab nello studio di fase 3B SEQUENCE. MP677. Poster presentato alla UEGW; Vienna, 12-15 ottobre 2024.
7 D’Haens, G., et al, Risankizumab come terapia di induzione per la malattia di Crohn: risultati degli studi di induzione di fase 3 ADVANCE e MOTIVATE. Lancet, 2022. 399(10340): p. 2015-2030.
8 Ferrante, M., et al, Risankizumab come terapia di mantenimento per la malattia di Crohn da moderatamente a gravemente attiva: risultati dello studio di mantenimento FORTIFY, multicentrico, randomizzato, in doppio cieco, controllato con placebo, fase 3 di ritiro.Lancet, 2022 (10340): p. 2031-2046.
9 Danese, S., G. Fiorino e L. Peyrin-Biroulet, Intervento precoce nella malattia di Crohn: verso gli studi di modifica della malattia. Gut, 2017. 66(12): p. 2179-2187.
10 Ben-Horin, S., et al, Efficacia dei farmaci biologici nella malattia infiammatoria intestinale di breve durata rispetto a quella di lunga durata: una revisione sistematica e una meta-analisi dei dati del singolo paziente di studi controllati randomizzati. Gastroenterologia, 2022 (2): p. 482-494.
11 Turner, D., et al, STRIDE-II: un aggiornamento dell’iniziativa Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) dell’Organizzazione Internazionale per lo Studio delle IBD (IOIBD): determinare gli obiettivi terapeutici per le strategie Treat-to-Target nelle IBD. Gastroenterologia, 2021. 160(5): p. 1570-1583.
Le referenze possono essere richieste dagli specialisti all’indirizzo medinfo.ch@abbvie.com.