L’anemia è un fattore di rischio per la morbilità e la mortalità materna e fetale. L’anemia da carenza di ferro lieve e la carenza di ferro senza anemia possono essere trattate peroralmente durante la gravidanza. Per via endovenosa, Ferinject® viene utilizzato come standard.
L’anemia è la malattia più comune in gravidanza e nel puerperio. L’incidenza dell’anemia nelle prime fasi della gravidanza in Svizzera è di circa il 18,5% [1]. Fino al 6,2% ha un’anemia da carenza di ferro e il 12,3% delle donne ha un’anemia dovuta ad altre cause [1]. Nonostante il buon stato nutrizionale in Svizzera, fino al 32% di tutte le donne in gravidanza presenta una carenza di ferro a causa della riduzione del ferro immagazzinato prima della gravidanza e dell’assorbimento limitato del ferro. Un’altra importante causa di anemia sono le emoglobinopatie. La migrazione in Europa ha portato ad un aumento significativo di emoglobinopatie, talassemie e anemie infettive in Svizzera.
Definizione di anemia in gravidanza e nel post-partum
Secondo l’Organizzazione Mondiale della Sanità (OMS), l'”anemia in gravidanza” è definita come emoglobina (Hb) inferiore a 110 g/l durante tutta la gravidanza. I Centri per il Controllo delle Malattie (CDC) definiscono l'”anemia in gravidanza” come Hb inferiore a 110 g/l nel primo e terzo trimestre e inferiore a 105 g/l nel secondo trimestre [2]. I diversi valori soglia possono essere spiegati dall’aumento dell’emodiluizione nel secondo trimestre. Si distingue tra anemia gravidica lieve (Hb 100-110 g/l), moderata (Hb 80-100 g/l) e grave (Hb <80 g/l) [2]. Secondo l’OMS, si parla di “carenza di ferro senza anemia” se il valore della ferritina è inferiore a 15 μg/l e il valore dell’emoglobina è nella norma. L'”anemia post-partum” è definita come Hb <110 g/l nella prima settimana dopo il parto e Hb <120 g/l dalla seconda settimana dopo il parto.
Diagnostica e diagnosi differenziale
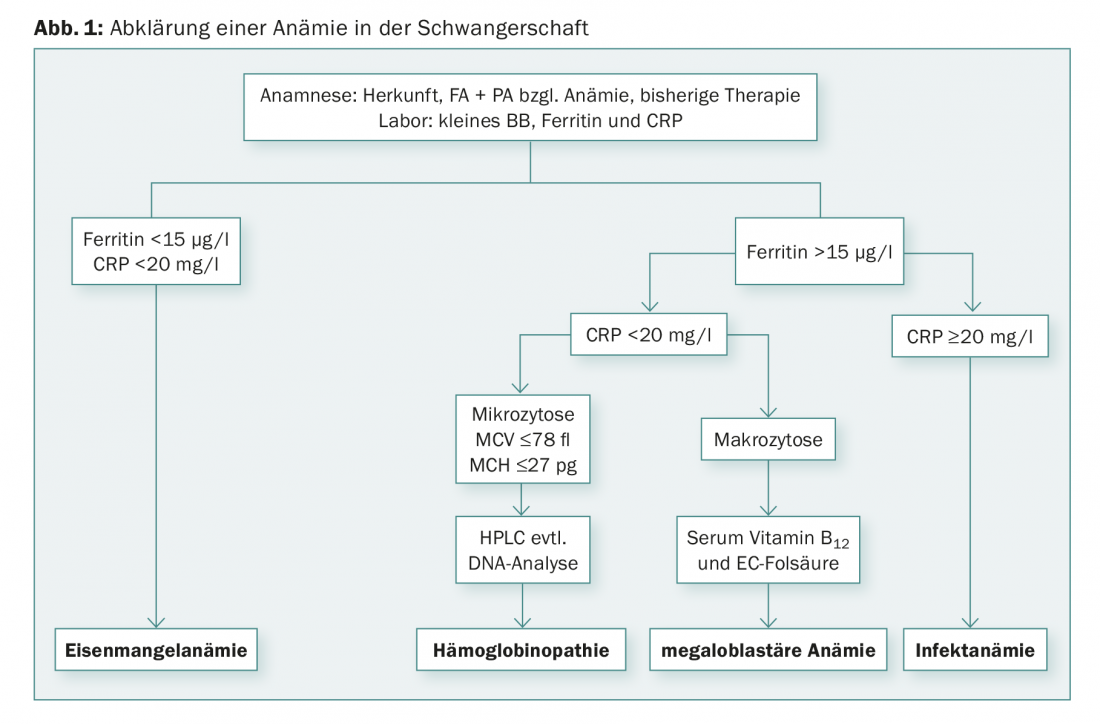
Il primo esame è il cosiddetto emocromo. Classicamente, l’anemia viene classificata in base al volume corpuscolare medio (MCV). In termini di diagnosi differenziale, si parla di anemie microcitiche (MCV ridotto), macrocitiche (MCV aumentato) e normocitiche. Per la diagnosi differenziale dell’anemia, si devono determinare CRP, ferritina, acido folico e vitamina B12 (Fig. 1) . L’attuale “gold standard” per rilevare gli stati di carenza di ferro è la determinazione dei livelli di ferritina nel plasma, che si correla bene con le riserve di ferro. Un valore di ferritina <15 µg/l è la prova di una carenza di ferro, indipendente dal valore di emoglobina [3,4]. Lo screening mediante determinazione della ferritina è consigliato nel primo trimestre. Se i valori di ferritina sono nella norma, si può praticamente escludere una carenza di ferro, a meno che non si sospetti contemporaneamente un’infezione. In questo caso, i livelli di ferritina possono essere falsamente normali, poiché l’apoferritina, simile alla proteina C-reattiva, è una proteina della fase acuta e aumenta durante le infezioni e le reazioni infiammatorie (ad esempio, nel post-operatorio). Nelle situazioni cliniche con CRP elevata, la carenza di ferro può essere rilevata utilizzando il recettore solubile della transferrina (elevato). Una macrocitosi significativa (MCV di >100 fl) indica la presenza di anemia megaloblastica. La maggior parte delle anemie megaloblastiche in gravidanza sono dovute alla carenza di acido folico, mentre le anemie da carenza di vitamina B12 sono meno comuni.
Se c’è una marcata microcitosi nell’emocromo, cioè un MCV <75 fl, un MCH <25 pg o una percentuale di microciti del >15%, con ferritina normale e CRP normale, si deve eseguire la cromatografia Hb o l’elettroforesi Hb per escludere la β-talassemia e l’emoglobinopatia [5,6]. La diagnosi di β-talassemia si effettua determinando l’HbA2, la cui percentuale è aumentata per compensare le catene β mancanti (>3,5%). Allo stesso modo, la frazione HbF può essere elevata (non obbligatoriamente). Tuttavia, se contemporaneamente è presente una carenza di ferro, la percentuale di HbA2 può essere inferiore. I pazienti con α-talassemia presentano una cromatografia dell’Hb normale; la diagnosi viene effettuata mediante test genetici, dopo aver escluso altre cause di anemia microcitica. Se la talassemia o l’emoglobinopatia sono note, è necessario chiarire anche il partner per escludere il rischio di talassemia omozigote infantile ed emoglobinopatia. Se entrambi i partner sono portatori eterozigoti di talassemia o emoglobinopatia, è indicata la diagnosi prenatale con amniocentesi o prelievo dei villi coriali.
Significato clinico
I rischi materni e fetali nel contesto dell’anemia da carenza di ferro dovrebbero essere correlati non solo al grado di anemia e all’età gestazionale, ma anche al grado di esaurimento delle riserve di ferro [7]. Le possibili conseguenze dell’anemia da carenza di ferro includono sintomi materni (pallore, affaticamento, spossatezza, vertigini, cefalea), riduzione dello stress cardiovascolare (palpitazioni, dispnea, ipotensione), aumento del rischio virale, infezioni batteriche e parassitarie, distacco prematuro della placenta, riduzione delle riserve di sangue al momento del parto e quindi aumento del rischio di emorragia post-partum e aumento del rischio di sintomi post-partum come stanchezza, problemi di allattamento e depressione. (Panoramica 1). Il feto è a maggior rischio di restrizione della crescita intrauterina, morte amniotica intrauterina, parto pretermine, morbilità neonatale in generale e ritardo nello sviluppo psicomotorio e cognitivo.

Terapia dell’anemia in gravidanza
La terapia dipende dalla causa dell’anemia. In caso di carenza di ferro o di anemia lieve da carenza di ferro, i preparati orali di ferro devono rimanere il mezzo di prima scelta; tranne nei pazienti che devono essere trattati con eritropoietina o che soffrono di malattia infiammatoria cronica intestinale [8]. Nella terapia, si utilizzano soprattutto preparati orali di ferro II e ferro III. Si differenziano per la tollerabilità, che può variare da paziente a paziente. Una buona informazione sui possibili effetti collaterali e raccomandazioni precise sull’assunzione possono essere utili per migliorare la compliance, che di solito è scarsa. Il trattamento con ferro per via orale è poco costoso ed efficace se seguito rigorosamente e per un periodo di tempo sufficientemente lungo. Tuttavia, un lungo periodo di trattamento dovuto al basso tasso di assorbimento e la comparsa di effetti collaterali compromettono l’aderenza disciplinata a tale terapia.
Se la terapia orale con ferro non ha successo o non è tollerata dal paziente, passare al trattamento con ferro per via endovenosa. Altre indicazioni per la terapia di ferro per via endovenosa in gravidanza sono: scarsa compliance, anemia grave, necessità di elevati livelli di emoglobina peripartum o di un rapido aumento dell’emoglobina (età gestazionale avanzata, aspettativa di emorragia peripartum, ad esempio placenta praevia, distensione uterina, fibroma uterino di grandi dimensioni, coagulopatia e Testimoni di Geova) (panoramica 2).
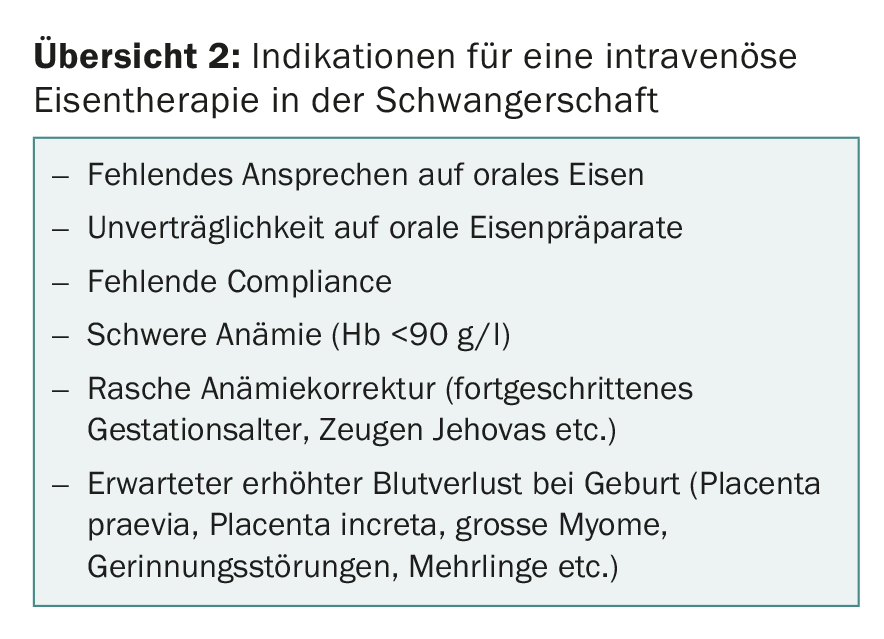
Poiché i vari studi hanno dimostrato che evitare le trasfusioni di sangue perioperatorie e postoperatorie migliora la morbilità e la mortalità, la terapia con ferro per via endovenosa ad alto dosaggio deve essere sempre presa in considerazione verso la fine della gravidanza nei parti programmati con un’elevata perdita di sangue prevista (placenta praevia, placenta increta, fibromi di grandi dimensioni, ecc.)
La somministrazione di ferro per via endovenosa è controindicata nel primo trimestre. Oggi, la terapia standard di ferro per via endovenosa in gravidanza e nel post-partum è il ferro carbossimaltosio (Ferinject®) [9,10]. I dati dimostrano che la somministrazione endovenosa di carbossimaltosio ferrico (Ferinject®) nel secondo e terzo trimestre di gravidanza è sicura quanto il saccarosio ferroso (Venofer®) in termini di effetti collaterali materni ed è meglio tollerata a dosi più elevate. Reazioni di intolleranza gravi dopo il carbossimaltosio ferrico non sono state descritte in nessuno studio. Il dosaggio viene determinato in base al livello di emoglobina e al peso corporeo. Entro due settimane, l’aumento dell’emoglobina dovrebbe essere di 10-20 g/l; se necessario, può essere somministrata una seconda infusione. L’obiettivo della terapia è un valore di emoglobina di almeno 110 g/l. In casi particolari, la terapia con ferro può essere combinata con l’eritropoietina umana ricombinante (rhEPO). Va notato che si tratta di un farmaco “off-label-use” e la copertura dei costi da parte della compagnia di assicurazione sanitaria deve essere chiarita in anticipo.
Terapia dell’anemia post-partum
Il nadir del valore di Hb postpartum si raggiunge 48 ore dopo la distribuzione primaria del volume plasmatico. Fondamentalmente, la terapia dipende dalla gravità dell’anemia e dalle condizioni della donna in travaglio. Nell’anemia lieve (Hb 95-110 g/l), si raccomanda una terapia di ferro perorale di circa 80-200 mg di ferro al giorno. In caso di anemia moderata (Hb 85-95 g/l), grave (Hb <85 g/l) e di intolleranza alla terapia di ferro perorale, si raccomanda il trattamento di ferro per via endovenosa come prima scelta. Con Hb <80 g/l, si può prendere in considerazione la somministrazione di rhEPO in aggiunta al ferro carbossimaltosio parenterale. Tuttavia, le prove dell’efficacia aggiuntiva della rhEPO in combinazione con la terapia di ferro per via endovenosa rispetto alla sola terapia di ferro per via endovenosa sono molto limitate. Se l’Hb è <60 g/l, si deve eseguire una trasfusione di sangue estraneo, a seconda dei sintomi clinici.
Messaggi da portare a casa
- La carenza di ferro è la causa più comune di anemia in tutto il mondo. Lo screening è raccomandato nel primo trimestre con la determinazione della ferritina.
- Un’altra causa importante di anemia sono le emoglobinopatie genetiche. La chiarificazione della β-talassemia e dell’emoglobinopatia viene effettuata con la cromatografia dell’emoglobina o l’elettroforesi dell’emoglobina.
- L’anemia, a seconda della sua gravità, è un fattore di rischio significativo in termini di morbilità e mortalità materna e fetale.
- In primo luogo, l’anemia da carenza di ferro lieve e la carenza di ferro senza anemia in gravidanza devono essere trattate con una terapia di ferro per via orale.
- Per la terapia di ferro per via endovenosa in gravidanza e nel puerperio, si utilizza il ferro carbossimaltosio standard (Ferinject®), che è molto ben tollerato.
Letteratura:
- Bencaiova G, Burkhardt T, Breymann C: Anemia – prevalenza e fattori di rischio in gravidanza. Eur J Intern Med 2012 Sep; 23(6): 529-533.
- Centri per il controllo delle malattie (CDC): Criteri CDC per l’anemia nei bambini e nelle donne in età fertile. MMWR Morb Mortal Wkly Rep 1989; 38(22): 400-404.
- Breyman C: Anemia da carenza di ferro in gravidanza. Expert Rev Obstet Gyn 2013; 8(6): 587-596.
- Milman N: Ferro in gravidanza – Come possiamo garantire uno stato di ferro appropriato nella madre e nel bambino? Ann Nutr Metab 2011; 59: 50-54.
- Merlo CM, Wuillemin WA: Prevalenza e cause dell’anemia in un ambulatorio di famiglia urbano. Practice 2008; 97(5): 713-718.
- Lopez A, et al: Anemia da carenza di ferro. Lancet 2016; 387(10021): 907-916.
- Breymann C: Anemia. In: Schneider H, Husslein P, Schneider KTM (eds.): Ostetricia. Springer Verlag 1999; 371-385.
- Consiglio medico svizzero: Trattamento orale o parenterale della carenza di ferro. Rapporto del 24 ottobre 2014.
- Breymann C, et al.: Lettera di esperti n. 48 del SGGG. Diagnosi e terapia dell’anemia da carenza di ferro in gravidanza e nel post-partum. Versione aggiornata dell’11.01.2017 (sostituisce la Lettera peritale n. 22).
- Breymann C, et al.; sperimentatori FER-ASAP: Carbossimaltosio ferrico vs. ferro orale nel trattamento delle donne in gravidanza con anemia da carenza di ferro: uno studio internazionale, open-label, randomizzato e controllato (FER-ASAP). J Perinat Med 2017 May 24; 45(4): 443-453.
InFo ONCOLOGIA & EMATOLOGIA 2018; 6(2): 28-32.











