I bambini e gli adolescenti affetti da psoriasi e/o artrite psoriasica spesso soffrono molto. Soprattutto quando i sintomi sono gravi, la qualità della vita delle persone colpite e delle loro famiglie è spesso significativamente ridotta. Per questa popolazione di pazienti, le terapie sistemiche efficaci e tollerabili sono una componente importante della gestione individuale della malattia.
Il secukinumab si lega alla citochina interleuchina-17A (IL-17A) e inibisce l’interazione con il suo recettore. In questo modo, il principio attivo dispiega effetti antinfiammatori e immunomodulanti. Cosentyx® (secukinumab) è stato approvato per gli adulti in Svizzera dal 2015 per il trattamento sistemico della psoriasi a placche e ora ha ricevuto anche l’approvazione per il trattamento dell’artrite psoriasica. Recentemente, l’anticorpo anti-IL17A ha dimostrato di essere un’opzione terapeutica efficace e sicura nei pazienti pediatrici con psoriasi. In questa popolazione di pazienti, è necessario ampliare lo spettro terapeutico. “Vivere con la psoriasi è impegnativo e può essere molto stressante per i bambini e i giovani”, afferma Randy Beranek, Presidente e CEO della National Psoriasis Foundation [1]. “L’ampliamento delle opzioni terapeutiche per questa popolazione di pazienti è un passo nella giusta direzione per ridurre il carico di malattia della psoriasi a placche” [1].
EMA e Swissmedic: autorizzazione di Cosentyx® per la psoriasi a placche giovanile
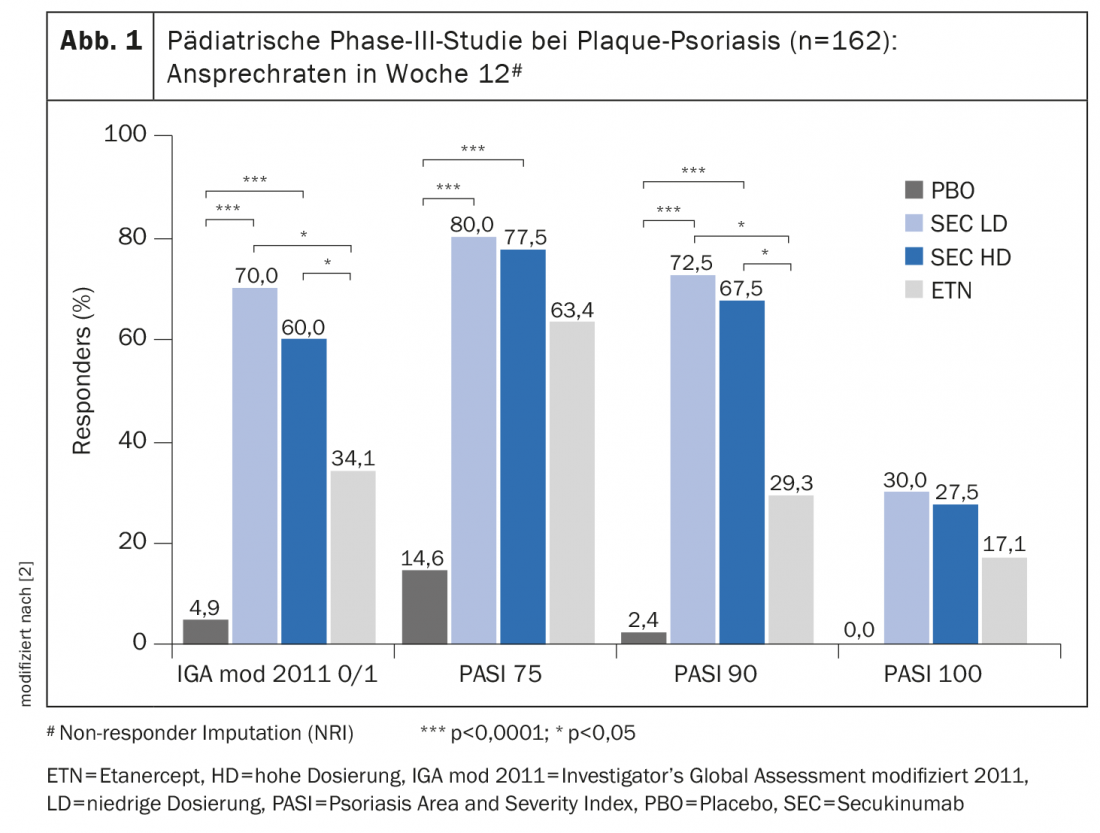
Nel trattamento di bambini e adolescenti, è particolarmente importante raggiungere il miglior equilibrio possibile tra i benefici e i rischi di una terapia sistemica. Il secukinumab è stato studiato in uno studio clinico randomizzato in doppio cieco (NCT02471144) su 162 bambini e adolescenti di età compresa tra 6 e <18 anni con psoriasi a placche grave [2]. Il secukinumab ha ottenuto un’efficacia significativamente migliore rispetto al placebo e all’etanercept (riquadro). La sicurezza del secukinumab è stata analizzata in questo e in un altro studio di fase III. Il secondo studio è stato uno studio in aperto su 84 pazienti (età compresa tra 6 e <18 anni) con psoriasi a placche da moderata a grave [1]. Il profilo di sicurezza riportato in questi due studi su un totale di 2874 anni-paziente era coerente con i segnali di sicurezza del secukinumab riportati nei pazienti adulti con psoriasi a placche [3]. “Nello studio pediatrico pivotal, la maggior parte dei pazienti trattati con Cosentyx® ha ottenuto una pelle priva di lesioni o quasi, con un profilo di sicurezza coerente con i precedenti studi clinici sugli adulti. A causa della natura sistemica di questa malattia, Cosentyx® è una gradita opzione di trattamento complementare per le famiglie che devono affrontare questa difficile condizione”, ha dichiarato John Browning, MD, Professore aggiunto di Pediatria e Dermatologia, University of Texas Health Science Center, San Antonio (USA) [1].

In Svizzera, l’estensione dell’indicazione per il trattamento della psoriasi a placche nei bambini e negli adolescenti a partire dai 6 anni di età è avvenuta nel gennaio 2021. Questa decisione fa seguito all’approvazione della Commissione Europea del secukinumab per il trattamento di prima linea della psoriasi a placche da moderata a grave nei bambini e negli adolescenti, avvenuta qualche mese prima. La dose raccomandata dipende dal peso corporeo (Tab. 1) e viene somministrata come iniezione sottocutanea con dosi iniziali alle settimane 0, 1, 2, 3 e 4, seguite da dosi mensili di mantenimento [3]. Ogni dose da 75 mg viene somministrata come iniezione sottocutanea di 75 mg e la dose da 150 mg viene somministrata come iniezione sottocutanea di 150 mg ciascuna.
L’FDA dà il via libera all’uso nell’artrite psoriasica giovanile (JPsA)
L’IL-17A non è solo rilevante per la patogenesi della psoriasi a placche, ma svolge anche un ruolo patogenetico chiave nell’artrite psoriasica (PsA). In Svizzera, Cosentyx® (secukinumab) è stato finora approvato solo per gli adulti con PsA che sono idonei alla terapia di sistema [3]. Poiché sono stati ottenuti notevoli successi terapeutici anche nella popolazione di pazienti pediatrici con PsA negli studi clinici di fase III, l’anno scorso è stata presentata all’Agenzia Europea dei Medicinali (EMA) una domanda di autorizzazione all’immissione in commercio per l’estensione dell’indicazione. Negli Stati Uniti, Cosentyx® è già stato approvato dalla FDA alla fine del 2021 per il trattamento di bambini e adolescenti con artrite legata all’entesite (ERA) e artrite psoriasica (PsA) [4]. Nello studio clinico pivotale JUNIPERA, è stata dimostrata una riduzione del rischio di ricadute acute e un miglioramento dell’attività della malattia sia per quanto riguarda l’ERA che la PsA nei pazienti pediatrici, per un periodo di osservazione di 2 anni, in un confronto con placebo. Il profilo di sicurezza era coerente con i segnali di sicurezza del secukinumab riportati in studi precedenti [4,5]. Cosentyx® è stato approvato dall’FDA per i bambini e gli adolescenti con ERA e PsA, rispettivamente, alla dose aggiustata per il peso di 75 mg (15-50 kg di peso corporeo) o 150 mg (>50 peso corporeo), come iniezione sottocutanea ogni 4 settimane, dopo una dose iniziale di carico. “I risultati dello studio JUNIPERA di fase III dimostrano che i pazienti pediatrici trattati con secukinumab hanno mostrato una risposta significativa per tutto il periodo dello studio. Questa approvazione è una notizia gradita per i pazienti che lottano con sintomi dolorosi come l’infiammazione delle articolazioni e il gonfiore delle dita delle mani e dei piedi”, ha dichiarato Hermine Brunner, MD, Cincinnati Children’s Hospital (USA) [4]. “I sintomi della PsA e dell’ERA possono essere angoscianti per i bambini e i giovani affetti da queste condizioni croniche e interferire con la loro vita quotidiana”, ha dichiarato Tiffany Westrich-Robertson, CEO di International Foundation for Autoimmune & Autoinflammatory Arthritis (AiArthritis). “È incoraggiante che ora ci sia un’opzione di trattamento complementare per questa popolazione di pazienti poco servita”.
Letteratura:
- “Novartis Cosentyx riceve l’approvazione della FDA per il trattamento di bambini e adolescenti con psoriasi a placche da moderata a grave”, Novartis, 01.06.2021
- Bodemer C, et al: Secukinumab dimostra un’elevata efficacia e un profilo di sicurezza favorevole nei pazienti pediatrici con psoriasi cronica a placche grave: risultati a 52 settimane di uno studio randomizzato e controllato di fase 3 in doppio cieco. J Eur Acad Dermatol Venereol 2021; 35: 938-947. doi: 10.1111/jdv.1700
- Compendio svizzero dei farmaci, https://compendium.ch, (ultimo accesso 07.04.2022)
- “Novartis Cosentyx® riceve l’approvazione della FDA per il trattamento di bambini e adolescenti con artrite legata all’entesite e artrite psoriasica”, Novartis, 23.12.2021
- Menter A, et al: Linee guida congiunte dell’American Academy of Dermatology-National Psoriasis Foundation per la gestione e il trattamento della psoriasi nei pazienti pediatrici. J Am Acad Dermatol 2020; 82(1): 161-201.
PRATICA DERMATOLOGICA 2022; 32(2): 36-37