Le opzioni di trattamento per i pazienti affetti da psoriasi nell’infanzia e nell’adolescenza sono molto più limitate rispetto allo spettro di trattamenti per gli adulti. Ma anche i pazienti pediatrici possono beneficiare di un trattamento mirato. Ciò è dimostrato, tra l’altro, dai corrispondenti dati degli studi clinici sul secukinumab. Anche i dati a lungo termine della fase di estensione degli studi di registrazione sono stati convincenti.
L’approvazione UE del secukinumab nei pazienti pediatrici si è basata sui risultati di un programma di studi di fase III, in cui il secukinumab ha portato a una guarigione rapida e duratura delle lesioni cutanee nei partecipanti allo studio di età compresa tra 6 e <18 anni con psoriasi a placche da moderata a grave [1]. Il farmaco biologico non solo si è dimostrato efficace, ma è stato anche generalmente ben tollerato [2,3]. Il profilo di sicurezza corrispondeva a quello dei pazienti adulti affetti da psoriasi.
| Terapia mirata per la psoriasi a placche giovanile |
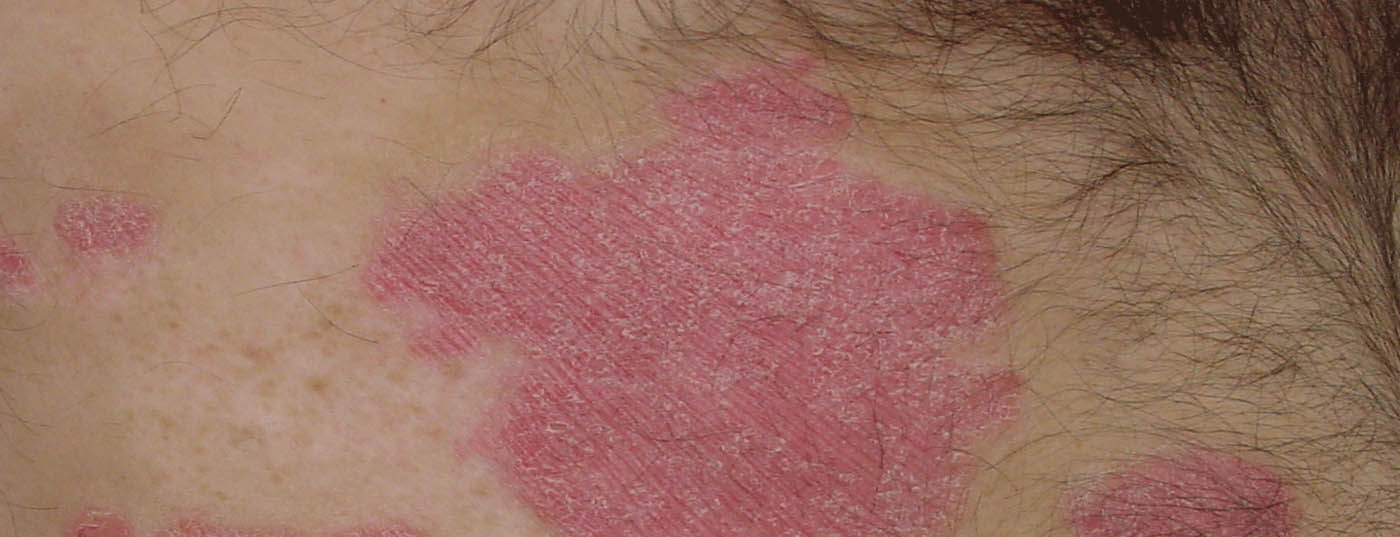
| [8–12]Circa l’1% dei bambini e degli adolescenti è affetto da psoriasi a placche. [8–12]La psoriasi è spesso associata a comorbidità metaboliche, cardiovascolari, gastrointestinali e psicologiche e a una qualità di vita significativamente ridotta. Nei pazienti pediatrici, si ritiene che l’impatto della psoriasi sulla qualità della vita sia simile a quello dell’asma o dell’artrite [7]. |
| [8–12]Mentre sono disponibili molte terapie efficaci e ben tollerate per il trattamento della psoriasi negli adulti, le opzioni terapeutiche per i pazienti pediatrici e adolescenti sono molto più limitate.
[13]Ciò è dovuto almeno in parte alla mancanza di prevedibilità della risposta alle opzioni terapeutiche approvate per gli adulti [8]. Diversi agenti biologici mirati sono stati recentemente approvati nell’UE per il trattamento della psoriasi a placche pediatrica, tra cui il secukinumab (Cosentyx®), un antagonista dell’IL-17A le cui proprietà farmacologiche sono state ampiamente studiate. [14]L’IL-17 è un’importante citochina proinfiammatoria coinvolta nella patogenesi della psoriasi, e l’IL-17A è upregolata nella pelle psoriasica lesionale e non lesionale. |
Risposta clinica sostenuta per un periodo di trattamento di 2 anni.
Il primo degli studi di fase III ha incluso pazienti pediatrici ai quali era stata diagnosticata una psoriasi cronica a placche grave da almeno tre mesi e che erano idonei alla terapia sistemica [2]. Al basale, i partecipanti allo studio avevano un punteggio PASI* di ≥20, un punteggio IGA# di 4 e un coinvolgimento della superficie corporea (BSA**) di ≥10%. L’età media era di 13,5 anni, la maggior parte (77,2%) aveva ≥12 anni. La BSA totale media era del 40% e la durata media della psoriasi a placche era di 5,22 anni. L’artrite psoriasica in comorbilità era presente nell’8,6% dei pazienti [2]. < < < I pazienti sono stati randomizzati in diversi gruppi di dosaggio in base al peso corporeo (bw): basso dosaggio (LD): 75 mg per bw 50 kg e 150 mg per bw ≥50 kg, alto dosaggio (HD): 75 mg per bw 25 kg, 150 mg per bw 25-50 kg e 300 mg per bw ≥50 kg. Nel braccio di trattamento di confronto, è stato somministrato etanercept (s.c) 0,8 mg/kg di peso corporeo (fino a un massimo di 50 mg).
* PASI = Psoriasis Area Severity Index # IGA = Investigator’s Global Assessment Modified 2011 ** BSA = Superficie corporea
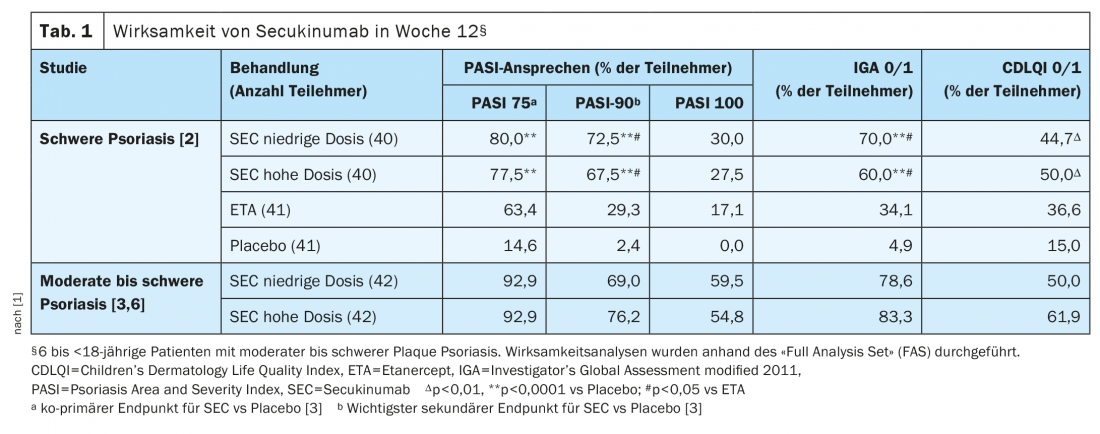
L’efficacia clinica del secukinumab era già evidente alla settimana 4. Alla settimana 12, i tassi di risposta PASI-75, IGA 0/1 e PASI-90 erano significativamente più alti sia con il secukinumab a basso che ad alto dosaggio rispetto al placebo (Tabella 1) . Rispetto a etanercept, il secukinumab (LD e HD) ha mostrato tassi di risposta IGA 0/1 e PASI-90 significativamente più elevati e tassi di risposta PASI-75 e PASI-100 numericamente più elevati alla settimana 12 (Tab. 1). <Nei pazienti con peso corporeo ≥25-50 kg, i tassi di risposta PASI-75/90/100 e IGA 0/1 alla settimana 12 erano numericamente più elevati con il secukinumab ad alto dosaggio (n=15) rispetto ai gruppi di secukinumab a basso dosaggio (n=17) [2]. Nello stesso periodo, i punteggi PASI medi sono migliorati rispetto al basale dell’82,9% nel gruppo secukinumab a basso dosaggio e del 79,9% nel gruppo secukinumab ad alto dosaggio, rispetto al 29,3% nel gruppo placebo e al 74,2% con etanercept [2]. Entrambi i tassi di risposta PASI e la risposta IGA 0/1 sono persistiti con il secukinumab fino alla settimana 104. Alla settimana 52, la percentuale di risposta PASI-75 era numericamente più alta con le dosi alte e basse rispetto a etanercept (87,5% e 87,5% contro 68,3%).
Tassi di risposta IGA 0/1 di oltre l’80% alla settimana 52
<18 Jahren, die seit mindestens drei Monaten von einer mittelschwer bis schwer ausgeprägten Plaque-Psoriasis betroffen waren und für eine systemische Therapie geeignet waren [3]. Einschlusskriterien waren ein PASI-Score>Il secondo degli studi clinici pivotal randomizzati e controllati comprendeva pazienti di età compresa tra 6 e 12 anni, punteggio IGA >3 e coinvolgimento della BSA >10%. Al basale, il 72,6% dei pazienti aveva una psoriasi moderata e il 27,4% una psoriasi grave. L’età media dei pazienti era di 12,6 anni e il 60,7% dei pazienti aveva un’età compresa tra 12 e <18 anni. La partecipazione media della BSA era del 30%. Anche in questo studio, i pazienti hanno ricevuto secukinumab a basso dosaggio (LD) o ad alto dosaggio (HD), a seconda del peso corporeo e della gravità della malattia. Nel sottogruppo LD, i pazienti con un peso corporeo (BW) <50 kg sono stati trattati con 75 mg e quelli con un BW ≥50 kg con 150 mg di secukinumab. Nel gruppo HD, i pazienti con un peso corporeo <25 kg hanno ricevuto una dose di secukinumab di 75 mg, quelli con un peso corporeo compreso tra 25 e <50 kg hanno ricevuto una dose di 150 mg e i pazienti con un peso corporeo ≥50 kg hanno ricevuto 300 mg.
Secukinumab è stato somministrato alle settimane 0, 1, 2, 3 e 4 e successivamente ogni 4 settimane. Per le analisi degli endpoint primari e secondari principali sono stati utilizzati i dati placebo di precedenti studi controllati su pazienti adulti e pediatrici con psoriasi a placche. L’endpoint co-primario era la percentuale di pazienti che hanno ottenuto una risposta PASI-75 e una risposta IGA 0/1 alla settimana 12 con il secukinumab rispetto al placebo (documentata da studi precedenti) [3].
Alla settimana 12, sia il secukinumab a basso che ad alto dosaggio erano superiori ai tassi di risposta al placebo di PASI-75, IGA 0/1 e PASI-90 documentati da studi precedenti. La probabilità stimata di un effetto positivo del trattamento era 1 (100%) [3]. [3,4]I tassi di risposta PASI-75 e IGA 0/1 sono aumentati fino alla settimana 24 (gruppi LD: 95,2% e 88,1%; gruppi HD: 95,2% e 92,9%) e sono rimasti fino alla settimana 52 (LD: 88,1% e 85,7%; HD: 90,5% e 83,3%). I tassi di risposta PASI 90/100 alla settimana 52 erano 76,2/52%/52,4% nel gruppo secukinumab a basso dosaggio e 83,3/69%/69,0% nel gruppo secukinumab ad alto dosaggio [4]. I tassi di risposta PASI90 alle settimane 32, 48 e 52 erano numericamente più alti nei gruppi di secukinumab ad alto dosaggio rispetto al gruppo a basso dosaggio. I tassi di risposta PASI-100 dalla settimana 32 alla settimana 52 hanno mostrato un andamento simile. Nel complesso, il secukinumab si è dimostrato efficace in tutti i sottogruppi, indipendentemente dal peso corporeo (<25 kg, da 25 a <50 kg e ≥50 kg) e dall’età (da 6 a <12 anni e da 12 a <18 anni) [5].
| Cosentyx® per i pazienti pediatrici: Ampliamento dello spettro terapeutico |
| Il secukinumab (Cosentyx®) ha dimostrato di essere un trattamento efficace per i bambini e gli adolescenti con psoriasi a placche da moderata a grave, con una tollerabilità generalmente buona. Si tratta di un’aggiunta preziosa alle limitate opzioni terapeutiche per questa popolazione di pazienti e ha ricevuto l’approvazione dell’EMA nel 2020. |
| Le terapie mirate con i biologici offrono diversi vantaggi rispetto alle terapie sistemiche convenzionali, tra cui un dosaggio meno frequente, una maggiore efficacia e una minore necessità di monitoraggio di laboratorio. |
| Come altri biologici approvati per la psoriasi vulgaris pediatrica, il secukinumab viene somministrato tramite iniezione sottocutanea.
Seguendo le istruzioni appropriate, Cosentyx® può essere somministrato da un assistente adulto utilizzando una siringa o una penna pre-riempita. A differenza di etanercept, che viene somministrato una volta alla settimana, e di adalimumab, che viene somministrato ogni 2 settimane, l’intervallo di dosaggio per il secukinumab nella terapia di mantenimento è di 4 settimane. La somministrazione meno frequente e la possibilità di trattamento domiciliare sono fattori che possono avere un effetto favorevole sull’aderenza al trattamento. |
| a [1,7] |
Profilo di sicurezza paragonabile a quello degli adulti
Il profilo di tollerabilità del secukinumab nei pazienti pediatrici era coerente con i dati di sicurezza osservati nei pazienti adulti affetti da psoriasi. Il secukinumab è stato generalmente ben tollerato, con la nasofaringite come evento avverso (AE) più comunemente riportato. I tassi di AE di particolare interesse sono stati generalmente bassi. Non sono stati identificati nuovi segnali di sicurezza durante i periodi di trattamento di 52 e 104 settimane dello studio di estensione.
Letteratura:
- Blair HA: Secukinumab: A Review in Moderate to Severe Pediatric Plaque Psoriasis. Pediatric Drugs 2021; 23: 601–608.
- Bodemer C, et al.: Secukinumab demonstrates high efficacy and a favourable safety profile in paediatric patients with severe chronic plaque psoriasis: 52-week results from a phase 3 double-blind randomized, controlled trial. J Eur Acad Dermatol Venereol 2020; 35(4): 938–947.
- Magnolo N, et al.: A phase III open-label, randomized multicenter study to evaluate efficacy and safety of secukinumab in pediatric patients with moderate to severe plaque psoriasis: 24-week results. J Am Acad Dermatol 2021; S0190-9622(21)02509-3
- Reich A, et al.: Secukinumab treatment demonstrated high efficacy and safety in paediatric patients with moderate-to-severe plaque psoriasis: 52-week results from a randomised trial [abstract no. P121 plus poster]. Pediatr Dermatol 2021; 38(Suppl. 1): 57–58.
- Szepietowski JC, et al.: Secukinumab demonstrated consistent efficacy across age and weight subgroups in pediatric patients with psoriasis: analyses from two phase 3 pediatric studies [abstract no. 78 plus poster]. In: Society for Pediatric Dermatology. 2021.
- Beissert S, et al. Secukinumab improves quality of life of paediatric patients with moderate-to-severe plaque psoriasis: 52-week results from a phase III, randomised study [abstract no. P080 plus poster]. Pediatr Dermatol. 2021;38(Suppl. 1): 43.
- Cordoro KM:. Toward optimal care of the pediatric patient with psoriasis: the new AAD-NPF management guideline. J Psoriasis Psoriatic Arthritis 2020; 5(1): 7–11.
- Nogueira M, Paller AS, Torres T: Targeted therapy for pediatric psoriasis. Paediatr Drugs 2021; 23(3): 203–212.
- Wu JJ, et al.: Treatment of psoriasis with secukinumab in challenging patient scenarios: a review of the available evidence. Dermatol Ther 2020; 10(3): 351–364.
- Menter A, et al.: Joint American Academy of Dermatology-National Psoriasis Foundation guidelines of care for the management and treatment of psoriasis in pediatric patients. J Am Acad Dermatol 2020; 82(1): 161–201.
- Eisert L, et al.: S2k guidelines for the treatment of psoriasis in children and adolescents – short version part 1. J Dtsch Dermatol Ges 2019; 17(8): 856–870.
- Haulrig MB, Zachariae C, Skov L: Off-label treatments for pediatric psoriasis: lessons for the clinic. Psoriasis (Auckl) 2021; 11: 1–20.
- Informazioni sui farmaci, www.swissmedicinfo.ch,(ultimo accesso 26 novembre 2021)
- Blauvelt A, Chiricozzi A: The immunologic role of IL-17 in psoriasis and psoriatic arthritis pathogenesis. Clin Rev Allergy Immunol 2018; 55(3): 379–390.
DERMATOLOGIE PRAXIS 2021; 31(6): 28–29