La nuova forma di somministrazione dell’inibitore dell’IL-17A approvata dall’EMA consente di somministrare il dosaggio raccomandato in una sola iniezione. Le analisi dei dati dello studio pivotale di fase IIIb MATURE sono state presentate alla World Psoriasis & Psoriatic Arthritis Conference 2021. Tra l’altro, questi dimostrano un alto livello di soddisfazione del paziente.
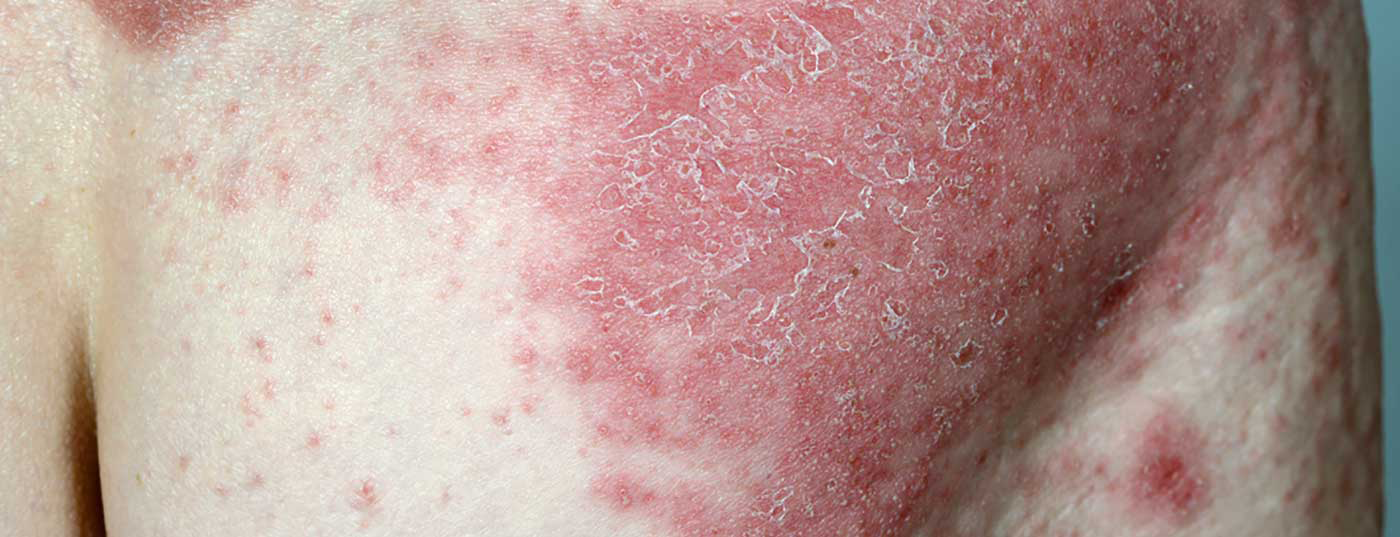
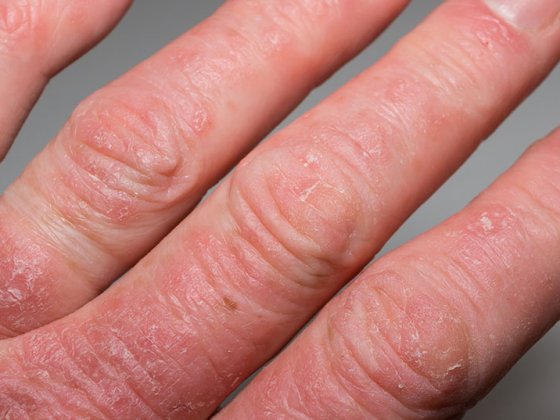
Il secukinumab è un anticorpo monoclonale che ha come bersaglio l’interleuchina (IL)-17A. L’evidenza clinica di questo biologico nel trattamento dei pazienti con psoriasi a placche e artrite psoriasica è ampiamente documentata [1,2]. La dose raccomandata di secukinumab (Cosentyx®) è di 300 mg come iniezione sottocutanea [3]. Oltre alla forma di applicazione da 150 mg, Cosentyx® è disponibile nell’UE come penna pronta all’uso da 300 mg da metà febbraio 2021 [4].
Studio MATURE: miglioramenti in vari parametri di esito
122 pazienti affetti da psoriasi sono stati randomizzati a tre bracci di studio [5]: Secukinumab 300 mg 2 mL autoiniettore (n=41), Secukinumab 300 mg 2× 1 mL siringa preriempita/PFS* (n=41) o placebo (n=40). Alla settimana 12, entrambi gli endpoint co-primari dello studio sono stati soddisfatti ed è stato dimostrato che il trattamento con secukinumab 300 mg 2 mL AI e 2× 1 mL PFS ha comportato tassi di risposta PASI75 superiori (95,1% e 83,2%, rispettivamente), nonché una pelle priva di lesioni o quasi, secondo IGA (75,6% e 68,1%, rispettivamente) rispetto al placebo (PASI75, 10,0%; IGA, 7,6%; p<0,0001). La percentuale di pazienti che hanno raggiunto DLQI 0/1 alla settimana 12 è stata simile nei gruppi di secukinumab 300 mg (2 mL AI [71,1%] e 2× 1 mL PFS [72,5%]); con il placebo questa percentuale era dell’8,1%.
* PFS=siringhe preriempite
Non sono state osservate lesioni da punture di ago in localizzazioni critiche né allergie di tipo immediato. La soddisfazione del paziente è stata valutata utilizzando, tra l’altro, il Self-Injection Assessment Questionnaire (SIAQ). Nel gruppo secukinumab 300 mg 2 mL autoiniettore, la percentuale di pazienti che hanno riferito di essere “molto soddisfatti” o “soddisfatti” è aumentata dal 31,6% (pre-SIAQ) al 78,3% (post-SIAQ) dopo la prima iniezione e ha continuato ad aumentare fino al 92,1% alla settimana 12.
Conclusione
In sintesi, il modulo di applicazione con secukinumab 300 mg 2 mL autoiniettore è stato convincente sia per la rapidità della risposta, sia per l’elevata efficacia e qualità di vita e per gli alti punteggi di soddisfazione del paziente e per il profilo di sicurezza favorevole. Nel presente studio non sono stati rilevati segnali di sicurezza nuovi o inaspettati.
Fonte: Novartis
Letteratura:
- Blauvelt A, et al: Il secukinumab è superiore all’ustekinumab nel liberare la pelle dei soggetti con psoriasi a placche da moderata a grave fino a 1 anno: risultati dello studio CLEAR. J Am Acad Dermatol. 2017; 76(1): 60-9 e9.
- Strober BE, et al: Nessun rischio elevato di depressione, ansia o suicidalità con il secukinumab in un’analisi congiunta dei dati di 10 studi clinici nella psoriasi a placche da moderata a grave. Br J Dermatol. 2018; 178(2): e105-e7.
- Informazioni sul farmaco, www.swissmedicinfo.ch (ultimo accesso 12.08.2021)
- “Prospettive in Dermatologia”. Secukinumab: 300 mg penna pronta all’uso – Alta soddisfazione del paziente”, Supplemento, Dtsch Arztebl 2021; 118(24).
- Browning J, et al: Secukinumab 300 mg in autoiniettore da 2 mL per il trattamento della psoriasi a placche: qualità di vita, usabilità, soddisfazione, sicurezza e tollerabilità, risultati dello studio randomizzato, in doppio cieco MATURE, Poster abstracts, P77, World Psoriasis & Psoriatic Arthritis Conference, Stoccolma, 30.06.-03.07.2021.
PRATICA DERMATOLOGICA 2021; 31(4): 32