L’epidemiologia dei batteri multiresistenti è cambiata in Svizzera: diminuzione significativa degli MRSA e forte aumento degli enterobatteri produttori di ESBL. I germi ESBL possono essere acquisiti attraverso il cibo (carne di pollame, verdure, ecc.). I viaggiatori di ritorno e i pazienti rimpatriati dall’estero presentano un rischio maggiore di microrganismi multiresistenti. Se non c’è risposta alla terapia antibiotica empirica, è indicata una chiarificazione microbiologica a causa della possibile resistenza. L’E. coli, compresi gli isolati ESBL, sono ancora ben sensibili alla fosfomicina e alla nitrofurantoina.
La crescente resistenza agli antibiotici minaccia molte conquiste della medicina moderna. Le autorità sanitarie dell’UE e degli Stati Uniti stimano circa 25.000 decessi all’anno attribuiti alla resistenza agli antibiotici. I pazienti sono turbati dalle notizie dei media sulle infezioni batteriche che non possono più essere trattate.
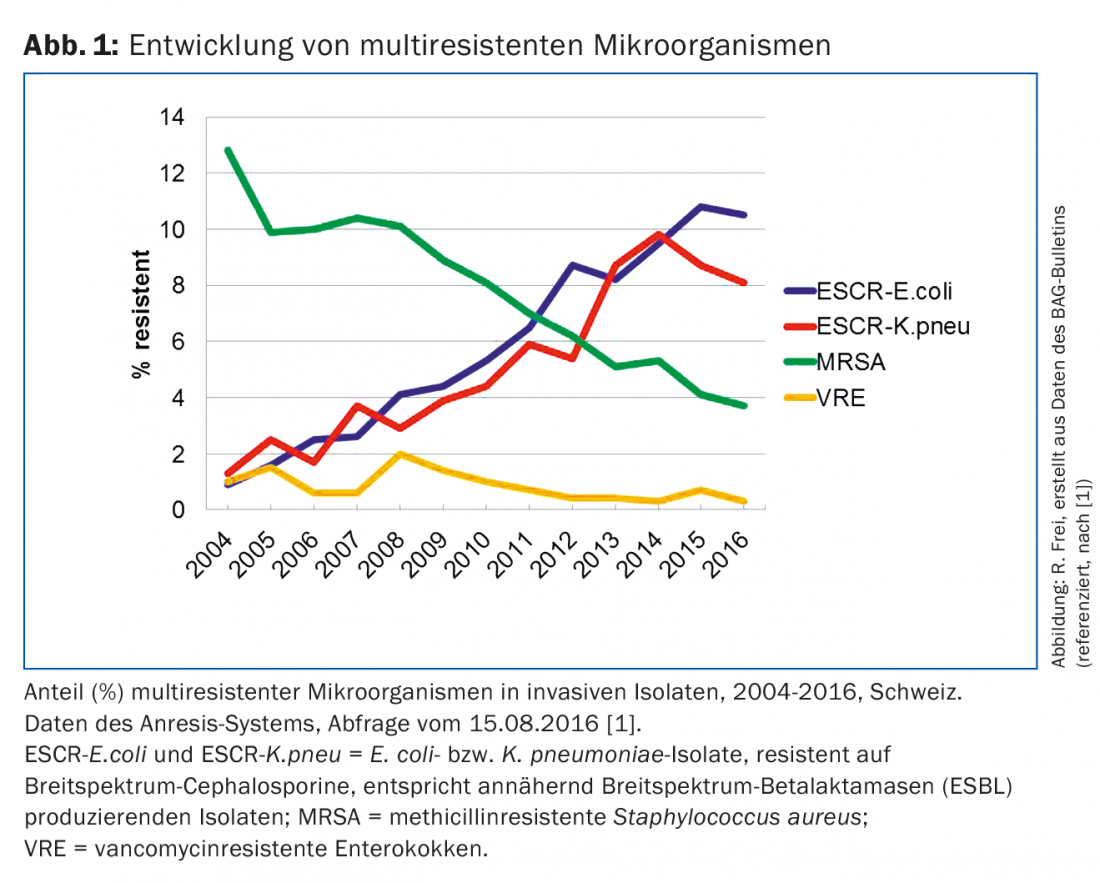
I batteri multiresistenti sono resistenti a diverse classi di antibiotici. I microrganismi multiresistenti stanno causando gravi problemi negli ospedali di tutto il mondo, tra cui vari enterobatteri, Pseudomonas aeruginosa, Acinetobacter baumannii, Staphylococcus aureus ed enterococchi. Rispetto a molti altri Paesi, la maggior parte dei tassi di resistenza in Svizzera sono più bassi. Il medico di base in questo Paese si confronta principalmente con l’Escherichia coli multiresistente , meno frequentemente con altri isolati enterobatterici resistenti e con lo S. aureus resistente alla meticillina (MRSA). Solo occasionalmente entra in contatto con altri germi multiresistenti, tra cui campylobacter resistente, gonococchi e patogeni della tubercolosi. Secondo il sistema di sorveglianza svizzero Anresis (www.anresis.ch), la prevalenza di batteri multiresistenti si è sviluppata in modo diverso negli ultimi 12 anni [1]. Mentre la percentuale di isolati MRSA è diminuita in modo significativo, gli enterobatteri con resistenza alle cefalosporine ad ampio spettro e ad altre classi di sostanze sono aumentati costantemente e fortemente (Fig. 1) [1].
MRSA
Nel 2015, poco meno del 6% degli isolati di S. aureus testati da pazienti ambulatoriali nella Svizzera tedesca erano ancora resistenti alla meticillina (MRSA). Nei Paesi dell’Europa meridionale e centrale, invece, il tasso di MRSA era significativamente più alto, ad esempio in Francia 17%, Italia 34% e Portogallo addirittura 47%. In passato, l’MRSA si è diffuso soprattutto negli ospedali e in altre istituzioni mediche (MRSA associato all’assistenza sanitaria). Da diversi anni, stanno emergendo nuovi ceppi con caratteristiche diverse, che possono causare infezioni aggressive nei pazienti ambulatoriali, anche in quelli più giovani senza precedenti contatti con il sistema sanitario (MRSA associato alla comunità). Negli ultimi anni, è stato anche osservato che le persone a stretto contatto con gli animali hanno un rischio maggiore di essere portatori di MRSA. L’MRSA è stato riscontrato in diversi animali, soprattutto cavalli e cani, ma in particolare negli animali da allevamento come polli e maiali [2]. In Svizzera, il tasso di colonizzazione da MRSA nei suini da ingrasso al macello è aumentato dal 2009, passando dal 2% al 26,5% nel 2014. Il responsabile è una linea clonale di MRSA (CC398), che si trova frequentemente anche negli animali da allevamento di altri Paesi europei. Appartiene all’MRSA “associato all’allevamento”, che colpisce in particolare le persone che hanno contatti professionali con i suini, come gli allevatori e i veterinari [3]. Altre persone a rischio di infezioni da MRSA sono le persone e i viaggiatori di ritorno dall’Europa meridionale o dagli Stati Uniti, i pazienti e i dipendenti di strutture sanitarie come i centri di riabilitazione o le case di cura con tassi di MRSA più elevati.
Misure per l’MRSA
Nei casi di infezioni aggressive della pelle e dei tessuti molli e/o di mancata risposta agli antibiotici beta-lattamici (come l’amoxicillina-acido clavulanico), si deve sospettare l’MRSA e avviare la diagnostica microbiologica. I portatori vengono individuati meglio con un tampone del naso e della gola. Dopo il contatto con il paziente nello studio medico, è importante disinfettare le mani e le superfici di contatto con preparati a base di alcol. Per un contatto più ravvicinato, ad esempio durante un esame, sono utili cappotti, maschere e guanti. I pazienti ricoverati devono essere isolati dal contatto. A causa della resistenza incrociata alle penicilline e alle cefalosporine, tutti gli antibiotici beta-lattamici perorali attualmente disponibili sono inefficaci. Clindamicina, cotrimoxazolo o linezolid (Zyvoxid®) per via orale sono adatti come monoterapia in ambulatorio nei casi di sensibilità accertata. La clindamicina deve essere utilizzata solo se il ceppo è risultato sensibile anche ai macrolidi o se è stata esclusa la resistenza all’MLSB. Per i pazienti immunosoppressi colonizzati o per gli operatori sanitari, il trattamento di decolonizzazione MRSA può essere effettuato dopo aver consultato un centro.
Enterobacteriaceae produttrici di ESBL
In Svizzera, il 7% degli isolati di Escherichia coliprovenienti dal tratto urogenitale di pazienti esterni è attualmente resistente alle cefalosporine di terza generazione (Tab. 1) . Circa il 95% di questi ceppi produce beta-lattamasi ad ampio spettro (ESBL), i cui geni sono mobili e localizzati su plasmidi. Ciò consente loro di essere trasferiti ad altre cellule, specie e generi batterici e di diffondersi rapidamente. Questi ceppi sono spesso multi-resistenti.
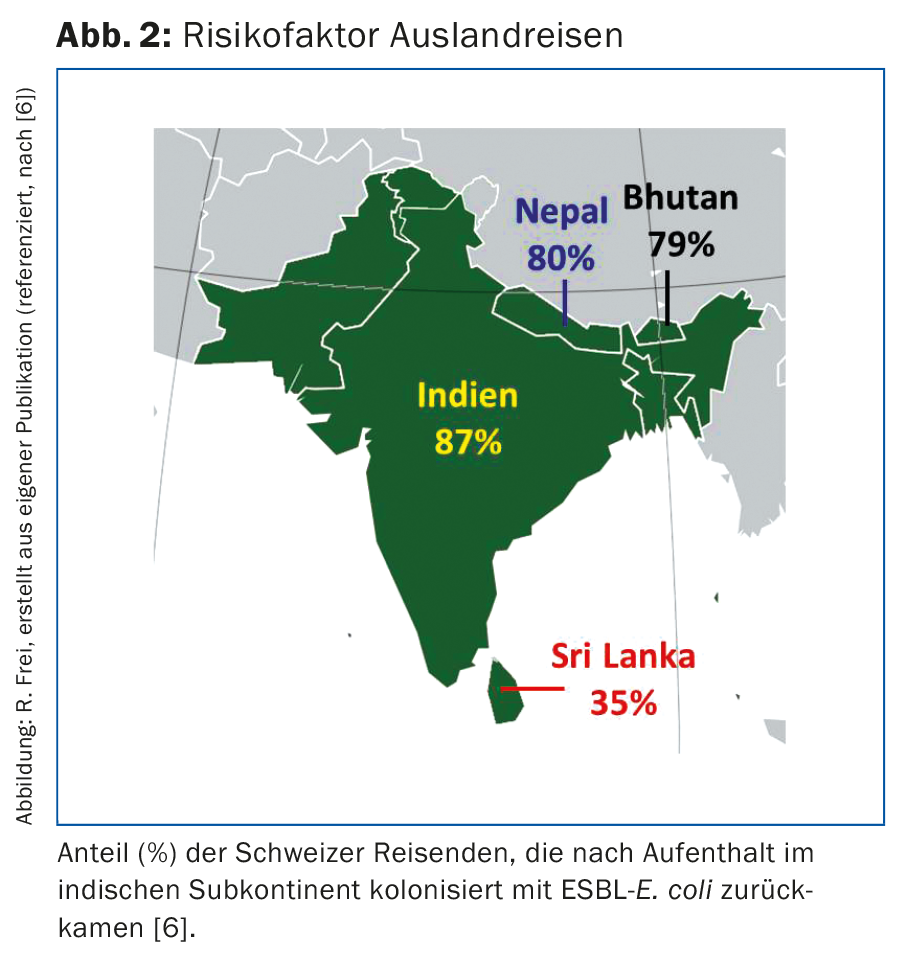
Prima del 2000, gli isolati di E. coli e Klebsiella pneumoniae che producono ESBL si trovavano principalmente nei pazienti di ospedali e case di cura. Oggi, la maggior parte delle E.coli ESBL viene acquisita al di fuori delle istituzioni mediche. I batteri produttori di ESBL si trovano in vari alimenti [2,4]. Ad esempio, le E.coli ESBL sono state rilevate nel 66% dei campioni di carne di pollo di produzione svizzera e nella carne di pollo di origine straniera addirittura nell’86% dei campioni [2]. Tali ceppi sono stati trovati anche in campioni di altro pollame, carne di maiale e di manzo, nonché in vari campioni di verdure. L’uso di antibiotici in medicina veterinaria favorisce la selezione, la moltiplicazione e la diffusione di batteri resistenti negli animali da allevamento e in agricoltura. Nel 2014, in Svizzera sono stati venduti quasi 50.000 kg di antibiotici per la medicina veterinaria [2]. Negli Stati Uniti, si utilizzano quattro volte più antibiotici per gli animali che per gli esseri umani. Anche se il riscaldamento sufficiente del cibo uccide i batteri, i germi possono essere trasmessi agli esseri umani attraverso utensili da cucina, mani e cibi crudi contaminati. Le nostre indagini hanno dimostrato che dopo la lavorazione della carne di pollo, l’8% delle lavagne delle cucine private e il 16% delle cucine degli ospedali erano contaminate da germi ESBL [5]. I guanti dei cuochi erano addirittura ESBL-positivi nel 50%. Viaggiare all’estero comporta un ulteriore rischio: L’87% dei viaggiatori svizzeri in India è stato colonizzato per via rettale con E.coli ESBL al ritorno, dopo che solo il 3% era portatore di ESBL prima della partenza (Fig. 2) [6]. Un tasso di portatori di almeno il 30% è stato riscontrato tra i viaggiatori provenienti da altri Paesi del subcontinente indiano, dell’Asia vicina e sudorientale, dell’Africa e del Sud America [7]. Altre persone a maggior rischio di ESBL sono i lavoratori dei macelli, i cuochi, i residenti delle case di riposo e delle case di cura, i pazienti di età superiore ai 65 anni o quelli con un pre-trattamento antibiotico [8].
Trattamento delle infezioni da ESBL
Le E. coli ESBL sono aumentate drasticamente anche in Svizzera [1]. Dal 2004 al 2014, la loro quota di isolati di E. coli invasivi è aumentata di dieci volte (dall’1 al 10%). Tassi simili o più alti sono stati riportati nella maggior parte dei Paesi europei, con tassi addirittura superiori al 25% in Italia, Romania e Bulgaria. L’elevata prevalenza di ESBL-former in tutte le parti della Svizzera, sia nei bambini che nei pazienti adulti e anziani, ha reso più difficile la terapia delle infezioni da E. coli e K. pneumoniae. La Tabella 1 riassume l’attuale resistenza degli isolati di E. coliprovenienti da pazienti ambulatoriali. La tabella mostra anche la multiresistenza degli isolati ESBL, con tassi di resistenza intorno al 70% ai chinoloni e al cotrimoxazolo. Al contrario, la fosfomicina, la nitrofurantoina e i carbapenemi presentano bassi tassi di resistenza, tra lo 0 e il 4%, che possono essere utilizzati terapeuticamente per le infezioni delle vie urinarie non complicate. La terapia di altre infezioni da ceppi ESBL può essere difficile e richiede un test di resistenza agli antibiotici. Per le infezioni gravi, i carbapenemi sono considerati il trattamento di scelta. Poiché l’ertapenem (Invanz®) deve essere somministrato solo una volta al giorno (1 g i.v.), può essere utilizzato anche in ambulatorio. L’effetto clinico dell’amoxicillina-acido clavulanico è incerto, anche in caso di provata suscettibilità del patogeno ESBL, tranne che nelle infezioni del tratto urinario. I portatori di ESBL sono rilevati in modo più affidabile attraverso un tampone rettale o un campione di feci, urina e campioni provenienti da siti clinicamente infetti [8]. Finora, però, nessuno schema di decolonizzazione ha purtroppo mostrato un successo a lungo termine. Poiché la trasmissione dell’E.coli ESBL si è spostata dall’ospedale alla comunità e il tasso di trasmissione negli ospedali per acuti è basso, molti ospedali per acuti hanno abbandonato il rigido isolamento da contatto per l’E.coli ESBL [8]. L’isolamento da contatto è ancora raccomandato per i pazienti colonizzati o infettati con altri enterobatteri produttori di ESBL (ad esempio, K. pneumoniae).
Incubo carbapenemasi
Oggi si conoscono più di 1000 diverse beta-lattamasi batteriche. Tra queste, le carbapenemasi sono le più temute, in quanto inattivano non solo i carbapenemi, ma praticamente tutti gli antibiotici beta-lattamici. La maggior parte dei bastoncini gram-negativi produttori di carbapenemasi sono anche estremamente multi-resistenti. Anche un test di resistenza agli antibiotici esteso spesso mostra solo 1 o 2 sostanze attive, come la colistina. A volte nessuno dei preparati disponibili sul mercato è più efficace in vitro. Finora tali ceppi si sono verificati solo sporadicamente in Svizzera e sono stati quasi sempre importati da altri Paesi. Le carbapenemasi del tipo KPC sono frequenti in Italia, Grecia, Israele e Stati Uniti e sono il tipo più comune in Svizzera fino ad oggi (circa il 45% delle carbapenemasi identificate) [9]. Le carbapenemasi di tipo NDM si sono diffuse soprattutto in India e nei Paesi balcanici e sono state portate in altri Paesi da viaggiatori, pazienti e migranti. Gli enzimi del gruppo OXA-48 sono stati introdotti nei Paesi europei dalla Turchia, dal Nord Africa e dal Medio Oriente e rappresentano circa un terzo delle carbapenemasi in Svizzera. Recentemente, è stato scoperto un meccanismo di resistenza alla colistina (MCR-1) in isolati provenienti dalla Cina e da altri Paesi, tra cui la Svizzera, che si diffonde con i plasmidi [10]. Il medico che si occupa di un paziente con batteri produttori di carbapenemasi dovrebbe consultare un reparto di malattie infettive.
Letteratura:
- Ufficio federale della sanità pubblica. Anresis.ch: Segnalazioni di microrganismi multiresistenti selezionati in Svizzera. Bollettino 2016;(35): 530.
- Ufficio federale per la sicurezza alimentare e veterinaria FSVO: ARCH-Vet. Rapporto sulla distribuzione degli antibiotici nella medicina veterinaria e sul monitoraggio della resistenza agli antibiotici negli animali da allevamento in Svizzera. Rapporto generale 2014. www.blv.admin.ch/blv/de/home/tiere/tierseuchen/tierarzneimittel/antibiotika/vertrieb.html
- Larsen J, et al: Prove di adattamento umano e di trasmissione alimentare dello Staphylococcus aureus meticillino-resistente associato al bestiame. Clin Infect Dis 2016; Sep 20. pii: ciw532. [Epub ahead of print]
- Zogg AL, et al.: Caratteristiche delle Enterobacteriaceae produttrici di ESBL e dello Staphylococcus aureus resistente alla meticillina (MRSA) isolati dalla carne di pollame cruda svizzera e importata, raccolta al dettaglio. Schweiz Arch Tierheilkd 2016; 158(6): 451-456.
- Tschudin-Sutter S, et al.: Enterobacteriaceae produttrici di β-lattamasi a spettro esteso (ESBL): una minaccia dalla cucina. Infect Control Hosp Epidemiol 2014; 35(5): 581-584.
- Kuenzli E, et al: Alti tassi di colonizzazione di Escherichia coli produttori di β-lattamasi a spettro esteso (ESBL) nei viaggiatori svizzeri in Asia meridionale – uno studio di coorte osservazionale prospettico multicentrico che analizza epidemiologia, microbiologia e fattori di rischio. BMC Infect Dis 2014; 14:528.
- Ostholm-Balkhed A, et al.: Colonizzazione fecale associata ai viaggi con Enterobacteriaceae produttrici di ESBL: incidenza e fattori di rischio. J Antimicrob Chemother 2013; 68(9): 2144-2153.
- Tissot F, et al.: Enterobacteriaceae con beta-lattamasi ad ampio spettro (ESBL) negli ospedali: nuove raccomandazioni Swissnoso 2014. www.swissnoso.ch/wp-content/uploads/pdf/v18_2_de.pdf
- Babouee B, et al: Emersione di quattro casi di Klebsiella pneumoniae portatrice di KPC-2 e KPC-3 introdotti in Svizzera, 2009-10. Euro Surveill 2011; 16(11). pii: 19817.
- Nordmann P, et al.: Resistenza alla colistina mediata da plasmidi: un’ulteriore minaccia di resistenza agli antibiotici. Clin Microbiol Infect 2016; 22(5): 398-400.
PRATICA GP 2016; 11(12): 16-19