“È più importante sapere quale persona ha una malattia che sapere quale malattia ha una persona” – questa frase è attribuita a Ippocrate, il che significa che l’antico greco conosceva già l’utilità della terapia personalizzata circa 2400 anni fa. La misura in cui tale approccio può aiutare anche in reumatologia a identificare precocemente i pazienti a rischio di RA e a trattarli in modo mirato è oggetto di studi attuali.
Il concetto di medicina “one size fits all”, cioè il ciclo di terapia standardizzato a prescindere dalle peculiarità del rispettivo paziente, naturalmente porta sempre con sé una percentuale relativamente alta di effetti collaterali (gravi) e di non rispondenti. Gli effetti della medicina personalizzata, basata sulla diagnostica molecolare (analisi dei biomarcatori) e sulla stratificazione dei pazienti basata sui biomarcatori, sono destinati a ridurre questi problemi e ad aumentare il tasso di pazienti che rispondono.
L’elenco dei farmaci per i quali è obbligatorio un test genetico in Germania si estende per 29 pagine sul sito web dell’Associazione tedesca delle aziende farmaceutiche basate sulla ricerca (vfa). Le malattie reumatiche non sono ancora presenti in questo elenco. Per il Prof. Dr. Andrea Rubbert-Roth della Clinica di Reumatologia dell’Ospedale Cantonale di San Gallo, questa è una chiara prova che il tema della medicina personalizzata non è ancora riuscito ad affermarsi nel campo della reumatologia.
È noto che, oltre ai fattori ambientali come il fumo, le polveri e le fibre tessili, esiste anche una predisposizione genetica all’artrite reumatoide (RA). Già nel 2007, un’ampia analisi di dati con 14.000 pazienti e 3.000 soggetti di controllo in 7 malattie ha mostrato che nel caso della RA con HLA e PTPN22, si distinguono due geni. Il Prof. Rubbert-Roth ha ricordato l’ipotesi chiamata Epitopo Condiviso (SE), secondo la quale gli alleli HLA-DRB1 associati alla RA codificano una sequenza comune di aminoacidi nella terza regione ipervariabile della catena DRβ1.
I pazienti SE-positivi traggono maggiori benefici
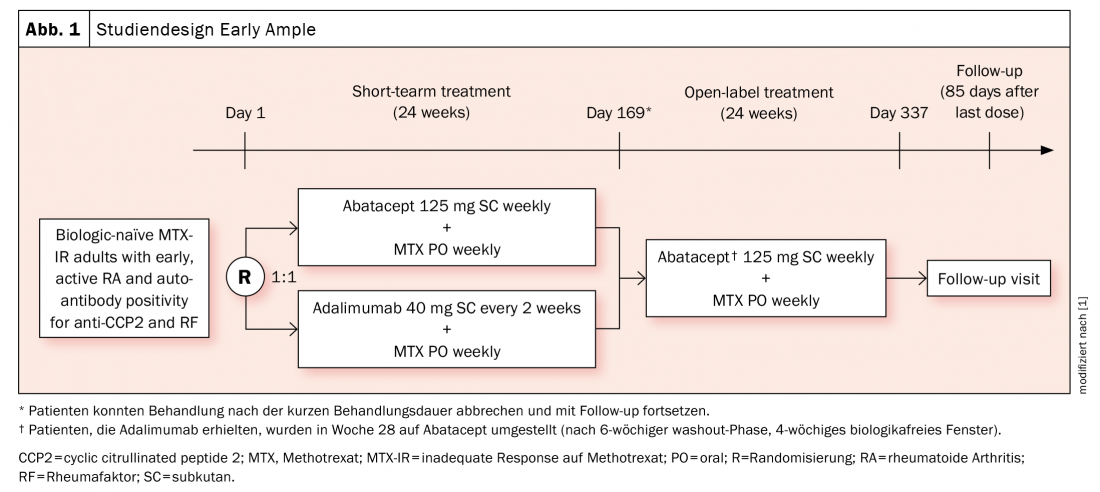
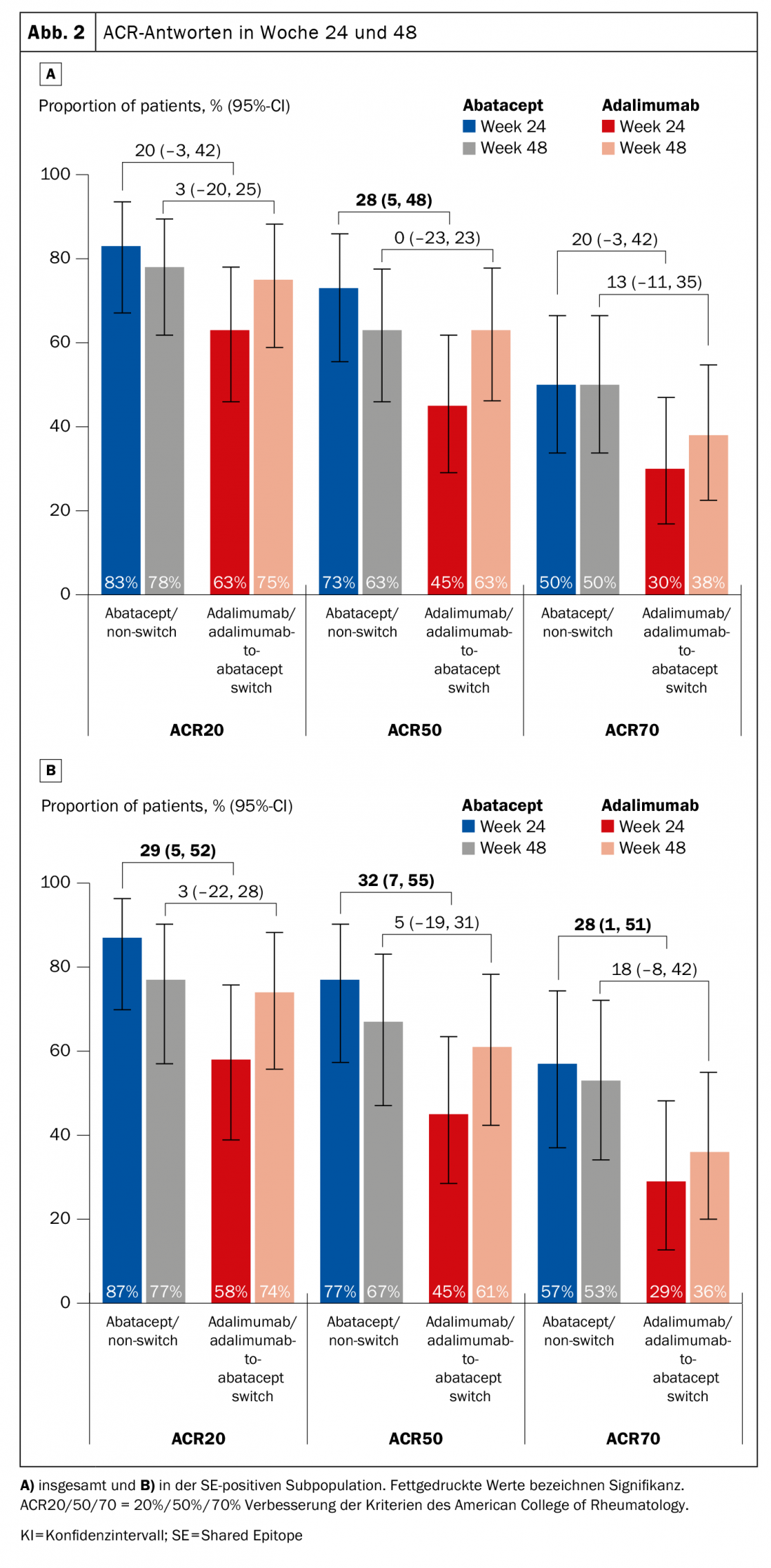
Valutazioni precedenti hanno dato indicazioni che i pazienti HLA-DRB1-positivi rispondono meglio ad abatacept (il che non significa che questo non possa valere anche per altri agenti, come ha sottolineato l’esperto). Lo studio di fase 4 Early Ample [1], pubblicato nel 2021, si basa su questo e ha diviso i pazienti con RA precoce biologicamente naïve che non avevano risposto adeguatamente al metotrexato (MTX) in un braccio abatacept (n=39, di cui 30 erano SE-positivi) e un braccio adalimumab (n=40, di cui 31 erano SE-positivi) (Fig. 1) . Le persone colpite dovevano essere positive al CCP2 e al fattore reumatoide. I soggetti sono stati randomizzati ad ABA o ADA per 24 settimane e poi tutti sono passati ad ABA. È stato dimostrato che i pazienti HLA-DRB1-positivi avevano già probabilità significativamente migliori di raggiungere un ACR20, -50 e -70 con abatacept dopo 24 e 48 settimane (Fig. 2A). Il risultato è stato ancora più forte a favore della sottopopolazione SE+ (Fig. 2B).
Si può prevenire l’AR nei pazienti a rischio?
I pazienti che non hanno ancora una sinovite clinicamente riconoscibile, ma che hanno già anticorpi CCP rilevabili, sono noti per essere a maggior rischio di sviluppare la RA. Se e come sia possibile prevenire lo sviluppo della RA in questo gruppo in fase precoce è il tema dello studio ARIAA, presentato al Congresso ACR 2021 [2]. I criteri di inclusione per questo studio di fase 2 erano: positività all’ACPA (+/- RF), artralgie da almeno 6 settimane, segni di infiammazione della mano dominante (sinovite, tenosinovite o osteite) alla risonanza magnetica ma senza gonfiore clinico, e nessuna terapia precedente con steroidi o DMARD. 49 pazienti identificati in questo modo sono stati trattati con abatacept per un periodo di 6 mesi rispetto al placebo (n=49). A questo è seguito un periodo di follow-up di 12 mesi senza trattamento.
L’endpoint primario, il miglioramento di almeno un parametro della risonanza magnetica (punteggio RAMRIS), è stato raggiunto: c’è stato un miglioramento significativo nel 61,2% dei pazienti nel braccio abatacept (rispetto al 30,6% del placebo; p=0,0043). Il gruppo verum ha ottenuto risultati significativamente migliori anche negli endpoint secondari di interruzione prematura dello studio e di progressione verso la RA clinica (interruzione 14,3% vs. 42,9%; p=0,0032; progressione 8,2% vs. 34,7%; p=0,0025). Il beneficio di Abatacept rispetto al placebo è quindi chiaramente visibile e il Prof. Rubbert-Roth spera di poter presentare gli ulteriori risultati del follow-up a lungo termine al prossimo EULAR. “Se i risultati fossero confermati durante il periodo di follow-up, sarebbe davvero spettacolare”, conclude.
Messaggi da portare a casa
- L’implementazione di nuovi concetti di studio, tra cui una strategia personalizzata, può contribuire a ottimizzare l’efficacia e la sicurezza della terapia DMARD in reumatologia.
- Prova di principio: idealmente, i biomarcatori sarebbero facilmente accessibili e facili da determinare in futuro.
- Questo concetto può essere implementato anche per altre malattie reumatologiche? (ad esempio, la firma dell’interferone nel LES)
Letteratura:
- Rigby W, Buckner JH, Louis Bridges S, et al: Gli alleli di rischio HLA-DRB1 per l’AR sono associati alla diversa responsività clinica ad abatacept e adalimumab: dati di uno studio testa a testa, randomizzato, in singolo cieco nell’AR precoce autoanticorpo-positiva. Arthritis Res Ther 2021; 23: 245; doi: 10.1186/s13075-021-02607-7.
- Rech J, et al: ACR 2021 [#0455].
InFo PAIN & GERIATURE 2022; 4(1-2): 20-21