Al Congresso DGK di Mannheim, si è tenuto un aggiornamento sulla moderna terapia dell’insufficienza cardiaca. Dove si trovano attualmente gli ARNI? Qual è la procedura per le richieste di pazienti speciali? Ci sono state anche novità sul problema dell’iperkaliemia nel trattamento dell’insufficienza cardiaca.
Lo studio di tutte le sperimentazioni sull’insufficienza cardiaca si è basato sul concetto di bloccare l’azione dell’angiotensina 2 tramite un antagonista AT1, inibendo al contempo la neprilisina, l’enzima di degradazione dei peptidi natriuretici prodotti nell’organismo. Questi ultimi danno sollievo al cuore e aumentano il flusso sanguigno verso i reni. L’ampio studio PARADIGM-HF ha dimostrato che la terapia con l’inibitore del recettore dell’angiotensina e della neprilisina (ARNI) sacubitril/valsartan ha ridotto significativamente gli endpoint clinicamente rilevanti, come i tassi di morte cardiovascolare e di ospedalizzazione per insufficienza cardiaca scompensata, nonché la mortalità per tutte le cause, rispetto alla terapia intensiva standard.
Con la revisione delle linee guida per il trattamento dell’insufficienza cardiaca cronica, la terapia combinata di sacubitril e valsartan è diventata il nuovo standard nel trattamento dell’insufficienza cardiaca sistolica sintomatica (“insufficienza cardiaca con frazione di eiezione ridotta” o HFrEF). Gli effetti della terapia ARNI iniziano presto, cioè nelle prime due settimane dopo l’inizio della terapia, ha riferito il Prof. Dr. med. Michael Böhm dell’Ospedale Universitario Saarland, Homburg. Ha fornito un aggiornamento sull’attuale terapia dell’insufficienza cardiaca e approfondimenti su nuovi aspetti (pratici).
Linee guida ESC 2016
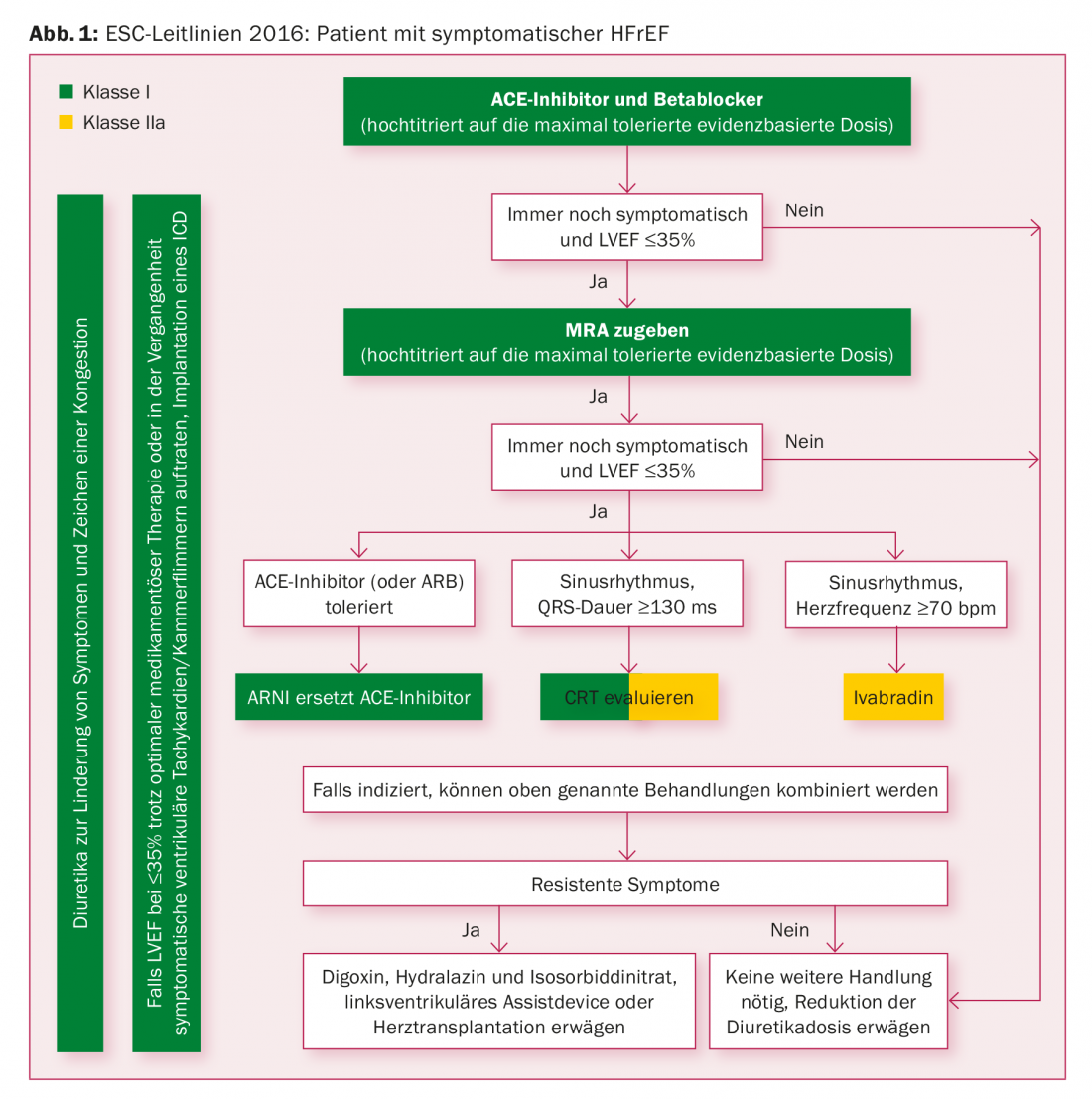
I capisaldi della farmacoterapia per l’HFrEF rimangono, secondo le linee guida ESC, gli ACE-inibitori (bloccanti del recettore AT1 se intolleranti) e i betabloccanti. Se i sintomi persistono, segue un antagonista del recettore mineralcorticoide (MRA), come lo spironolattone o l’eplerenone, come terzo agente neuroumorale nel regime di trattamento. Nell’algoritmo di trattamento delle linee guida ESC, la combinazione di sacubitril/valsartan dovrebbe sostituire l’ACE inibitore o l’antagonista AT1, a condizione che l’insufficienza cardiaca rimanga sintomatica – e a condizione che queste sostanze siano tollerate (Fig. 1).
L’uguaglianza migliore?
“Il principio dell’ARNI è migliore di quello della (sola) inibizione del RAAS”, afferma il Prof. Böhm. L’ARNI non solo inibisce il sistema renina-angiotensina-aldosterone, ma aumenta anche l’attività dei peptidi natriuretici vasoattivi, con un pronunciato effetto di abbassamento della pressione sanguigna. “Prestando attenzione alla pressione arteriosa e ai consueti criteri di esclusione, come un tasso di filtrazione glomerulare (GFR) inferiore al 30%, tutti i pazienti con insufficienza cardiaca significativa dovrebbero essere passati a sacubitril/valsartan”.
La questione di come trattare il paziente informato che sviluppa un’insufficienza cardiaca sintomatica e desidera una terapia ARNI in prima linea, o con costellazioni speciali come l’ipotensione o la funzione renale compromessa, è stata recentemente ripresa da un documento di consenso pubblicato, come ha riferito il Prof. Böhm. In risposta alla prima domanda, sono stati forniti consigli pratici concreti su come trattare i pazienti ACE-naive con un ARNI (cioè iniziando con la dose più bassa). In altre costellazioni, l’obiettivo è identificare le barriere che impediscono l’implementazione ottimale della terapia per l’insufficienza cardiaca (pressione bassa e/o funzione renale compromessa). Molti pazienti con insufficienza cardiaca cronica e frazione di eiezione ridotta hanno anche una pressione sanguigna bassa. Gli studi hanno ripetutamente dimostrato che i bassi livelli di pressione sanguigna nell’insufficienza cardiaca sono associati a un aumento della mortalità. Tuttavia, i bassi valori pressori nei pazienti con insufficienza cardiaca sistolica non sono un motivo per abbandonare la terapia con sacubitril/valsartan, se è tollerata. L’efficacia relativa di sacubitril/valsartan è stata addirittura maggiore nel gruppo di pazienti con i valori più bassi di pressione arteriosa sistolica (<110 mmHg). Questi pazienti beneficiano anche di una riduzione del rischio di morte, come suggeriscono i risultati di un’analisi dello studio PARADIGM-HF.
“Terapie abilitanti: leganti di potassio
Secondo il Prof. Böhm, la paura dell’iperkaliemia è un’altra barriera alla terapia ottimale nella pratica. Le sostanze non verrebbero somministrate nella dose raccomandata – con la conseguenza che il loro effetto benefico sulla morbilità e sulla mortalità non si realizzerebbe o si realizzerebbe in modo insufficiente. Una novità nella terapia dell’insufficienza cardiaca è l’uso di patiromer. Il legante di potassio non assorbibile, che lega il potassio in cambio di calcio durante il transito intestinale, dovrebbe migliorare l’ampiezza terapeutica degli inibitori del RAAS e potrebbe essere utile per il trattamento/prevenzione dell’iperkaliemia. L’iperkaliemia è un problema comune nel trattamento dei pazienti con insufficienza cardiaca, soprattutto quando la funzione renale è compromessa. Le sostanze che possono aumentare il potassio sierico includono gli inibitori del sistema renina-angiotensina-aldosterone, i bloccanti del recettore AT1, i diuretici risparmiatori di potassio e gli antagonisti del recettore mineralcorticoide. Con il nuovo legante del potassio, si spera di aiutare a prevenire l’iperkaliemia a lungo termine, consentendo così ai pazienti con una tendenza a livelli elevati di potassio di ricevere una terapia basata sulle linee guida.
Attivatore della miosina Omecamtiv
Una terapia con l’attivatore della miosina omecamtiv mecarbil è ancora un sogno del futuro. Come importante proteina motrice nelle fibre muscolari, la miosina è coinvolta nella conversione dell’energia chimica in forza e movimento. Insieme all’actina, forma l’unità contrattile del muscolo. Omecamtiv Mecarbil prolunga l’interazione ciclo-dipendente della miosina con l’actina e quindi provoca anche un prolungamento della durata sistolica e un miglioramento delle prestazioni di pompaggio. In un primo grande studio internazionale, l’uso degli attivatori di miosina sembrava promettente, dice il Prof. Böhm.
Preso in prestito dai diabetologi:Nuovi farmaci per l’insufficienza cardiaca?
Gli inibitori SGLT2 sono una classe di farmaci con effetti favorevoli sui tassi di eventi cardiovascolari e sui ricoveri ospedalieri per insufficienza cardiaca scompensata. In primo luogo ci sono stati i dati su canagliflozin: la sostanza ha ridotto la probabilità di ricovero per insufficienza cardiaca nei diabetici con fattori di rischio cardiovascolare. Nel programma di sperimentazione CANVAS, è stata dimostrata una riduzione significativa del rischio di complicanze cardiovascolari (morte cardiovascolare, infarto miocardico, ictus) del 14%. Il rischio relativo di essere ricoverati in ospedale per insufficienza cardiaca è diminuito del 33%. Una riduzione significativa del rischio è stata ottenuta soprattutto nei pazienti che avevano già un’insufficienza cardiaca.
Nel 2018, i cardiologi sono interessati alle seguenti domande: gli inibitori SGLT2 possono essere utilizzati nella terapia dell’insufficienza cardiaca – invece che (come prima) nella prevenzione? E soprattutto, gli inibitori SGLT2 serviranno in futuro come farmaci per l’insufficienza cardiaca nei non diabetici?
Consigli pratici: Utilizzare l’NT-proBNP per il monitoraggio della terapia
Il BNP e il prodotto di scissione NT-proBNP sono biomarcatori dell’insufficienza cardiaca e vengono utilizzati per la diagnostica e soprattutto per la valutazione del decorso clinico. Il BNP è un substrato della neprilisina, che viene inibita dal sacubitril durante la terapia ARNI. Di conseguenza, la concentrazione di BNP circolante aumenta. In caso di terapia ARNI, solo l’NT-proBNP, ma non il BNP, è adatto come parametro di follow-up. L’NT-proBNP non è influenzato dalla neprilisina e riflette in modo invariato la gravità e il decorso dell’insufficienza cardiaca.
Fonte: Conferenza annuale della DGK, 4-7 aprile 2018, Mannheim (D)
Ulteriori letture:
- Ponikowski P, et al.: Linee guida ESC 2016 per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica: La Task Force per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica della Società Europea di Cardiologia (ESC). European Heart Journal 2016 Jul 14; 37(27): 2129-2200.
- Yancy CW, et al: 2017 ACC Expert Consensus Decision Pathway for Optimization of Heart Failure Treatment: Answers to 10 Pivotal Issues About Heart Failure With Reduced Ejection Fraction: A Report of the American College of Cardiology Task Force on Expert Consensus Decision Pathways. J Am Coll Cardiol 2018 Jan 16; 71(2): 201-230.
- Cowie MR, et al: Nuovi prodotti medicinali per l’insufficienza cardiaca cronica: progressi nella progettazione di studi clinici e nella valutazione dell’efficacia. European Journal of Heart Failure 2017; 19: 718-727.
- Packer M: Amore per gli inibitori dell’enzima di conversione dell’angiotensina in tempo di colera. JACC Heart Fail 2016 Apr 12. pii: S2213-1779(16)30045-2.
- Böhm M, et al.: Primum non nocere: i pericoli del rinvio della terapia dell’insufficienza cardiaca. Eur J Heart Fail 2017 Nov; 19(11): 1410-1411.
- Böhm M, et al.: Associazioni di rischio per la pressione sanguigna nello scompenso cardiaco: effetti reali o causalità inversa? JACC Heart Fail 2017 Nov; 5(11): 820-822.
- Radholm K, et al: Effetti degli inibitori del cotrasportatore-2 di sodio-glucosio sulle malattie cardiovascolari, sulla mortalità e sulla sicurezza nel diabete di tipo 2 – una revisione sistematica. Diabetes Res Clin Pract 2018 Mar 28. pii: S0168-8227(17)31784-9.
- Verma S: La promessa metabolizzante dell’inibizione del cotrasportatore di glucosio 2 dipendente dal sodio: la ricerca del punto di forza nell’insufficienza cardiaca. JAMA Cardiol 2017 Sep 1; 2(9): 939-940.
CARDIOVASC 2018; 17(3): 29-32











