Oggi esiste un’ampia gamma di opzioni di trattamento per l’alopecia androgenetica (AGA). I preparati topici con il principio attivo minoxidil e gli inibitori orali della 5-α-reduttasi finasteride e dutasteride sono tra le misure terapeutiche classiche basate sull’evidenza. Tuttavia, ora ci sono anche diversi studi sulla terapia laser a basso livello e sul plasma ricco di piastrine (PRP).
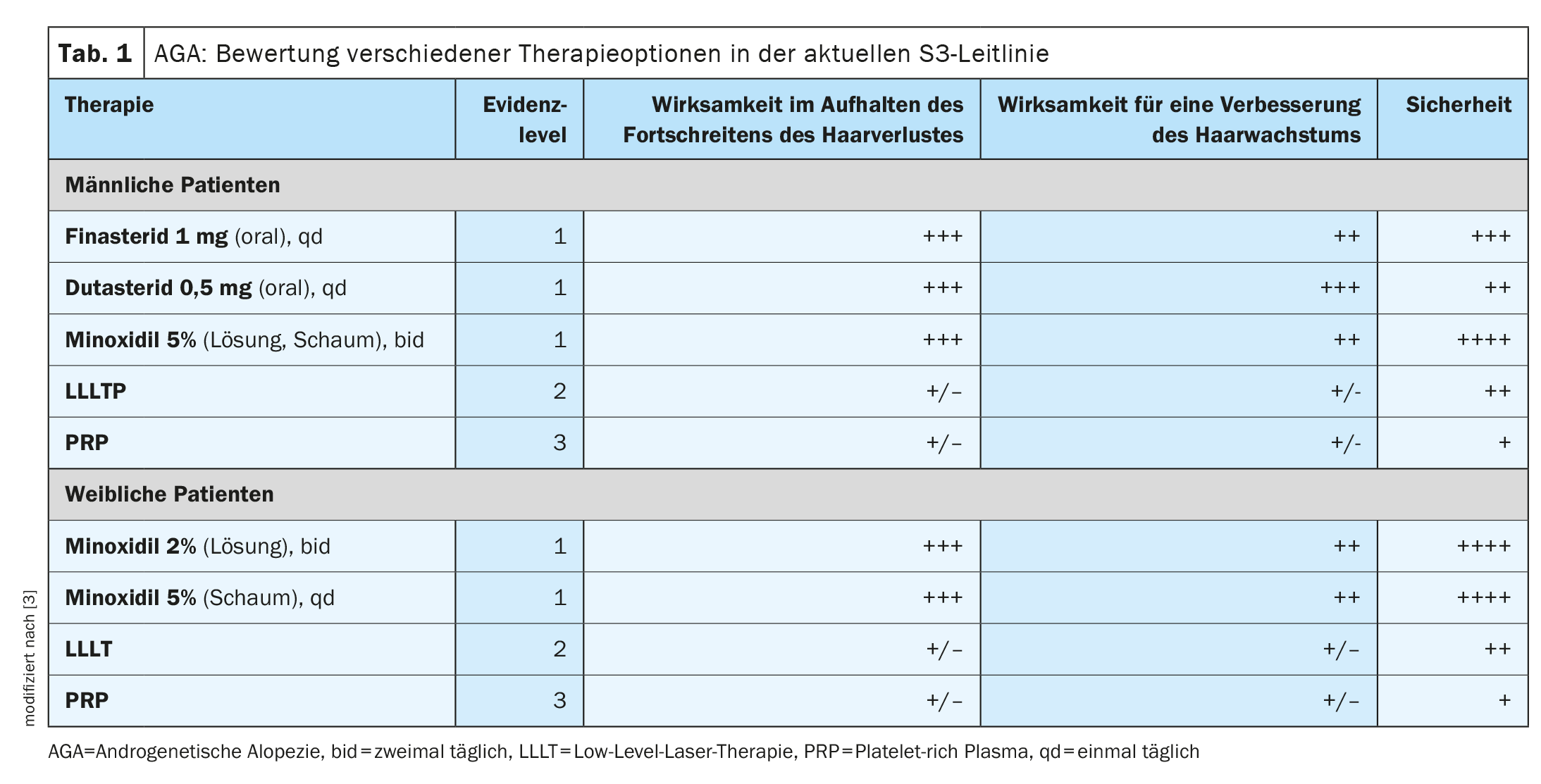
La perdita dei capelli è un sintomo che altera notevolmente l’aspetto e può influire in modo significativo sulla qualità della vita. Sia negli uomini che nelle donne, circa il 95% di tutti i casi di perdita di capelli sono causati dall’alopecia androgenetica ( AGA). Questa perdita di capelli congenita (box) è quindi la causa più comune di alopecia in entrambi i sessi [1,4–7]. Kaiser et al. hanno riassunto le prove attuali sulle varie opzioni di trattamento per l’AGA in un articolo di revisione pubblicato nel 2023 [2]. E la linea guida S3 per il trattamento dell’AGA negli uomini e nelle donne, pubblicata su JEADV nel 2018, si basa sulla valutazione delle terapie attuali in base all’analisi di 47 articoli scientifici che soddisfano i criteri di inclusione secondo gli standard AGREE [3]. I criteri di valutazione includevano l’efficacia nell’arrestare la progressione della perdita di capelli, l’efficacia nel migliorare la crescita dei capelli e la sicurezza della rispettiva opzione di trattamento (Tabella 1) .
Minoxidil topico: l’attività della solfotransferasi nel follicolo pilifero è rilevante
Il minoxidil è autorizzato per il trattamento topico del cuoio capelluto nell’alopecia androgenetica negli uomini e nelle donne. L’effetto è mirato alla radice del capello. Negli uomini, è stato dimostrato che la soluzione al 5% è più efficace di quella al 2%, se utilizzata due volte al giorno [8]. Nelle donne, le soluzioni al 2% e al 5% hanno ottenuto un’efficacia approssimativamente simile [9,10]. L’enzima solfotransferasi, che converte il minoxidil nella sua forma biologicamente attiva minoxidil solfato, sembra svolgere un ruolo importante. Diversi studi hanno dimostrato che il successo dell’applicazione di minoxidil è correlato alla quantità di solfotransferasi nei follicoli piliferi [11]. Questa è una possibile spiegazione del perché non tutte le persone con AGA rispondono al minoxidil. Goren et al. ha riferito che dopo 16 settimane di applicazione topica continua di minoxidil, circa il 40% dei pazienti ha mostrato una risposta alla terapia [12]. Si presume che il 60% dei pazienti di sesso maschile non risponda alla terapia con minoxidil topico a causa dei bassi livelli iniziali di solfotransferasi [14]. E l’analisi dell’attività della solfotransferasi nei follicoli piliferi strappati sembra essere un predittore accurato della risposta delle donne al trattamento topico con minoxidil [11]. I primi effetti del minoxidil sulla crescita dei capelli si manifestano solitamente dopo 6-8 settimane e raggiungono il massimo dopo 12-16 settimane [13]. I prodotti a base di minoxidil (soluzione o schiuma) devono essere applicati due volte al giorno. Se l’applicazione viene interrotta, gli effetti scompaiono di nuovo dopo un po’. Gli effetti collaterali occasionali del minoxidil possono includere prurito, arrossamento, infiammazione e forfora del cuoio capelluto [16]. Può verificarsi anche l’ipertricosi, soprattutto nelle donne [10]. Un altro effetto collaterale è il cosiddetto “shedding”, che comporta un aumento temporaneo della perdita di capelli all’inizio del trattamento. Se il paziente non viene informato, ciò può comportare l’interruzione prematura del trattamento [10,15].
| Negli uomini, l’AGA si manifesta con una perdita di capelli gradualmente crescente nell’area frontoparietale (“stempiatura”), frontale e/o del vertice. Circa la metà degli uomini di età superiore ai 65 anni ha l’AGA. Le donne sono caratterizzate da un assottigliamento uniforme dei capelli nella regione della corona, mentre l’attaccatura dei capelli frontali rimane intatta. L’AGA può manifestarsi nelle donne dopo la pubertà; la prevalenza nelle 70enni è di circa il 38%. |
| a [27] |
Quando la finasteride orale fallisce: la dutasteride come possibile alternativa
È stato dimostrato che la finasteride al dosaggio di 1 mg/die riduce la progressione dell’AGA [17]. In una revisione sistematica di Mella et al. La finasteride orale è risultata migliorare significativamente la crescita dei capelli e il numero medio di capelli rispetto al placebo in dieci studi [18]. In uno studio di follow-up di 10 anni condotto da Rossi et al. è stato anche riscontrato che l’uso quotidiano di finasteride negli uomini con AGA per 5 anni ha portato a un miglioramento duraturo della conta dei capelli nel 21% dei pazienti. I migliori risultati di crescita dei capelli sono stati ottenuti nell’area della corona del cuoio capelluto, mentre solo minimi miglioramenti clinici sono stati osservati nell’area della fronte [19]. Gli effetti collaterali più comuni della finasteride includono la disfunzione sessuale; a seconda dello studio, la frequenza varia dall’1% al 40% [20,21]. La base di prove sulla sicurezza dell’uso a lungo termine della finasteride orale è piuttosto limitata.
I pazienti per i quali la finasteride orale non è efficace possono beneficiare del trattamento con dutasteride. Uno studio di Jung et al. hin. I pazienti maschi (n=31) hanno ricevuto invece dutasteride orale 0,5 mg/d dopo un tentativo di trattamento con finasteride fallito [22]. Circa l’80% ha mostrato un miglioramento clinico dopo 6 mesi. La densità dei capelli è aumentata di un 10% statisticamente significativo e lo spessore dei capelli è aumentato del 20%. Effetti collaterali simili sono stati segnalati con la dutasteride, come riduzione della libido, impotenza, disturbi dell’eiaculazione e ginecomastia.
| Cambiamenti correlati all’età nel metabolismo degli androgeni Si ritiene che la causa principale dell’AGA siano i cambiamenti legati all’età nel metabolismo degli androgeni, che portano a un progressivo accorciamento della fase anagen della crescita dei capelli e a una diminuzione delle dimensioni del follicolo pilifero [2,4]. Inoltre, si verifica una fase telogen prolungata, che porta alla regressione dei follicoli piliferi [5]. A causa della maggiore attivazione dei recettori degli androgeni nell’AGA, i follicoli piliferi diventano sempre più corti, fino a quando non riescono più a penetrare nell’epidermide [6]. Nei pazienti con AGA sono stati riscontrati livelli elevati di diidrotestosterone (DHT) e le regioni del cuoio capelluto colpite da AGA presentano un aumento dei recettori degli androgeni [6]. In genere, l’AGA comporta la perdita dei capelli terminali e la loro sostituzione con piccoli capelli vellutati, di solito nelle aree temporali, parietali e medio-frontali del cuoio capelluto [7]. |
Terapia laser a basso livello (LLLT)
Nella LLLT, la crescita dei capelli viene stimolata dalla luce laser emessa dai diodi laser. La LLLT può essere eseguita a casa, indossando un casco con un laser integrato. In generale, la LLLT è ben tollerata e gli effetti collaterali sono di solito minori (ad esempio, secchezza del cuoio capelluto, prurito, sensibilità e sensazione di calore) [3]. Un totale di tre studi sulla LLLT ha soddisfatto i criteri di inclusione della linea guida S3. La LLLT ha portato a un aumento del numero di capelli dopo 16 e 26 settimane di applicazione con protocolli diversi e con due dispositivi diversi. Tuttavia, non è stato effettuato un follow-up a lungo termine [3]. Una recente meta-analisi di Liu et al. ha rilevato che 11 studi randomizzati, in doppio cieco e controllati hanno trovato un miglioramento statisticamente significativo della densità dei capelli nei pazienti trattati con LLLT rispetto ai dispositivi placebo [23].
Ultimo, ma non meno importante: il PRP
Il plasma ricco di piastrine (PRP) si ottiene dal sangue del paziente stesso. Tre studi sul PRP sono stati inclusi nella linea guida S3 [3,24–26]. I pazienti di sesso maschile e femminile sono stati inclusi in due di essi [24,25]. Con il trattamento PRP è stato osservato un aumento della densità dei capelli [24–26]. Tuttavia, il PRP è stato effettuato in piccoli campioni, con protocolli diversi e senza un gruppo di controllo. Secondo Kaiser et al. Il PRP è particolarmente interessante come opzione terapeutica per i pazienti in cui diverse modalità di trattamento di prima linea hanno fallito [2]. Indipendentemente dall’opzione di trattamento, è importante discutere con i pazienti le loro aspettative e i loro obiettivi e affrontare i rischi di effetti collaterali e i costi del trattamento.
Letteratura:
- Deutsches Endokrinologisches Versorgungszentrum: Anlagebedingter Haarausfall, www.endokrinologen.de, (ultimo accesso 19.01.2024)
- Kaiser M, et al.: Treatment of Androgenetic Alopecia: Current Guidance and Unmet Needs. Clin Cosmet Investig Dermatol 2023; 16: 1387–1406.
- Kanti V, et al.: Evidence-based (S3) guideline for the treatment of androgenetic alopecia in women and in men – short version. JEADV 2018; 32(1): 11–22.
- Trüeb RM. Molecular mechanisms of androgenetic alopecia. Exp Gerontol 2002; 37(8–9): 981–990.
- Kaliyadan F, Nambiar A, Vijayaraghavan S: Androgenetic alopecia: an update. Indian J Dermatol Venereol Leprol 2013; 79(5): 613.
- Ho CH, Sood T, Zito PM:Androgenetic alopecia. In: StatPearls. StatPearls Publishing; 2021.
- Rathnayake D, Sinclair R: Male androgenetic alopecia. Expert Opin Pharmacother 2010;11(8): 1295–1304.
- Olsen EA, et al.: A randomized clinical trial of 5% topical minoxidil versus 2% topical minoxidil and placebo in the treatment of androgenetic alopecia in men. JAAD 2002; 47(3): 377–385.
- Lucky AW, et al.: A randomized, placebo-controlled trial of 5% and 2% topical minoxidil solutions in the treatment of female pattern hair loss. JAAD 2004; 50(4): 541–553.
- Blumeyer A, et al.: Evidence-based (S3) guideline for the treatment of androgenetic alopecia in women and in men. JDDG 2011; 9: S1–S57.
- Roberts J, et al.: Sulfotransferase activity in plucked hair follicles predicts response to topical minoxidil in the treatment of female androgenetic alopecia. Dermatol Ther 2014; 27(4): 252–254.
- Goren A, et al.: Clinical utility and validity of minoxidil response testing in androgenetic alopecia. Dermatol Ther 2015; 28(1): 13–16.
- Messenger A, Rundegren J: Minoxidil: mechanisms of action on hair growth. BJD 004; 150(2): 186–194.
- Goren A, et al.: Novel enzymatic assay predicts minoxidil response in the treatment of androgenetic alopecia. Dermatol Ther 2013; 27(3): 171–173.
- Randolph M, Tosti A: Oral minoxidil treatment for hair loss: a review of efficacy and safety. JAAD 2021; 84(3): 737–746.
- Suchonwanit P, Thammarucha S, Leerunyakul K: Minoxidil and its use in hair disorders: a review. Drug Des Devel Ther 2019; 13:2777.
- Kaufman KD, et al.: Finasteride in the treatment of men with androgenetic alopecia. JAAD 1998; 39(4): 578–589.
- Mella JM, et al.: Efficacy and safety of finasteride therapy for androgenetic alopecia: a systematic review. Arch Dermatol 2010; 146(10): 1141–1150.
- Rossi A, et al.: Finasteride, 1 mg daily administration on male androgenetic alopecia in different age groups: 10-year follow-up. Dermatol Ther 2011; 24(4): 455–461.
- Hirshburg JM, et al.: Adverse effects and safety of 5-alpha reductase inhibitors (finasteride, dutasteride): a systematic review. J Clin Aesthet Dermatol 2016; 9(7): 56.
- Ganzer CA, Jacobs AR, Iqbal F: Persistent sexual, emotional, and cognitive impairment post-finasteride: a survey of men reporting symptoms. Am J Men Health 2015; 9(3): 222–228.
- Jung JY, et al: Effetto della dutasteride 0,5 mg/d negli uomini con alopecia androgenetica recalcitrante alla finasteride. Int J Dermatol 2014; 53(11): 1351-1357.
- Liu K-H, et al.: Comparative effectiveness of low-level laser therapy for adult androgenic alopecia: a system review and meta-analysis of randomized controlled trials. Lasers Med Sci 2019; 34(6): 1063–1069.
- Jha AK, et al.: Platelet-rich plasma and microneedling improves hair growth in patients of androgenetic alopecia when used as an adjuvant to minoxidil. J Cosmet Dermatol 2019; 18(5): 1330–1335.
- Aggarwal K, et al.: Dermoscopic assessment of microneedling alone versus microneedling with platelet-rich plasma in cases of male pattern alopecia: a split-head comparative study. Int J Trichology 2020; 12(4): 156.
- Sinclair RD: Female pattern hair loss: a pilot study investigating combination therapy with low-dose oral minoxidil and spironolactone. Int J Dermatol 2018; 57(1): 104–109.
- Beise U: Guideline Haarausfall, www.medix.ch/wissen/guidelines, (ultimo accesso 22.01.2024).
DERMATOLOGIE PRAXIS 2024; 34(1): 48–49