La sopravvivenza complessiva dei pazienti con leucemia mieloide cronica non può essere modificata dall’ottimizzazione della terapia con imatinib. Questo nonostante il fatto che le valutazioni precedenti fossero in grado di dimostrare un’influenza sulla risposta.
L’imatinib ha rivoluzionato il trattamento della leucemia mieloide cronica (CML). Di conseguenza, i tassi di sopravvivenza sono aumentati notevolmente. I pazienti che rispondono ai TKI hanno oggi un’aspettativa di vita quasi normale. I ricercatori stanno quindi esaminando se la dose abituale di 400 mg sia adatta a tutti i pazienti per ottenere un risultato ottimale. Diversi studi stanno esaminando il potenziale beneficio della terapia con imatinib modificato. L’approccio con imatinib ad alto dosaggio (800 mg) o adattato alla dose (o anche la combinazione con interferone) può effettivamente modificare la risposta rispetto alla variante standard, come Hehlmann e colleghi hanno dimostrato in precedenza [2,4] (anche se in parte contraddicendo altri studi randomizzati [3]). Ma questo beneficio si traduce in una migliore, cioè più lunga, sopravvivenza a lungo termine? Quindi, è possibile ottenere tassi di sopravvivenza più elevati con diverse ottimizzazioni della terapia?
Lo studio CML IV
Tra l’altro, questa domanda è stata indagata nel grande studio randomizzato CML IV – con la partecipazione della Svizzera. L’obiettivo era quello di verificare fino a che punto la terapia standard con 400 mg/d di imatinib può essere ottimizzata. A tal fine, 1551 pazienti di nuova diagnosi in fase cronica sono stati randomizzati in cinque bracci. Due bracci, ovvero quelli che hanno testato l’imatinib in combinazione con la citarabina o dopo il fallimento dell’interferone, sono stati chiusi ad un ulteriore reclutamento di pazienti dopo una fase pilota. Le altre tre consistevano nella dose standard di 400 mg/d, nella terapia ad alto dosaggio di 800 mg/d e nella combinazione di imatinib con interferone. L’età mediana dei pazienti era di 53 anni e il 61% era di sesso maschile.
Al congresso EHA di Madrid, sono stati discussi i dati di sopravvivenza a lungo termine, più precisamente la sopravvivenza globale dopo un periodo di osservazione mediano di 9,5 anni. Era dell’82% in tutti i gruppi (sopravvivenza libera da progressione 80%).
Sopravvivenza dopo un decennio
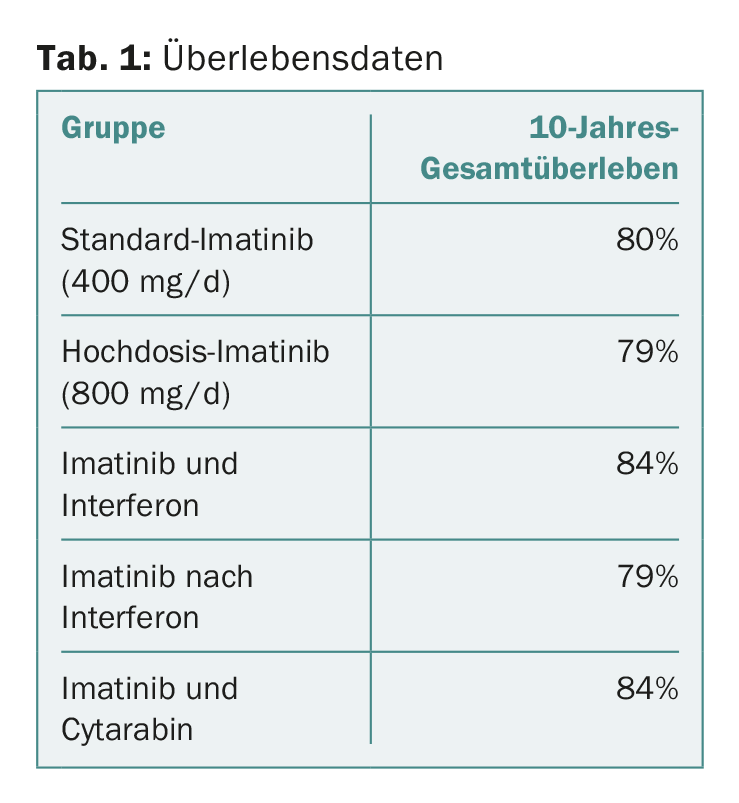
I dettagli dei singoli gruppi sono riportati nella tabella 1. I risultati mostrano che non ci sono state differenze significative tra i diversi approcci o ottimizzazioni del trattamento. Questo nonostante il fatto che una risposta più rapida sia stata ottenuta con la terapia ad alto dosaggio, come dimostrato in pubblicazioni precedenti [2]. Tuttavia, ciò che ha giocato un ruolo nella sopravvivenza a lungo termine è stato il raggiungimento dei valori target (“pietre miliari”) nella risposta molecolare dopo tre, sei e dodici mesi – anche in linea con i dati precedentemente pubblicati dello studio [2,4]. Nell’analisi multivariata, anche le comorbidità e lo stato di fumatore sono risultati fattori rilevanti che influenzano la sopravvivenza. Anche il fatto che il centro di trattamento fosse accademico o meno ha giocato un ruolo significativo, ma non il sesso del paziente.
È stato raggiunto il capolinea?
Di conseguenza, è stata dimostrata la CML IV: I tassi di sopravvivenza dei pazienti con CML che assumono imatinib sono elevati e non sono necessariamente influenzati da un regime di trattamento iniziale con una risposta più rapida, ma piuttosto da fattori esterni come il fumo, il tipo di centro di trattamento e le comorbidità del paziente.
Il rischio di morire dopo dieci anni a causa di parametri indipendenti dalla CML, anziché della malattia stessa, è stato significativamente maggiore per i partecipanti, vale a dire due volte più alto – in definitiva un effetto da aspettarsi con i farmaci ad alta efficacia [5]. Inoltre, il cosiddetto punteggio “European Treatment and Outcome Study” (EUTOS) sulla sopravvivenza a lungo termine, che valuta il rischio di mortalità associato alla CML, è stato anche un predittore significativo della prognosi: i gruppi con rischio elevato sono sopravvissuti meno a lungo di quelli con rischio basso.
Quindi, da un lato, la sopravvivenza è indipendente dal tempo alla risposta (almeno in questo studio e nell’impostazione del trattamento o nel periodo di osservazione). La terapia ad alto dosaggio non ha quindi causato una differenza significativa. Al contrario, il tempo alla risposta non è un marcatore surrogato adeguato per la sopravvivenza globale. D’altra parte, non bisogna dimenticare che il raggiungimento dei valori target nella risposta molecolare in determinati momenti ha certamente giocato un ruolo nella prognosi, come era prevedibile. I pazienti con BCR-ABLIS <1% a sei mesi avevano una sopravvivenza a 5 anni del 97% rispetto all’89% con BCR-ABLIS >1% (p<0,001) [6].
La sopravvivenza globale è un indicatore adeguato del successo di una terapia?
La presentazione dell’EHA lascia quindi un po’ perplessi. Sebbene un maggior numero di pazienti raggiunga una risposta (più rapidamente) con la dose più alta e questo sia associato a una migliore sopravvivenza globale, le differenze tra le varianti di dose non sembrano avere un effetto significativo a lungo termine: Tutti vivono lo stesso tempo, indipendentemente dal regime di imatinib ricevuto. Altri fattori non direttamente correlati alla CML diventano più importanti: il paziente è altrimenti sano? Fuma?
Si può anche formulare l’intera questione al contrario: La sopravvivenza globale potrebbe non essere adatta a valutare il successo a lungo termine di trattamenti specifici per la CML [5]. Se ci si basasse solo su questo, il capolinea sarebbe raggiunto con l’imatinib al dosaggio standard.
Naturalmente, anche gli endpoint come il raggiungimento di una risposta profonda per poter forse interrompere il TKI (vedi studio EURO-SKI [7] con aggiornamento al congresso EHA dello scorso anno [8]), o la protezione dalla progressione, svolgono un ruolo centrale per i pazienti con CML e non devono essere dimenticati in questo contesto.
Fonte: Congresso dell’Associazione Europea di Ematologia (EHA) 2017, 22-25 giugno 2017, Madrid
Letteratura:
- Hehlmann R, et al: Valutazione di Imatinib 400 mg come trattamento di prima linea della leucemia mieloide cronica: risultati di sopravvivenza a 10 anni dello studio randomizzato Cml IV. EHA 2017; Abstract S424.
- Hehlmann R, et al: La risposta molecolare profonda viene raggiunta dalla maggior parte dei pazienti trattati con Imatinib, predice la sopravvivenza e viene raggiunta più rapidamente con l’Imatinib ottimizzato ad alto dosaggio: risultati dello studio randomizzato CML-Study IV. Journal of Clinical Oncology 2014; 32(5): 415-423.
- JE Cortes, et al.: Studio di fase III, randomizzato, in aperto, di imatinib mesilato 400 mg al giorno rispetto a 800 mg nei pazienti con leucemia mieloide cronica di nuova diagnosi, precedentemente non trattata, in fase cronica, utilizzando punti finali molecolari: Studio di ottimizzazione e selettività degli inibitori della tirosin-chinasi. J Clin Oncol 2010; 28: 424-430.
- Hehlmann R, et al: Imatinib adattato alla tollerabilità 800 mg/d versus 400 mg/d versus 400 mg/d più interferone-α nella leucemia mieloide cronica di nuova diagnosi. Journal of Clinical Oncology 2011; 29(12): 1634-1642.
- Saussele S, et al: Impatto delle comorbidità sulla sopravvivenza globale nei pazienti con leucemia mieloide cronica: risultati dello studio randomizzato CML IV. Sangue 2015; 126(1): 42-49.
- Hanfstein B, et al.: La risposta molecolare e citogenetica precoce è predittiva della sopravvivenza libera da progressione e globale a lungo termine nella leucemia mieloide cronica (LMC). Leucemia 2012; 26(9): 2096-2102.
- Mahon FX, et al: Analisi intermedia di uno studio pan-europeo sugli inibitori della tirosin-chinasi nella leucemia mieloide cronica: lo studio EURO-SKI. Sangue 2014; 124: 151.
- Richter J, et al: Interruzione degli inibitori della tirosin-chinasi in una coorte molto ampia di pazienti europei affetti da leucemia mieloide cronica: risultati dello studio EURO-SKI. EHA 2016; Abstract S145.
InFo ONCOLOGIA & EMATOLOGIA 2017; 5(4): 7-8











