Os novos anticoagulantes orais (NOAKs) há muito que se tornaram parte da prática clínica diária na profilaxia do AVC para a fibrilação atrial. Devido à sua utilização mais simples, segura e eficaz, espera-se que substituam a terapia com antagonista de vitamina K (VKA) na maioria dos pacientes. Contudo, como em qualquer terapia, há alguns aspectos práticos importantes que precisam de ser considerados para uma utilização correcta e segura. A utilização não selectiva das substâncias deve ser evitada em qualquer caso.
Os grandes estudos de registo dos novos anticoagulantes orais (NOAK) para a profilaxia do tromboembolismo em fibrilação atrial – RE-LY (dabigatran) [1], ROCKET-AF (rivaroxaban) [2], ARISTOTLE (apixaban) [3] e ENGAGE-TIMI 48 (edoxaban) [4] – mostraram, que estas substâncias não só são pelo menos equivalentes, se não superiores, aos antagonistas da vitamina K (VKA) em termos de prevenção de AVC, mas também reduzem significativamente o risco de hemorragias graves e/ou intracranianas. [5–7]. Um dos maiores erros, contudo, é encarar estas substâncias indiscriminadamente como medicamentos de “tamanho único” e utilizá-las de forma acrítica e pouco selectiva. Este artigo resume dez aspectos importantes na aplicação diária (com base e em complemento de trabalhos anteriores [5–9]).
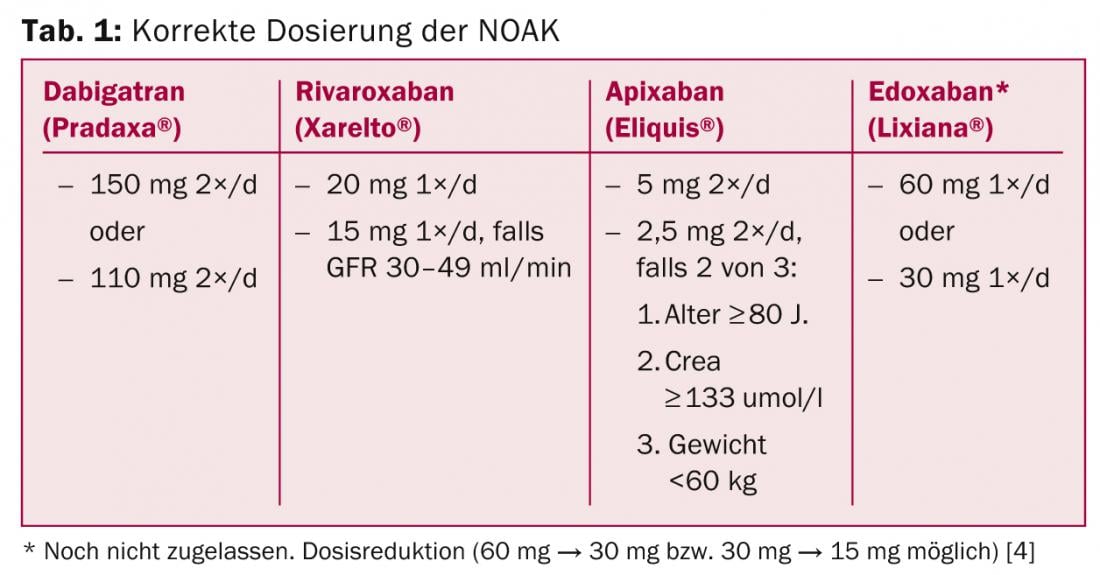
Pergunta 1: Qual é a dosagem correcta?
A tabela 1 resume a dosagem correcta de NOAKs. Os desvios desta são utilizações “fora do rótulo” e devem ser evitados uma vez que não existem dados disponíveis para tal (por exemplo, prescrição de 10 mg de rivaroxaban em doentes com FVC e “elevado risco de hemorragia”). A terapia inicial é muito mais fácil do que com a VKA, pois o efeito total ocorre após duas a três horas – sem necessidade de fazer a ponte com a heparina ou NMH.
Pergunta 2: O que devo fazer se me esquecer de uma dose?
A conformidade/aderência de medicamentos é crítica com os NOAKs e não se deve perder a oportunidade de recordar isto ao doente. No entanto, os erros de dosagem ocorrem naturalmente na prática clínica diária. Com base em extrapolações farmacocinéticas, recomenda-se que uma dose perdida seja tomada até seis horas (para dose 2×/dose, ou seja, apixaban/dabigatran) ou até doze horas (para dose 1×/dose, ou seja, rivaroxaban) após a dose programada [10]. Se o erro só for notado após esta janela de tempo, a dose deve ser ignorada e continuar com a próxima dose programada.
Pergunta 3: O que fazer em caso de ingestão dupla acidental?
Para NOAKs tomados 2×/d, em caso de dose dupla acidental, a próxima dose programada deve ser ignorada e o ciclo regular retomado com a dose após a próxima [10]. Com dose 1×/d, o ciclo normal deve ser continuado, uma vez que após 24 horas, mesmo com dose dupla acidental, uma grande parte da substância já é eliminada novamente.
Pergunta 4: E se o doente não tiver a certeza sobre a ingestão?
Não é raro que surjam situações na vida quotidiana em que o paciente não tem a certeza se já tomou ou não a sua medicação. Para NOAKs tomados 2×/d, recomenda-se não tomar outra dose (para evitar overdose, pois a dose seguinte é tomada em 12 horas de qualquer forma). Com uma ingestão 1×/d, por outro lado, recomenda-se tomar a dose potencialmente esquecida mais tarde, uma vez que a próxima ingestão não terá lugar durante mais 24 horas, o que de outra forma resultaria num período mais longo sem protecção relevante [10].
Pergunta 5: Como é que os NOAKs são utilizados na insuficiência renal?
Os doentes com insuficiência renal representam uma população de doentes difícil, pois tanto as complicações tromboembólicas como as hemorrágicas são mais frequentes [11, 12]. Em insuficiência renal grave e fibrilação atrial, os NOAK não foram praticamente estudados e não devem, portanto, ser utilizados (mesmo que também sejam parcialmente aprovados aqui) [13]. O problema é encontrar uma boa alternativa – porque os VKA também estão formalmente contra-indicados em função renal gravemente afectada. De facto, foi demonstrado que o benefício da VKA diminui com a diminuição crescente da função renal [14]. No entanto, os VKAs parecem ser actualmente a melhor opção para pacientes com fibrilação atrial e insuficiência renal grave – tendo em conta as advertências acima mencionadas. Aqui, um ajuste óptimo do INR é mais crucial do que nunca.
A dosagem de apixaban (50% de depuração renal da substância absorvida) e rivaroxaban (37% de depuração renal) é reduzida em função renal moderadamente reduzida (GFR 50 – 30 ml/min). (Tab. 1). Ambos os agentes demonstraram ser eficazes e seguros neste grupo de doentes (em comparação com a VKA), com o apixaban em particular a demonstrar um perfil de segurança muito bom em comparação com a VKA [11, 15]. Especialmente na presença de outros factores de risco de hemorragia (como a idade ≥ 80 anos, pontuação HAS-BLED ≥ 3), recomenda-se a redução da dose de dabigatran (80% de depuração renal) para 2 × 110 mg/d a partir de um GFR <50 ml/min [13]. Em princípio, a utilização de dabigatran em doentes com um GFR <40 ml/min deve ser bem considerada, pois a experiência demonstrou que nestes doentes pode ocorrer rapidamente uma maior deterioração da função renal com a correspondente acumulação da substância, por exemplo no contexto de doenças intercorrentes, co-medicação (AINEs!), ou desidratação.
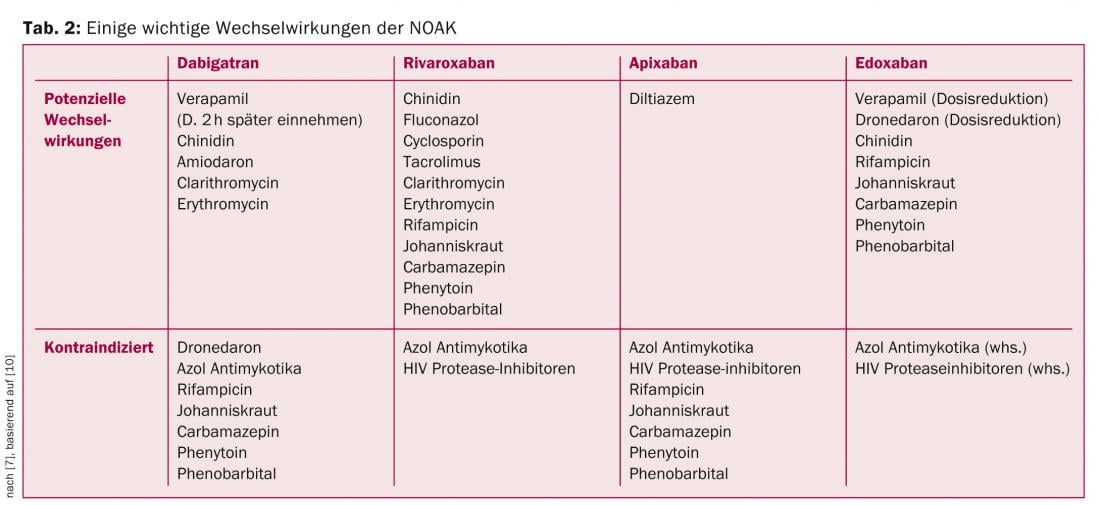
Pergunta 6: Existe alguma interacção com outros medicamentos?
Embora os NOAK tenham um potencial muito menor para interacções medicamentosas do que os VKAs, há algumas interacções importantes a ter em conta. Algumas das interacções mais importantes estão resumidas no Quadro 2, com base nas recomendações da EHRA [10].
Pergunta 7: Qual é o procedimento para sangrar sob NOAKs?
As complicações hemorrágicas, especialmente as hemorragias intracranianas e com risco de vida, ocorrem significativamente menos frequentemente com NOAKs do que com VKAs.
Estão em desenvolvimento antídotos específicos e de acção rápida para os NOAK; no entanto, o mais provável é que passem vários anos antes de serem introduzidos na prática clínica. Por conseguinte, os procoagulantes inespecíficos tais como PCC, aPCC ou FVIIa recombinante devem ser utilizados para uma antagonização rápida. Esta situação não é totalmente diferente da da VKA, uma vez que também aqui a antagonização “específica” por meio da vitamina K é tudo menos rapidamente eficaz na situação de emergência. Em princípio, a anticoagulação antagónica – seja por VKA ou NOAK – não está isenta de riscos, pois induz um estado pró-coagulante. Assim, uma normalização dos parâmetros de coagulação não está necessariamente correlacionada com um resultado clínico melhorado, especialmente após uma hemorragia intracraniana [16–18]. As recomendações da EHRA, baseadas principalmente em dados pré-clínicos e extrapolações farmacocinéticas, têm este facto em conta (Fig. 1) [10]. Consequentemente, a utilização de procoagulantes só é recomendada em casos de hemorragias graves e com risco de vida, enquanto que as medidas gerais são utilizadas principalmente em casos de hemorragias leves e moderadas.
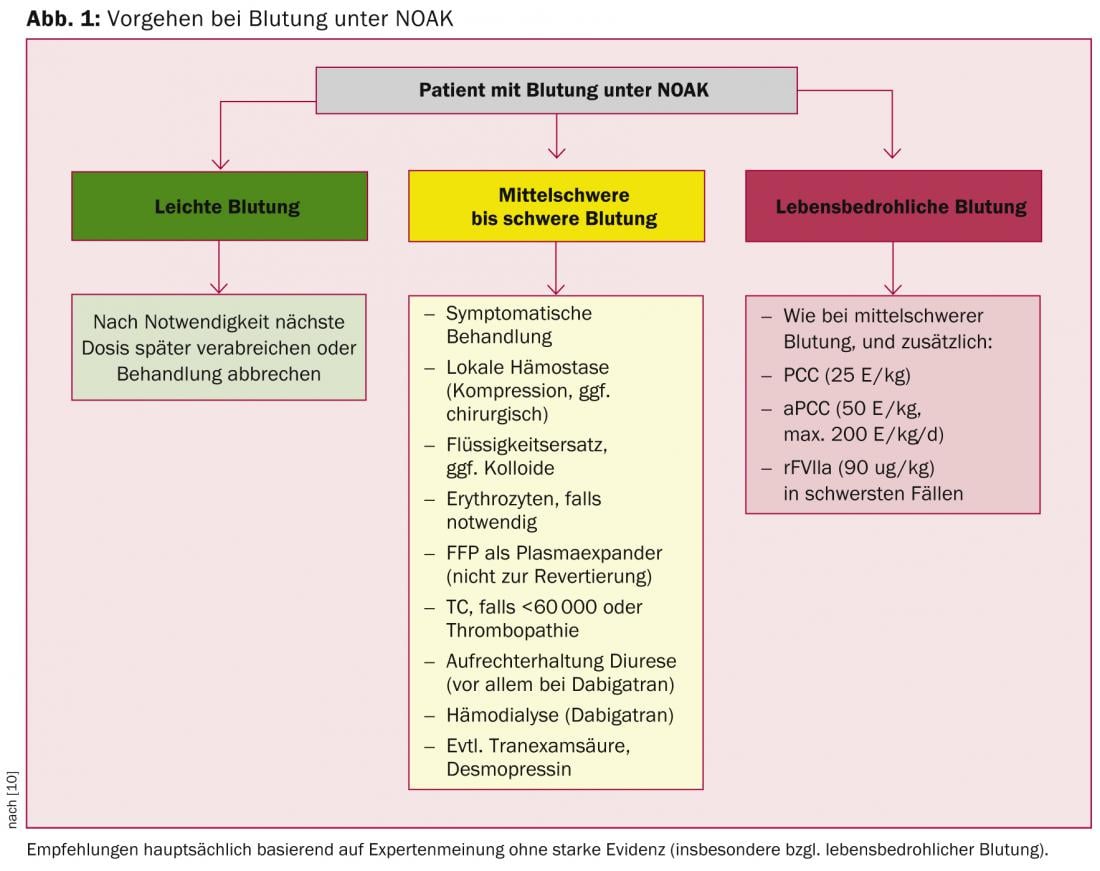
Pergunta 8: Qual é o melhor procedimento para a “tripla anticoagulação”?
Os doentes com fibrilação atrial que requerem formalmente uma dupla terapia antiplaquetária (a chamada “tripla anticoagulação”) para além da anticoagulação plasmática (NOAK/VKA) devido à ACS e/ou implante de stents têm um risco muito maior de hemorragia grave [19]. Actualmente, para além de alguns pacientes do estudo RE-LY, não existem dados sobre a utilização de NOAK em combinação com aspirina e clopidogrel. Da mesma forma, não há dados disponíveis sobre a combinação de NOAKs com a nova geração de antagonistas dos receptores ADP prasugrel e ticagrelor. Por conseguinte, uma combinação destas substâncias deve ser desencorajada no momento presente. Espera-se que as recomendações sejam ainda mais ajustadas à medida que surgirem novos dados – tanto sobre stents de última geração como sobre a combinação de NOAK, bem como sobre os novos medicamentos antiplaquetários. Actualmente, no entanto, a abordagem proposta nas directrizes do CES utilizando ASA, clopidogrel e VKA parece ser a melhor alternativa (Quadro 3) [20]. No estudo recentemente publicado WOEST, a combinação de clopidogrel e VKA demonstrou ser superior à clássica “tripla anticoagulação” – tanto em termos de eventos hemorrágicos como de pontos terminais isquémicos [21]. Na vida quotidiana, a duração da “tripla anticoagulação” originalmente recomendada nas directrizes do CES já é, portanto, significativamente reduzida, dependendo do cenário clínico.
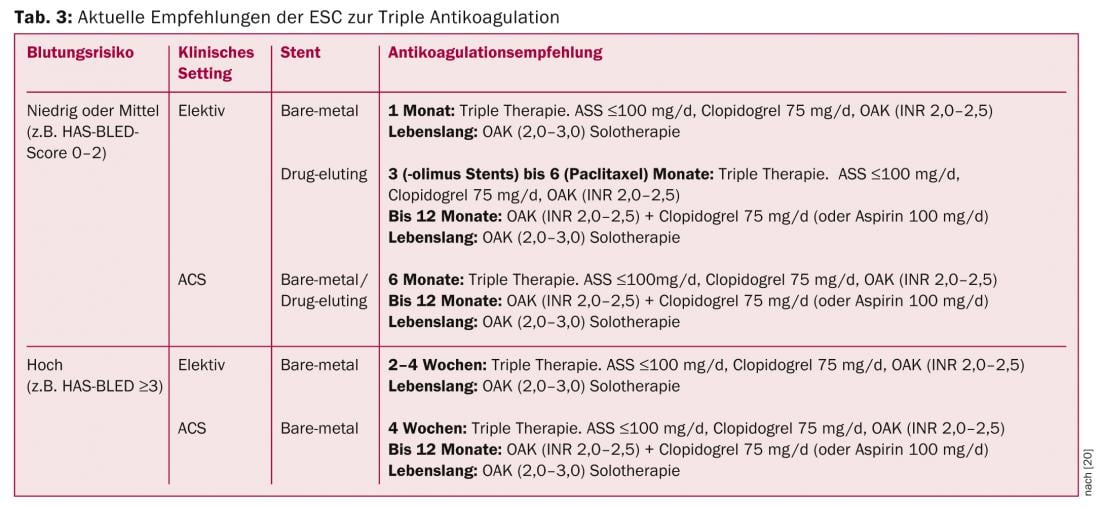
Pergunta 9: Podem os NOAKs ser utilizados em cardioversão?
Os melhores dados sobre cardioversão com NOAK estão disponíveis para dabigatran (a partir do estudo RE-LY): Esta última foi tão eficaz como a VKA em termos de AVC e hemorragia [22]. Para rivaroxaban e apixaban, os números de doentes publicados até agora são mais pequenos, mas apontam na mesma direcção. O factor decisivo na vida quotidiana é o cumprimento! Se for possível garantir que o paciente tomou o NOAK regularmente durante as três semanas anteriores (de preferência quatro a cinco), a cardioversão sob NOAK parece ser viável em segurança [10]. Caso contrário, um trombo deve ser excluído por meio de TEE. Os estudos e registos em curso fornecerão mais dados sobre o procedimento óptimo.
Pergunta 10: Como funciona a gestão perioperatória?
Devido à farmacocinética dos NOAKs, não é necessária nenhuma ponte perioperatória (que também é praticada cada vez mais raramente para os VKAs). A recomendação de descontinuar o NOAK baseia-se no risco de hemorragia do procedimento, bem como na função renal (maior influência com a dabigatran; Separador. 4).
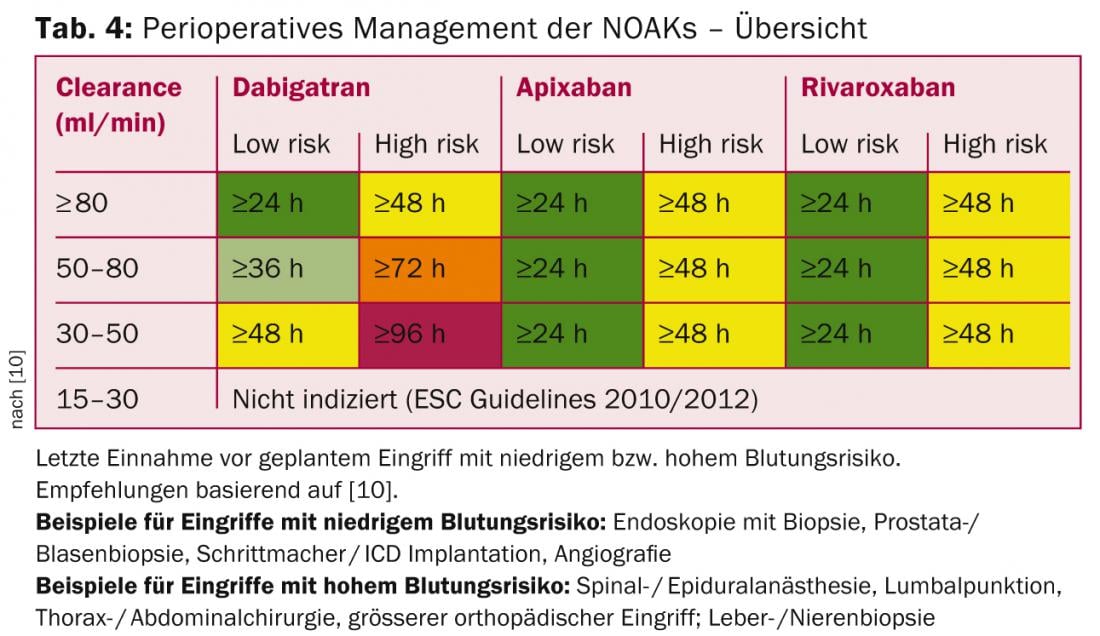
Para procedimentos com um risco de hemorragia muito baixo (intervenções dentárias, cataratas, glaucoma, endoscopia sem intervenção), o procedimento pode normalmente ser realizado ao nível do vale do NOAK (ou seja, antes da dose seguinte planeada), sendo a dose seguinte tomada seis horas mais tarde (se a hemostasia for boa) [10].
Seguindo o procedimento, o NOAK pode ser reiniciado após seis a oito horas em caso de hemostasia directa ou completa. Para procedimentos importantes onde ainda há risco de hemorragia, pode ser necessário esperar dois a três dias antes de reiniciar. Nestas situações, a heparina não fracionada ou de baixo peso molecular deve ser iniciada com uma dose profiláctica de seis a oito horas após a intervenção. Após hemostasia segura, a mudança para o NOAK é feita na dosagem completa.
Resumo
Devido aos resultados convincentes do estudo e à facilidade de utilização, os NOAK há muito que se tornaram parte da prática clínica diária de profilaxia de AVC para a fibrilação atrial. Não estão disponíveis dados de ensaios aleatorizados para muitas das recomendações práticas mencionadas. Contudo, ocorrem na vida quotidiana, pelo que são necessárias recomendações sobre a melhor forma de lidar com estas situações, com base na opinião de peritos, como o Guia Prático detalhado da EHRA [10]. Para um estudo mais detalhado, consultar esta e outras publicações [6, 7, 10].
PD Jan Steffel, MD
Declarações de conflito de interesses: O PD Dr. Jan Steffel recebeu honorários de consultoria e/ou conferências da AstraZeneca, Bayer HealthCare, Boehringer Ingelheim, Bristol-Myers Squibb, Daiichi Sankyo, Pfizer e Roche.
Literatura:
- Connolly SJ, et al: Dabigatran versus warfarin em doentes com fibrilação atrial. N Engl J Med 2009; 361: 1139-1151.
- Patel MR, et al: Rivaroxaban versus warfarin em fibrilação atrial não-valvar. N Engl J Med 2011; 365: 883-891.
- Granger CB, et al: Apixaban versus warfarin em doentes com fibrilhação atrial. N Engl J Med 2011; 365: 981-992.
- Giugliano RP, et al: Edoxaban versus warfarin em doentes com fibrilação atrial. N Engl J Med 2013.
- Steffel J, Braunwald E: Novos anticoagulantes orais: Foco na prevenção e tratamento do tromboembolismo venoso. Eur Heart J 2011; 32: 1968-1976.
- Steffel J, Brunckhorst C: Profilaxia do AVC em fibrilação atrial. Bremen: UniMed; 2012.
- Steffel J, et al: Prevenção do AVC na fibrilação atrial. Bremen: UniMed; 2014 (no prelo).
- Steffel J: Novos anticoagulantes: prevenção e tratamento de eventos tromboembólicos. Principais opiniões Cardiologia + Medicina Vascular 2011; 2: 14-19.
- Steffel J: Os novos anticoagulantes – aspectos práticos na aplicação. Leading Opinions Cardiology + Vascular Medicine 2012; 2: 10-14.
- Heidbuchel H, et al: guia prático da associação europeia de ritmo cardíaco sobre a utilização de novos anticoagulantes orais em doentes com fibrilação atrial não-valvar. Europace 2013; 15: 625-651.
- Steffel J, Hindricks G: Apixaban em insuficiência renal: Navegação bem sucedida entre o scylla e o charybdis. Eur Heart J 2012; 33: 2766-2768.
- Steffel J: Novos anticoagulantes orais em função renal deficiente e diálise. Leading Opinions Nephrology 2013; 2: 73-75.
- Camm AJ, et al: 2012 actualização focalizada das orientações do esc para a gestão da fibrilação atrial: Uma actualização das orientações do esc de 2010 para a gestão da fibrilação atrial. Desenvolvido com a contribuição especial da associação europeia do ritmo cardíaco. Europace 2012.
- Marinigh R, Lane DA, Lip GY: Deficiência renal grave e prevenção de AVC na fibrilação atrial: Implicações para tromboprofilaxia e risco de hemorragia. J Am Coll Cardiol 2011; 57: 1339-1348.
- Hohnloser SH, et al.: Eficácia do apixaban quando comparado com a warfarina em relação à função renal em doentes com fibrilação atrial: Percepções do ensaio de aristóteles. Eur Heart J 2012.
- Dowlatshahi D, et al: Mau prognóstico na hemorragia intracraniana associada à warfarina, apesar da inversão da anticoagulação. Stroke 2012; 43: 1812-1817.
- Lee SB, et al: Progressão da hemorragia intracerebral associada à warfarina após a normalização com ffp. Neurologia 2006; 67: 1272-1274.
- Kuwashiro T, et al: Efeito do complexo de protrombina concentrado no aumento do hematoma e resultado clínico em doentes com hemorragia intracerebral associada a anticoagulantes. Cerebrovasc Dis 2011; 31: 170-176.
- Sourgounis A, et al: Stents coronários e anticoagulação crónica. Circulação 2009; 119: 1682-1688.
- Camm AJ, et al: Guidelines for the management of atrial fibrillation: The task force for the management of atrial fibrillation of the european society of cardiology (esc). Europace 2010; 12: 1360-1420.
- Dewilde WJ, et al: Utilização de clopidogrel com ou sem aspirina em doentes em terapia anticoagulante oral e submetidos a intervenção coronária percutânea: Um ensaio aberto, aleatório, controlado. Lancet 2013; 381: 1107-1115.
- Nagarakanti R, et al: Dabigatran versus warfarin em pacientes com fibrilação atrial: Uma análise de pacientes submetidos a cardioversão. Circulação 2011; 123: 131-136.
CARDIOVASC 2014; 13(2): 12-16
PRÁTICA DO GP 2014; 9(6): 32-37