Com a aprovação do Dupilumab como a primeira biologia para o tratamento da dermatite atópica, foram feitos progressos significativos. Como mostra uma análise dos ensaios clínicos em curso, a investigação tem mais setas na sua aljava. Entre os biólogos, os programas de estudo para o tralokinumabe de anticorpos IL13 são os mais avançados. Entre os inibidores JAK, o baricitinib é um promissor candidato a medicamento que já recebeu uma extensão de indicação para a dermatite atópica na UE.
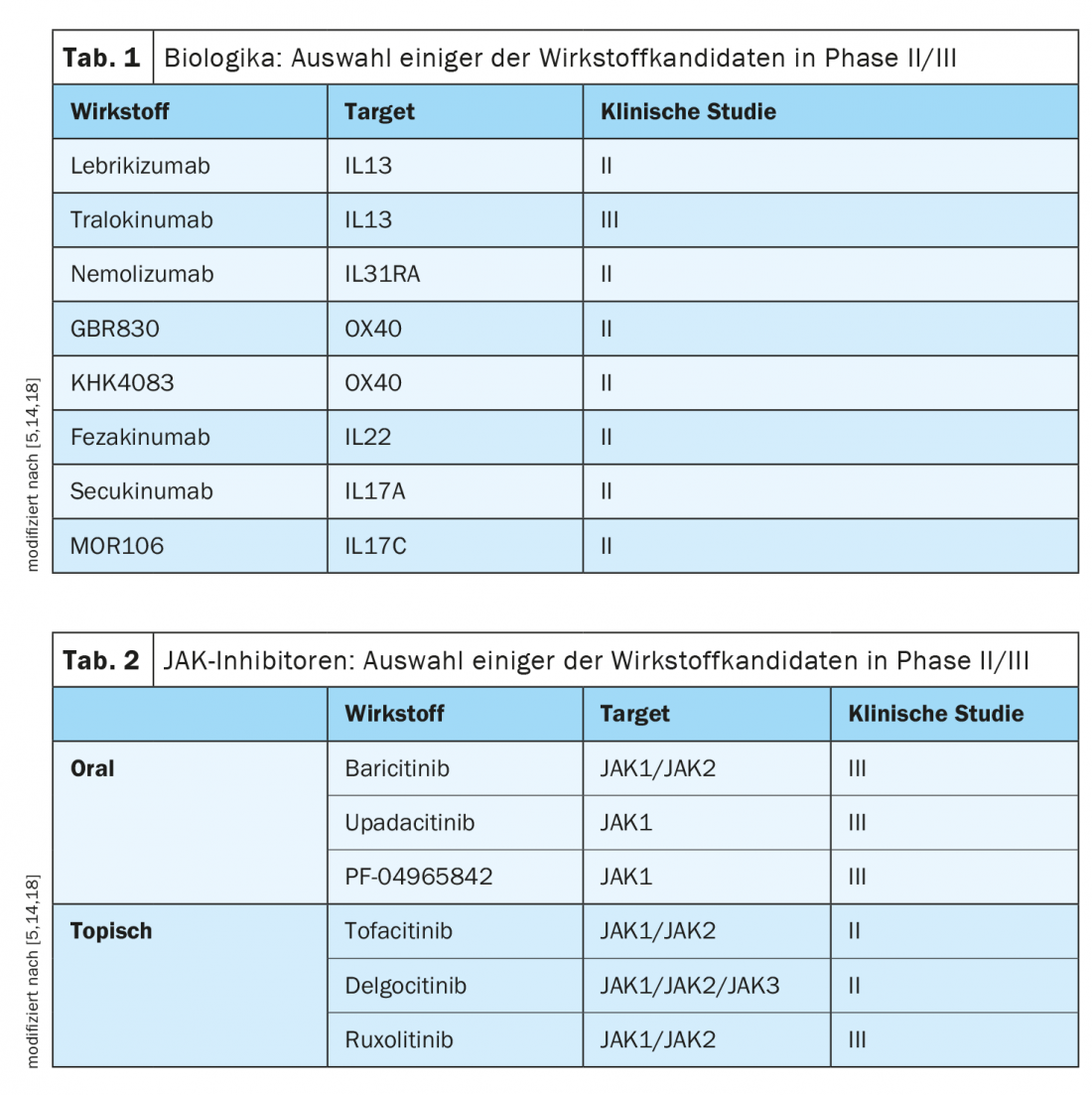
O desenvolvimento de abordagens terapêuticas específicas baseia-se, entre outras coisas, em avanços na compreensão da base imunopatológica complexa e heterogénea da dermatite atópica [1]. Segundo os especialistas, o panorama terapêutico desta complexa doença inflamatória irá mudar rapidamente nos próximos anos. Há uma boa hipótese de que, para além do dupilumab, outros representantes da classe de medicamentos biológicos expandam o espectro de tratamento para formas moderadas a severas da doença num futuro não muito distante. (Tab.1). E também no campo dos inibidores JAK, há vários compostos promissores que estão a ser testados em ensaios clínicos (Tab.2). Em contraste com a cortisona ou ciclosporina, os inibidores biológicos e JAK influenciam selectivamente as cascatas de activação individual do sistema imunitário. Como resultado, estas abordagens terapêuticas modernas têm não só um elevado grau de eficácia, mas também um perfil de efeito secundário favorável, o que oferece grandes vantagens, especialmente tendo em conta o facto de a dermatite atópica ser um quadro clínico crónico e recaída.
O Dupilumab biológico (Dupixent®), aprovado na Suíça desde 2019 para dermatite atópica moderada a grave, provou ser extremamente eficaz e tem um excelente perfil de risco-benefício. É o primeiro representante dos anticorpos monoclonais para esta indicação. Dupilumab inibe as vias de sinalização das duas principais citocinas IL4 e IL13, que são consideradas importantes motores do processo inflamatório em curso na dermatite atópica [2,3]. Que os resultados de grandes ensaios clínicos como SOLO1/2, CHRONOS ou CAFE também são confirmados na prática é demonstrado pelos dados sobre a avaliação desta opção terapêutica no cenário do “mundo real” [2,4,5]. Os doentes beneficiam grandemente deste tratamento, o que também se reflecte numa boa adesão [5]. Uma análise dos ensaios clínicos em curso mostra que, para além do dupilumab, outras terapias orientadas poderiam fazer um avanço nos próximos anos (Tab. 1 e 2).
Além do tralokinumab, também lebrikizumab com resultados promissores
Estudos dos mecanismos imunopatológicos na dermatite atópica mostraram que as citocinas IL4, IL13 e IL31 produzidas por células Th2 são de importância fisiopatológica central [6]. Entre os agentes actualmente testados clinicamente, os estudos sobre o tralokinumab inibidor da IL13 são os mais avançados [5]. Nos ensaios ECZTRA 1 e 2 fase III, a condição tralokinumab (300 mg a cada 2 semanas) mostrou uma melhoria significativa no IGA* em comparação com o placebo (p<0,001) após apenas 16 semanas [19]. Isto confirmou os bons resultados do estudo da fase IIb, em que taxas de resposta até 70% para EASI50 e até 40% para EASI75 foram alcançadas em doentes com dermatite atópica moderada a grave [7].
* IGA = Avaliação Global dos Investigadores
|
A dermatite atópica pode levar a altos níveis de sofrimento Vários estudos empíricos mostram que a dermatite atópica é frequentemente acompanhada por uma considerável deterioração da qualidade de vida. Num estudo populacional com adultos, mais de metade das pessoas afectadas referiu que o estado da pele estava associado a limitações na sua vida diária e, por mais de um terço, o aparecimento levou a evitar o contacto social [15]. Além disso, verificou-se que estas consequências negativas eram significativamente mais pronunciadas em doentes com dermatite atópica moderada a grave do que nas formas ligeiras da doença. De acordo com dados actuais da investigação dos serviços de saúde, cerca de um em cada dez pacientes com neurodermatite é afectado por sintomas moderados a graves [16,17]. |
Dados de eficácia igualmente bons estão disponíveis para o lebrikizumab. Este é também um inibidor da IL13. Ao contrário do tralokinumab, o lebrikizumab impede a ligação do receptor de sinalização IL13R-α1 e IL4R-α-heterodimer, mas não a ligação do IL13 ao “receptor de engodo IL13R-α2”, que pode ocupar o excesso de IL13 [8]. Os resultados dos ensaios em curso da fase III estão ainda pendentes. Nos dois estudos aleatórios da fase II controlados por placebo realizados até à data, os doentes tratados com lebrikizumab mostraram uma redução rápida e dependente da dose do prurido, bem como uma melhoria significativa na EASI 50/75 e na BSA [9,10]. Os doentes foram aleatorizados para os braços de tratamento de 125 mg a cada quatro semanas, 250 mg a cada quatro semanas ou 250 mg a cada quinzena durante 16 semanas [11].
Um candidato interessante à droga que visa a IL31 é o nemolizumab. Tanto as provas de conceito como as observações mais longas na fase IIb demonstraram um valor acrescentado na área do controlo da coceira [12]. Outros estudos mostrarão qual é o potencial de efeito no que diz respeito a outros parâmetros. Também em ensaios clínicos há representantes de anticorpos anti-OX40, anti-IL22 e anti-IL17 [5].
Baricitinib em breve também aprovado na Suíça?
Ao contrário das terapias baseadas em anticorpos, que normalmente visam citocinas ou receptores de citocinas, as pequenas moléculas interferem com as vias de sinalização intracelular. O maior grupo destas substâncias de pequenas moléculas são os inibidores de Janus kinase (JAK). As JAK são enzimas intracelulares que medeiam a cascata de sinalização de um receptor de citocinas para a célula. Até agora, foram desenvolvidos vários inibidores JAK com diferentes capacidades de ligação a subformas individuais das Janus kinases (JAK1-3). Baricitinib, uma substância dirigida contra a JAK1/2, é um dos inibidores orais de JAK mais promissores [5]. Nas avaliações da primeira fase II dos ensaios clínicos, a eficácia na gama de 60-82% é relatada em relação às taxas EASI50, dependendo dos períodos terapêuticos e dos protocolos de estudo [13]. Na UE, já foi concedida uma extensão de indicação para a dermatite atópica para o baricitinib [20]. Na Suíça, no entanto, esta opção de tratamento só é actualmente aprovada para a indicação de artrite reumatóide activa. Dados promissores estão também disponíveis no upadacitinib inibidor JAK1. Os resultados de análises intercalares de um estudo de fase IIb mostram uma boa eficácia e tolerabilidade numa dose de 30 mg/d em doentes adultos com dermatite atópica moderada a grave [10].
Em resumo, os inibidores JAK demonstraram ser eficazes no tratamento da dermatite atópica em estudos até à data, sendo o seu rápido início de acção particularmente interessante [5]. No que diz respeito ao perfil de efeitos secundários, foi demonstrado que é necessária uma monitorização intensiva dos doentes para controlar o risco de infecção e possíveis alterações do hemograma. Os inibidores JAK podem ser úteis no futuro, especialmente para terapias de intervalo curto [5]. O perfil do efeito secundário varia em função da substância e da dose e pode ser reduzido por aplicação tópica; estão actualmente em curso vários estudos (por exemplo, sobre tofacitinibe, delgocitinibe, ruxolitinibe). Devido ao pequeno tamanho molecular dos inibidores JAK, a penetração através da pele é possível, o que é um bom pré-requisito para a aplicação tópica.
Fonte: Reunião Anual da EADV 2020
Literatura:
- Langley RGB: Emerging Biologics for Atopic Dermatitis in Adults and Children, Professor Richard GB Langley MD, Halifax (Canadá), EADV (Virtual) 31.10.2020.
- Simpson EL, et al: Duas experiências fase 3 de dupilumab versus placebo em dermatite atópica. N Engl J Med 2016; 375: 2335-2348.
- Swiss Drug Compendium, www.compendium.ch (último acesso 17.2.2021)
- Thaci: Eficácia e segurança da monoterapia dupilumab em adultos com dermatite atópica moderada a grave: uma análise conjunta de dois ensaios aleatórios da fase 3 (LIBERTY AD SOLO 1 e LIBERTY AD SOLO 2). J Dermatol Sci 2019 266-275.
- Worm M, et al: Modern therapy of atopic dermatitis: biologics and small molecule drugs. JDDG 2020; 18: 10: 1085-1093.
- Bieber T, et al: Novas terapias baseadas na patofisiologia da dermatite atópica. JDDG 2019 17; 11: 1150-1163.
- Wollenberg A, et al: Tratamento de dermatite atópica com tralokinumab, um anti-IL 13mAb. J Allergy Clin Immunol 2019; 143(1): 135-141.
- Maul JT: O que há de novo 2019/2020: Dermatoses inflamatórias. Julia-Tatjana Maul, MD, Zürcher Dermatologische Fortbildungstage (ZDFT), 14/15.05.2020.
- Simpson EL, Flohr C, Eichenfield LF, et al: Eficácia e segurança do lebrikizumab (um anticorpo monoclonal anti-IL-13) em adultos com dermatite atópica moderada a severa controlada inadequadamente por corticosteróides tópicos: Um ensaio aleatório, controlado por placebo fase II (TREBLE). J Am Acad Dermatol 2018; 78(5): 863-871.e811
- Guttman-Yassky E, et al: Eficácia e Segurança de Lebrikizumab, um Inibidor da Interleucina 13 de Alta Afinidade, em Adultos com Dermatite Atópica Moderada a Grave: Um Ensaio Clínico Aleatório de Fase 2b. JAMA Dermatol 2020: 156(4): 411-420.
- Loh TY, et al: Potencial terapêutico de Lebrikizumab no Tratamento da Dermatite Atópica. J Alergia à asma 2020; 13: 109-114.
- Ruzicka T, et al. Receptor anti-interleucina-31 Um anticorpo para a dermatite atópica. N Engl J Med 2017; 376: 826-835.
- Fragoulis GE, McInnes IB, Siebert S: inibidores JAK. Novos intervenientes no campo das doenças imuno-mediáticas, para além da artrite reumatóide. Reumatologia 2019; 58: i43-i54.
- Clinicaltrial.gov, www.clinicaltrial.gov (último acesso 17.2.2021).
- Silverberg JI, et al: Patient burden and quality of life in atopic dermatitis in US adults Um estudo transversal baseado na população. Annals of Allergy, Asthma and Immunology 2018, DOI: https://doi.org/10.1016/j.anai.2018.07.006
- Augustin, et al.: Datenanalyse CVderm 2020. Versorgungsexpertise Neurodermitis in Deutschland, dados em ficheiro.
- Kirsten N: Terapia da neurodermatite durante a Corona: conceitos actuais postos à prova e o que é importante para si agora. Evento para doentes, Dra. Natalia Kirsten, Hautnetz Hamburgo, 17.09.20
- Li R, Hadi S, Guttman-Yassky E: terapias biológicas actuais e emergentes e pequenas moléculas para dermatites atópicas. Parecer de especialista Biol Ther 2019; 4: 367-380.
- Wollenberg A: Tralokinumab para dermatite atópica moderada a grave: resultados de dois ensaios de fase III (ECZTRA 1 e ECZTRA 2) de 52 semanas, aleatorizados, duplo-cegos, multicêntricos e controlados por placebo, https://doi.org/10.1111/bjd.19574
- Hüttemann D: Inibidores JAK: Novo modo de acção aprovado para a dermatite atópica. Jornal Farmacêutico (Online), 03.11.2020
DERMATOLOGIE PRAXIS 2021; 31(1): 33-34 (publicado 22.2.21, antes da impressão).











