Com o envelhecimento da sociedade, as doenças MDS estão também a aumentar. No entanto, os desenvolvimentos no diagnóstico molecular e as novas terapias irão também alterar a gestão dos pacientes mais velhos. Uma abordagem multidisciplinar e o intercâmbio são importantes.
As síndromes mielodisplásticas (MDS) são diagnosticadas como doenças dos idosos, principalmente em doentes >70 anos. Na Suíça, com uma incidência de 2-3/100.000 doentes-ano, é de esperar um pouco mais de 300 novos casos por ano. Estima-se actualmente que existam 1600 pacientes com MDS a viver no nosso país [1]. As opções terapêuticas permaneceram essencialmente inalteradas nos últimos anos, com o transplante alogénico de células estaminais como tratamento curativo possível apenas para alguns pacientes, e várias opções para melhorar as citopénias nas restantes situações paliativas [2–5]. Em contraste, o rápido desenvolvimento da “sequenciação da próxima geração” (NGS) também levou a novas descobertas relevantes na rotina clínica da hematologia [6,7] que desempenham um papel para os doentes com MDS no que diz respeito ao diagnóstico e avaliação do prognóstico. Com base na classificação actualizada da OMS de 2016, serão apresentados a seguir os desenvolvimentos e conceitos mais importantes.
Revisão da Classificação da OMS 2016
Mesmo na era da biologia molecular, a avaliação morfológica de esfregaços de sangue periféricos e aspirados de medula óssea continua a ser a base do diagnóstico. Basicamente, as formas MDS com excesso de explosão distinguem-se daquelas sem proliferação de explosivos. O número de linhas de células afectadas por citopenias e displasias, a detecção de sideroblastos em anel (RS) e as alterações citogenéticas típicas são decisivas para uma maior subdivisão. Uma nova característica da classificação de 2016 da OMS é a nomenclatura (Tab. 1) [8,9]. Os termos “anemia refratária” ou “citopenia refratária” foram abandonados e o termo “síndrome mielodisplásica” é agora utilizado para todas as entidades, complementado pelo achado morfológico do núcleo. Isto esclarece algumas incongruências da terminologia anterior, tais como o termo “anemia refratária” para as formas de MDS com excesso de explosão que são frequentemente acompanhadas por pancitopenia.

A citogenética convencional em metafase continua a ser o segundo pilar indispensável do diagnóstico MDS. Em doentes com citopenias sem proliferação de explosões e sem displasias (significativas), o diagnóstico pode ser feito através da detecção de certas anomalias citogenéticas de definição de MDS (Tab. 2). Neste caso, é atribuído o diagnóstico “MDS não-classificável”. Esta categoria inclui também casos com pancitopenia e displasia de linha única ou com detecção constante de explosão de 1% no sangue periférico sem multiplicação de explosão na medula óssea [8,9].
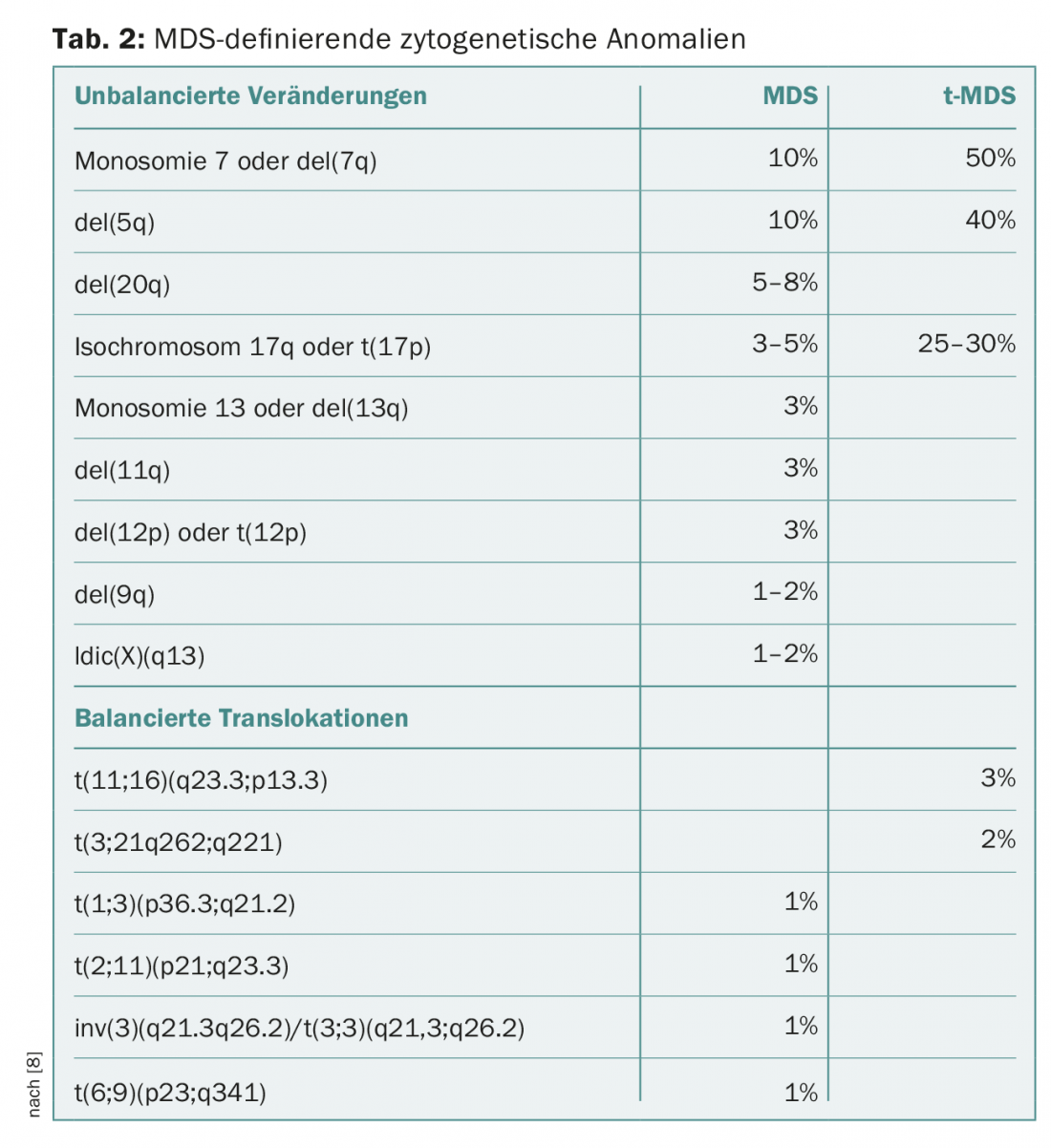
A categoria do MDS caracterizada por uma eliminação no braço curto do cromossoma 5 com del(5q) foi alargada na sua definição. Agora, os casos com uma segunda anomalia citogenética também podem ser atribuídos a esta categoria, excepto no caso de anomalias adicionais no cromossoma 7, que estão associadas a um prognóstico significativamente pior [8–10].
A citogenética convencional (a análise de pelo menos 20 metafases é necessária para um exame conclusivo) pode ser complementada por outros métodos em situações seleccionadas, por exemplo, no caso de uma suspeita morfologicamente elevada de MDS del(5q) mas kariótipo normal. Podem ser utilizados painéis FISH centrados em anomalias cromossómicas típicas do MDS ou microarrays de hibridização genómica comparativa de todo o genoma (array-CGH) [11]. Contudo, estes dois métodos não oferecem um substituto a priori para a citogenética convencional. Em particular, o significado prognóstico das anomalias que só podem ser detectadas na matriz CGH ainda não foi esclarecido com certeza.
Importância diagnóstica da sequência de “próxima geração” em citopénias pouco claras
Nos últimos anos, foram identificadas numerosas mutações em genes que estão associadas ao desenvolvimento do MDS e à progressão para AML. O espectro dos “genes condutores” mutantes é diversificado e inclui frequentemente componentes da modificação epigenética do ADN e das histórias ou da maquinaria de emenda modificadora do ARN (“spliceosome”). Componentes da regulação do ciclo celular, complexos de coesina, factores de transcrição ou componentes da transdução de sinal intracelular também podem ser afectados (Tab. 3) [2,12–18].
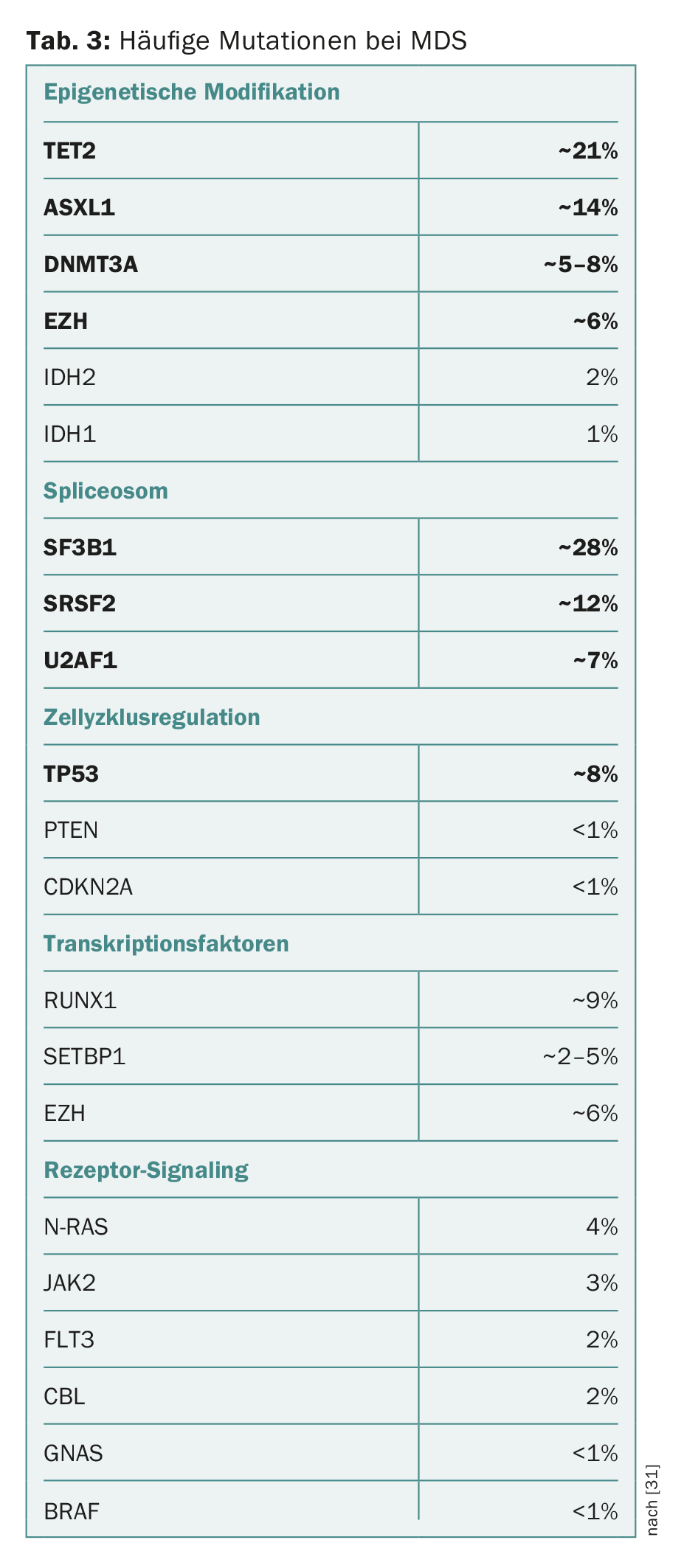
Por um lado, é de salientar que a maioria das mutações do gene condutor encontradas no MDS também ocorrem em outras neoplasias mielóides, embora em frequências ou combinações diferentes. Além disso, vários estudos demonstraram que as mutações típicas das neoplasias mielóides também podem ocorrer em indivíduos hematologicamente saudáveis. A incidência aumenta acentuadamente com a idade, de 10% em jovens de 60 anos para 15-20% em >jovens de 80 anos (mas <1% em <jovens de 40 anos). Este fenómeno tem sido denominado “Hematopoiese Clonal de Potencial Indeterminado” (CHIP) [19,20]. Semelhante à gamopatia monoclonal de importância desconhecida (MGUS) e à linfocitose monoclonal de células B (MBL), é uma condição pré-cancerosa facultativa que pode progredir para doença hematológica maligna a uma taxa de cerca de 1% por ano. Além disso, os pacientes com CHIP também aumentaram a morbilidade cardiovascular [21].
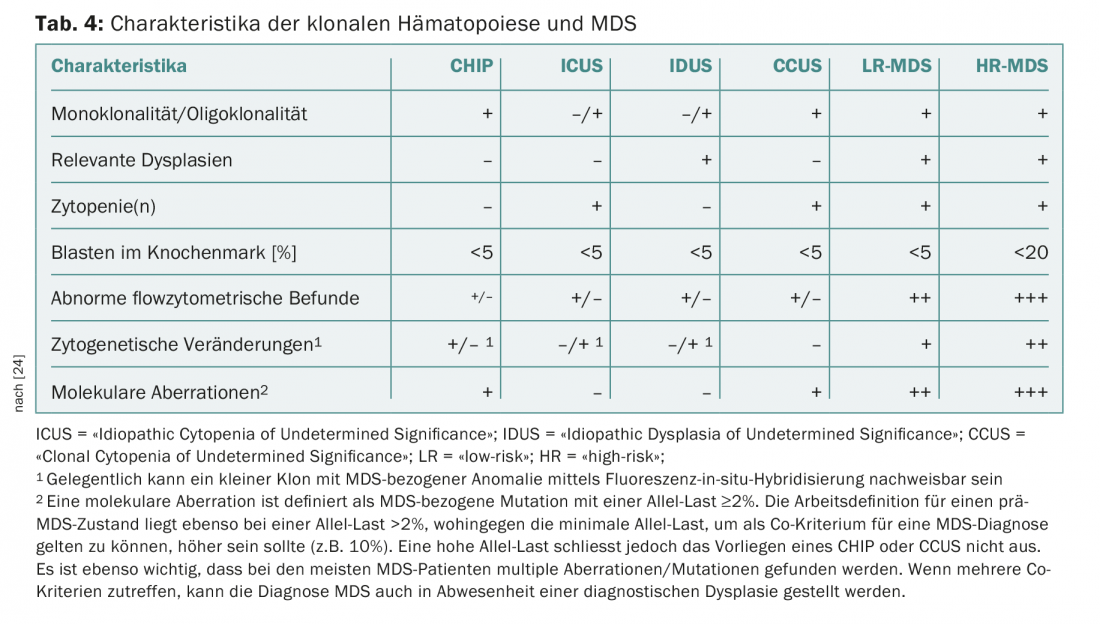
Um problema recorrente na prática e clínica são pacientes com citopenias persistentes para os quais não é possível encontrar causas definitivas. Na ausência de displasia ou de anomalias citogenéticas definidoras de MDS, estas foram até agora agrupadas sob o termo “Idiopathic Cytopenia of Undetermined Significance” (ICUS) [22]. A detecção de mutações recorrentes pode ajudar a distinguir as citopenias reactivas das citopenias clonais. A interpretação de uma detecção de mutação depende do tamanho do clone (medido como “frequência alelo variante”, VAF) e do número de mutações detectadas. Se uma mutação recorrente com um VAF superior a 2% for encontrada numa constelação ICUS, esta é referida como uma “Citopenia Clonal de Significado Indeterminado” (CCUS). Entre os doentes com CCUS, aqueles com pelo menos duas mutações com FVA >10% estão em alto risco de desenvolver uma neoplasia hematológica nos próximos cinco anos [23]. Os critérios recentemente apresentados por um painel internacional de peritos para distinguir CHIP, ICUS, CCUS do manifesto MDS [24] estão resumidos no quadro 4. Este consenso define também novos critérios menores relacionados com o MDS, que podem ser utilizados para um diagnóstico provisório do MDS em situações inconclusivas (Tab. 5).

A acumulação sequencial de alterações genéticas nas HSC foi há muito postulada como um correlato patogénico da evolução clonal, e o conceito de hematopoiese clonal demonstra uma sobreposição entre alterações na hematopoiese com a idade e a patogénese das neoplasias mielóides. Contudo, ainda não está claro quais os factores responsáveis pela transição do CHIP e CCUS para a neoplasia manifesta. A evolução clonal parece ser causada não só por células intrínsecas (mutações nas células estaminais hematopoiéticas), mas também por mecanismos extrínsecos das células. A este respeito, o microambiente na medula óssea e os componentes do sistema imunitário inato e adquirido desempenham um papel importante. O “stress imunológico” explica provavelmente também a associação com doenças ou fenómenos inflamatórios e imunológicos concomitantes parcialmente não classificáveis que podem ocorrer em doentes com MDS [25–28]. A perda do controlo do tumor imunológico, bem como a facilitação de mudanças no nicho da medula óssea, são actualmente o foco da investigação básica. No futuro, isto poderá levar a novas abordagens terapêuticas que poderão ser utilizadas precocemente no desenvolvimento de neoplasias mielóides (Fig. 1).
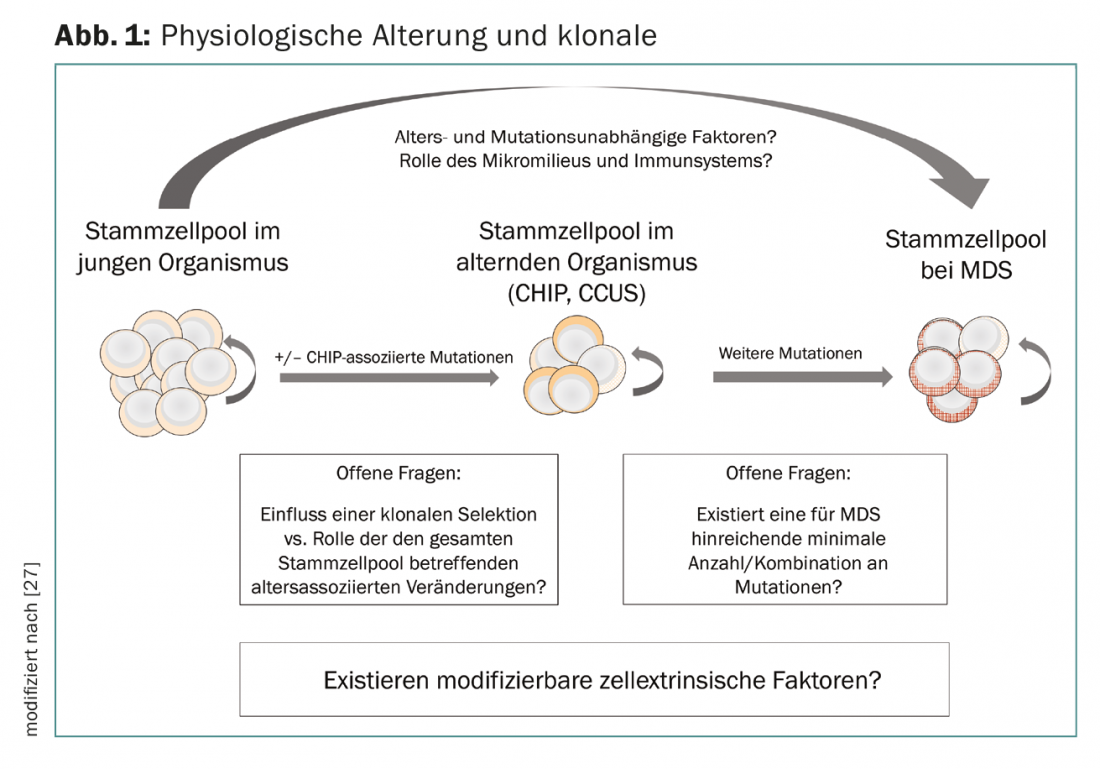
Devido à sobreposição no espectro de mutação entre CHIP, CCUS e o MDS, as análises de mutação não foram deliberadamente incluídas na actual classificação da OMS. Uma excepção são as mutações no gene condutor do componente spliceosome SF3B1, que estão muito fortemente associadas a um fenótipo ringideroblástico [29]. Segundo a OMS 2016, no caso de uma mutação SF3B1, a detecção de 5% RS é suficiente para a classificação no grupo de MDS com RS, em vez dos 15% exigidos de outra forma. Os pacientes com mutação SF3B1 têm um prognóstico muito bom com baixa probabilidade de progressão para LMA. Uma vez que os pacientes com displasia multilineaginosa e RS também beneficiam da influência prognóstica de uma mutação SF3B1, a entidade MDS com displasia multilineaginosa e RS foi reintroduzida na classificação de 2016.
Mais prognóstico e significado preditivo das mutações do gene condutor
De um ponto de vista prognóstico, alguns cenários clínicos adicionais já podem ser nomeados, nos quais as análises de mutação podem fornecer informações relevantes. Cerca de 15% dos doentes com MDS del(5q) têm uma mutação TP53. Embora estes também respondam hematologicamente à lenalidomida, são menos susceptíveis de alcançar a remissão citogenética e têm um risco mais elevado de transição AML. Portanto, se uma mutação TP53 for detectada no MDS del(5q), terapias alternativas podem ser consideradas [3,30].
Outro cenário para a pesquisa da mutação diz respeito ao grupo heterogéneo de pacientes no grupo “intermédio” de acordo com a IPSS-R. Dependendo da presença ou ausência de outras características de risco, estes pacientes podem ser tratados de acordo com as recomendações aplicáveis a pacientes de “baixo” ou “alto risco” [2–5,30]. Até agora, para além do exame isolado de citogenética (constelação de alto risco?), só estão disponíveis para este fim marcadores de risco convencionais (por exemplo, elevação de LDH, fibrose da medula óssea >grau 2 de acordo com a OMS). Várias mutações recorrentes estão associadas a um risco significativamente aumentado e justificam um aumento do prognóstico para a categoria de “alto risco” e, em pacientes seleccionados, transplante alogénico de células estaminais [15]. A pesquisa de mutações TP53, ASXL1, RUNX1, EZH2 e ETV6 em pacientes que se qualificam para terapia intensiva é, portanto, explicitamente recomendada nas actuais directrizes [4,15]. Um projecto internacional patrocinado pela Fundação MDS está actualmente empenhado no desenvolvimento de uma “IPSS-R molecular” complementada pelo estatuto de mutação.
Os dados clinicamente úteis sobre o valor preditivo do perfil da mutação no MDS são actualmente limitados. Está a surgir para o futuro uma relevância para a estratificação no que diz respeito às terapias orientadas. Luspatercept (ACE-356) é um inibidor da superfamília TGF-β [10], que mostrou uma elevada taxa de resposta eritróide em pacientes MDS EPO-refractários com RS e/ou mutações em SF3B1. Além disso, os inibidores de emendas (H3B-8800) estão actualmente a ser investigados em AML e MDS que, devido à insuficiência de haplo-insuficiência, eliminam preferencialmente os clones com mutações nos genes de emendas (efeito ciclops). Além disso, as substâncias midostaurina (mutações FLT3), enasidenibe (mutações IDH2) e ivosidenibe (mutações IDH1), que já foram aprovadas para AML, estão actualmente também em desenvolvimento clínico para MDS de alto risco com um perfil de mutação correspondente, quer como uma única substância, quer em combinação com terapia hipometilante (HMT) ou quimioterapia padrão.
Mensagens Take-Home
- Devido ao envelhecimento da nossa sociedade, é de esperar um aumento significativo da doença MDS.
- Os desenvolvimentos no diagnóstico molecular, bem como novas opções terapêuticas, irão mudar as estratégias de tratamento também para os pacientes mais velhos.
- A gestão multidisciplinar é um pré-requisito importante e representa novos desafios para os sistemas de saúde. Isto diz respeito não só aos cuidados adequados na prática clínica de rotina, mas também à realização de ensaios clínicos, que requerem um elevado grau de cooperação e coordenação no caso de doenças raras na era da medicina personalizada.
- Em resposta a estes desafios, o Grupo de Estudo Suíço MDS lançou o Swiss MDS Registry/Biobank em 2015 para facilitar o intercâmbio clínico e científico dentro de uma rede internacional.
Literatura:
- Bonadies N, et al: Tendências de classificação, incidência, mortalidade e sobrevivência dos doentes com MDS na Suíça entre 2001 e 2012. Epidemiologia do cancro 2017; 46: 85-92.
- Malcovati L, et al: Diagnóstico e tratamento de síndromes mielodisplásticas primárias em adultos: Recomendações da European LeukemiaNet. Sangue 2013; 122(17): 2943-2964.
- Fenaux P, et al: Myelodysplastic syndromes: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Anais de oncologia: revista oficial da Sociedade Europeia de Oncologia Médica 2014; 25(Suplemento 3): iii57-69.
- Hofmann WK, Platzbecker U, Götze K: Síndrome de Onkopedia-Leitlinie Myelodysplastische. Situação Março de 2016.
- Greenberg PL, et al: Myelodysplastic Syndromes, Version 2.2017, NCCN Clinical Practice Guidelines in Oncology. Journal of the National Comprehensive Cancer Network: JNCCN 2017; 15(1): 60-87.
- Johnsen JM, Nickerson DA, Reiner AP: sequenciação maciçamente paralela: A nova fronteira da genómica hematológica. Sangue 2013; 122(19): 3268-3275.
- Kuo FC, et al: As utilidades relativas de todo o genoma, painel genético, e sequenciação individual de genes na prática clínica. Sangue 2017; 130(4): 433-439.
- Swerdlow SH, et al. (Eds.): Classificação da OMS de tumores de tecidos hematopoiéticos e linfóides. 4ª edição revista. Lyon: Agência Internacional de Investigação sobre o Cancro 2017.
- Arber DA, et al: A revisão de 2016 da classificação da Organização Mundial de Saúde das neoplasias mielóides e da leucemia aguda. Sangue 2016; 127(20): 2391-2405.
- Mies A, Platzbecker U: Aumentar a eficácia da hematopoiese em síndromes mielodisplásticas: agentes estimulantes da eritropoiese e factores de crescimento transformadores-β superfamiliares inibidores. Seminários em hematologia 2017; 54(3): 141-146.
- Ouahchi I, et al.: A hibridação genómica comparativa baseada em microarranjos revela aberrações recorrentes adicionais em pacientes adultos avaliados para síndrome mielodisplásica com cariótipo normal. Revista britânica de hematologia 2018. DOI: 10.1111/bjh.15068 [Epub ahead of print].
- Kon A, et al.: Mutações recorrentes em múltiplos componentes do complexo de coesina em neoplasias mielóide. Genética da natureza 2013; 45(10): 1232-1237.
- Yoshida K, et al.: Mutações frequentes do caminho de emendas de máquinas de emenda em mielodisplasia. Natureza 2011; 478(7367): 64-69.
- Bejar R, Levine R, Ebert BL: Desvendando a patofisiologia molecular das síndromes mielodisplásticas. Journal of clinical oncology: revista oficial da Sociedade Americana de Oncologia Clínica 2011; 29(5): 504-515.
- Bejar R, et al.: Efeito clínico de mutações pontuais em síndromes mielodisplásticas. The New England journal of medicine 2011; 364(26): 2496-2506.
- Abdel-Wahab O, Figueroa ME: Interpretando a nova genética molecular em síndromes mielodisplásticas. Programa de Educação em Hematologia da Sociedade Americana de Hematologia 2012; 2012: 56-64.
- Leeke B, et al.: Cohesin mutations in myeloid malignancies: Underlying mechanisms. Hematologia experimental & oncologia 2014; 3: 13.
- Tothova Z, Steensma DP, Ebert BL: Novas estratégias em síndromes mielodisplásticas: Aplicação de diagnósticos moleculares à prática clínica. Clinical cancer research: um jornal oficial da Associação Americana para a Investigação do Cancro 2013; 19(7): 1637-1643.
- Jan M, Ebert BL, Jaiswal S: Hematopoiese clonal. Seminários em hematologia 2017; 54(1): 43-50.
- Heuser M, Thol F, Ganser A: Hematopoiese Clonal de Potencial Indeterminado. Deutsches Arzteblatt international 2016; 113(18): 317-322.
- Fuster JJ, Walsh K: Mutações Somáticas e Hematopoiese Clonal: Potenciais Novos Condutores Inesperados de Doenças Cardiovasculares Relacionadas com a Idade. Pesquisa de circulação 2018; 122(3): 523-532.
- Valent P, et al.: Citopenia idiopática de significado indeterminado (ICUS) e displasia idiopática de significado incerto (IDUS), e a sua distinção do MDS de baixo risco. Investigação da leucemia 2012; 36(1): 1-5.
- Malcovati L, et al.: Significado clínico da mutação somática em citopenia sanguínea inexplicada. Sangue 2017; 129(25): 3371-3378.
- Valent P, et al: Proposta de critérios mínimos de diagnóstico para síndromes mielodisplásticas (MDS) e potenciais condições pré-MDS. Oncotarget 2017; 8(43): 73483-73500.
- Gañán-Gómez I, et al.: Desregulamentação da sinalização imune e inflamatória inata em síndromes mielodisplásticas. Leucemia 2015; 29(7): 1458-1469.
- Glenthøj A, et al: Mecanismos Imunitários na Síndrome Mielodisplásica. Revista internacional de ciências moleculares 2016; 17(6): 944.
- Chung SS, Park CY: Envelhecimento, hematopoiese, e as síndromes mielodisplásticas. O sangue avança 2017; 1(26): 2572-2578.
- Cooper JN, Young NS: Clonalidade no contexto: Clones hematopoiéticos no seu ambiente medular. Sangue 2017; 130(22): 2363-2372.
- Malcovati L, et al: A mutação SF3B1 identifica um subconjunto distinto de síndrome mielodisplásica com anéis sideroblastos. Sangue 2015; 126(2): 233-241.
- Nordic MDS Study Group: Guidelines to Patient Management of Myelodysplastic Syndromes and Chronic Myelomonocytic Leukemia. 8ª actualização. www.nmds.org/index.php/guidelines (citado 14.03.2018).
- Montalban-Bravo G, Garcia-Manero G: Síndromes mielodisplásticas: 2018 actualização sobre diagnóstico, estratificação de risco e gestão. Am J Hematol 2018 Jan; 93(1): 129-147.
Leitura adicional:
- Lista A, Ebert BL, Fenaux P: Uma década de progresso na síndrome mielodisplásica com eliminação do cromossoma 5q. Leucemia de 2018. DOI: 10.1038/s41375-018-0029-9 [Epub ahead of print].
- Platzbecker U, et al: Luspatercept for the treatment of anemia in patients with lower-risk myelodysplastic syndromes (PACE-MDS): Um estudo multicêntrico, aberto, fase 2 de pesquisa de dose com estudo de extensão a longo prazo. The Lancet Oncology 2017; 18(10): 1338-1347.
InFo ONCOLOGy & HaEMATOLOGy 2018; 6(2): 22-26.