Devido ao crescente envelhecimento da população, bem como à melhoria dos cuidados médicos, o número de pacientes com procedimentos de substituição dos rins aumentou nos últimos anos. No final de 2015, cerca de 4100 pacientes estavam num programa de diálise, 423 pacientes estavam em diálise domiciliária (principalmente diálise peritoneal) [1], os restantes estavam em hemodiálise central. Além disso, há cerca de 5000 pacientes na Suíça com um transplante funcional. Muitas especialidades médicas estão envolvidas no tratamento de doentes com insuficiência renal crónica. Para a fase CKD 1-3, o médico de clínica geral é o prestador de cuidados primários, enquanto que para a fase CKD 4+5 (pacientes de diálise), é mais provável que os cuidados sejam prestados pelo nefrologista (Fig. 1). Se a função renal for <30% (GFR <30 ml/min.), o encaminhamento para um nefrologista deve ser feito de modo a que a preparação cuidadosa do doente para um procedimento de substituição renal possa ter lugar [2].
Como regra, a diálise crónica é iniciada quando a TFG se situa entre 8-12 ml/min., em que a decisão de começar não se baseia apenas nos valores do laboratório [3]. Em doentes assintomáticos, a indicação para iniciar a diálise pode ser feita cautelosamente [4]. Uma indicação absoluta é a hipercalemia que não pode ser controlada com medidas conservadoras, ou a hipervolaemia que não pode ser controlada com diuréticos (especialmente na síndrome cardiorenal). Com uma boa cooperação entre nefrologista, clínico geral e paciente, o quadro clínico de pericardite uraémica ou encefalopatia uraémica não deveria ocorrer; ambas as condições clínicas seriam uma indicação de emergência para o início da diálise.
Diálise peritoneal [5]
- CAPD = diálise peritoneal ambulatorial contínua
- APD = diálise peritoneal automatizada
Sendo um procedimento de diálise aguda em adultos, a diálise peritoneal não tem lugar. Em contraste, o procedimento é estabelecido para a insuficiência renal crónica que requer diálise. Na Suíça, a proporção de doentes em diálise peritoneal aumentou nos últimos anos (10-12%). Não existem ensaios aleatórios prospectivos com comparação directa de mortalidade e morbilidade entre DP e DH, mas pelo menos nos primeiros anos de terapia de substituição renal os procedimentos parecem equivalentes. Em casos de insuficiência cardíaca grave (e instabilidade circulatória durante a DH) e falta de acesso vascular em hemodiálise, a DP é preferível. Uma boa alternativa à hemodiálise central é a DPA nocturna, especialmente para os pacientes mais jovens que trabalham.
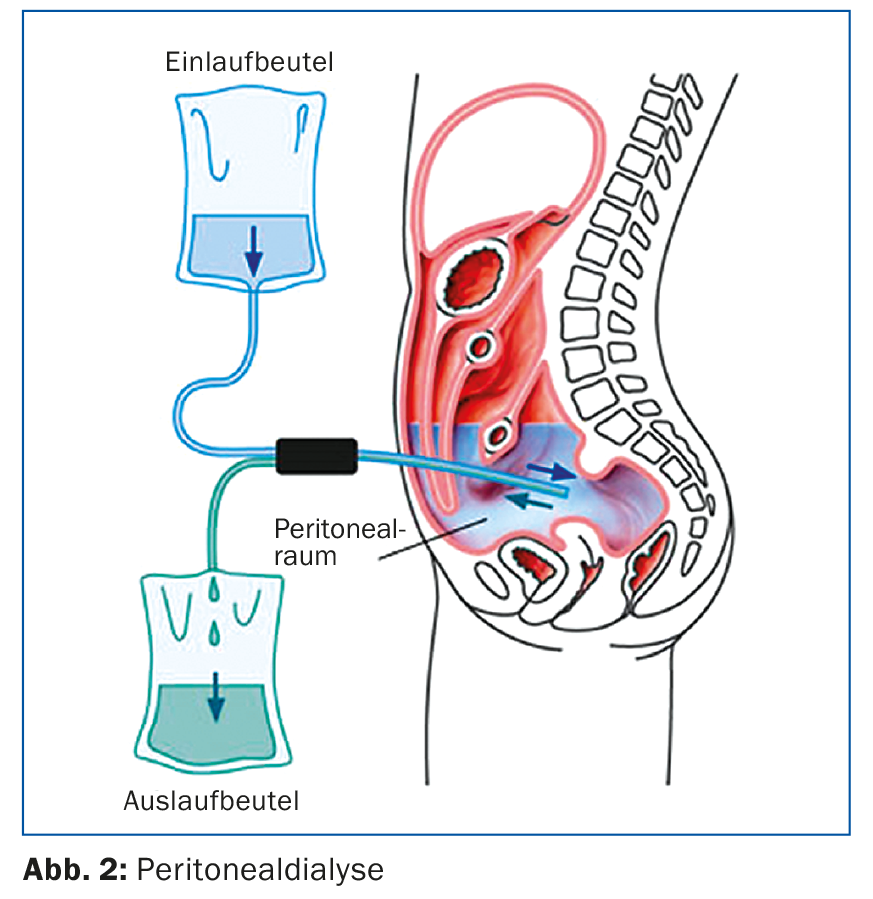
A figura 2 mostra os aspectos técnicos: a DP é realizada através de um cateter de diálise intraperitoneal, geralmente inserido por via laparoscópica. O procedimento utiliza o peritoneu como membrana semipermeável para remover produtos metabólicos por difusão e osmose. Na diálise peritoneal, a adesão do paciente é muito essencial, uma vez que ele próprio efectua a terapia. É formado e monitorizado por pessoal de enfermagem especializado, e se o curso for estável, as verificações e consultas nefrológicas têm lugar a cada 4-6 semanas.
Uma possível vantagem da diálise peritoneal em comparação com a hemodiálise é que a função residual ou o fluxo sanguíneo pode ser reduzido. A diurese residual é preservada por mais tempo. Por esta razão, é importante que sejam efectuados o menor número possível de exames radiológicos com meio de contraste iodado. Os anti-inflamatórios não esteróides também devem ser evitados a fim de preservar a função residual, que é importante para a diálise peritoneal. No caso de complicações de diálise peritoneal, o centro de nefrologia é geralmente responsável, especialmente por problemas de cateteres, tais como deslocamento de cateteres ou fuga de cateteres. Com os actuais sistemas de diálise peritoneal, a peritonite é rara mas ainda perigosa [5]. Se ocorrer dialisado nublado ou dor abdominal, o dialisado deve ser examinado numa emergência e a antibioticoterapia deve ser iniciada (geralmente intraperitoneal, a hospitalização pode muitas vezes ser evitada).
Hemodiálise
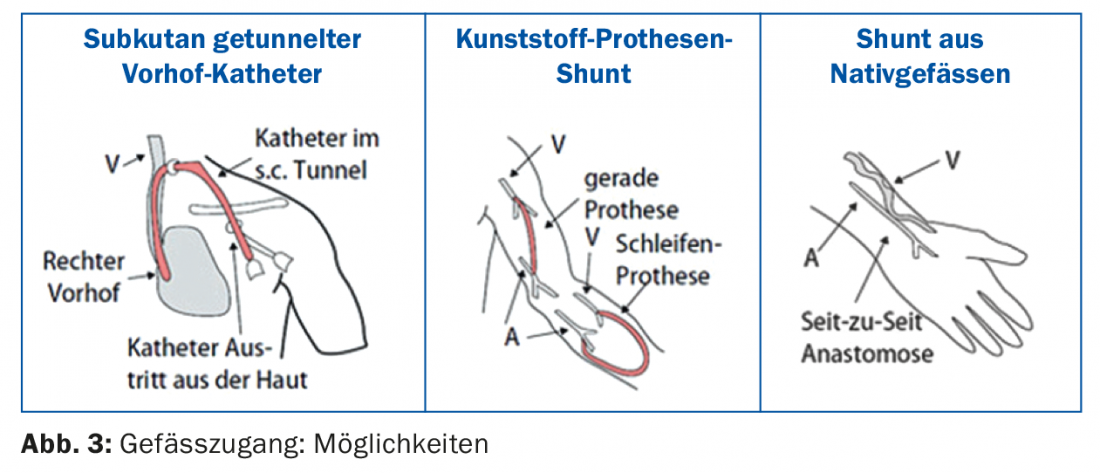
Para a maioria dos doentes, a hemodiálise é realizada no centro de diálise (diálise central), apenas alguns doentes realizam diálise em casa (hemodiálise caseira). Um único tratamento de hemodiálise leva 3,5-4,5 horas, dependendo da função residual e de outros factores individuais. São geralmente realizadas três sessões de hemodiálise por semana. Na maioria dos centros é tecnicamente possível realizar a chamada hemodiafiltração (desintoxicação através de uma combinação de hemodiálise e hemofiltração). Para uma diálise eficiente, é necessário um acesso vascular [6] que forneça fluxo sanguíneo suficiente (>300 ml/min.) é permitido. O acesso vascular ainda é chamado “pé de cavalo de diálise” devido a vários problemas técnicos. As diferentes possibilidades são mostradas na figura 3 : Se não estiver disponível nenhum shunt no início da diálise, o procedimento é realizado através de um cateter atrial subcutaneamente tunelado. A vantagem é que a diálise pode ser iniciada imediatamente. Um cateter atrial também pode ser a principal escolha de acesso vascular, particularmente em doentes idosos e doentes com condições vasculares periféricas muito pobres e insuficiência cardíaca grave. Após cada diálise, os volumes dos cateteres são bloqueados com uma solução especial (por exemplo, solução liqueminina ou citrato). A manipulação de cateteres de diálise de longa duração só deve ser efectuada por pessoal de diálise formado, caso contrário complicações como disfunção do cateter ou infecções do cateter são pré-programadas [7].
O melhor acesso vascular ainda é uma fístula arterio-venosa (AV) nativa. Preferencialmente, a fístula é criada no antebraço não dominante (Fig. 4) . Uma alternativa é utilizar a veia cefálica do antebraço, mas com um grande diâmetro de vaso há o risco de um shunt hiperdinâmico com o perigo de stress cardíaco.
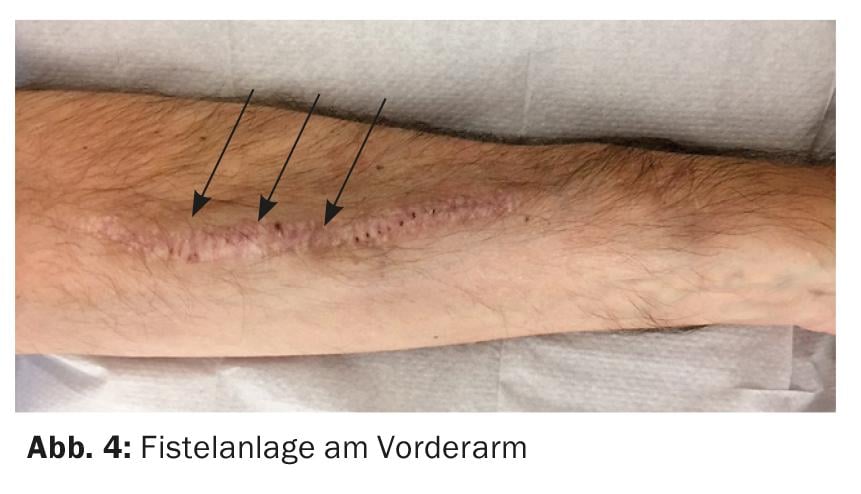
A alternativa a uma fístula nativa é um shunt protético de plástico, por exemplo, sob a forma de uma prótese de laço no antebraço. É importante que o braço com um shunt de diálise funcional seja utilizado apenas como acesso vascular para diálise, amostragem de sangue ou cânulas residentes.
Aspectos dietéticos
Os aspectos dietéticos têm de ser considerados tanto na DP como na HD. No decurso do tratamento de diálise, é de esperar uma diminuição da função residual, e em paralelo, a restrição de potássio, fosfato, sal e fluidos torna-se mais importante. Para ambos os procedimentos, aplica-se o princípio relativo à ingestão de líquidos: diurese residual + 800 ml por dia, ingestão de soro fisiológico 4-6 g por dia. Especialmente em doentes de hemodiálise, é necessária a restrição nutritiva do potássio (Tab. 1) , bem como a utilização de permutadores de iões de gato (por exemplo, poliesterol sulfonato, Ressónio A). As drogas que aumentam o soro de potássio (inibidores da ECA, bloqueadores da angiotensina II) devem ser usadas com cautela; a espirolonactona e a dose elevada de Bactrim não devem ser usadas.

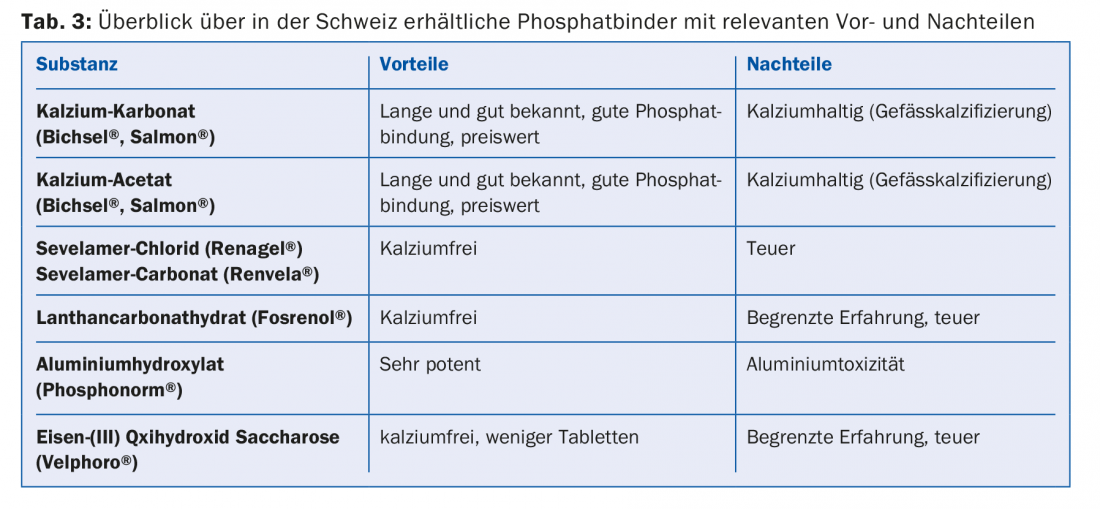
Outro problema é a hiperfosfatemia, pois a diálise só pode eliminar parte do fosfato reabsorvido. A hiperfosfatemia persistente é acompanhada por uma calcificação crescente dos vasos [9], de modo que os pacientes de diálise a longo prazo sofrem frequentemente de arteriosclerose grave generalizada. Ao mesmo tempo, a hiperfosfatemia promove o hiperparatiroidismo secundário renal [8]. Por estas razões, por um lado, é necessária uma dieta pobre em fosfatos (alimentos contendo fosfatos, tab. 2) com ingestão simultânea de aglutinantes fosfatados. Distinguimos entre os ligantes de fosfato contendo cálcio e os que não contêm cálcio, que diferem em potência, perfil de efeitos secundários e interacções (Tab. 3).

Aspectos farmacológicos
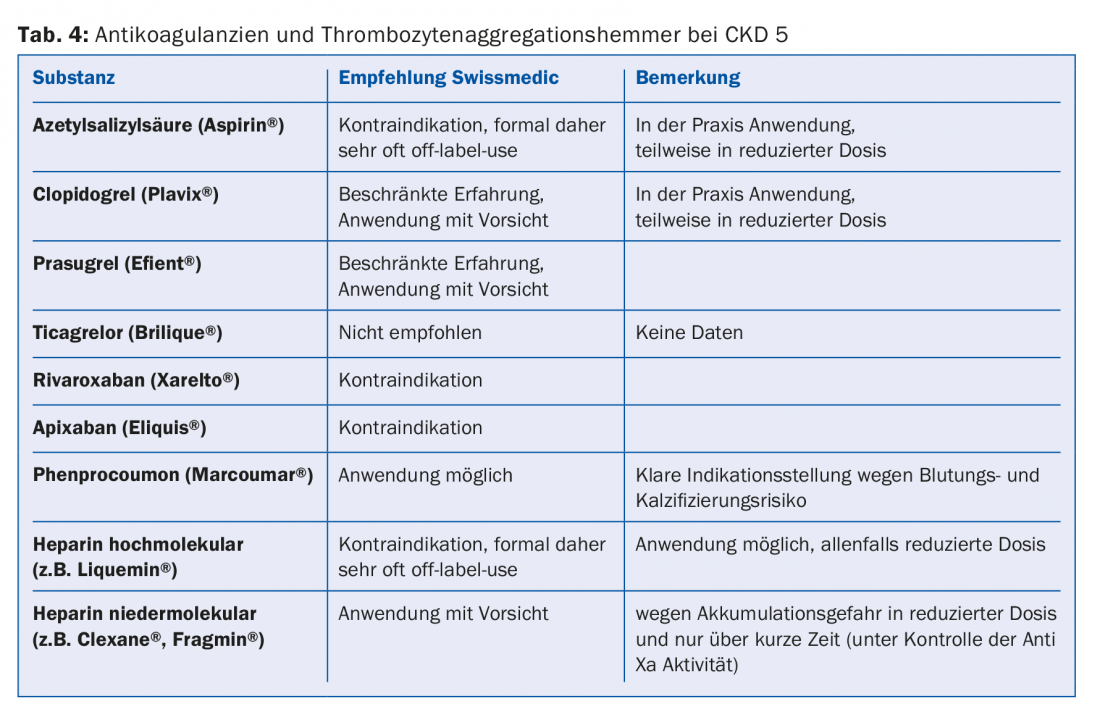
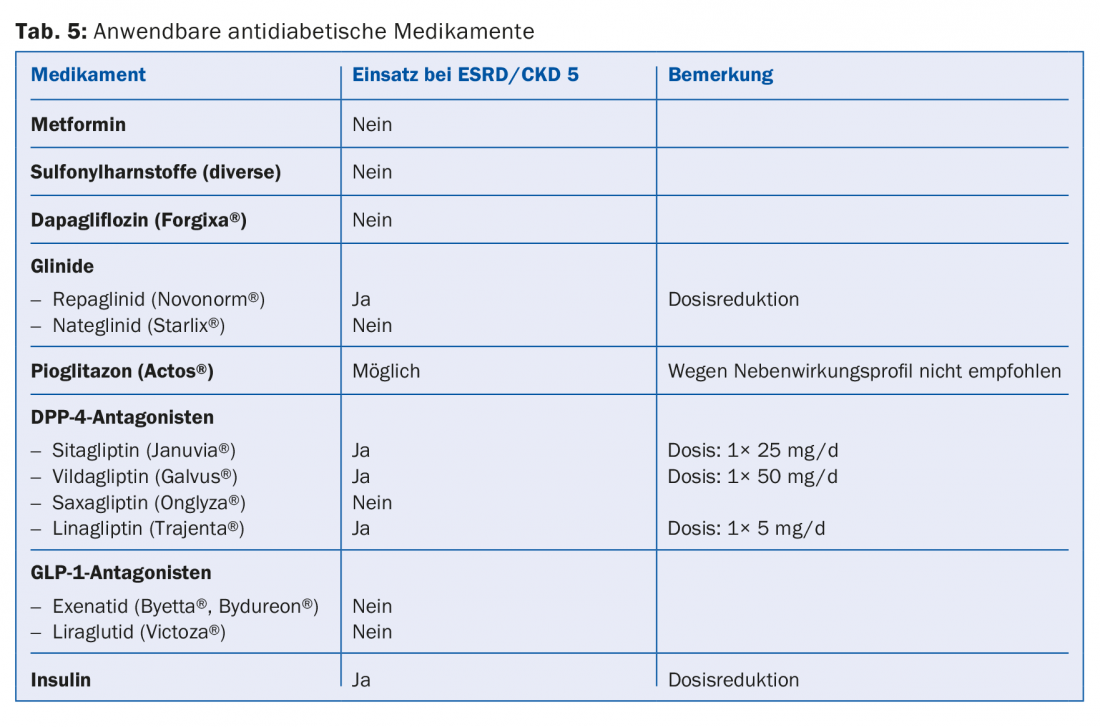
Uma grande proporção dos medicamentos ou os seus metabólitos são renalmente eliminados. Portanto, as contra-indicações absolutas e relativas devem ser ajustadas de acordo com as directrizes (por exemplo, Compêndio). Isto é especialmente verdade para a maioria dos antibióticos, anticoagulantes e agentes antiplaquetários (tab. 4). Uma vez que 30-40% dos doentes em diálise têm diabetes, é importante evitar completamente certos medicamentos antidiabéticos (por exemplo, metformina, sulfonilureias) ou reduzir a dose (por exemplo, sitagliptin, vildagliptin, etc.) (separador. 5) [10]. No que diz respeito aos medicamentos contra a dor, os anti-inflamatórios não esteróides só devem ser administrados por um curto período de tempo, se for o caso (risco de hipercalemia, redução de diurese residual, distúrbio adicional de agregação plaquetária). As preparações de paracetamol (até 3 g/dia) e metamizol são consideradas relativamente seguras. Os opiáceos devem ser tomados em doses baixas; também aqui a acumulação de metabolitos deve ser tida em conta. As preparações de buprenorfina ou fentanil são bem adequadas para este fim (geralmente num GFR <15 ml/min). Dose a reduzir para metade [11]. As preparações de codeína são menos adequadas (risco de acumulação e potencial de interacção). Do mesmo modo, o tramadol só deve ser doseado baixo. Contra-indicada é a petidina (risco de convulsões).
Importância dos cuidados de GP
Em pacientes de hemodiálise que são visitados três vezes por semana, o nefrologista é frequentemente também o médico de clínica geral. Para os pacientes que estão mais longe do centro de diálise ou que vivem numa instituição de cuidados, o médico de família ainda tem uma alta prioridade. Isto também é verdade para pacientes com CAPD que só são atendidos no centro de diálise de 1 a 2 meses.
O médico de família também é importante como confidente quando um paciente idoso com uma qualidade de vida em declínio decide interromper o tratamento de diálise. A interrupção da diálise activa é responsável por quase 20% das mortes anuais em doentes de substituição renal. O médico de família, que conhece o doente há anos, está em posição de julgar se se trata de um equilíbrio de vida ou, na melhor das hipóteses, de uma depressão (tratável). Isto deve ser abordado com medicação antes de ser tomada a importante decisão de interromper o tratamento de diálise.
Literatura:
- Associação Suíça para as Tarefas Comuns de Seguros de Saúde (SVK): www.svk.org/assets/uploads.
- Elsässer H, et al: Planear um procedimento de substituição renal: O que precisa de saber? Schweiz Med Forum 2008; 8: 70-74.
- Kleophas W: Quando é o momento certo para iniciar a terapia de substituição renal? Nefrologista 2012; 7: 96-103.
- Cooper BA, et al: Uma pista aleatória e controlada de início precoce versus tardio de diálise. N Engl J Med 2010; 363: 609-619.
- Kribben A, et al: Estado, indicações e limitações da diálise peritoneal. Nefrologista 2007; 2: 74-81.
- KDOQI. Directrizes de prática clínica para o acesso vascular. Am J Kidney Dis 2006; 48: 176-247.
- Quick-Alert: “Uso indevido de cateteres de diálise”; em curso (Segurança dos Pacientes Suíça).
- CKD-MBD Grupo de Trabalho sobre a doença renal: melhorar os resultados globais (KDIGO). KDIGO clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of chronic kidney disease-mineral and bone disorder (CKD-MBD), Kidney Int 2009; 76(Suppl): 1-130.
- Herzog CA, et al: Doenças cardiovasculares em doenças renais crónicas. Uma actualização clínica de Kidney Disease; Improving Global Outcomes (KDIGO. Kidney Int 2011; 80: 572-586.
- Zanchi A, et al: Insuficiência renal e diabetes, agindo com previdência. Schweiz Med Forum 2014; 14(6): 100-104.
- Liechti ME: Farmacologia de analgésicos para a prática, parte 2: Opiáceos. Swiss Med Forum 2014; 14: 460-464.
PRÁTICA DO GP 2016; 11(10): 32-38