A doença arterial periférica, como uma das causas mais comuns de morbidade e mortalidade, tem agora um carácter pandémico. Este desenvolvimento promove o progresso técnico e estimula a investigação farmacêutica. Infelizmente, pouco mudou nos últimos anos no que diz respeito à frequência das amputações em diabéticos. No entanto, 85% das amputações poderiam ser evitadas. É importante pensar cedo na síndrome do pé diabético, restaurar a perfusão e acompanhar de perto o paciente para detectar a sua recorrência no tempo. Os DOAK tornaram a terapia farmacológica e a profilaxia do tromboembolismo venoso mais simples e segura, mas também mais dispendiosa. Há também a abordagem de cateterização do tromboembolismo venoso agudo.
A angiologia é um assunto muito dinâmico que tem evoluído muito nos últimos anos – felizmente, uma vez que 202 milhões de pessoas em todo o mundo são afectadas pela doença arterial periférica (PAOD) [1]. Isto é quase cinco vezes mais do que há doentes seropositivos em todo o mundo. O que também é novo neste desenvolvimento é que já não existe uma diferença na prevalência da doença arterial periférica em todo o mundo. As fronteiras nacionais, o rendimento e o nível de vida já não desempenham um papel em termos de morbidez.
Anamnese, medição ABI e oscilograma são os dados básicos mínimos necessários para o diagnóstico da doença oclusiva arterial periférica. Contudo, é importante lembrar que dois terços dos pacientes com PAOD manifesto não têm sintomas. A medição de rotina ABI na prática do GP, tal como um ECG, é algo que temos vindo a exigir há anos. O objectivo não é recrutar o maior número possível de pacientes para uma terapia. As pessoas que estão livres de sintomas normalmente não necessitam de terapia vascular específica. Um pAVK é uma indicação clara de aterosclerose manifesta e tem um significado semelhante às perturbações de repolarização no ECG, que indicam isquemia miocárdica silenciosa. 50% dos pacientes com PAOD têm um envolvimento coronário significativo e 43% têm um envolvimento cerebral significativo [2]. Não diagnosticar PAOD significa perder uma abordagem preventiva nestes pacientes.
Disfunção eréctil: Gostaria também de salientar um importante factor de risco que muitas vezes não é detectado. A disfunção eréctil afecta até 50% dos homens, dependendo da sua idade. Uma associação significativa entre diabetes, hipertensão, tabagismo, obesidade e dislipidemia, ou seja, precisamente os clássicos factores de risco para a aterosclerose, é impressionante. 50% dos homens com síndrome coronária aguda têm disfunção eréctil, e em 70% a disfunção eréctil é um precursor da síndrome coronária aguda e precede o evento coronário em média de três anos [3]. A disfunção eréctil é portanto um importante biomarcador para a aterosclerose a que se deve prestar maior atenção. Mas honestamente, quem pergunta sobre isto na prática durante uma consulta?
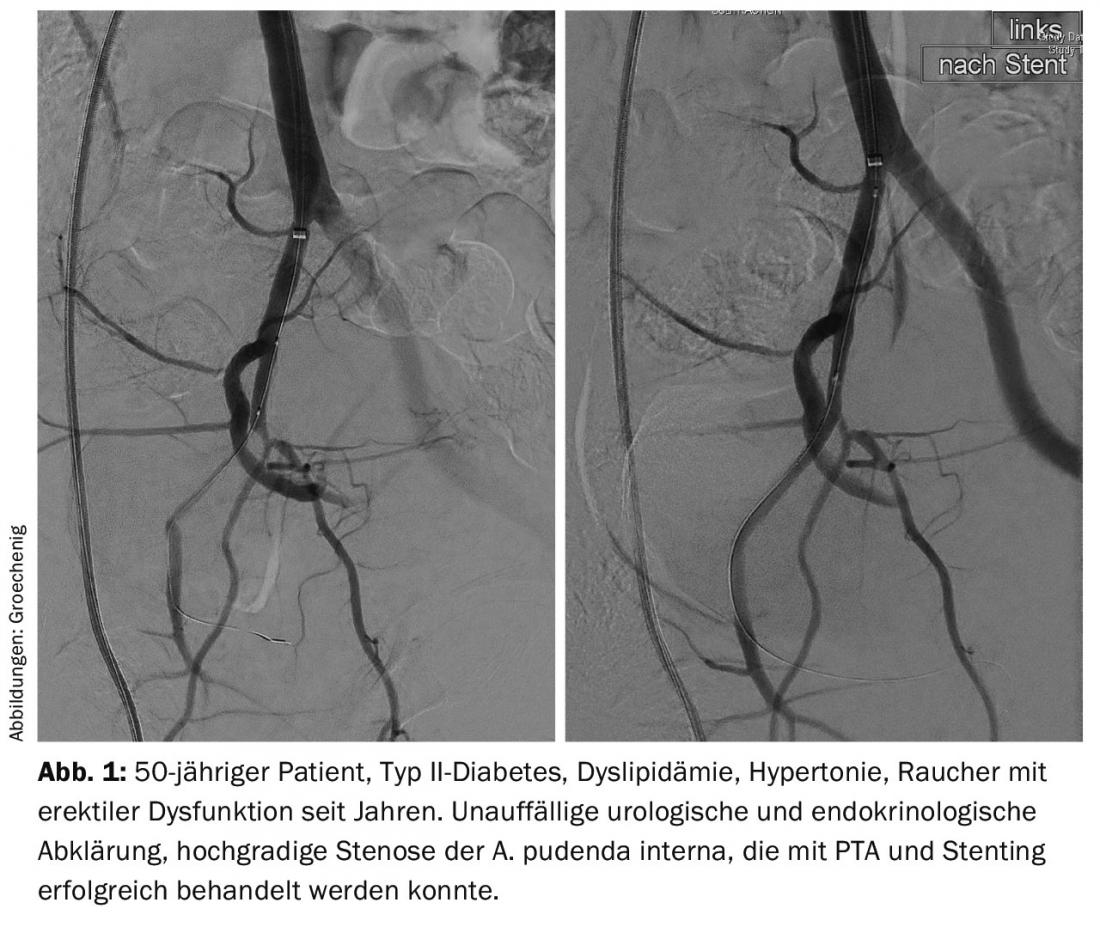
Para além da abordagem preventiva para prevenir um evento cardiovascular, existem também opções terapêuticas reais. Em Aarau, estabelecemos uma hora de consulta para a disfunção eréctil juntamente com o departamento de urologia e endocrinologia desde Janeiro de 2015. Se tiverem sido descartadas perturbações urológicas, hormonais ou outras, não é raro encontrar um fornecimento de sangue perturbado, que pode agora ser tratado por cateterização (Fig. 1).
Detecção precoce, profilaxia e diagnóstico
Evidentemente, a solução ideal seriam programas de detecção precoce que permitissem a identificação de pessoas com danos vasculares precoces e ainda reversíveis e criassem aqui uma abordagem preventiva principalmente através de mudanças no estilo de vida. Infelizmente, os estudos sobre medição da espessura intima-média, “rigidez arterial”, velocidade de onda de pulso ou febre aftosa da artéria braquial, que foram tão elogiados há alguns anos atrás, já não são vistos como euforicamente hoje em dia como o eram na altura da publicação.
É importante estar ciente de que a maioria dos pacientes com PAOD morrem de outras manifestações de aterosclerose, especialmente ataques cardíacos e acidentes vasculares cerebrais. E isto poderia ser evitado hoje em dia através da moderna terapia medicamentosa. A eficácia da profilaxia secundária intensificada, por exemplo, é demonstrada em estudos sobre a terapia da estenose carotídea assintomática, onde a taxa de AVC poderia ser reduzida em 1% com medicamentos antiplaquetários, inibidores da ECA e estatinas <e é assim consideravelmente inferior à das intervenções terapêuticas, independentemente de se proceder a cateteres – técnica ou cirúrgica [4].
Os médicos de clínica geral têm um papel crucial a desempenhar na detecção do que é frequentemente uma doença assintomática, na educação do paciente, na promoção da mudança de estilo de vida e da adesão, e mais importante ainda, na avaliação do momento certo para confiar o paciente a um especialista.
A sonografia duplex desenvolveu-se tanto nos últimos anos com equipamento muito mais potente, novas sondas e sonografia contrastada que a angiografia praticamente já não é realizada para o diagnóstico de PAOD. Na grande maioria dos casos, o planeamento do tratamento é possível com a ajuda de sonografia duplex, e a angiografia intra-arterial como diagnóstico de base é então realizada como parte de um procedimento de intervenção, o que poupa tempo, custos e recursos consideráveis.
Terapia: Perguntas abertas e novos desenvolvimentos
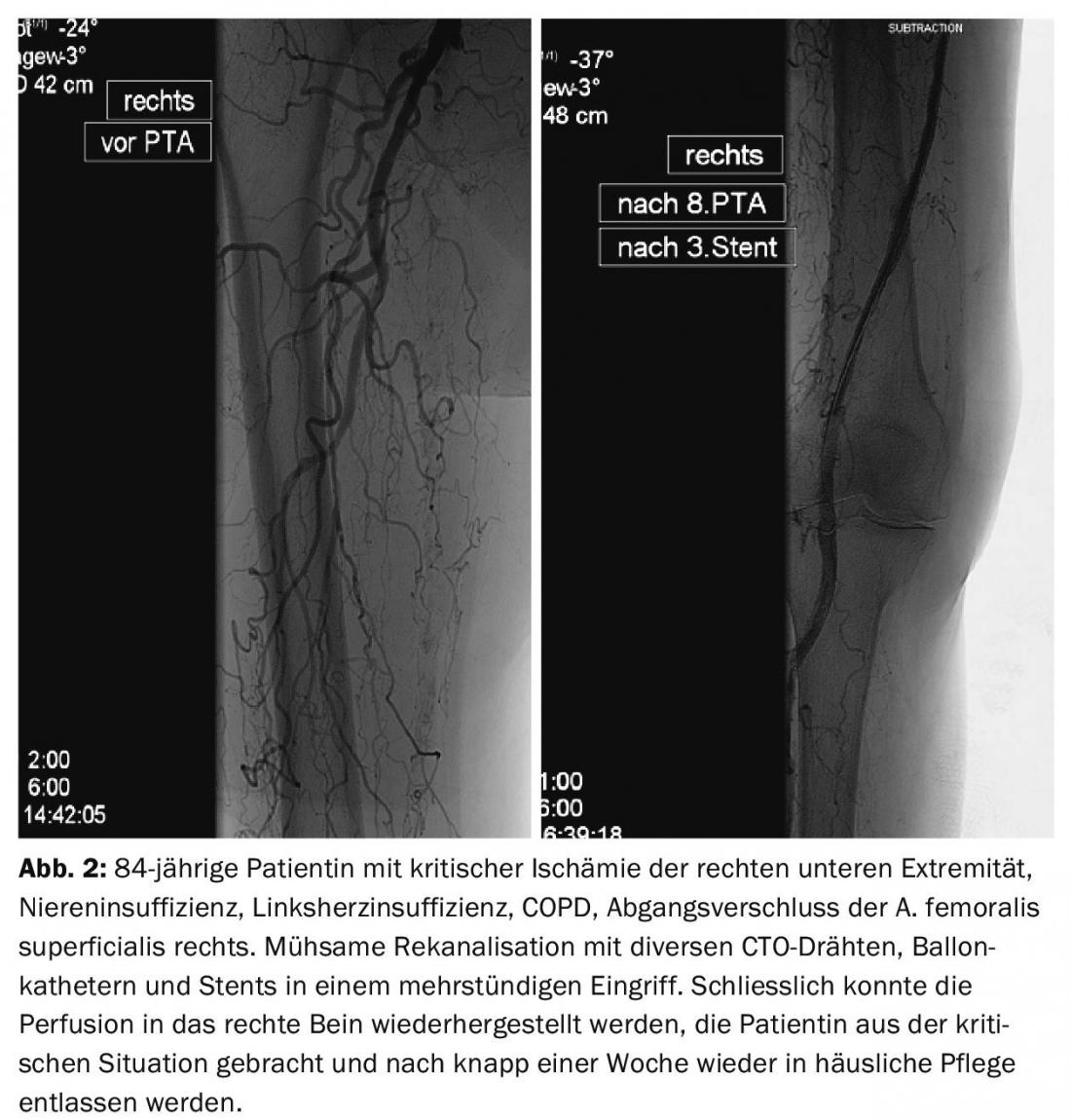
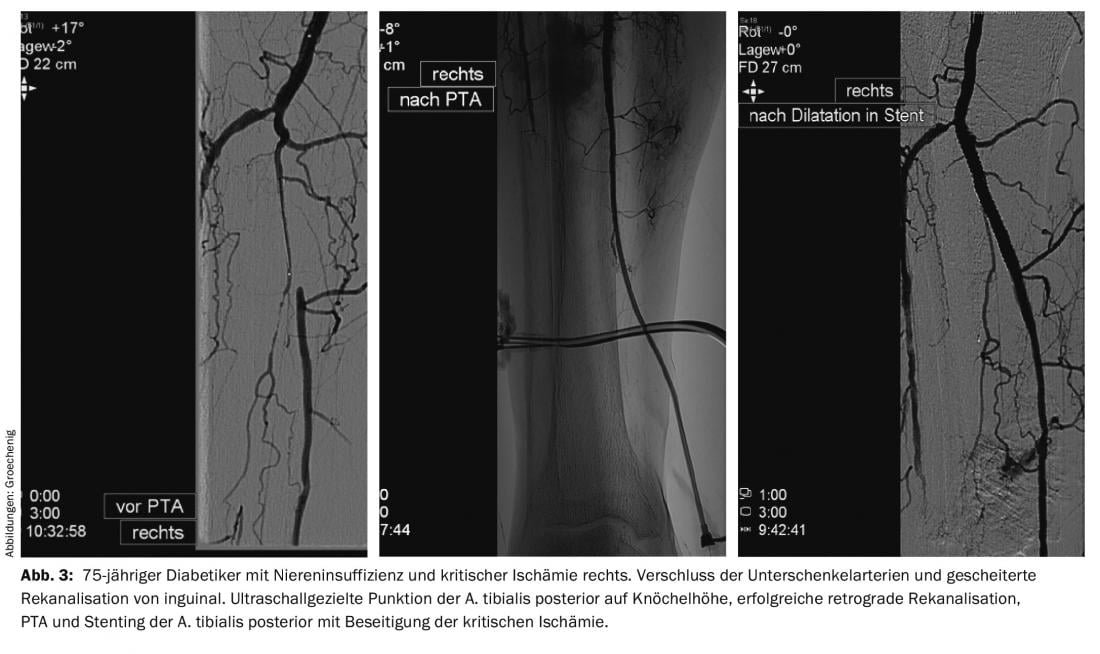
Em termos de terapia, os procedimentos baseados em cateteres são actualmente o tratamento mais importante para o PAOD. O desenvolvimento de fios refinados, dispositivos de reentrada [5], cateteres balões ultrafinos e escorregadios, dispositivos de aterectomia, lise e cateteres de aspiração permitem procedimentos considerados impossíveis há alguns anos atrás (Figs. 2 e 3).
Como resultado, os procedimentos de intervenção tornaram-se também muito mais exigentes e requerem consideravelmente mais tempo e recursos, que não se reflectem, ou apenas de forma inadequada, na actual estrutura de remuneração. Isto leva a uma considerável pressão de custos nos hospitais com uma função central.
O problema hoje em dia não é tanto a recanalização das oclusões de longa data, mas sim mantê-las abertas durante um período de tempo mais longo. Muitas perguntas permanecem sem resposta: “Inibição de plaquetas com monoterapia ou dupla?”, “Anticoagulação?”, “Se sim, com o quê?” etc. Grandes estudos randomizados semelhantes aos da cardiologia praticamente não existem, pelo que temos de nos cingir ao modelo de cardiologia infelizmente não completamente transferível. Afinal, há alguns anos, foi publicada uma opinião de peritos [6] que pode ser utilizada como guia. A profilaxia de recaída bem sucedida compra sempre uma tendência crescente para a hemorragia, mas felizmente algo também está a acontecer aqui: o desenvolvimento de novos inibidores de plaquetas está a caminho. O primeiro ingrediente activo aprovado pela FDA é vorapaxar. Estas substâncias actuam especificamente nos locais onde o seu efeito é necessário [7] – ou seja, onde as plaquetas são activadas devido a uma lesão intimal, estas são bloqueadas selectivamente. A fibrina, que é importante na hemostasia, não é afectada. Isto dá uma melhor eficácia adicional com maior segurança terapêutica.
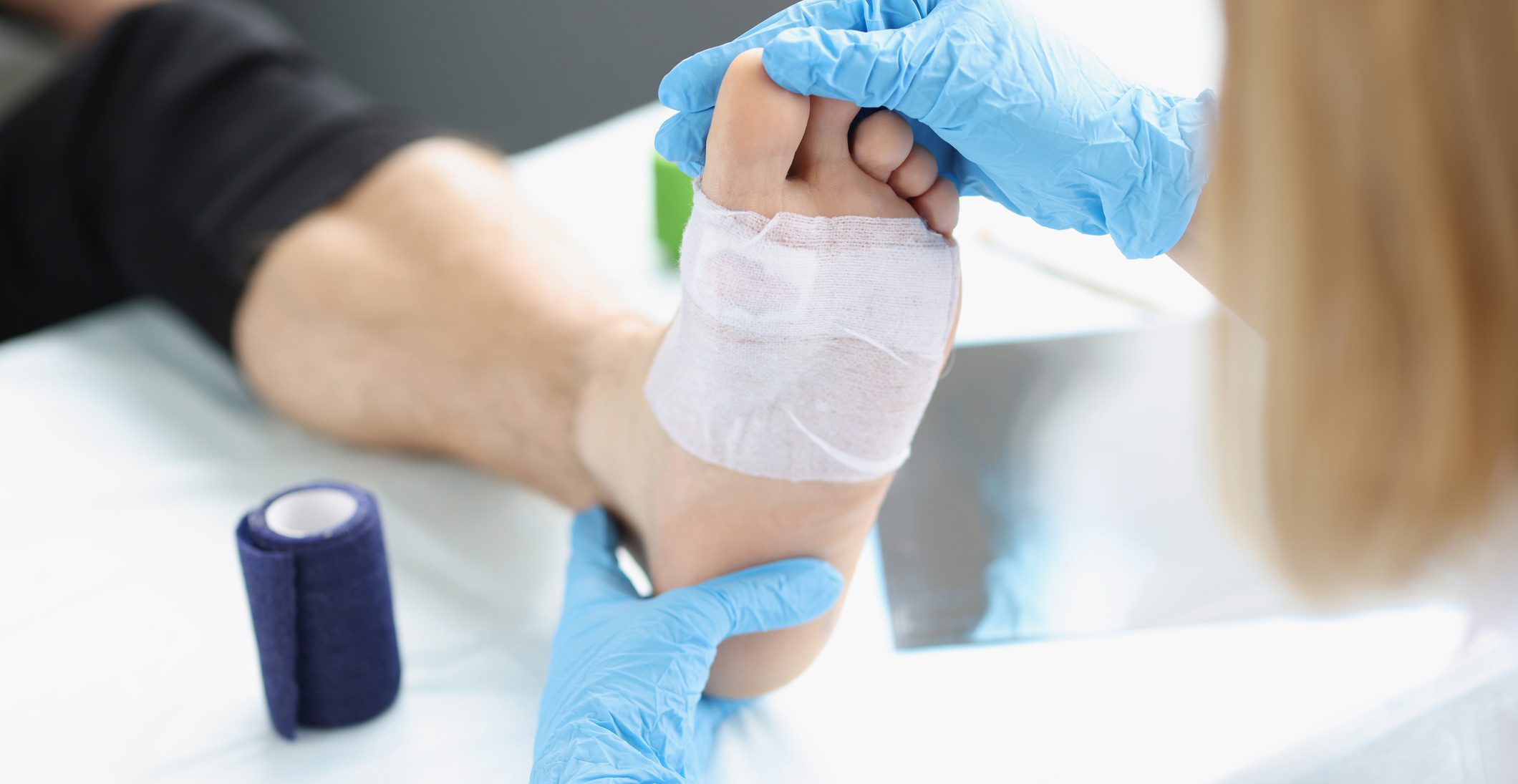
Síndrome do pé diabético
Gostaria de vos dizer algo novo, especialmente desde que a OMS lançou um programa há dez anos com o objectivo de reduzir a frequência das amputações em diabéticos em 50% [8]. Em todo o mundo, é efectuada uma amputação diabética de 30 em 30 segundos. 12-25% dos diabéticos desenvolvem a síndrome do pé diabético. Uma úlcera no pé num diabético significa um risco 24 vezes maior de amputação. Quando a OMS efectuou uma revisão do objectivo dez anos após o início do programa acima mencionado, teve de concluir que nada tinha mudado. E isso é triste como tudo, porque 85% das amputações poderiam ser evitadas!
Nos diabéticos, existe uma situação específica resultante da interacção de muitos factores que são potenciados e muitas vezes subestimados. Os indivíduos afectados mostram frequentemente não só isquemia crítica isolada mas também neuropatia, lesão por pressão e infecção. Além disso, o diagnóstico é mais difícil: por um lado, os valores ABI são falsamente elevados devido à mediasclerose. Em segundo lugar, o pulso pode parecer palpável, mas na realidade é apenas um pulso de paragem com a artéria ocluída proximalmente, ou o paciente não apresenta sintomas.
Os pacientes com síndrome do pé diabético pertencem imediatamente a um centro que tem todos os departamentos especializados disponíveis 24 horas por dia. Verifica-se que mais de 50% dos doentes afectados têm uma doença vascular arterial. O objectivo mínimo é abrir pelo menos um recipiente – se for possível abrir vários recipientes, tanto melhor. Contudo, o número de artérias reabertas não tem qualquer influência na taxa de preservação das pernas [9]. A taxa de abertura ao longo de 36 meses também não tem influência; as segundas intervenções são frequentemente necessárias para melhorar a taxa de patência. [10]. É importante pensar nisso cedo, restaurar agressivamente a perfusão por todos os meios, e depois monitorizar de perto o paciente para detectar a recorrência no tempo e melhorar a taxa de abertura com uma nova cirurgia, se necessário.
Tromboembolismo venoso
Em termos de terapia farmacológica, os novos anticoagulantes directos (DOAKs) tornaram a terapia mais simples e segura, mas também mais cara. Os quatro DOAcs aprovados na Suíça (Tab. 1) diferem nas suas indicações, dosagens e restrições de utilização. O que todos eles têm em comum é que falta (ainda) um antídoto e que não são aprovados nos casos de deficiência da função renal. Este último apenas porque não foi investigado. Os pacientes com função renal prejudicada simplesmente não foram incluídos nos estudos.

Não inteiramente nova, mas cada vez mais em ascensão, é a abordagem de cateterização do tromboembolismo venoso agudo. As lises locais devem reduzir a carga de trombos e o risco de embolia pulmonar, desmascarar quaisquer obstruções anatómicas como a síndrome de May-Turner e, mais importante ainda, reduzir a incidência de síndrome pós-trombótica. No entanto, estão ainda em curso grandes estudos multicêntricos, de modo que nenhuma recomendação definitiva pode ser feita no momento actual.
Espero que com esta pequena visão geral tenha sido capaz de vos dar uma visão dos desenvolvimentos actuais num assunto altamente interessante e muito dinâmico. Terei todo o prazer em responder pessoalmente a quaisquer perguntas, sugestões ou críticas que possam ter.
Literatura:
- Fowkes GR, et al: Comparação das estimativas globais de prevalência e factores de risco de doenças das artérias periféricas em 2000 e 2010: uma revisão e análise sistemática. A Lanceta 2013; 382: 1329-1340.
- Marsico F, et al: Prevalência e gravidade da doença coronária e arterial carotídea assintomática em doentes com doença arterial dos membros inferiores. Aterosclerose 2013; 228: 386-389.
- Montorsi F, et al: Disfunção eréctil, prevalência, tempo de início e associação com factores de risco em 300 doentes consecutivos com dor torácica aguda e doença coronária angiograficamente documentada. Eur Urol 2003, 44; 360-365.
- Spence JD, DG Hackam: Tratar artérias em vez de factores de risco. Uma mudança de paradigma na gestão da aterosclerose. Stroke 2010; 41: 1193-1199.
- Langhoff R, et al: Revascularização bem sucedida da oclusão total crónica das artérias das extremidades inferiores: apenas um fio e a abordagem do dispositivo de reentrada. J Cardiovasc Surg (Torino) 2013 Out; 54(5): 553-559.
- Jäger KA, et al.: Consenso suíço sobre terapia com inibidores de função plaquetária em angiologia. Schweiz Med Forum 2009; 9(39): 690-693.
- Morrow DA, et al: Vorapaxar na prevenção secundária de eventos aterotrombóticos. N Engl J Med 2012; 366: 1404-1413.
- Boulton AJ, et al: A carga global da doença do pé diabético. Lancet 2005; 366: 1719- 1724.
- Iida O, et al: Importância do conceito de angiossoma para a terapia endovascular em pacientes com isquemia de membros críticos. Cateter Cardiovasc Interv 2010; 75(6): 830-836.
- Romiti M, et al: Meta-análise de angioplastia infrapoplítica para isquemia crónica de membros críticos. J Vasc Surg 2008 Maio; 47(5): 975-981.
PRÁTICA DO GP 2015; 10(11): 8-12