O enfarte peri-operatório do miocárdio/lesão (IMC) após cirurgia não-cardíaca é uma complicação cardíaca comum. Uma melhor compreensão da etiologia e das consequências subjacentes é urgentemente necessária.
O enfarte ou lesão miocárdica perioperatória (IMC) é cada vez mais reconhecido como uma complicação cardíaca perioperatória comum após uma grande cirurgia não-cardíaca e é um grande contribuinte para a mortalidade pós-operatória [2–6]. Devido à forte analgesia administrada no período perioperatório, a maior parte do PMI ocorre sem sintomas típicos de isquemia e, portanto, são negligenciados na prática clínica de rotina sem monitorização activa [2–4,7,8]. Como a mortalidade associada ao IMC assintomático é comparável à associada ao IMC sintomático, a vigilância activa do IMC com medidas pré e pós-operatórias de troponina cardíaca (cTn) é cada vez mais defendida como parte dos cuidados clínicos de rotina para permitir a detecção e tratamento precoces [9–12]. Recentemente, a Sociedade Europeia de Cardiologia emitiu uma recomendação de classe IB para esse controlo activo do PMI [12].
Estudos anteriores em que foi realizada uma vigilância activa do IMC mostraram que o IMC não é uma doença homogénea, mas uma síndrome heterogénea com várias etiologias subjacentes diferentes, incluindo o enfarte do miocárdio tipo 1 (T1MI), causado por ruptura da placa, enfarte do miocárdio tipo 2 (IAMT) causado por um desajuste entre a oferta e a procura, taquiarritmia, insuficiência cardíaca aguda e IAM extracardíaco primário, que pode ser devido, por exemplo, a uma septicemia grave. por exemplo, devido a sepsis grave ou embolia pulmonar (EP) [2–4,13–16]. Uma melhor compreensão da etiologia subjacente é um pré-requisito para intervenções preventivas e/ou terapêuticas específicas para o IMC em pacientes individuais [9,17,18]. Ao determinar centralmente a etiologia do IMC, foram recentemente observadas, num estudo-piloto, diferenças inesperadas na incidência e mortalidade a curto prazo aos 30 dias, sublinhando ainda mais a importância clínica da fenotipagem detalhada [16]. No entanto, pouco se sabe sobre as consequências a longo prazo das várias etiologias do PMI [3]. Um estudo multicêntrico prospectivo recente investigou, portanto, os eventos cardíacos adversos graves (MACE) e a mortalidade por todas as causas associadas às diferentes etiologias do PMI avaliadas centralmente no prazo de um ano [1].
População
Entre Maio de 2014 e Junho de 2018, um total de 10 772 pacientes foram inscritos, dos quais 7754 eram elegíveis para esta análise. Pacientes consecutivos submetidos a grandes cirurgias não cardíacas internados em três hospitais (Hospital Universitário da Basileia, Kantonsspital Aarau, ambos na Suíça, e Instituto do Coração, InCor, Universidade de São Paulo, Brasil) elegíveis para o programa institucional de vigilância e resposta activa do IMC para pacientes de alto risco submetidos a grandes cirurgias não cardíacas internados foram matriculados prospectivamente [2].
Os pacientes foram examinados se estavam em maior risco de mortalidade, tinham ≥65 anos de idade ou ≥45 anos de idade e tinham doença arterial coronária, doença arterial periférica ou acidente vascular cerebral e foram submetidos a cirurgia não-cardíaca em regime de internamento com uma estadia pós-operatória planeada de ≥24 horas. As concentrações plasmáticas de cTn foram medidas nos 30 dias anteriores à cirurgia e nos dias de pós-operatório um e dois como parte da vigilância activa e quando clinicamente indicadas após a cirurgia. Um electrocardiograma de doze derivações (ECG) foi realizado no dia em que um PMI foi detectado e quando clinicamente indicado.
Avaliação da etiologia do PMI
A etiologia do IMP identificado num programa de vigilância e resposta activa foi avaliada centralmente por dois médicos independentes com base em todas as informações obtidas durante a investigação do IMP clinicamente indicado, incluindo imagens cardíacas em pacientes consecutivos de alto risco submetidos a grandes cirurgias não cardíacas, num estudo multicêntrico prospectivo. A etiologia do IMC foi hierarquicamente dividida em “extracardíaco” quando causado por uma condição principalmente extracardíaca, como sepse grave ou embolia pulmonar, e “cardíaco”, subdividido ainda em enfarte do miocárdio tipo 1 (T1MI), taquiarritmia, insuficiência cardíaca aguda (FAA) ou provável enfarte do miocárdio tipo 2 (IT2MI).
Pontos finais
Os principais pontos finais foram a ocorrência de MACE e mortes de todos os tipos de acordo com diferentes etiologias do PMI no prazo de um ano. Os óbitos foram classificados como cardiovasculares ou não cardiovasculares de acordo com as mais recentes directrizes [19]. MACE foi definido como um ponto final composto de enfarte agudo do miocárdio, AHF, arritmias que ameaçam a vida e morte cardiovascular. O acompanhamento começou após a cirurgia, no dia do procedimento. Para evitar o viés de definição, o índice de IMC não foi contado como um evento terminal em doentes com IMC classificados como T1MI ou FHA; em vez disso, o seguimento do enfarte agudo do miocárdio ou FHA começou após o 3º dia pós-operatório. Um composto de MACE e morte por todas as causas foi um desfecho secundário.
Para optimizar a relação evento/ruído para as análises de tempo/evento e prognóstico, a ocorrência de MACE e morte por todas as causas aos 120 dias foi escolhida como o parâmetro secundário e utilizada para as análises de prognóstico e tempo/evento porque um estudo anterior sugeria um período vulnerável de 120 dias após intervenções não cardíacas [20].
Características das aetiologias do PMI
PMI ocorreu em 1016/7754 pacientes (13,1%), dos quais 109/1016 (10,7%) foram classificados centralmente como extracardíacos primários. O PMI foi classificado como T1MI em 71/1016 pacientes (7,0%), taquiarritmia em 47/1016 pacientes (4,6%) e AHF em 39/1016 (3,8%). Dos pacientes diagnosticados com T1MI, a angiografia coronária foi realizada em sete dias em 42/71 pacientes, em 30 dias em 47/71 pacientes, e foi tomada uma decisão sem angiografia coronária em 24 pacientes. Os restantes 750/1016 (73,8%) foram classificados como lT2MI.
As características de base diferem entre as etiologias pré-especificadas do PMI, sendo, por exemplo, as CHD conhecidas mais comuns em T1MI e AHF do que em todas as outras etiologias do PMI. Critérios adicionais para o diagnóstico de IAM espontâneo estavam presentes em 260/1016 (25%) dos doentes com IMC, por exemplo, sintomas isquémicos ou dispneia em 143/1016 (14%), mais uma vez com grandes diferenças entre as etiologias do IAM. Em 34/1016 pacientes (3%), o PMI foi avaliado sem um valor cTn pré-operatório com base na mudança entre os valores pós-operatórios.
Seguimento
O acompanhamento foi completado em 7754/7833 pacientes (99%) com uma duração média de 388 dias. Pelo menos um MACE ocorreu em 684/7754 pacientes após um ano (8,8%). Um total de 818/7754 pacientes morreu no prazo de um ano (10,5%), tendo a morte ocorrido em 154/817 pacientes durante a estadia hospitalar indexada. 1160/7754 pacientes (15,0%) sofreram MACE ou morte como causa geral.
MACE de acordo com o PMI, dependendo da etiologia
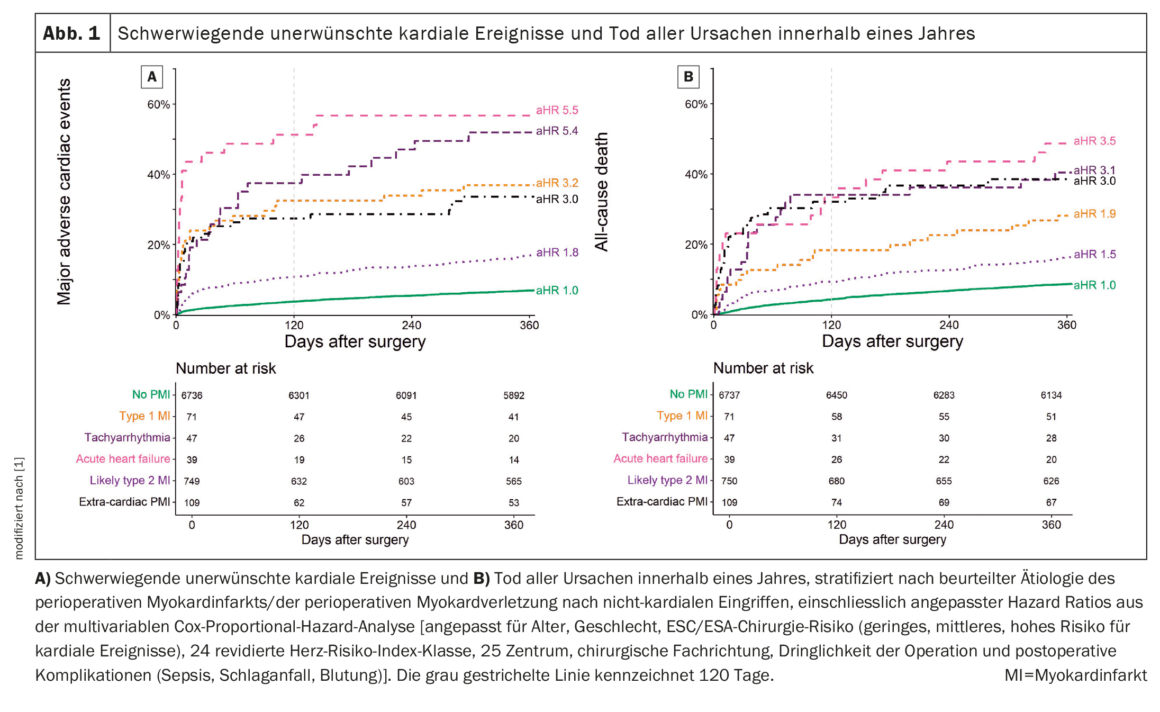
Para todas as aetiologias PMI, a taxa de MACE de 1 ano foi significativamente aumentada em comparação com os pacientes sem PMI. Em doentes sem IMC (7%, 95% CI 6%-8%), e dentro da etiologia do IMC houve diferenças significativas (Fig. 1A) [1]: Extracardiac PMI, T1MI, taquiarritmia e AHF foram associados a taxas muito elevadas de MACE [30% (95% CI 20-47), 37% (95% CI 24-47), 49% (95% CI 34-75) e 56% (95% CI 38-70), respectivamente], e lT2MI foi também associado a taxas elevadas de MACE (17%, 95% CI 22-28). As associações foram confirmadas em análise multivariável com relações de perigo ajustadas (aHRs) de 3,0 (2,0-4,5), 3,2 (95% CI 2,1-4,8), 5,4 (3,5-8,4) e 5,5 (3,5-8,7) para PMI extracardíaco, T1MI, taquiarritmia e AHF, e 1,8 (1,5-2,2) para lT2MI.
Foi observada uma associação semelhante para o MACE aos 120 dias, com uma RAH numericamente mais elevada na análise multivariável em comparação com as associações de 1 ano, mas com menor potência devido a menos eventos. O tempo desde a cirurgia até ao início da MACE dentro de 120 dias diferiu significativamente entre as etiologias do PMI, desde uma mediana de três dias após AHF até 13 dias após lT2MI e 26 dias em doentes sem PMI. Ao examinar o número total de MACE estratificados pela etiologia do PMI, ocorreram múltiplos eventos em 3% a 23% dos doentes, em comparação com 1% nos doentes sem PMI. A associação do PMI aetiology com MACE foi mais forte nos primeiros 120 dias do que ao fim de um ano.
Mortalidade total de acordo com o PMI
Todas as aetiologias PMI tiveram uma taxa de mortalidade por todas as causas aumentada de 1 ano em comparação com os pacientes sem PMI. Em doentes sem IMC (9%, 95% CI 8-9%), e dentro das etiologias de IMC, houve diferenças significativas (Fig. 1B) [1]: PMI extracardíaco, T1MI, taquiarritmia e AHF foram associados a elevadas taxas de mortalidade [38% (95% CI 29-47), 28% (95% CI 17-38), 40% (95% CI 25-53) e 49% (95% CI 30-62), respectivamente], e lT2MI foi também associado a elevadas taxas de mortalidade (17%, 95% CI 14-20). Esta relação foi confirmada na análise multivariável.
Modelo de previsão para lT2MI
MACE ou morte por todas as causas ocorreu em 117/750 pacientes com IT2MI no prazo de 120 dias. A presença de dor no peito ou dispneia, um aumento absoluto de cTn >2 × 99º percentil em comparação com a base de referência, cirurgia de alto risco de acordo com a pontuação de risco cirúrgico ESC/ESA e cirurgia não-eletiva foram associadas a um aumento do risco de MACE, enquanto que a hemorragia foi associada a um menor risco de MACE. A validação interna mostrou um bom acordo entre a taxa de eventos previstos e observados após o bootstrapping com 1000 iterações e uma pontuação Brier de 0,16.
O modelo prognóstico mostrou um AUC moderado de 0,71 (95% CI 0,66-0,76). Em comparação com o RCRI máximo (disponível em 747/750 casos), classe ASA (disponível em 718/750 casos) e hs-cTnT-delta absoluto (disponível em 564/750 casos), o modelo prognóstico mostrou a AUC numericamente mais elevada, que era estatisticamente diferente da classe ASA e hs-cTnT-delta (p=0,003) e comparável ao RCRI (p=0,195). A combinação do modelo prognóstico com a classe ASA ou RCRI aumentou ainda mais significativamente a AUC em comparação com a classe RCRI ou ASA apenas (modelo+ASA 0,75, 95% CI 0,71-0,80, p<0,001; modelo+RCRI 0,75, 95% CI 0,70-0,80, p<0,001). Após categorização pelo modelo prognóstico, o grupo de “muito alto risco” do IMC do lT2MI teve uma taxa de 31% de MACE ou morte (comparável ao IMC do T1MI), enquanto que o grupo de “baixo risco” teve taxas de 7% (comparáveis aos pacientes sem IMC).
Altas taxas de MACE e mortes por todas as causas após um ano
O grande estudo multicêntrico internacional prospectivo avaliou centralmente a etiologia do PMI identificada durante a vigilância activa em pacientes de alto risco submetidos a grandes cirurgias não cardíacas e monitorizou de perto o MACE durante o acompanhamento a longo prazo. Após um ano, a maioria das aetiologias PMI apresentam taxas inaceitavelmente elevadas de MACE e de morte por todas as causas, salientando a necessidade urgente de tratamentos mais intensivos.
Literatura:
- Puelacher C, et al.: Long-term outcomes of perioperative myocardial infarction/injury after non-cardiac surgery. EurHeartJ 2023.
https://doi.org/10.1093/eurheartj/ehac798 - Puelacher C, Lurati Buse G, Seeberger D, et al.: Perioperative myocardial injury after noncardiac surgery: incidence, mortality, and characterization. Circulation 2018;137: 1221–1232. https://doi.org/10.1161/CIRCULATIONAHA.117.030114
- Botto F, Alonso-Coello P, Chan MT V, et al.: Myocardial injury after noncardiac surgery: a large, international, prospective cohort study establishing diagnostic criteria, characteristics, predictors, and 30-day outcomes. Anesthesiology 2014;120: 564–578.
https://doi.org/10.1097/ALN.0000000000000113 - Devereaux PJ, Biccard BM, Sigamani A, et al.: Association of postoperative high-sensitivity troponin levels with myocardial injury and 30-day mortality among patients undergoing noncardiac surgery. JAMA 2017;317: 1642–1651.
https://doi.org/10.1001/jama.2017.4360 - Landesberg G, Mosseri M, Zahger D, et al.: Myocardial infarction after vascular surgery: the role of prolonged stress-induced, ST depression-type ischemia. J Am Coll Cardiol 2001;37:1839–1845. https://doi.org/10.1016/S0735-1097(01)01265-7
- Landesberg G, Shatz V, Akopnik I, et al.: Association of cardiac troponin, CK-MB, and postoperative myocardial ischemia with long-term survival after major vascular surgery. J Am Coll Cardiol 2003;42: 1547–1554. https://doi.org/10.1016/j.jacc.2003.05.001
- Devereaux PJ, Xavier D, Pogue J, et al.: Characteristics and short-term prognosis of perioperative myocardial infarction in patients undergoing noncardiac surgery: a cohort study. Ann Intern Med 2011;154: 523–528. https://doi.org/10.7326/0003-4819-154-8-201104190-00003
- Devereaux PJ, Chan MT V, Alonso-Coello P, et al.: Association between postoperative troponin levels and 30-day mortality among patients undergoing noncardiac surgery. JAMA 2012;307: 2295–2304. https://doi.org/10.1001/jama.2012.5502
- Thygesen K, Alpert JS, Jaffe AS, et al.: Fourth universal definition of myocardial infarction (2018). Eur Heart J 2019;40: 237–269. https://doi.org/10.1093/eurheartj/ehy462.
- Duceppe E, Parlow J, MacDonald P, et al.: Canadian Cardiovascular Society guidelines on perioperative cardiac risk assessment and management for patients who undergo noncardiac surgery. Can J Cardiol 2017;33: 17–32. https://doi.org/10.1016/j.cjca.2016.09.008
- Gualandro DM, Yu PC, Caramelli B, et al.: 3rd guideline for perioperative cardiovascular evaluation of the Brazilian society of cardiology. Arq Bras Cardiol 2017;109: 1-104. https://doi.org/10.5935/abc.20170140
- Halvorsen S, Mehilli J, Cassese S, et al.: 2022 ESC guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J 2022;43: 3826–3924. https://doi.org/10.1093/eurheartj/ehac270.
- Gualandro DM, Campos CA, Calderaro D, et al.: Coronary plaque rupture in patients with myocardial infarction after noncardiac surgery: frequent and dangerous. Atherosclerosis 2012;222: 191–195. https://doi.org/10.1016/j.atherosclerosis.2012.02.021
- Duvall WL, Sealove B, Pungoti C, et al.: Angiographic investigation of the pathophysiology of perioperative myocardial infarction. Catheter Cardiovasc Interv 2012;80: 768–776. https://doi.org/10.1002/ccd.23446
- Sheth T, Natarajan MK, Hsieh V, et al.: Incidence of thrombosis in perioperative and non-operative myocardial infarction. Br J Anaesth 2018;120: 725–733. https://doi.org/10.1016/j.bja.2017.11.063
- Puelacher C, Gualandro DM, Lurati Buse G, et al.: Etiology of peri-operative myocardial infarction/injury after noncardiac surgery and associated outcome. J Am Coll Cardiol 2020;76: 1910–1912. https://doi.org/10.1016/j.jacc.2020.08.043
- Landesberg G, Beattie WS, Mosseri M, et al.: Perioperative myocardial infarction. Circulation 2009;119: 2936–2944. https://doi.org/10.1161/CIRCULATIONAHA.108.828228.
- Howell SJ, Brown OI, Beattie WS: Aetiology of perioperative myocardial injury: a scientific conundrum with profound clinical implications. Br J Anaesth 2020;125: 642-646. https://doi.org/10.1016/j.bja.2020.08.007.
- Hicks KA, Tcheng JE, Bozkurt B, et al.: 2014 ACC/AHA key data elements and definitions for cardiovascular endpoint events in clinical trials. Circulation 2015;132: 302–361.
- Sazgary L, Puelacher C, Lurati Buse G, et al.: Incidence of major adverse cardiac events following non-cardiac surgery. Eur Heart J Acute Cardiovasc Care 2020;10: 550–558. https://doi.org/10.1093/ehjacc/zuaa008.
CARDIOVASC 2023; 22(1): 46–48