No estudo SEQUENCE, o risankizumab foi comparado com o ustekinumab para o tratamento da doença de Crohn (DC) em doentes que tinham falhado as terapêuticas anti-TNF. Foram também medidos biomarcadores como a calprotectina fecal (CF) e a proteína C-reactiva (PCR) [1]. Para além dos parâmetros clínicos e endoscópicos, estes biomarcadores permitiram uma avaliação objetiva da evolução da doença [1].
A DC é extremamente stressante para as pessoas afectadas: a inflamação subjacente no trato gastrointestinal pode causar danos intestinais permanentes e prejudicar significativamente a qualidade de vida [2, 3]. Os dois inibidores da interleucina (IL)-23 e IL-12/-23, risankizumab (SKYRIZI®) e ustekinumab, entre outros, estão autorizados para o tratamento da DC na Suíça [4, 5]. As duas opções de tratamento foram comparadas no estudo comparativo SEQUENCE publicado no New England Journal of Medicine (NEJM) [1]. Este é o primeiro estudo comparativo em DC a mostrar a superioridade de um biológico sobre outro(leia o resumo do estudo aqui) [1].
[1,6] Uma análise aprofundada mostra agora também a melhor resposta com risankizumab em vários subgrupos e em relação aos biomarcadores.
Risankizumab também é favorável na análise de subgrupo
Mais de 500 doentes que não responderam a um ou mais inibidores do TNF foram aleatorizados e tratados de forma aberta durante 48 semanas com risankizumab (N=255) ou ustekinumab (N=265) [1]. Numa comparação frente a frente com ustekinumab, o risankizumab foi superior e todos os endpoints primários e secundários foram atingidos [1]. Estes incluíram endpoints clínicos e endoscópicos, tais como remissão clínica (CDAI* < 150) ou remissão endoscópica na semana 48 (SES-CD* ≤ 4 e pelo menos 2 pontos abaixo da linha de base). Além disso, os resultados nos subgrupos predefinidos foram geralmente consistentes com os resultados da análise primária. Por exemplo, o risankizumab demonstrou ser vantajoso em relação ao ustekinumab em termos de obtenção de remissão endoscópica após 48 semanas em doentes com diferentes durações, gravidades e localizações da doença [1].
Redução significativamente maior dos biomarcadores com risankizumab [6]
Uma possível limitação do estudo SEQUENCE foi o desenho do estudo aberto, que pode ter influenciado o relato dos sintomas. No entanto, para além dos endpoints endoscópicos, que foram analisados centralmente sem conhecimento da alocação do grupo de cada doente, a análise de biomarcadores objectivos como a FC e a PCR também sublinha a eficácia superior do risankizumab em comparação com o ustekinumab [1]. A FC e a PCR são os dois biomarcadores mais utilizados na DC e servem como marcadores objectivos da inflamação intestinal [7]. A normalização da FC e da PCR é, por isso, também recomendada como um objetivo de tratamento a médio prazo nas orientações STRIDE II [7]. No estudo SEQUENCE, a FC e a PCR foram medidas nos doentes antes do início do tratamento e às semanas 8, 24 e 48. Após 24 e 48 semanas, o nível de FC no grupo do risankizumab tinha reduzido significativamente mais em média do que nos doentes com ustekinumab (Fig. 1) [6]. Resultados semelhantes foram obtidos através da análise dos valores de PCR. Após apenas 8 semanas, foi observada uma redução significativamente maior em relação à linha de base com risankizumab do que com ustekinumab (Fig. 1) [6]. Globalmente, a redução da FC e da PCR correlacionou-se com as taxas de remissão clínica e endoscópica após 48 semanas, nas quais o risankizumab mostrou superioridade em relação ao ustekinumab [1].
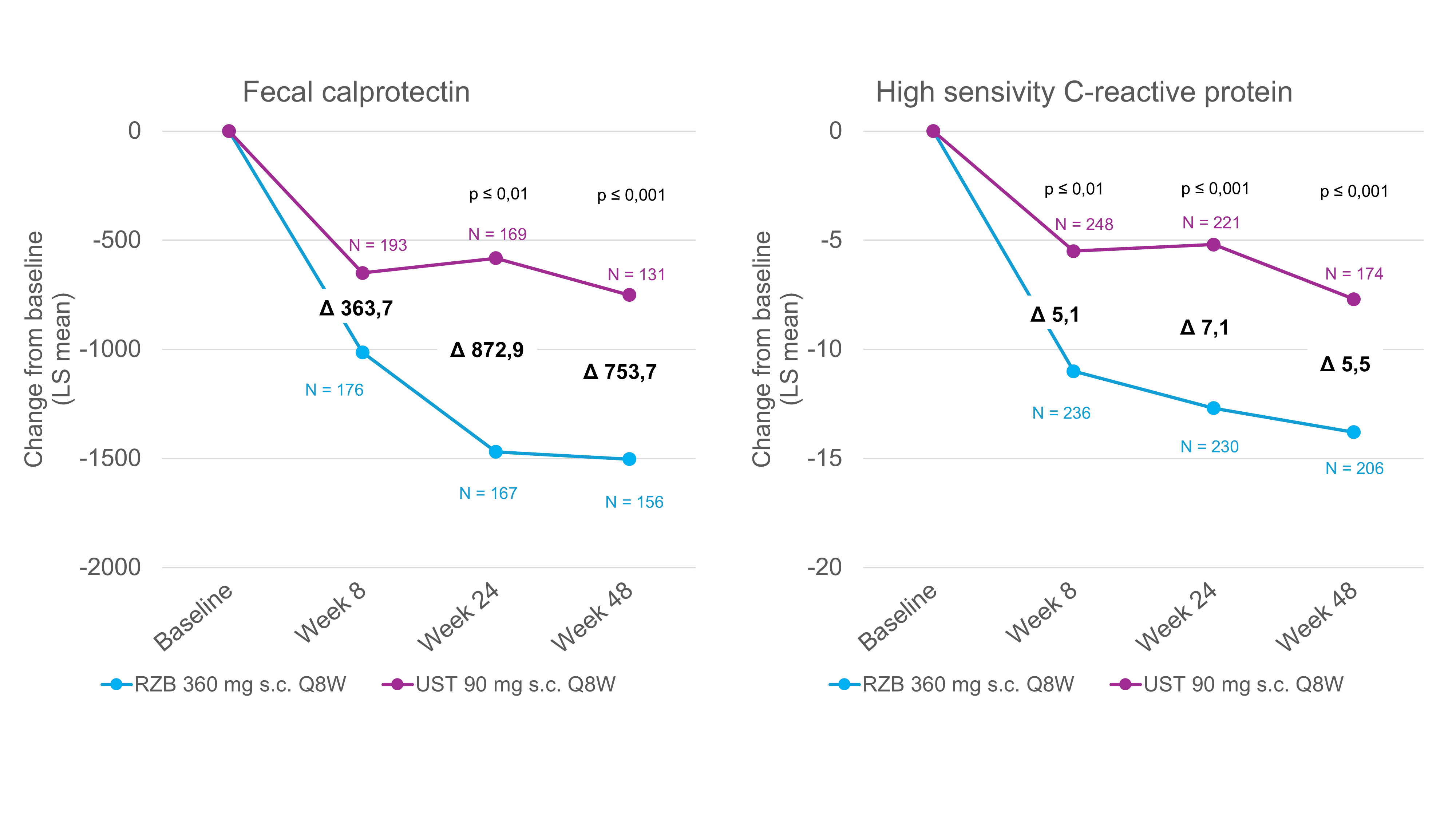
Fig. 1. O risankizumab conduz a uma redução significativamente maior dos biomarcadores em comparação com o ustekinumab. LS = mínimos quadrados; Q8W = a cada 8 semanas; RZB = risankizumab; s.c. = subcutâneo; UST = ustekinumab. Análise post-hoc, todos os valores de P são nominais e não controlados por multiplicidade. Adaptado de [6]
Conclusão
O estudo SEQUENCE mostra que o risankizumab não só é clinicamente e endoscopicamente superior ao ustekinumab no tratamento da DC, como também permite uma redução mais rápida e maior dos biomarcadores objectivos FC e PCR [1]. A melhoria dos valores dos biomarcadores realça o potencial do risankizumab para permitir um controlo sustentado da atividade da doença e oferecer aos doentes uma melhor qualidade de vida a longo prazo.
* Abreviaturas: CDAI = Índice de Atividade da Doença de Crohn; SES-CD = Simple Endoscopic Score for Crohn’s Disease.
Breve informação técnica SKYRIZI® SKYRIZI
Relatório: Dr. sc. Stefanie Jovanovic

Este artigo foi produzido com o apoio financeiro da AbbVie AG, Alte Steinhauserstrasse 14, Cham.
CH-SKZG-240070 10/2024 Este artigo foi publicado em alemão.
Literatura
1 Peyrin-Biroulet, L., et al, Risankizumab versus ustekinumab para a doença de Crohn moderada a grave. N Engl J Med, 2024. 391(3): p. 213-223.
2 Jairath, V. e B.G. Feagan, Global burden of inflammatory bowel disease (Peso global da doença inflamatória intestinal). Lancet Gastroenterol Hepatol, 2020. 5(1): p. 2-3.
3 O peso global, regional e nacional da doença inflamatória intestinal em 195 países e territórios, 1990-2017: uma análise sistemática para o Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol, 2020. 5(1): p. 17-30.
4. Resumo atual das caraterísticas do produto SKYRIZI® (risankizumab) Doença de Crohn em www.swissmedicinfo.ch.
5. Resumo atual das caraterísticas do produto do ustekinumab em www.swissmedicinfo.ch.
6 Dubinsky, M., et al. Risankizumab versus Ustekinumab para a obtenção de remissão clínica e redução dos biomarcadores inflamatórios em doentes com doença de Crohn moderada a grave: resultados do ensaio de fase 3B SEQUENCE. Apresentação oral 763 na DDW 2024; Washington D.C., EUA, 19-21 de maio de 2024.
7 Turner, D., et al, STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organisation for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology, 2021. 160(5): p. 1570-1583.
As referências podem ser solicitadas por especialistas em medinfo.ch@abbvie.com.