A compreensão cada vez melhor das relações patogénicas do carcinoma de células renais tem contribuído para o desenvolvimento de novos medicamentos. Estes interferem especificamente com as vias de sinalização VEGF, PDGF e mTOR. Nos últimos anos, foram também desenvolvidas terapias que orientam o sistema imunitário para o combate a tumores. Onde estamos hoje no mRCC? O que dizem as directrizes actuais?
O carcinoma das células renais é relativamente raro na Suíça, com uma incidência de cerca de 950 casos e 1,8% de mortes por ano por cancro. Os homens são afectados significativamente mais frequentemente que as mulheres (67,9% vs. 32,1%) e cerca de um terço dos doentes já têm metástases locais ou distantes no momento do diagnóstico [1]. Em cerca de 25% dos doentes com doença localizada, as metástases distantes ocorrem após uma nefrectomia de concepção curativa [2].
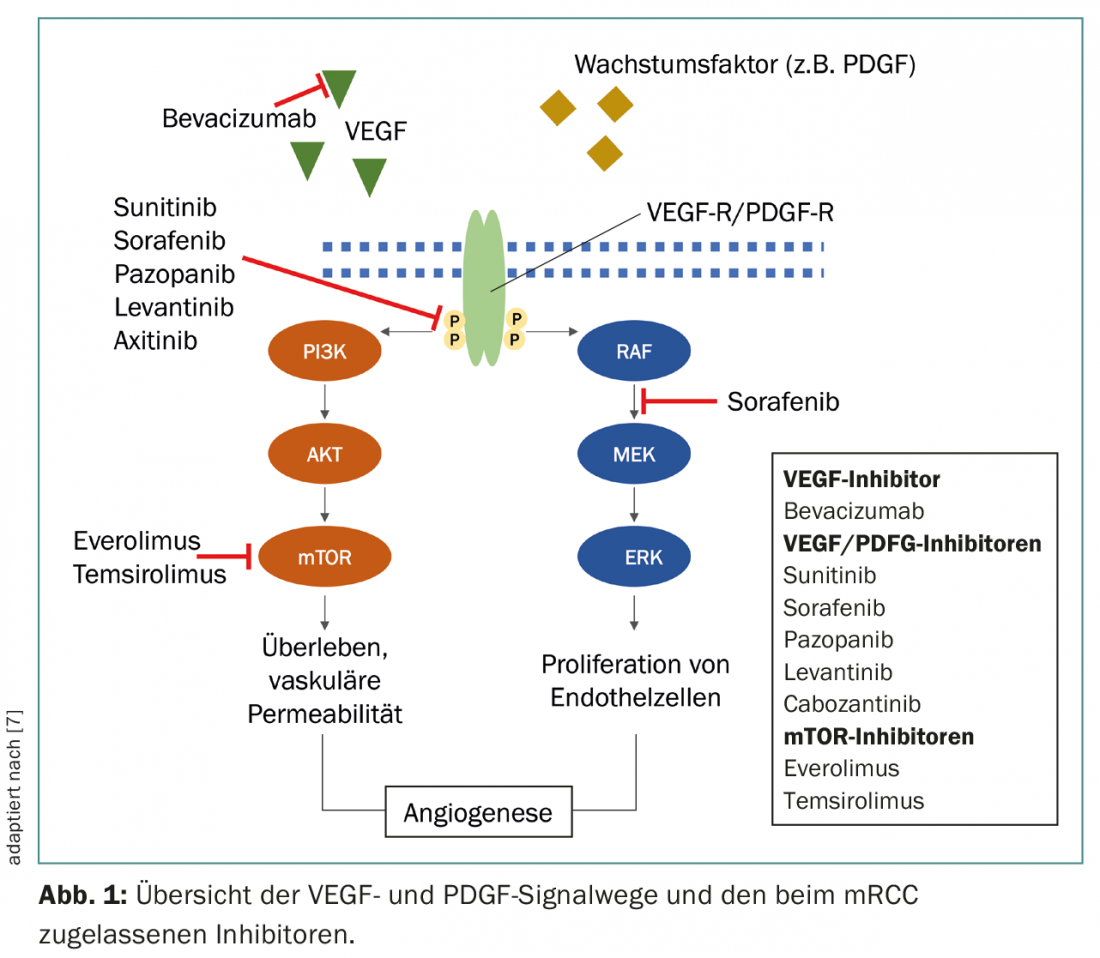
Dos numerosos subtipos, o carcinoma de células renais leves é o mais comum, sendo responsável por 70-75% dos casos, e está associado à inactivação dos genes Von Hippel-Lindau (BVS), levando ao aumento da actividade do factor induzido pela hipoxia (HIF) e, em última análise, à sobreexpressão do factor de crescimento vascular endotelial (VEGF) e do factor de crescimento derivado de plaquetas (PDGF) [3,4]. A actividade da HIF também pode ser reforçada pelo caminho de sinalização do Mammalian Target of Rapamycin (mTOR) [5]. A compreensão destas relações contribuiu significativamente para o desenvolvimento de novos medicamentos que interferem especificamente com as vias de sinalização VEGF, PDGF e mTOR (Fig. 1).
Nos últimos anos, foram também desenvolvidas terapias que orientam o sistema imunitário para combater o tumor. A expressão do CTLA-4 e PD-1 por células T activadas leva a uma redução da actividade das células T em diferentes fases da resposta imunitária. O anticorpo monoclonal anti-CTLA-4 (mAB) ipilimumab e o anti-PD-1 mAB nivolumab ajudam a induzir uma resposta eficaz anti-células T anti-tumor, bloqueando estes receptores de ponto de controlo [6].
Classificação de grupos de risco e orientações
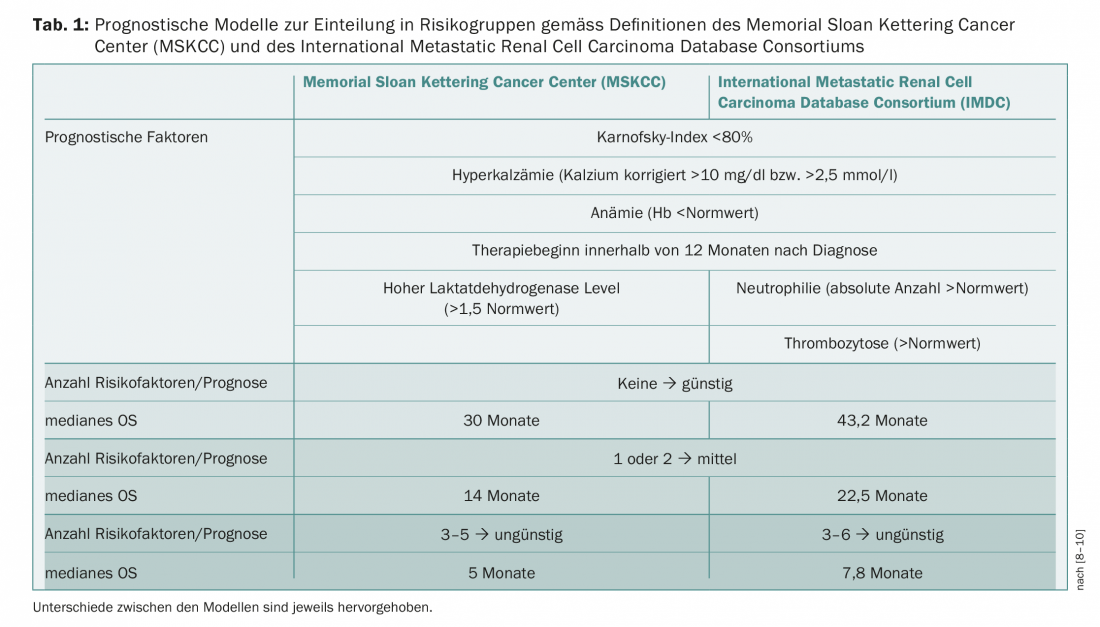
Os modelos prognósticos e a classificação dos pacientes em diferentes grupos de risco constituem uma base importante para as decisões terapêuticas. Os critérios do Memorial Sloan Kettering Cancer Center (MSKCC) são anteriores ao estabelecimento de terapias orientadas [8]. Em alternativa, o International Metastatic Renal Cell Carcinoma Database Consortium (IMDC) definiu factores como base para a avaliação de risco [9,10]. Os dois sistemas diferem apenas em alguns pontos e dividem os pacientes em grupos de risco favoráveis, intermediários e desfavoráveis (Tab. 1) . O tratamento do mRCC tem estado em constante fluxo desde a primeira aprovação de uma terapia orientada (sunitinib, 2006). Novas directrizes da Associação Europeia de Urologia (EAU) foram publicadas no início de 2018, que, com base no estudo CheckMate-214, já enumeram a terapia de combinação com nivolumab/ipilimumab em doentes com risco intermédio/desfavorável [11]. No estudo, a combinação de nivolumab e ipilimumab alcançou uma taxa de sobrevivência de 1,5 anos de 75% em comparação com 60% com o sunitinib após um seguimento médio de 25,2 meses (HR 0,63, p<0,001). A mediana de sobrevivência sem progressão (PFS) foi de 11,6 meses no grupo nivolumab/ipilimumab e 8,4 meses no grupo sunitinib; contudo, esta diferença entre os braços de tratamento não foi estatisticamente significativa (HR 0,82, p=0,03) [12]. A taxa de resposta objectiva foi de 42% contra 27% (p<0,001) e a taxa de remissões completas foi também mais elevada com a combinação de imunoterapia (9%) do que com o sunitinib (1%). A terapia combinada ipilimumab/nivolumab foi recentemente aprovada na Suíça para o tratamento do mRCC. Actualmente, a Associação Suíça para a Investigação Clínica do Cancro (SAKK) está a realizar um ensaio de fase II com ipilimumab e nivolumab na primeira ou segunda linha de terapia (SAKK 07/17).
A seguir, será discutida principalmente a gestão terapêutica com os inibidores de tirosina cinase (TKI) anti-angiogénicos visados e os inibidores de mTOR. O quadro 2 mostra uma visão geral das directrizes actuais, com destaque para as substâncias aprovadas na Suíça.

Nefrectomia como padrão de cuidados no mRCC
A nefrectomia tem sido parte integrante da terapia de mRCC há quase 20 anos, pois foi demonstrado que a cirurgia antes da terapia de interferão alfa (IFN-α) confere um benefício de sobrevivência em comparação com o tratamento de IFN-α apenas [17,18]. No entanto, o papel da nefrectomia no contexto das terapias anti-angiogénicas específicas não tem sido claro, embora estudos retrospectivos tenham tendido a confirmar o benefício do procedimento [19]. Dados sobre a nefrectomia de sequência → sunitinib versus sunitinib → nefrectomia (SURTIME) foram apresentados na ESMO 2017. Embora o estudo tenha sido interrompido prematuramente devido ao longo recrutamento de pacientes, pode ser utilizado como uma fonte de dados prospectiva. Não houve diferença na mediana PFS aos 7 meses (42,0% vs 42,9%, p>0,99) entre os grupos de tratamento, mas foi mostrada uma tendência para uma melhor sobrevivência global (OS) no grupo de cirurgia secundária (HR 0,57, 95% CI 0,34-0,95, p=0,032) [20]. Com o ensaio CARMENA fase III, recentemente publicado, estão disponíveis dados prospectivos que mostram a não-inferioridade da terapia com sunitinibe apenas em comparação com a nefrectomia mais sunitinibe em doentes de risco intermédio e desfavorável [21]. O estudo randomizou 450 doentes para tratamento com nefrectomia/sunitinibe ou sunitinibe. Os doentes tratados apenas com sunitinibe apresentaram um SO mediano mais longo do que o grupo da nefrectomia (18,4 vs. 13,9 meses, HR 0,89) e os critérios de não-inferioridade do sunitinibe foram cumpridos em conformidade [21]. Os autores concluem que embora a nefrectomia possa ser útil para o controlo dos sintomas (macrohaematúria, dor renal), a terapia com um inibidor VEGF sem nefrectomia não tem desvantagens em termos de OS [21]. Se o risco for baixo, a nefrectomia continuará provavelmente a ser escolhida para a maioria dos pacientes no futuro.
Escolha da terapia de primeira linha
Sunitinib e pazopanibe são as terapias de primeira linha mais utilizadas para doentes com risco favorável e intermédio, respectivamente [22]. Os dados do estudo CheckMate-214 e a aprovação do nivolumab/ipilimumab conduzirão a uma mudança no algoritmo terapêutico. Os dados do ensaio IMmotion151 (atezolizumab e bevacizumab vs. sunitinib) sobre a sobrevivência global são também aguardados com interesse. No entanto, a escolha da terapia de primeira linha também se baseia nas condições individuais de cada paciente e em quaisquer comorbidades [22]. Sunitinib mais do dobro da mediana PFS (11 vs. 5 meses, HR 0,539, p<0,001) e atingiu a mediana OS de mais de dois anos (26,4 vs. 21,8 meses, HR 0,821, p=0,051) em comparação com IFN-α [23]. No estudo de Acesso Expandido ao Mundo Real, observou-se também que o sunitinib tem um PFS mediano de 9,4 meses e um OS mediano de 18,7 meses [24]. Após mais de dez anos de experiência, o sunitinib substituiu agora o IFN-α como padrão de cuidados na terapia de primeira linha [25].
No ensaio COMPARZ randomizado, fase III, não-inferioridade, o pazopanibe era não-inferior ao sunitinibe (9,5 meses) com uma PFS mediana de 8,4 meses (HR 1,05). O SO mediano foi também comparável entre as duas terapias (pazopanibe: 28,3 meses, sunitinib 29,1 meses, HR 0,92), e a taxa de resposta objectiva foi de 31% com pazopanibe vs. 25% com sunitinib [26]. Num ensaio aleatório de preferência de pacientes (PICES), o pazopanibe teve um desempenho estatisticamente significativamente melhor do que o sunitinib [27]. Como outra opção na terapia de primeira linha, foi observada uma melhoria de 3,3 meses na PFS mediana com a combinação de bevacizumab com IFN-α em comparação com IFN-α (8,5 vs. 5,2 meses, HR 0,71) [28]. Em doentes com risco desfavorável, foi também observado um prolongamento significativo do SO mediano com temsirolimus versus IFN-α (10,9 versus 7,3 meses, HR 0,73) [29].
Escolha da terapia de segunda linha e tratamentos de seguimento
Para além da duração da resposta à terapia de primeira linha, da sintomatologia do doente e das comorbilidades existentes, as toxicidades individuais anteriores também têm influência na escolha da terapia de segunda linha [22,30]. Os doentes que tenham sofrido graves efeitos secundários ou perdas de qualidade de vida com a sua terapia anterior podem, portanto, beneficiar de uma mudança de classe de medicamentos [22]. Por exemplo, a diabetes de tipo 2 mal controlada pode ser agravada pela utilização de um inibidor de mTOR, as doenças cardiovasculares podem ser um factor de risco no contexto das terapias anti-VEGF, e as doenças auto-imunes existentes têm de ser consideradas no contexto das terapias baseadas em inibidores de pontos de controlo [31–33].
No ensaio AXIS fase III, a mediana PFS (HR 0,66, p<0,0001) e o SO mediano foram alcançados com axitinibe versus sorafenibe na segunda linha de terapia (20,1 meses versus 19,2 meses, HR 0,97, p=0,37) [34]. Além disso, em comparação com o everolimus, tanto o cabozantinib no ensaio METEOR fase III (21,4 vs. 17,1 meses, HR 0,70, p=0,0002) como o nivolumab no ensaio CheckMate-025 fase III (25,0 vs. 19,6 meses, HR 0,73, 98,5% CI 0,57-0,93, p=0,002) levaram a uma melhoria significativa no OS mediano [35,36]. No entanto, nenhum benefício PFS foi mostrado com nivolumab (4,6 vs. 4,4 meses, HR 0,88, p=0,11) [36]. A combinação de lenvatinib e everolimus resultou num prolongamento significativo do PFS mediano em comparação com o everolimus (14,6 vs. 5,5 meses, HR 0,40, p=0,0005), mas associado a toxicidade [37,38].
Terapia e gestão dos efeitos secundários
O sucesso do tratamento no mRCC depende da escolha da terapia, mas também da gestão dos efeitos secundários.
No estudo COMPARZ, foram observados diferentes perfis de efeitos secundários sob sunitinibe e pazopanibe, o que pode influenciar a escolha individual da substância [26]. Fadiga, síndrome do pé de mão e mucosite oral aumentaram no braço do solitinibe e alteraram os níveis de enzimas hepáticas e a perda de peso aumentou no braço do pazopanibe. A terapia de estudo foi interrompida mais frequentemente no grupo do pazopanibe do que no grupo do solitinibe devido a efeitos adversos [26].
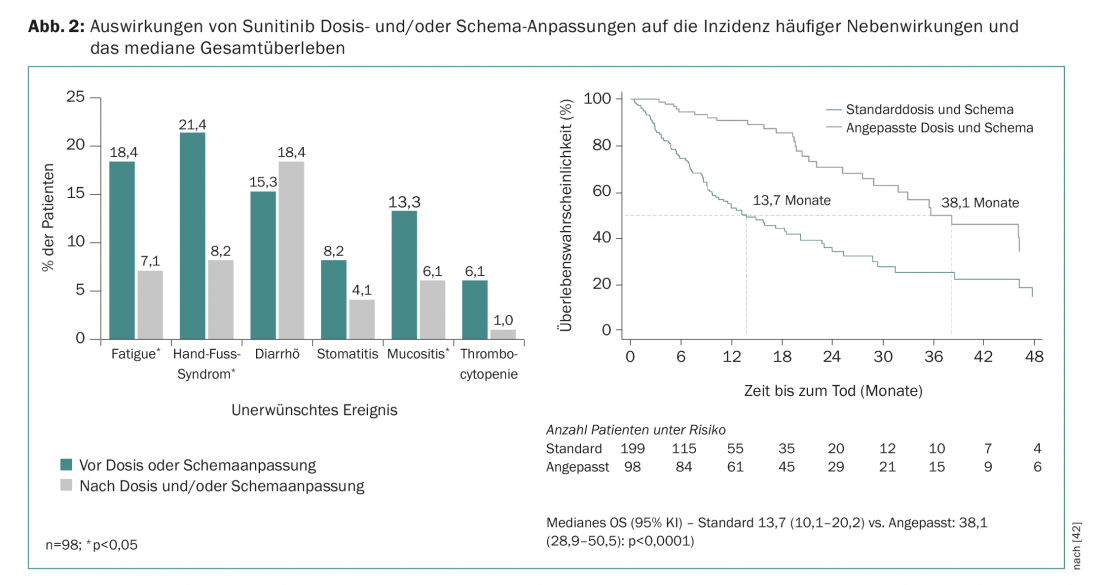
As análises farmacológicas retrospectivas indicam que uma maior exposição solaritinibe está associada a melhores resultados clínicos mas também a uma maior taxa de eventos adversos [39]. Sabe-se agora por vários estudos que o ajustamento do regime de tratamento do sunitinibe de “4 semanas de terapia/2 semanas de repouso (4/2)” para “2 semanas de terapia/1 semana de repouso (2/1)” pode ajudar a reduzir os efeitos adversos mais comuns sem comprometer a eficácia da terapia [40,41]. Isto também é confirmado pelos dados do futuro registo STAR-TOR, do mundo real, na Alemanha. Os ajustamentos da dose e/ou do regime durante a terapia com sunitinibe resultaram numa redução dos eventos adversos comuns (excepto diarreia) e numa melhoria do SO mediano (Fig. 2) [42]. Os ajustamentos das doses são também frequentemente necessários e comuns durante o tratamento com pazopanibe [43].
Perspectivas
Com a agora ampla gama de opções de tratamento em mRCC e os agentes adicionais esperados, a questão da escolha e sequência óptima do tratamento continua a ser uma questão chave. Por exemplo, a coorte EuroTARGET está a avaliar diferentes biomarcadores para personalizar a terapia de mRCC utilizando dados de doentes tratados com sunitinib-, pazopanib- ou sorafenib [44]. No futuro, a gestão proactiva e individualizada da terapia e dos efeitos secundários terá também uma influência significativa nos resultados clínicos.
Mensagens Take-Home
- Em risco intermédio/não favorável, a nefrectomia paliativa primária não demonstrou uma vantagem sobre a terapia anti-VEGF primária em termos de sobrevivência global. Se o risco for favorável, a nefrectomia citoreducativa primária continua a ser o padrão.
- Na terapia de primeira linha, o sunitinibe e o pazopanibe são recomendados para risco favorável/intermediário, enquanto que o temsirolimus pode ser utilizado para risco desfavorável ou histologia não celular.
- Nivolumab/ipilimumab pode ser utilizado se os custos forem aprovados ou no âmbito do estudo SAKK 07/17 e agora também é aprovado na Suíça. O Cabozantinib, por outro lado, ainda não tem aprovação para a primeira linha.
- O tratamento de segunda linha depende de vários factores individuais, bem como da resposta e toxicidade durante a terapia de primeira linha.
- O ajustamento do regime de tratamento com sunitinib de “4 semanas de terapia/2 semanas de folga (4/2)” para “2 semanas de terapia/1 semana de folga (2/1)” pode ajudar a melhorar a tolerabilidade sem perda de eficácia do tratamento.
Literatura:
- Krebsliga Schweiz: Cancro na Suíça: figuras importantes. Situação em Out. 2017 www.krebsliga.ch/ueber-krebs/zahlen-fakten/-dl-/fileadmin/downloads/sheets/zahlen-krebs-in-der-schweiz.pdf
- Choueiri TK, Motzer RJ: Terapia Sistémica para Carcinoma Renal-Celular Metástático. New England Journal of Medicine 2017; 376(4): 354-366.
- Clark PE: O papel da BVS no carcinoma de células claras de células renais e a sua relação com a terapia orientada. Kidney international 2009; 76(9): 939-945.
- Nickerson ML, et al: Melhoria da Identificação de Alterações Genéticas von Hippel-Lindau em Tumores Renais de Células Claras. Clinical Cancer Research 2008; 14(15): 4726-4734.
- Thomas GV, et al: O factor induzível de hipoxia determina a sensibilidade aos inibidores de mTOR no cancro renal. Nature medicine 2006; 12(1): 122-127.
- Sathianathen NJ, et al: O estado actual das terapias imunobaseadas para o carcinoma metastásico de células renais. ImmunoTargets and Therapy 2017; 6: 83-93.
- Rini BI, Pequeno EJ: Biologia e Desenvolvimento Clínico do Fator de Crescimento Endotelial Vascular – Terapia Orientada para o Carcinoma Renal de Células. Journal of Clinical Oncology 2005; 23(5): 1028-1043.
- Motzer RJ, Bacik J, Murphy BA, Russo P Mazumdar M: Interferon-Alfa como Tratamento Comparativo para Ensaios Clínicos de Novas Terapias Contra o Carcinoma Renal Avançado de Células Renais. Journal of Clinical Oncology 2002; 20(1): 289-296.
- Heng DYC, et al: Validação externa e comparação com outros modelos do modelo de prognóstico do Consórcio Internacional Metástático de Carcinoma Renal-Cell: um estudo baseado na população. Lanceta. Oncologia 2013; 14(2): 141-148.
- Heng DYC, et al: Factores Prognósticos para a Sobrevivência Global em Pacientes com Carcinoma Metástático de Células Renais Tratados com Agentes Orientados para o Factor de Crescimento Vascular Endotelial: Resultados de um Estudo Multicêntrico de Grande Porte. Journal of Clinical Oncology 2009; 27(34): 5794-5799.
- Powles T, et al: Updated European Association of Urology Guidelines Recommendations for the Treatment of First-line Metastatic Clear Cell Renal Cancer. Urologia Europeia 2017.
- Motzer RJ, et al: Nivolumab mais ipilimumab versus sunitinib em carcinoma avançado de células renais. New England Journal of Medicine 2018; 378(14): 1277-1290.
- Directriz S3 Diagnóstico, terapia e acompanhamento do carcinoma de células renais. Versão longa 1.2 – Abril 2017, AWMF número de registo: 043/017-OL.
- Escudier B, et al: Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up†. Anais de Oncologia 2016; 27(5): v58-v68.
- NCCN: National Comprehensive Cancer Network Clinical Practice Guidelines in Oncology – Kidney Cancer Version 3.2018. NCCN.org Fev. 6 2018.
- www.swissmedicinfo.ch.
- Flanigan RC, et al: Nefrectomia Seguida de Interferon Alfa-2b Comparado com Interferon Alfa-2b Sozinho para o Câncer Metástático de Células Renais. New England Journal of Medicine 2001; 345(23): 1655-1659.
- Mickisch GH, Garin A, et al: nefrectomia radical mais imunoterapia à base de interferão-alfa- em comparação com o interferão alfa sozinho no carcinoma metastático de células renais: um ensaio aleatório. Lancet 2001; 358(9286): 966-970.
- Culp SH: nefrectomia citoreducativa e o seu papel no actual período de terapia orientada. Ther Adv Urol 2015; 7(5): 275-285.
- Bex A, et al: Nefrectomia citoreducativa imediata versus diferida em doentes com carcinoma sincrónico de células renais metastásicas (mRCC) que recebem sunitinib (EORTC 30073 SURTIME). Anais de Oncologia 2017; 28(5): v605-v649; doi: 10.1093/annonc/mdx440.
- Mejean A, et al: Sunitinib Sozinho ou após Nefrectomia no Carcinoma Renal-Celular Metástático. The New England journal of medicine 2018. doi: 10.1056/NEJMoa1803675
- Osorio JC, et al: Optimizing Treatment Approaches in Advanced Renal Cancer. Oncologia 2017; 31(12): 919-926, 928-930.
- Motzer RJ, et al: Sobrevivência global e resultados actualizados para Sunitinib em comparação com Interferon Alfa em doentes com Carcinoma Metástático de Células Renais. Journal of Clinical Oncology 2009; 27(22): 3584-3590.
- Gore ME, et al: Resultados finais do grande ensaio global de acesso expandido ao sunitinib em carcinoma metastático de células renais. Revista britânica do cancro 2015; 113(1): 12-19.
- Motzer RJ, et al: Sunitinib: Dez Anos de Uso e Estudo Clínico com Sucesso no Carcinoma Renal Avançado de Células Renais. O Oncologista 2017; 22(1): 41-52.
- Motzer RJ, et al: Pazopanibe versus sunitinib em carcinoma metastático de células renais. New England Journal of Medicine 2013; 369(8): 722-731.
- Escudier B, et al: Randomized, Controlled, Double-Blind, Cross-Over Trial Assessing Treatment Preference for Pazopanib Versus Sunitinib in Patients With Metastatic Renal Cell Carcinoma: Estudo PISCES. Journal of Clinical Oncology 2014; 32(14): 1412-1418.
- Rini BI, et al: Bevacizumab Plus Interferon Alfa comparado com Interferon Alfa Monoterapia em Pacientes com Carcinoma Metástático de Células Renais: CALGB 90206. Journal of Clinical Oncology 2008; 26(33): 5422-5428.
- Hudes G, et al: Temsirolimus, Interferon Alfa, ou Both for Advanced Renal-Cell Carcinoma. New England Journal of Medicine 2007; 356(22): 2271-2281.
- Fischer S, et al: Sequência de tratamento em carcinoma de células renais localmente avançado e metastástico. Translational andrology and urology 2015; 4(3): 310-325.
- Johnson DB, et al: Immune Checkpoint Inhibitor Therapy in Patients With Autoimmune Disease. Oncologia 2018; 32(4): 190-194.
- Morviducci L, et al.: Everolimus é uma nova molécula anti-câncer: efeitos secundários metabólicos como perturbações lipídicas e hiperglicemia. Investigação e prática clínica da diabetes em 2018.
- Schmidinger M, et al.: Toxicidade cardíaca do sunitinibe e sorafenibe em doentes com carcinoma metastático de células renais. Journal of clinical oncology : revista oficial da Sociedade Americana de Oncologia Clínica 2008; 26(32): 5204-5212.
- Rini BI, et al: eficácia comparativa da axitinibe versus sorafenibe no carcinoma avançado de células renais (AXIS): um ensaio aleatório de fase 3. Lancet 2011; 378(9807): 1931-1939.
- Motzer RJ, et al: Acompanhamento a longo prazo da sobrevivência global do cabozantinibe versus everolimus no carcinoma avançado de células renais. Revista britânica do cancro 2018; 118(9): 1176-1178.
- Motzer RJ, et al: Nivolumab versus everolimus em carcinoma avançado de células renais. The New England journal of medicine 2015; 373(19): 1803-1813.
- Motzer RJ, et al: Lenvatinib, everolimus, e a combinação em doentes com carcinoma de células renais metastásicas: um ensaio randomizado, fase 2, aberto, multicêntrico. Lancet Oncol 2015; 16(15): 1473-1482.
- Rothermundt C, et al.: Tratamento de segunda linha para o cancro de células renais metástáticas claras: algoritmos de consenso de especialistas. Revista mundial de urologia 2017; 35(4): 641-648.
- Houk BE, et al.: Relação entre a exposição ao sunitinib e os parâmetros de eficácia e tolerabilidade em doentes com cancro: resultados de uma meta-análise farmacocinética/farmacodinâmica. Quimioterapia e Farmacologia do Cancro 2009; 66(2): 357-371.
- Atkinson BJ, et al: Clinical Outcomes in Metastatic Renal Cell Carcinoma Patients Treated with Alternative Sunitinib Schedules. The Journal of Urology 2014; 191(3): 611-618.
- Najjar YG, et al: A 2 semanas de solitinibe e 1 semana de folga está associada à diminuição da toxicidade no carcinoma metastático das células renais. European Journal of Cancer 2014; 50(6): 1084-1089.
- Boegemann M, et al.: Modificação do tratamento com sunitinib em carcinoma de células renais metastásicas (mRCC) de primeira linha (1L): Uma análise do registo STAR-TOR. Journal of Clinical Oncology 2018; 36(6_suppl): 602-602.
- Iacovelli R, et al: Resultado clínico dos pacientes que reduziram o sunitinib ou pazopanibe durante o tratamento de primeira linha do cancro renal avançado. Oncologia urológica 2017; 35(9): 541.e547-541.e513.
- van der Zanden LFM, et al: Descrição da coorte EuroTARGET: Um projecto colaborativo europeu sobre a terapia TArgeted no cancro de células renais – biomarcadores magnéticos e relacionados com tumores para resposta e toxicidade. Oncologia urológica 2017; 35(8): 529.e529-529.e516.
InFo ONcOLOGy & HaEMATOLOGy 2018; 6(4): 17-22.